文档内容
第三章 晶体结构与性质
第二节 金属晶体与离子晶体
第二课时 离子晶体 过渡晶体与混合型晶体
一.选择题
1. 下列叙述正确的是
A. 任何晶体中,若含有阳离子,就一定含有阴离子
B. 金属晶体的形成是因为晶体中存在金属阳离子间的相互作用
C. 价电子数越多的金属原子的金属性越强
D. 含有金属元素的离子不一定是阳离子
2. 下列说法正确的是
A. 、 、 的分子间作用力依次增大
B. 和晶体硅都是共价化合物,都是原子晶体
C. NaOH和 的化学键类型和晶体类型相同
D. 加热熔化时破坏了该物质中的离子键和共价键
3. 下列物质性质的变化规律,与化学键的强弱无关的是
A. 、 、 、 的熔点、沸点逐渐升高
B. HF、HCl、HBr、HI的热稳定性依次减弱
C. 金刚石的硬度、熔点、沸点都高于晶体硅
D. NaF、NaCl、NaBr、NaI的熔点依次降低
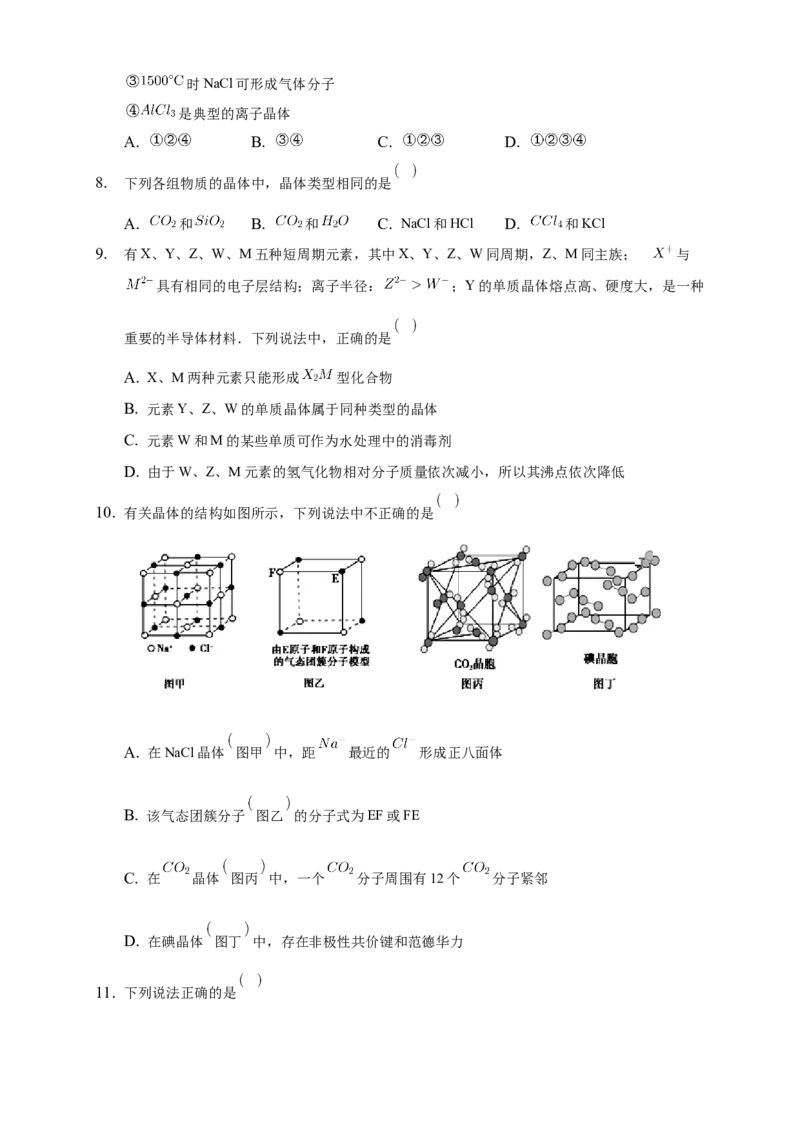
4. 有关晶体的结构如图所示,下列说法中不正确的是
A. 在NaCl晶体中,距 最近的 形成正八面体
B. 在 晶体中,每个晶胞平均占有4个C. 在金刚石晶体中,6个碳原子形成一个环且不在同一平面上
D. 该气态团簇分子的分子式为EF或FE
5. 下列说法不正确的是
A. 晶体沸点由高到低:金刚石
B. 碳酸盐的分解温度:
C. 无机含氧酸的酸性:
D. 与 ZnS 晶格能分别为 、 ,岩浆晶出次序为:
6. 氧化钙在 时熔化,而氯化钠在 时熔化,两者的离子间距离和晶体结构类似,
有关它们熔点差别较大的原因叙述不正确的是
A. 氧化钙晶体中阴、阳离子所带的电荷数多
B. 氧化钙的晶格能比氯化钠的晶格能大
C. 氧化钙晶体的结构类型与氯化钠晶体的结构类型不同
D. 在氧化钙与氯化钠的离子间距离类似的情况下,晶格能主要由阴、阳离子所带电荷的多少
决定
7. 下表给出几种化合物的熔点和沸点。
物质 NaCl
熔点 801 190
沸点 1465 178
关于表中三种化合物的说法正确的是
在加热时可升华
属于分子晶体时NaCl可形成气体分子
是典型的离子晶体
A. B. C. D.
8. 下列各组物质的晶体中,晶体类型相同的是
A. 和 B. 和 C. NaCl和HCl D. 和KCl
9. 有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期,Z、M同主族; 与
具有相同的电子层结构;离子半径: ;Y的单质晶体熔点高、硬度大,是一种
重要的半导体材料.下列说法中,正确的是
A. X、M两种元素只能形成 型化合物
B. 元素Y、Z、W的单质晶体属于同种类型的晶体
C. 元素W和M的某些单质可作为水处理中的消毒剂
D. 由于W、Z、M元素的氢气化物相对分子质量依次减小,所以其沸点依次降低
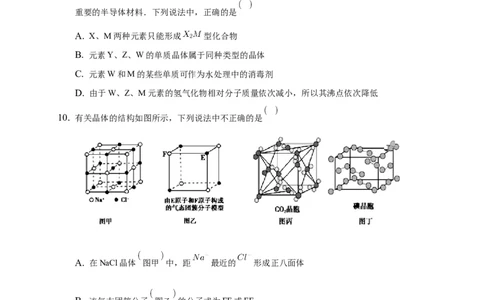
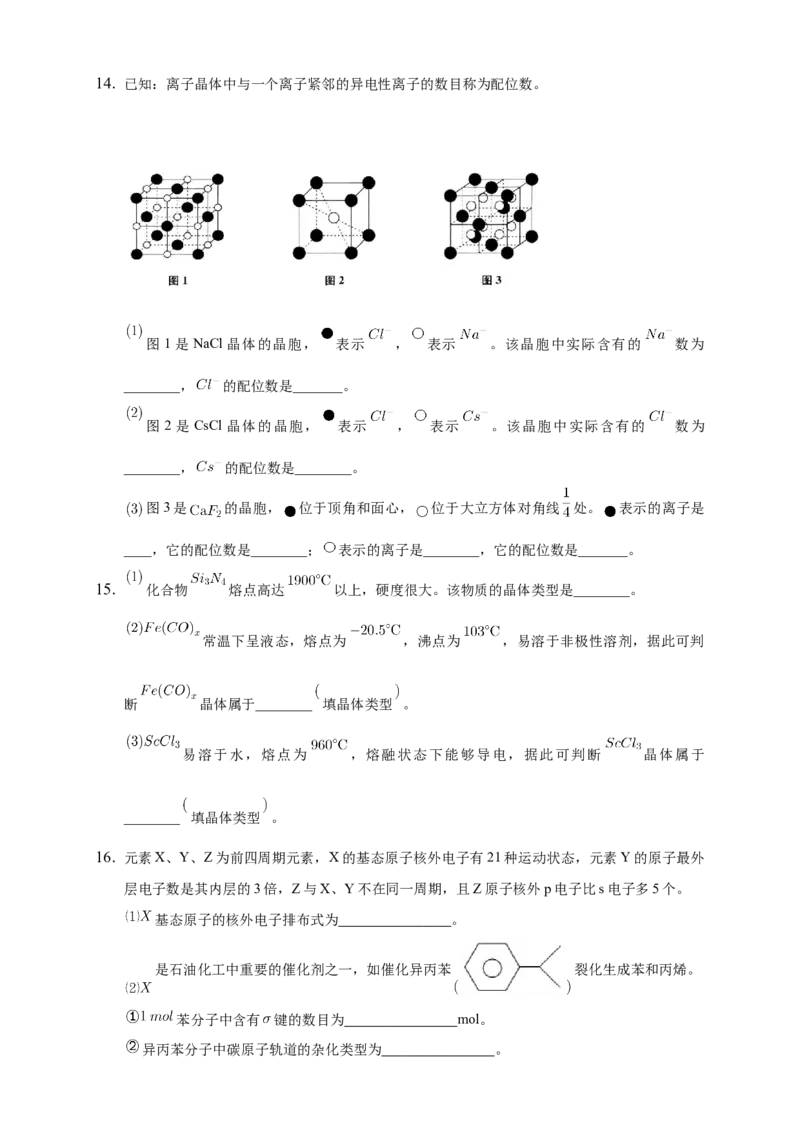
10. 有关晶体的结构如图所示,下列说法中不正确的是
A. 在NaCl晶体 图甲 中,距 最近的 形成正八面体
B. 该气态团簇分子 图乙 的分子式为EF或FE
C. 在 晶体 图丙 中,一个 分子周围有12个 分子紧邻
D. 在碘晶体 图丁 中,存在非极性共价键和范德华力
11. 下列说法正确的是A. 晶体中含有共价键
B. HI气体受热分解的过程中,只需克服分子间作用力
C. 金刚石和石墨均属于原子晶体
D. 的三种同分异构体因为分子间作用力大小不同,因而沸点不同
12. 下列数据是对应物质的熔点 ,据此做出的下列判断中错误的是
NaCl
920 801 1291 190
2073 1723
A. 铝的化合物形成的晶体中有的是离子晶体
B. 表中只有 和干冰是分子晶体
C. 同族元素的氧化物可形成不同类型的晶体
D. 不同族元素的氧化物可形成相同类型的晶体
二、填空题
13. 有A、B、C三种晶体,分别由H、C、Na、Cl四种元素中的一种或几种组成,对这三种晶体
进行实验,结果如表:
熔点 硬度 水溶性 导电性 水溶液与 反应
水溶液或熔
A 811 较大 易溶 白色沉淀
融导电
B 3500 很大 不溶 不导电 不反应
C 很小 易溶 液态不导电 白色沉淀
晶体的化学式分别为A__________、B__________、C__________。
晶体的类型分别是A__________、B__________、C__________。
晶体中微粒间作用力分别是A_____________、B_____________、C_____________
。14. 已知:离子晶体中与一个离子紧邻的异电性离子的数目称为配位数。
图1是NaCl晶体的晶胞, 表示 , 表示 。该晶胞中实际含有的 数为
________, 的配位数是_______。
图 2 是 CsCl 晶体的晶胞, 表示 , 表示 。该晶胞中实际含有的 数为
________, 的配位数是________。
图3是 的晶胞, 位于顶角和面心, 位于大立方体对角线 处。 表示的离子是
____,它的配位数是________; 表示的离子是________,它的配位数是_______。
15. 化合物 熔点高达 以上,硬度很大。该物质的晶体类型是________。
常温下呈液态,熔点为 ,沸点为 ,易溶于非极性溶剂,据此可判
断 晶体属于________ 填晶体类型 。
易溶于水,熔点为 ,熔融状态下能够导电,据此可判断 晶体属于
________ 填晶体类型 。
16. 元素X、Y、Z为前四周期元素,X的基态原子核外电子有21种运动状态,元素Y的原子最外
层电子数是其内层的3倍,Z与X、Y不在同一周期,且Z原子核外p电子比s电子多5个。
基态原子的核外电子排布式为 。
是石油化工中重要的催化剂之一,如催化异丙苯 裂化生成苯和丙烯。
苯分子中含有 键的数目为 mol。
异丙苯分子中碳原子轨道的杂化类型为 。与 分子互为等电子体的阳离子为 。
易溶于水,熔点为 ,熔融状态下能够导电,据此可判断 晶体属于
填晶体类型 。
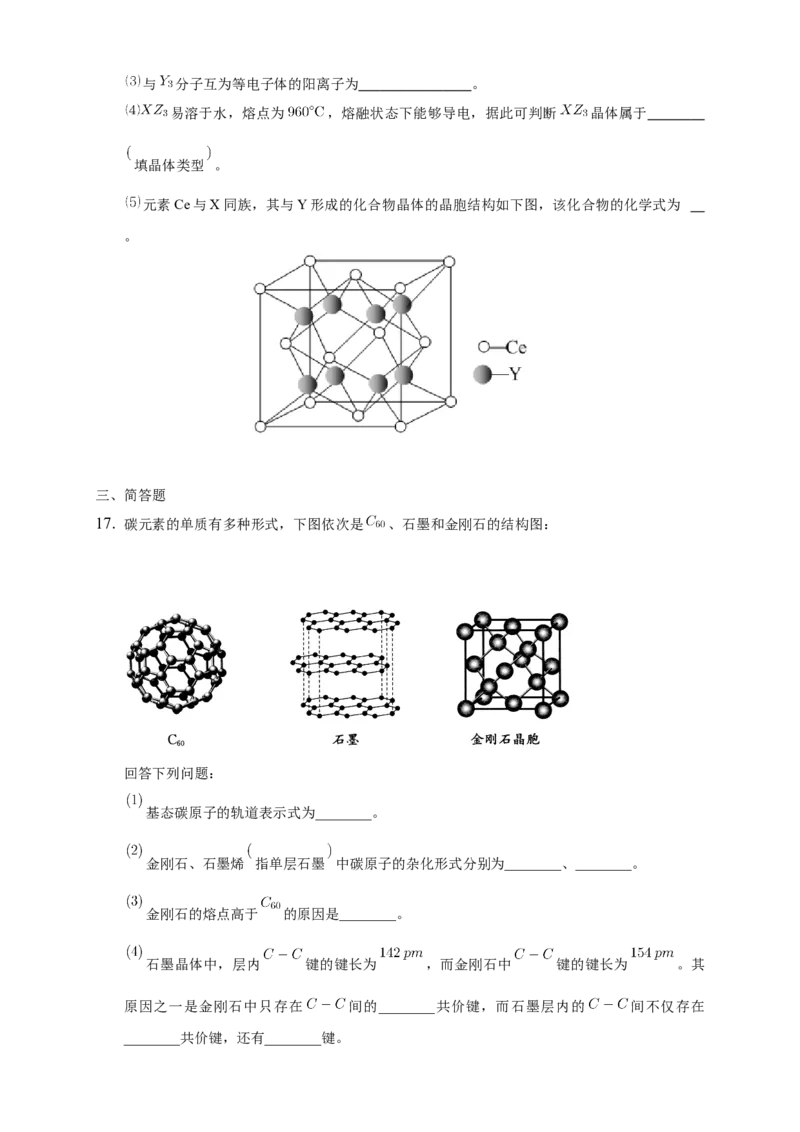
元素Ce与X同族,其与Y形成的化合物晶体的晶胞结构如下图,该化合物的化学式为
。
三、简答题
17. 碳元素的单质有多种形式,下图依次是 、石墨和金刚石的结构图:
回答下列问题:
基态碳原子的轨道表示式为________。
金刚石、石墨烯 指单层石墨 中碳原子的杂化形式分别为________、________。
金刚石的熔点高于 的原因是________。
石墨晶体中,层内 键的键长为 ,而金刚石中 键的键长为 。其
原因之一是金刚石中只存在 间的________共价键,而石墨层内的 间不仅存在
________共价键,还有________键。金刚石晶胞含有________个碳原子。若碳原子半径为r,金刚石晶胞的边长为a,根据硬球
接触模型,则 ________a,列式表示碳原子在晶胞中的空间占有率________ 不要求计算结
果 。
18. 2019年诺贝尔化学奖由来自美、英、日的三人获得,以表彰他们在锂离子电池研究方面做出
的贡献,他们最早发明用 作离子电池的正极,用聚乙炔作负极。回答下列问题:
基态Co原子价电子排布图为______ 轨道表达式 。第四电离能 比 小,是因
为______。
的熔点 比LiF的熔点 低,其原因是______。
乙炔 分子中 键与 键的数目之比为______。
锂离子电池的导电盐有LiBF4等,碳酸亚乙酯 是一种锂离子电池电解液的添
加剂。
中阴离子的空间构型是______;与该阴离子互为等电子体的分子有______。 列一种
碳酸亚乙酯分子中碳原子的杂化方式有______。
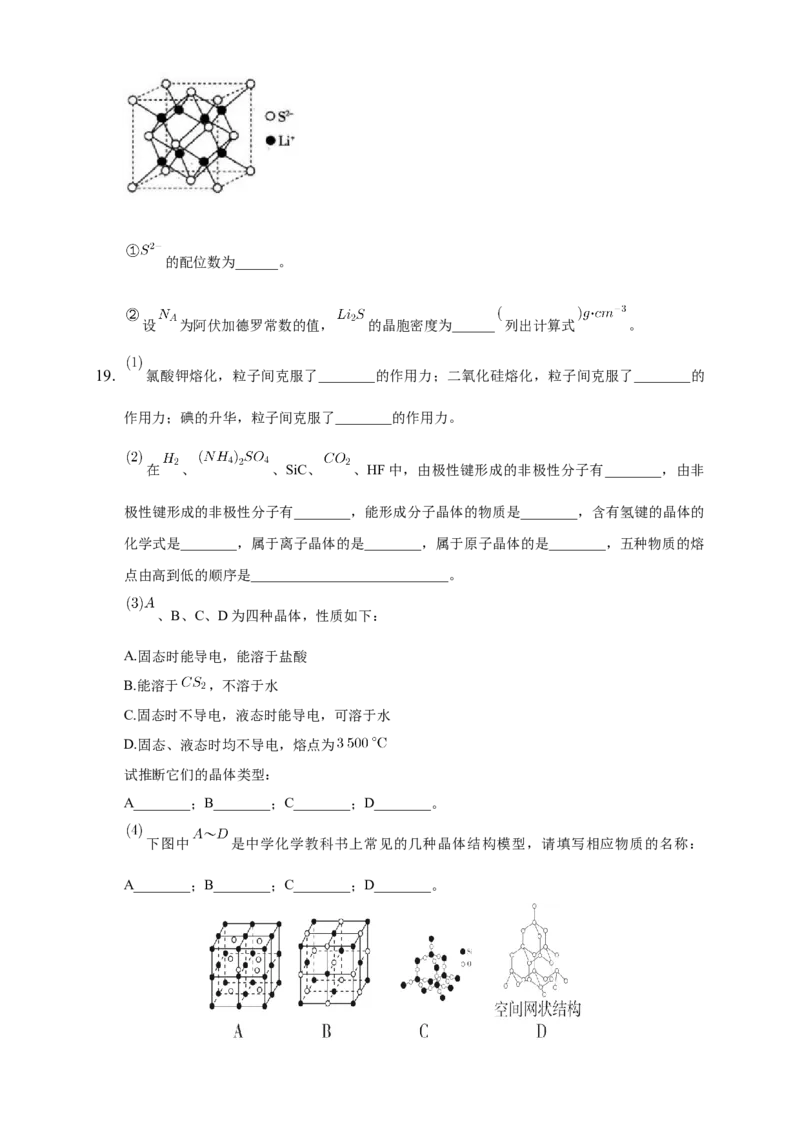
是目前正在开发的锂离子电池的新型固体电解质,其晶胞结构如图所示,已知晶胞参
数 。的配位数为______。
设 为阿伏加德罗常数的值, 的晶胞密度为______ 列出计算式 。
19. 氯酸钾熔化,粒子间克服了________的作用力;二氧化硅熔化,粒子间克服了________的
作用力;碘的升华,粒子间克服了________的作用力。
在 、 、SiC、 、HF中,由极性键形成的非极性分子有________,由非
极性键形成的非极性分子有________,能形成分子晶体的物质是________,含有氢键的晶体的
化学式是________,属于离子晶体的是________,属于原子晶体的是________,五种物质的熔
点由高到低的顺序是____________________________。
、B、C、D为四种晶体,性质如下:
A.固态时能导电,能溶于盐酸
B.能溶于 ,不溶于水
C.固态时不导电,液态时能导电,可溶于水
D.固态、液态时均不导电,熔点为
试推断它们的晶体类型:
A________;B________;C________;D________。
下图中 是中学化学教科书上常见的几种晶体结构模型,请填写相应物质的名称:
A________;B________;C________;D________。