文档内容
8.1 自然资源的开发利用(精练)
题组一 金属矿物的开发利用
1.(2021·安徽合肥·高一期末)下列关于金属冶炼的说法正确的是:
A.所有的金属在自然界都是以化合态形式存在
B.可用铝热法制备高熔点且活动性小于铝的金属
C.可用电解熔融AlCl 制备金属Al
3
D.可用热还原法制备金属Na
【答案】B
【解析】A. 活泼性较差的金属在自然界是以游离态形式存在,如金,故A错误;
B. 可用铝热法制备高熔点且活动性小于铝的金属,故B正确;
C. 可用电解熔融Al O 制备金属Al,氯化铝是共价化合物,液态时不导电,故C错误;
2 3
D. 可用电解法制备金属Na,故D错误;
故选B。
2.(2021·山西怀仁·高一期末)下列反应原理中,不符合工业冶炼金属实际情况的是
A. B.
C. D.
【答案】C
【解析】A.银的活泼性差,用加热分解氧化银的方法冶炼银,所以2Ag O 4Ag+O↑符合工业冶炼金属
2 2
实际情况,A正确;
B.工业上电解熔融氧化铝冶炼金属铝,所以2Al O(熔融) 4Al+3O ↑符合工业冶炼金属实际情况,
2 3 2
B正确;
C.工业上冶炼镁可采用电解法,其原料应选用MgCl 而不是MgO,因为MgO的熔点比MgCl 的高,会消
2 2
耗大量电能,成本较高,C错误;
D.该反应中Fe O 被CO还原,属于热还原法,铁性质较活泼,工业上常采用热还原法制取,D正确;
3 4答案选C。
3.(2021·广东揭东·高一期末)下列关于金属冶炼的说法正确的是
A.金属的冶炼都是把金属单质从其矿物中分离出来
B.古代火烧孔雀石炼铜的方法属于热还原法中的焦炭法
C.工业上可用电解熔融态的MgCl 、AlCl 来制备Mg、Al
2 3
D.利用该铝热反应 炼铁,1mol氧化剂参加反应转移9N 个电子
A
【答案】B
【解析】A.金属的冶炼是将化合物中的金属转化为金属单质,不是把金属从其矿物中分离出来,故A错
误;
B.孔雀石受热发生的是碱式碳酸铜分解生成氧化铜、二氧化碳和水,氧化铜和焦炭反应生成铜和二氧化
碳,因此古代火烧孔雀石炼铜的方法属于热还原法中的焦炭法,故B正确;
C.工业上可用电解熔融态的Al O 来制备Al,故C错误;
2 3
D.利用该铝热反应 炼铁,1mol氧化剂( )参加反应转移[(+3−0)×2+
(+2−0)×1]N =8 N 个电子,故D错误。
A A
综上所述,答案为B。
4.(2021·广西桂林·高一期末)下列冶炼金属的方法错误的是
A.火法炼 B.电解食盐水炼 C.铝热法炼 D.热分解法炼
【答案】B
【解析】A.可以用火法炼铜,如 ,故A正确;
B.电解食盐水生成氢氧化钠、氢气和氯气,不能生成钠,应该电解熔融的氯化钠冶炼钠,故B错误;
C.可以用铝单质和铁的氧化物高温下发生铝热反应冶炼铁,故C正确;
D.可以用加热氧化银的方法冶炼银,故D正确;
故选B。
5.(2021·河北邯郸·高一期末)下列有关金属冶炼的说法不正确的是
①可以用电解熔融氯化钠的方法来制取金属钠
②银可以采用热分解法,即通过加热 制得③用电解法冶炼铝时,原料是氯化铝
④高炉炼铁中利用焦炭直接将铁矿石还原为铁单质
⑤工业上可以用铝热反应来冶炼某些熔点较高的金属,如铬、锰
A.③④ B.①③ C.①②④ D.③⑤
【答案】A
【解析】①金属钠很活泼,可以用电解熔融氯化钠的方法来制取金属钠,①项正确;
②银的性质很稳定,可以采用热分解法,即通过加热 制得,②项正确;
③用电解法冶炼铝时,氯化铝为共价化合物,不用其作原料,原料是氧化铝,③项错误;
④高炉炼铁中利用焦炭与氧气反应生成二氧化碳,二氧化碳再与焦炭反应生成一氧化碳,利用生成的一氧
化碳将铁矿石还原为铁单质,④项错误;
⑤工业上可以用铝热反应来冶炼某些熔点较高的金属,如铬、锰,⑤项正确;
综上错误的为③④,答案选A。
6.(2021·重庆·高一阶段练习)下列关于金属冶炼的说法正确的是
A.利用该铝热反应 炼铁,1mol氧化剂参加反应转移8N 个电子
A
B.金属的冶炼都是把金属单质从其矿物中分离出来
C.工业上可用电解熔融态的 来制备Mg、Al
D.古代火烧孔雀石炼铜的方法属于热分解法中的焦炭法
【答案】A
【解析】A.利用该铝热反应 炼铁,反应中氧化剂是Fe O,反应中转移了24
3 4
个电子,故1 mol氧化剂参加反应转移8N 个电子,A符合题意;
A
B.大多数金属的冶炼都是利用还原剂或者通电把金属从其化合物中还原出来,只有少数不活泼金属如
Pt、Au等单质能直接从其矿物中分离出来,B不合题意;
C.工业上可用电解熔融态的MgCl 和Al O 来制备Mg、Al,反应为 Mg+Cl 、
2 2 3 2
,C不合题意;D.古代火烧孔雀石炼铜的方法反应为: , ,故
属于热还原法中的焦炭法,D不合题意;故选A。
7.(2021·全国·高一期末)工业上制备下列物质的生产流程合理的是
A.由铝士矿冶炼铝:铝土矿 Al O A1Cl Al
2 3 3
B.从海水中提取镁:海水 Mg(OH) MgO Mg
2
C.由NaCl制漂白粉:饱和食盐水 Cl 漂白粉
2
D.由黄铁矿制硫酸:黄铁矿 SO SO HSO
2 3 2 4
【答案】D
【解析】A.氯化铝是共价化合物,熔融氯化铝不导电,不能电解氯化铝制备金属铝,工业上一般电解氧
化铝冶炼金属铝,故A不合理;
B.工业上一般用电解熔融氯化镁的方法冶炼金属镁,故B不合理;
C.工业上用氯气和石灰乳反应制备漂白粉,故C不合理;
D.工业上灼烧黄铁矿生成二氧化硫,二氧化硫发生催化氧化生成三氧化硫,三氧化硫用浓硫酸吸收生成
硫酸,故D合理;
选D。
8.(2021·浙江·金华市方格外国语学校高一阶段练习)铝土矿主要成分为Al O,主要杂质为Fe O、
2 3 2 3
SiO,某实验小组设计了如图流程制备铝:
2
下列说法不正确的是
A.步骤①过滤得到的滤渣主要为SiO
2
B.步骤②的沉淀剂可以选用NaOH、氨水或Ca(OH) ,考虑成本,Ca(OH) 最合适
2 2
C.步骤④加入冰晶石的目的是降低Al O 熔融的温度,降低能耗
2 3
D.该方案的缺陷在于未能很好的将Fe O 杂质除去
2 3
【答案】B
【解析】A.二氧化硅不溶于HCl,故步骤①得到的滤渣为二氧化硅,A正确;
B.步骤②的沉淀剂应选用弱碱,否则生成的氢氧化铝会溶于强碱,B错误;C.加入冰晶石可降低三氧化二铝熔融的温度,降低能耗,C正确;
D.在步骤②时得到的沉淀有氢氧化铝和氢氧化铁,故灼烧会得到三氧化二铁,D正确;
答案选B。
9.(2021·广东广州·高一期末)以高硫铝土矿(主要成分为 、 ,少量 等)为原料,生产氧化
铝并获得 的部分工艺流程如下:
(1)为了提高第一次焙烧后的烧渣在碱浸时的溶出速率,可采取的有效措施为_______、_______。(任写两
点)。
(2)已知:①第一次焙烧的主要目的是脱硫(降低矿粉中硫化物型硫的含量),以免影响产品 的质量;
②此过程中 与氧气发生了氧化还原反应: 。第一次焙烧结束后,硫最终
主要以_______(填物质的化学式)的形式存在。
(3)碱浸时发生的主要反应的离子方程式为_______。
(4)第二次焙烧过程中产生了污染性气体 ,工业生产中可选用以下哪些溶液除去 _______(填选项字
母)。
A.澄清石灰水B.品红溶液C.石灰乳D.NaOH溶液
(5)纯度检验:将少量磁选后的产品溶于稀硫酸中,再滴入酸性 溶液,若酸性 褪色,
_______(填“能”或“不能”)说明产品中含有 ,理由是_______。
(6)第二次焙烧是在缺氧的条件下进行的,此步骤发生的主要反应的化学反应方程式为_______。
【答案】(1)将烧渣粉碎、加热、搅拌 增大 的浓度
(2)(3)
(4) C、D
(5)不能 和稀硫酸反应会生成 和 ,生成的 能让酸性高锰酸钾褪色
(6)
【解析】(1)提高碱浸时的溶出速率,可采取将烧渣粉碎、加热、搅拌等,增大 的浓度;
(2)第一次焙烧是二氧化硫和氧化钙反应生成了亚硫酸钙,亚硫酸钙又被氧气氧化为硫酸钙;
(3)碱浸时,氧化铝与氢氧化钠反应 ;
(4)A澄清石灰水吸收 的量较少,不选;B品红可用于检验 ,吸收不充分,故不选;C石灰乳可以
吸收 ,故选;D氢氧化钠溶液可以吸收 ,故选;故选CD;
(5) 中有 的检验方法: 和稀硫酸反应会生成 和 ,生成的 能让酸性高锰酸钾褪色;
(6)在缺氧的条件下,FeS 生成Fe O 的化学方程式为 。
2 3 4
10.(2021·河北·曹妃甸一中高一阶段练习)下图所示是从铝土矿(主要成分是 ,含 、 等杂
质)中提取氧化铝的工艺流程之一。已知: 能和氢氧化钠反应,不和盐酸反应。
回答下列问题:
(1)用盐酸溶解铝土矿后,所得溶液中的阳离子有_______。
(2)固体 的主要成分是_______。
(3)进行步骤Ⅱ时,为了达到分离要求,加入的 应过量。进行步骤Ⅲ时,一般通入过量 ,其反应
的化学方程式是_______。(4)溶液 和盐酸反应的离子方程式为_______。
【答案】(1) 、 、
(2)
(3)
(4)
【解析】(1)用盐酸溶解铝土矿后,所得溶液中的阳离子有: 、 、 ;
(2)固体 的主要成分是: ;
(3)进行操作Ⅱ时,为了达到分离要求,为除尽铁离子,故加入的 应该过量,得到偏铝酸钠溶液,通
入过量 ,其反应的化学方程式是 ;
(4)溶液 为碳酸氢钠和盐酸反应生成氯化钠、二氧化碳、水,离子方程式为: 。
11.(2021·四川仁寿·高一阶段练习)铝土矿(主要成分为Al O,还含有SiO、Fe O)是工业上制备金属铝
2 3 2 2 3
的主要原料。工业上提取铝的工艺流程如下:
(1)沉淀A的化学式是_______,试剂a的化学式为_______。
(2)步骤③中通入过量CO,产生沉淀C的离子方程式为_______
2
(3)步骤③中通入过量CO 气体而不加入过量盐酸的理由是_______
2
(4)AlO 中所含的化学键的类型为_______
2 3
(5)在生活中,常利用Al与Fe O 间的铝热反应来进行焊接钢轨。除了Fe O,铝粉还可以与很多金属氧化
2 3 2 3
物组成铝热剂。下列氧化物中不能与铝粉组成铝热剂的是_______。
a.MgO b.ZnO c.Fe O d.Na O
3 4 2
(6)准确称取8g铝土矿样品,加入过量的稀盐酸充分反应,过滤,然后,向滤液中加入10mol·L-1的NaOH溶液,产生沉淀的质量与加入NaOH溶液的体积关系如图所示,则样品中Al O 的百分含量为___。
2 3
【答案】(1)SiO NaOH
2
(2)
(3) 过量盐酸能使生成的Al(OH) 溶解
3
(4) 离子键
(5) ad
(6) 51%
【解析】铝土矿主要成分为Al O,还含有SiO、Fe O,用盐酸溶解,SiO 和盐酸不反应,Al O、Fe O
2 3 2 2 3 2 2 3 2 3
与盐酸反应生成AlCl 、FeCl ,过滤分离,沉淀A为SiO,滤液甲含有AlCl 、FeCl 及过量的HCl,步骤
3 3 2 3 3
③通入的为二氧化碳得到Al(OH) 与NaHCO ,则滤液乙含有AlO-,步骤②应加入NaOH,除去Fe3+离
3 3 2
子,将Al3+离子转化为AlO-,加热氢氧化铝分解得到氧化铝,电解氧化铝得到Al。
2
(1) 由分析可知,沉淀A是不溶于盐酸的SiO;试剂a是氢氧化钠,故答案为:SiO;NaOH
2 2
(2) 溶液中过量的二氧化碳与AlO−2反应生成的沉淀为氢氧化铝、碳酸氢根,反应离子方程式为:
,
故答案为: ;
(3) 过量盐酸能使生成的Al(OH) 溶解,而碳酸不能溶解,故通入过量的二氧化碳,而不是加入过量的盐酸,
3
故答案为:过量盐酸能使生成的Al(OH) 溶解;
3
(4) Al O 属于离子晶体,含有离子键,故答案为:离子键;
2 3
(5) 铝热反应本质是置换反应,铝热剂中氧化物应是不如Al活泼的金属氧化物,故选项中MgO、NaO不
2
能与Al组成铝热剂,故答案为:ad;
(6)37-45ml阶段是NaOH溶液是溶解Al(OH) ,消耗NaOH物质的量为:
3
,Al(OH) +NaOH=NaAlO +2H O,可知Al(OH) 为0.08mol,根据Al
3 2 2 3原子守恒:n(AlO)= n[Al(OH) ]=0.04mol,故m(Al O)=0.04mol×102g/mol=4.08g,氧化铝质量分数
2 3 3 2 3
=(4.08g÷8g)×100%=51%,
故答案为:51%。
12.(2021·福建·厦门双十中学高一期中)除金、铂等极少数金属外,绝大多数金属元素以化合物形式存
在于自然界中,将金属元素从其化合物中还原出来的工业工程称为金属的冶炼。下列材料描述了部分常见
金属的冶炼方法。
①工业上冶炼镁的方法有两种,电解法和皮江法。电解法是电解熔融的氯化镁;皮江法是硅在高温下还原
氧化镁。
②霍尔-埃鲁铝电解法是以氧化铝为原料、冰晶石(Na AlF)为熔剂组成的电解质,在950-970℃的条件下通
3 6
过电解的方法使电解质熔体中的氧化铝分解为铝和氧气。
③冶炼锰一般用铝热法,即在高温下用铝还原二氧化锰。
④相关各物质熔点见下表:
物质 Al O AlCl MgO MgCl Al Mn Mg
2 3 3 2
熔点/℃ 2303 190 2800 712 660 1244 649
Ⅰ.根据上述信息回答下列问题:
(1)冶炼镁时电解熔融MgCl 而不电解熔融MgO的原因是_______
2
(2)将铝和镁作电极插入稀硫酸中,镁、铝分别作_______极、_______极;写出正极的电极反应式:
_______。
Ⅱ.下面是皮江法冶炼镁的工业流程示意图:
(3)气体a是_______。
(4)还原炉需控制温度为1200℃左右,并抽空气到近似真空。还原炉中发生的主要反应有_______、_______。
(5)还原炉中抽空气到近似真空的原因是_______。
【答案】(1)MgO的熔点比MgCl 更高,电解时需要更多的能量,故选用MgCl
2 2
(2)负 正 2H++2e-=H ↑
2
(3)CO
2(4) 2MgO+Si 2Mg↑+SiO SiO +CaO CaSiO
2 2 3
(5)防止已还原的Mg在高温条件下再次被氧化
【解析】(1)冶炼镁时通常采用电解熔融MgCl 的方法而不是电解熔融MgO,是由于MgCl 的熔点比MgO
2 2
低,电解时消耗的能量少,若采用电解熔融的MgO,就需消耗更多的能量;
(2)Mg、Al都是比较活泼的金属,能够与硫酸发生置换反应,由于金属活动性:Mg>Al,所以若将铝和镁
作电极插入稀硫酸中,活动性比较强的镁为负极,活动性比较弱的铝为正极,在负极上Mg失去电子变为
Mg2+进入溶液,在正极上,溶液中的H+得到电子变为H 逸出,故正极的电极反应式为:2H++2e-=H ↑;
2 2
(3)白云石在高温下煅烧,反应产生CaO、MgO和CO 气体,所以气体a是CO;
2 2
(4)将回转炉煅烧产生的固体CaO、MgO与硅铁混合、粉碎研磨,并压制成球状,然后在1200℃高温条件
下,抽成真空,发生主要反应是:2MgO+Si 2Mg↑+SiO,SiO+CaO CaSiO ;
2 2 3
(5)Mg是活泼金属,在高温下能够与O 反应产生MgO,在还原炉中抽空气到近似真空,就可以防止已还原
2
的Mg在高温条件下再次被氧化。
题组二 海水资源的开发利用
1.(2021·四川·树德中学高一期中)已知苯的密度为0.81g/cm3; 。从海带中提取碘的
实验过程如下:
以上过程中,涉及到下列操作的示意图,其中正确的是
A.①将海带灼烧成灰 B.②过滤得含 的溶液C.③碘的苯溶液从下层放出 D.④分离碘并回收苯
【答案】D
【解析】A.灼烧在坩埚中进行,不能在烧杯中灼烧,故A错误;
B.过滤需要玻璃棒引流,图中缺少玻璃棒,故B错误;
C.苯的密度比水的密度小,分层后在上层,应从分液漏斗的上口倒出,故C错误;
D.碘与苯互溶,沸点不同,图中装置可分离碘并回收苯,故D正确;
故选:D。
2.(2021·江苏东海·高一期中)某工厂对海水提纯后的母液(苦卤)进行再次资源综合开发利用的部分工艺
流程如下图所示。下列说法不正确的是
A.步骤①中可用热空气对 进行富集
B.可以用 溶液除去工业 中微量的
C.工业上可通过电解 溶液的方法获得镁单质
D.步骤②通入 可制得 ,说明 的氧化性大于
【答案】C
【解析】A. 易挥发,可用热空气吹出 进行富集,A正确;
B. 可与Br-反应得到 ,符合除杂的原则,B正确;
C.工业上可通过电解熔融 的方法获得镁单质,而不是 溶液,C错误;
D.氧化剂的氧化性大于氧化产物的氧化性,通入 可制得 ,则氧化性: > ,D正确;
故选C。
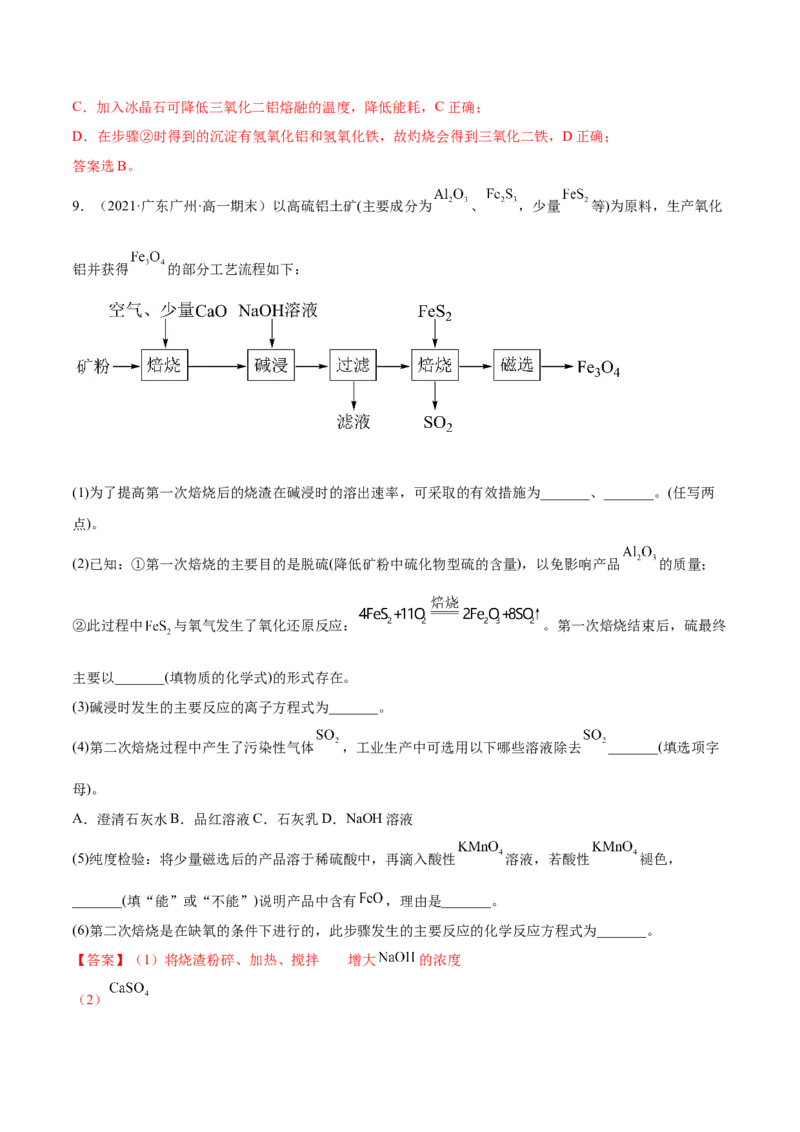
3.(2021·广东·佛山市南海区桂城中学高一阶段练习)海水开发利用的部分过程如图所示。下列说法错误的是
A.粗盐可采用溶解过滤和重结晶等过程提纯
B.向苦卤中通入Cl 是为了提取溴
2
C.实际生产常选用Ca(OH) 作为沉淀剂
2
D.工业生产中电解氯化镁溶液的方法制取镁
【答案】D
【解析】A.粗盐中含泥沙、钙离子、镁离子、硫酸根离子等,可过滤除去泥沙,加试剂沉淀杂质离子后
过滤、蒸发结晶提纯NaCl,A正确;
B.苦卤中含溴离子,通入Cl 是为了提取溴, B正确;
2
C.工业生产中常选用石灰乳作为沉淀剂,便宜易得,C正确;
D.工业生产中电解熔融的氯化镁的方法制取镁,MgCl (熔融) Mg+Cl ↑,而电解氯化镁溶液得不到
2 2
Mg,MgCl +2H O Mg(OH) ↓+Cl↑+H ↑,D错误;
2 2 2 2 2
故答案为:D。
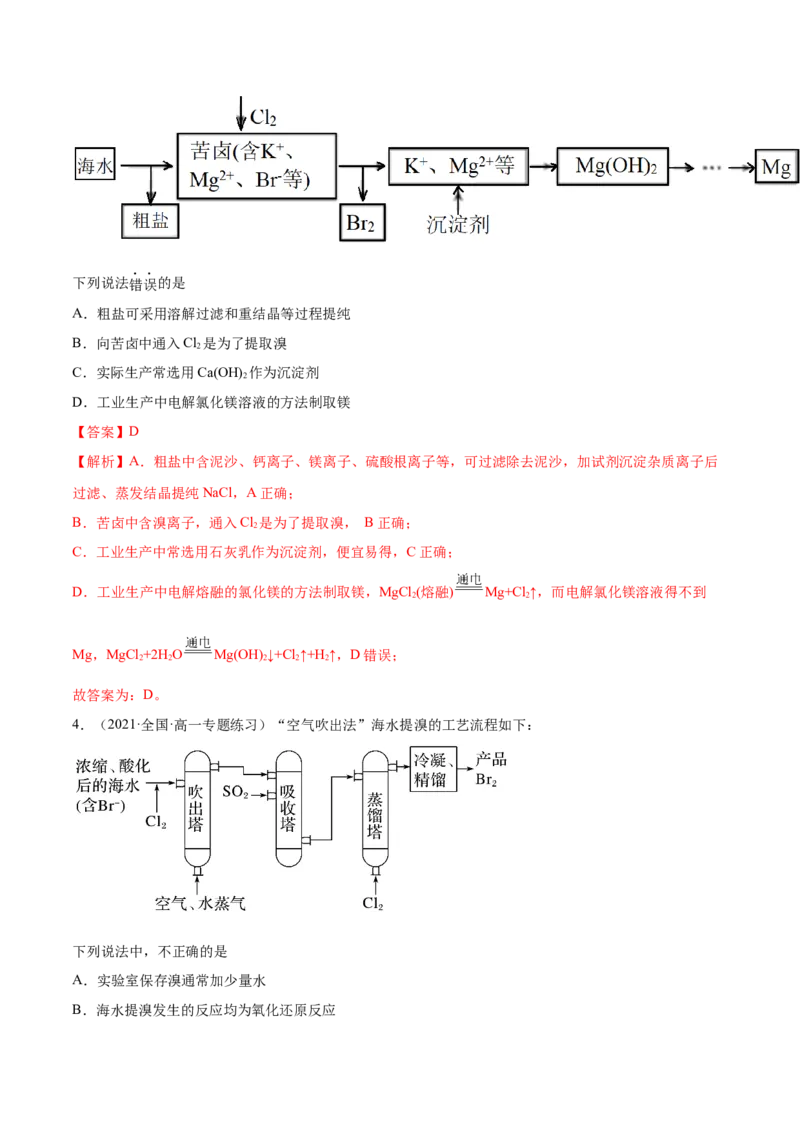
4.(2021·全国·高一专题练习)“空气吹出法”海水提溴的工艺流程如下:
下列说法中,不正确的是
A.实验室保存溴通常加少量水
B.海水提溴发生的反应均为氧化还原反应C.经过吸收塔后,溴元素得到了富集
D.蒸馏塔中只发生了物理变化
【答案】D
【解析】A.溴易挥发,加水液封可以减少挥发损失,A正确;
B.海水提溴的过程中,均存在元素化合价的变化,均为氧化还原反应,B正确;
C.经过吸收塔后,所得溶液中的Br-浓度远大于进入吹出塔之前的海水中的Br-浓度,因此溴元素得到了富
集,C正确;
D.蒸馏塔中发生了化学反应为:2Br-+Cl=2Cl-+Br ,D错误;
2 2
答案选D。
5.(2021·天津静海·高一阶段练习)空气吹出法是目前海水提溴最成熟的工业方法,部分工艺流程如下:
下列说法错误的是
A.步骤②利用了溴易挥发的性质 B.溶液中Br 的浓度:I