文档内容
第八章 化学与可持续发展
第一节 自然资源的开发利用
第二课时 海水资源的开发利用
【学习目标】1.通过阅读理解、原理分析,了解海水资源的利用方法和从海水中获得化学物质(如氯
化钠、溴、金属镁、氢氧化钠、氯气)的方法,初步认识海水资源的广泛性和多样性。
2.通过讨论交流,原理分析,认识海水提溴工艺流程图的设计与分析,形成工业上提取物质的一般思
路和方法,培养模型认知和证据推理的能力。
3.通过思考交流,问题探究,能从化学的角度分析从自然资源到产品的转化途径,认识化学方法在实
现物质转化中的作用和贡献,感受化学科学在生产、生活中的应用价值。
【学习重点】海水提溴的工艺流程、原理和分离提纯方法
【学习难点】理解海水提溴的流程与原理
【课前预习】
旧知回顾:1.蒸馏实验的原理及所需主要仪器是什么?
【答案要点】蒸馏的原理是 利用液体混合物中各组分挥发度(沸点)的差别,使液体混合物部分成分
汽化并随之使蒸气部分冷凝,从而实现其所含组分的分离的方法 ;蒸馏实验的主要仪器名称为 蒸馏烧瓶、
酒精灯、温度计、冷凝管(含尾接管)、锥形瓶、铁架台等 。
2.合理开发和利用金属资源的主要途径主要有哪些?
【答案要点】①提高金属矿物的利用率;②开发环保高效的金属冶炼方法;③防止金属的腐蚀;④加
强废旧金属的回收和再利用;⑤使用其他材料代替金属材料,减少金属的使用量。
新知预习:1.海水资源的利用主要包括哪些内容?
【答案要点】①海水的淡化:通过从海水中提取淡水或从海水中把盐分离出去,都可以达到淡化海水
的目的。
②海水制盐:从海水中制得的氯化钠,可以食用,同时也是生产烧碱、纯碱、钠、氯气、盐酸的工业
原料。
③从海水中可以提取镁、钾、溴及其他化工产品。
④从海水中获取能量:从海水中提取铀和重水,用于核能开发;开发潮汐能、波浪能等新型能源等。
2.海水淡化有哪些主要的方法?
【答案要点】海水淡化的方法主要有 蒸馏法、电渗析法、离子交换法 等。其中 蒸馏法 的历史最
久,技术和工艺也比较成熟,但成本较高。因此,海水淡化与化工生产结合、与能源技术结合,成为海水
综合利用的重要方向。
【课中探究】
情景导入:地球表面海洋面积占到71%,海洋是人类千万年来取之不尽、用之不竭的巨大资源宝库。
其中的水资源和其他化学资源具有十分巨大的开发潜力。(视频见PPT)
一、海水水资源的利用活动一、认识海水水资源的利用方法
任务一、查阅资料,阅读教材P100页第一、二自然段,结合教材P100页图8-3,思考从海洋资源的
性质、特点、存在形态等方面分析,海洋资源有哪些类型?
【答案要点】按照海洋资源的性质、特点、存在形态,将海洋资源分为 6个大类:
①海洋生物资源(包括渔业资源、药物资源、珍稀物种资源);
②海底矿产资源(包括金属矿产资源、非金属矿产资源、石油和天然气资源);
③海洋空间资源(包括土地资源、港口和交通资源、环境空间资源);
④海水资源(包括盐业资源、溶存的化学资源、水资源);
⑤海洋新能源(包括潮汐能资源、波浪能资源、海流能资源、温差和盐差能资源、海上风能资源);
⑥海洋旅游资源(包括海洋自然景观旅游资源、娱乐和运动旅游资源、人类海洋历史遗迹旅游资源、
海洋科学旅游资源、海洋自然保护区旅游资源)。
注意:海水中水的储量约为1.3×1018 t,约占地球上总水量的97%。海水水资源的利用,主要包括
海水淡化和直接利用海水进行循环冷却等。
任务二、讨论交流:海水水资源的利用主要包括哪些方面?海水淡化有哪些主要的方法?
【答案要点】①海水中水资源的利用,主要包括海水的淡化和直接利用海水进行循环冷却。如用作工
业冷却用水、部分生活用水和耐盐植物灌溉用水等。
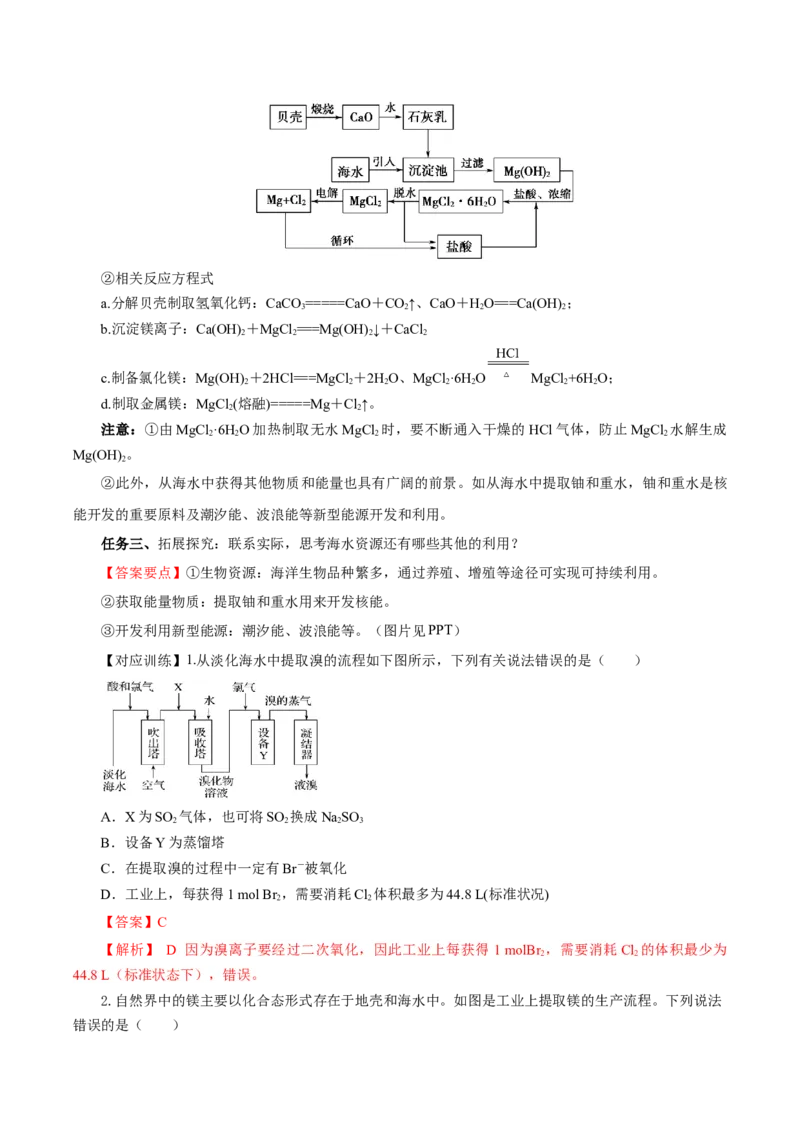
②从海水中取得淡水的过程叫海水的淡化。现在所用的海水淡化方法有海水冻结法、电渗析法、蒸馏
法、反渗透法、以及可实现盈利的碳酸铵离子交换法,目前应用反渗透膜的反渗透法以其设备简单、易于
维护和设备模块化的优点迅速占领市场,逐步取代蒸馏法成为应用最广泛的方法。
【对应训练】1.关于海水资源的综合利用,下列说法错误的是( )
A.海水中含量最高的盐是NaCl
B.电解饱和食盐水可以制得金属钠
C.从海水中提取的镁可用于制造火箭、飞机D.食用含碘丰富的海产品可防治甲状腺肿大
【答案】B
【解析】A项,海水中含量最多的金属元素是Na,其次是Mg,含量最多的非金属是Cl,所以海水中
含量最高的盐是NaCl,说法正确;B项,电解饱和食盐水可以制得NaOH、氢气和氯气,不能得到Na,说
法错误;C项,从海水中提取的镁,制造的镁铝合金具有硬度大,质量轻的特点,可用于制造火箭、飞
机,说法正确;D项,碘是合成甲状腺激素的重要物质,食用含碘丰富的海产品可防治甲状腺肿大,说法
正确。
2.水资源是发展国民经济不可缺少的重要自然资源。在世界许多地方,对水的需求已经超过水资源所
能负荷的程度,同时有许多地区也存在水资源利用不平衡。下列关于水的说法错误的是( )
A.蒸馏法是海水淡化的方法之一
B.淡水的密度小于海水的密度
C.融化的雪水中矿物质含量比深井水中的少
D.0℃以上,温度越高,水的密度越小
【答案】D
【解析】海水中溶有Na+、Mg2+、Cl-和SO等,这些离子所组成的物质的沸点比水的沸点高,可用
蒸馏法将其分离,A正确;上述杂质的溶入使水溶液的密度增大,B正确;雪和雨水成分相同,是水蒸发
形成的水蒸气凝结而成的,含矿物质很少,而深井中的水不断地与硅酸盐矿物质接触,其中溶有许多矿物
质,C正确;由于水在4℃时密度最大,故D错误。
活动二、探究海水的蒸馏
任务一、结合蒸馏实验原理,思考如何进行海水的蒸馏?
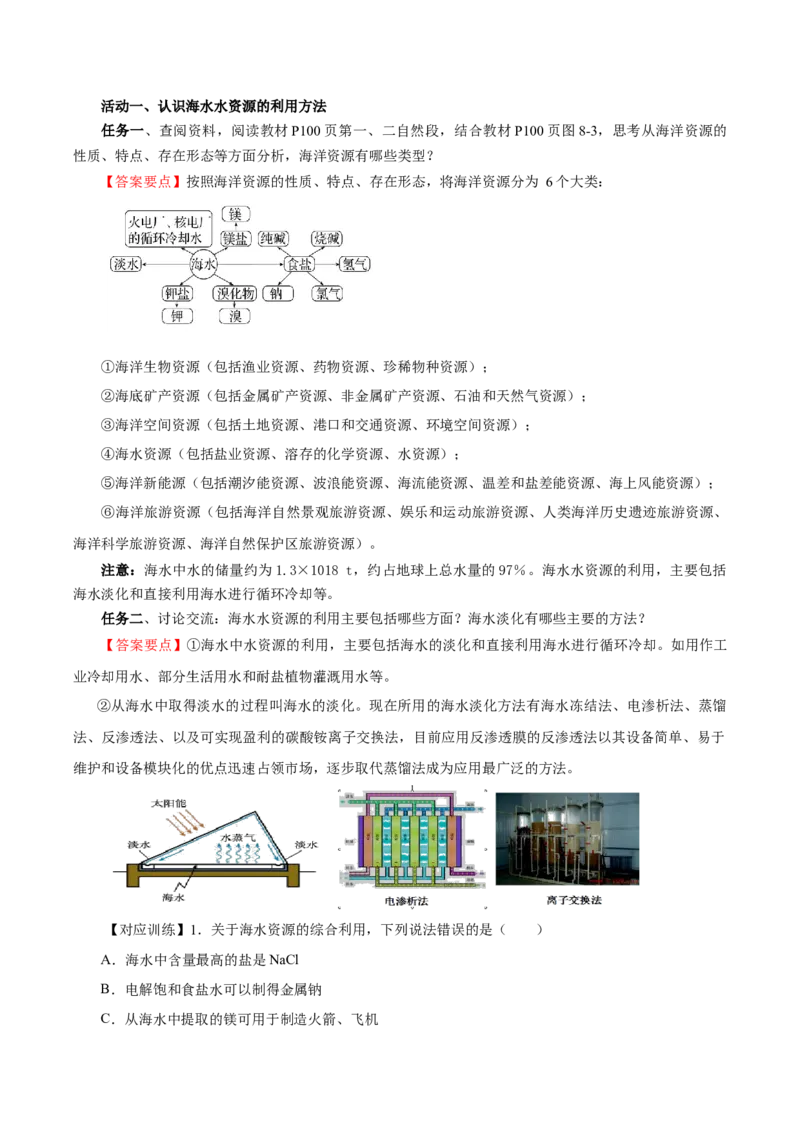
【答案要点】①实验原理及装置:
②实验的操作步骤:连接装置→检查装置气密性→向烧瓶中加入海水和碎瓷片→接通冷却水→给烧瓶
加热→收集蒸馏水→停止对烧瓶加热→待冷却至室温后停止通入冷却水→整理仪器。
③注意事项:A.烧瓶需垫石棉网加热;B.烧瓶所盛液体不能超过烧瓶容积的,也不能少于;C.需向烧
瓶中加几粒沸石或几片碎瓷片,以防液体暴沸;D.冷凝器里的冷却水要从冷凝器的下口进、上口出。
任务二、问题探究:海水的蒸馏装置与普通的蒸馏装置有何区别?蒸馏法淡化海水有何优缺点?海水
淡化的前景如何?
【答案要点】①因为海水蒸馏得到的是淡水,水的沸点为 100 ℃(常压下)无需用温度计,因此可不用
蒸馏烧瓶,而换为圆底烧瓶。
②蒸馏法的历史最久,技术和工艺也比较成熟,但耗能大、成本较高,是目前海水淡化的主要方法。③海水淡化与化工生产结合、与能源技术结合,成为海水综合利用的重要方向。如:将发电厂等企业
的工业余热用于海水淡化是一种经济合理的途径。
【对应训练】1.下列有关水的说法不正确的是( )
A.静置沉淀、吸附沉淀、过滤、蒸馏净化水的程度由低到高
B.用活性炭可以吸附水中的色素和异味
C.电解水实验中正极产生的氧气,负极产生的氢气,二者的质量比是 1:2
D.水是生命之源,爱护水资源包括防止水体污染和节约用水两方面
【答案】C。
【解析】A、静置沉淀、吸附沉淀、过滤、蒸馏净化水的程度由低到高,该选项正确。B、用活性炭可
以吸附水中的色素和异味,该选项正确。C、电解水实验中正极产生的氧气,负极产生的氢气,二者的质
量比是 8:1,该选项不正确。D、水是生命之源,爱护水资源包括防止水体污染和节约用水两方面,该选
项正确。故选:C。
2.化学在人类社会的可持续发展中发挥着重要作用,下列说法不正确的是( )
A.工业上常用加热分解的方法冶炼不活泼金属
B.海水淡化的方法有蒸馏法、渗析法和离子交换法
C.“原子经济性反应”就是反应物的原子全部转化为期望的最终产物
D.不合理施用化肥会影响土壤的酸碱性和土壤结构
【答案】B
【解析】A.制取不活泼的金属,如金属汞,银等,工业上一般加热金属氧化物使其分解成金属单质
和氧气,A项正确;B.海水淡化的方法有蒸馏法、电渗析法和离子交换法,B项错误;C.绿色化学中最
理想的原子经济性反应是反应物的原子全部转化为希望的产物,C项正确;D.化肥需要合理使用,如果
不合理施用化肥会影响土壤的酸碱性和土壤结构,D项正确;答案选B。
二、海水化学资源的开发利用
活动一、认识海水化学资源的特点
任务一、阅读教材P100页第三自然段,结合“资料卡片”栏目,思考海水化学资源有何特点?
【答案要点】①多样性:海水中溶解和悬浮着大量的有机物和无机物,包括常量元素 H、O 、Cl、
Na、Mg、S、Ca、K、Br、C、Sr、B 、F 等13种(超过总量的 99%),其中含量最高的是 Cl占
55.06%,其次Na是占30.62%。其余微量元素元素,总计含有80多种元素。(各元素含量见PPT)
②分散性:海水中含有元素的种类多、总储量很大,但许多元素的富集程度很低。这是从海水中提取
物质需要解决的问题。
任务二、讨论交流:结合教材P100页图8-3,思考如何从海水中提取食盐?以食盐为原料可以制备哪
些物质?
【答案要点】①从海水中提取食盐的方法是盐田法(又叫滩晒法),其原理是把海水引到盐滩上,利用
日光和风力使水分蒸发,得到食盐;盐田法历史最悠久,而且也是最简便和经济有效的方法,现在还在广泛采用 。
②食盐用途广泛,除了供食用外,还作为化工原料用于生产烧碱、纯碱、钠、氯气、盐酸等。
a.氯碱工业:2NaCl+2HO=====2NaOH+H↑+Cl↑。
2 2 2
b.制钠和氯气:2NaCl(熔融)=====2Na+Cl↑。
2
c.制盐酸:H+Cl=====2HCl。
2 2
d.制漂白液:Cl+2NaOH===NaCl+NaClO+HO。
2 2
e.制漂白粉:2Cl+2Ca(OH) ===CaCl +Ca(ClO) +2HO。
2 2 2 2 2
【对应训练】1.“关注海洋健康,守护蔚蓝星球”,我们每个公民义不容辞。下列有关说法不正确
的是( )
A.可通过蒸馏法、电渗析法、离子交换法从海水中获得淡水
B.地球上99%的溴元素存在于海洋中,故溴称为“海洋元素”
C.从海水中提取的NaCl可进一步用于生产NaOH
D.海水只能提供物质资源,不能提供能量资源
【答案】D
【解析】A.海水中含有丰富的资源,从海水中得到淡水的方法有蒸馏法、电渗析法、离子交换法,
故A正确;B.地球上99%的溴元素存在于海水中,所以人们也把溴称为“海洋元素”,故B正确;C.
从海水中能提取氯化钠,电解饱和氯化钠溶液可以制得氢氧化钠,故C正确;D.海洋资源指的是与海水
水体及海底、海面本身有着直接关系的物质和能量,海水既能提供物质资源,也能提供能量资源,如波
浪、潮汐、潮流等会产生能量,故D错误;故选D。
2.除去粗盐中的杂质MgCl 、CaCl 和NaSO ,过程如下:
2 2 2 4
下列有关说法中,不正确的是( )
A.试剂①②③依次加入过量的NaCO、NaOH、BaCl 溶液
2 3 2
B.溶解、过滤都用到玻璃棒,其作用搅拌,加速溶解:引流
C.除去Ca2+的主要反应:Ca2++CO=CaCO ↓
3
D.向滤液中加入盐酸是为了除去过量的氢氧化钠和碳酸钠【答案】A
【解析】由实验流程可知,粗盐溶解后,先加NaOH除去MgCl ,再加BaCl 除去NaSO ,然后加
2 2 2 4
NaCO 除去CaCl 及过量的BaCl ,且NaCO 一定在BaCl2之后,过滤后,滤液中加浓盐酸,最后蒸发结
2 3 2 2 2 3
晶得到NaCl固体,以此来解答。A.碳酸钠一定在氯化钡之后,可除去过量的钡离子,则试剂①、②、③
分别是NaOH、BaCl 、NaCO,或BaCl 、NaOH、NaCO,故A错误;B.溶解、过滤都用到玻璃棒,其
2 2 3 2 2 3
作用是:搅拌,加速溶解;引流,故B正确;C.加NaCO 除去CaCl ,则除去Ca2+的主要反应:Ca2+
2 3 2
+CO=CaCO ↓,故C正确;D.加入的除杂试剂都是过量的,向滤液中加入盐酸是为了除去过量的氢氧化
3
钠和碳酸钠,故D正确;故选A。
活动二、海水中溴、镁等其他化学资源的开发利用
任务一、讨论交流:根据教材P101页“思考与讨论”栏目,结合图8-4分析、思考如何从海水中提取
溴?
【答案要点】工业规模提取溴的常用方法是空气吹出法,工艺流程为:
①浓缩:海水晒盐和海水淡化过程中的副产物Br-得到浓缩。
②氧化:向酸化的浓缩海水中通入适量的氯气,使溴离子转化为溴单质,化学方程式为 2NaBr+
Cl===2NaCl+Br 。
2 2
③富集(吹出与吸收):向含溴单质的水溶液中通入空气和水蒸气,将溴单质吹入盛有二氧化硫溶液
的吸收塔内以达到富集的目的,化学方程式为Br +SO +2HO===2HBr+HSO 。
2 2 2 2 4
④提取(蒸馏):向吸收塔内的溶液中通入适量的氯气将氢溴酸氧化为溴后蒸馏分离),化学方程式
为2HBr+Cl===2HCl+Br 。
2 2
注意:空气吹出法进行海水提取溴时,常用纯碱溶液代替二氧化硫溶液来吸收单质溴:
3Br +3NaCO===NaBrO+5NaBr+3CO↑;
2 2 3 3 2
然后用硫酸酸化,即可得到产品溴:NaBrO +5NaBr+3HSO ===3Br +3NaSO +3HO。
3 2 4 2 2 4 2
任务二、问题探究:海水中的镁元素主要以可溶性的镁盐操作,思考如何从海水中提取镁?
【答案要点】①工艺流程:②相关反应方程式
a.分解贝壳制取氢氧化钙:CaCO =====CaO+CO↑、CaO+HO===Ca(OH) ;
3 2 2 2
b.沉淀镁离子:Ca(OH) +MgCl ===Mg(OH) ↓+CaCl
2 2 2 2
c.制备氯化镁:Mg(OH) +2HCl===MgCl +2HO、MgCl ·6H O MgCl +6H O;
2 2 2 2 2 2 2
d.制取金属镁:MgCl (熔融)=====Mg+Cl↑。
2 2
注意:①由MgCl ·6H O加热制取无水MgCl 时,要不断通入干燥的HCl气体,防止MgCl 水解生成
2 2 2 2
Mg(OH) 。
2
②此外,从海水中获得其他物质和能量也具有广阔的前景。如从海水中提取铀和重水,铀和重水是核
能开发的重要原料及潮汐能、波浪能等新型能源开发和利用。
任务三、拓展探究:联系实际,思考海水资源还有哪些其他的利用?
【答案要点】①生物资源:海洋生物品种繁多,通过养殖、增殖等途径可实现可持续利用。
②获取能量物质:提取铀和重水用来开发核能。
③开发利用新型能源:潮汐能、波浪能等。(图片见PPT)
【对应训练】1.从淡化海水中提取溴的流程如下图所示,下列有关说法错误的是( )
A.X为SO 气体,也可将SO 换成NaSO
2 2 2 3
B.设备Y为蒸馏塔
C.在提取溴的过程中一定有Br-被氧化
D.工业上,每获得1 mol Br ,需要消耗Cl 体积最多为44.8 L(标准状况)
2 2
【答案】C
【解析】 D 因为溴离子要经过二次氧化,因此工业上每获得 1 molBr ,需要消耗Cl 的体积最少为
2 2
44.8 L(标准状态下),错误。
2.自然界中的镁主要以化合态形式存在于地壳和海水中。如图是工业上提取镁的生产流程。下列说法
错误的是( )A.煅烧贝壳得到生石灰,该反应为氧化还原反应
B.先将海水中的镁沉淀,再转化为MgCl ,是为了提高溶液中镁离子的浓度
2
C.沉淀池中主要发生的反应为Ca(OH) +MgCl =Mg(OH) ↓+CaCl
2 2 2 2
D.工业上利用电解熔融氯化镁的方法制取镁的原因是氯化镁的熔点比氧化镁低得多
【答案】A
【解析】A.煅烧贝壳得到生石灰,化合价没有发生变化,因此该反应为非氧化还原反应,故A错
误;B.先将海水中的镁沉淀变为Mg(OH) ,再加入盐酸转化为MgCl ,是为了提高溶液中镁离子的浓
2 2
度,故B正确;C.沉淀池主要将镁离子沉淀,其主要发生的反应为Ca(OH) +MgCl =Mg(OH) ↓+CaCl ,故
2 2 2 2
C正确;D.工业上利用电解熔融氯化镁的方法制取镁,而不采用电解熔融氧化镁的原因是氯化镁的熔点
比氧化镁低得多,故D正确。综上所述,答案为A。
【课后巩固】1.下列有关工业生产的叙述不正确的是( )
A.用海水淡化后的浓缩海水作原料提取溴
B.在太阳能资源相对充足的沿海地区建造海水淡化厂
C.利用“海水→氯化钠→金属钠→氢氧化钠”的工艺流程生产烧碱
D.利用“海水→氢氧化镁→氯化镁→金属镁”的工艺流程生产金属镁
【答案】C
【解析】A.用海水淡化后的浓缩海水作原料提取溴;B.在太阳能资源相对充足的沿海地区建造海水淡
化厂;C.工业上通过电解饱和食盐水来生产烧碱,C错误;D.利用“海水→氢氧化镁→氯化镁→金属镁”
的工艺流程生产金属镁。
2.海水是一个巨大的化学资源宝库,下列有关海水综合利用的说法正确的是( )
A.海水中含有钾元素,只需经过物理变化就可以得到钾单质
B.海水蒸发制海盐的过程中只发生了化学变化
C.从海水中可以得到NaCl,电解熔融NaCl可制备Cl
2
D.利用潮汐发电是将化学能转化为电能
【答案】C
【解析】海水中的钾元素以化合态形式存在,要使化合态转化为游离态,一定发生氧化还原反应,A
不正确;海水蒸发制海盐,是发生了物理变化,B不正确;电解熔融NaCl可以制得Na和Cl,C正确;潮
2
汐发电是将机械能转化为电能,因此D也不正确。
3.一种工业制备无水氯化镁的工艺流程如下:下列说法错误的是( )
A.物质X常选用生石灰
B.工业上常月电解熔融MgCl 制备金属镁
2
C.氯化过程中发生的反应为:MgO+C+Cl====MgCl +CO
2 2
D.氯化过程中,生成95 g MgCl 时,理论上消耗22.4 L Cl
2 2
【答案】D
【解析】A项,物质X的作用是使镁离子转化为氢氧化镁沉淀,工业上常选用生石灰与水反应生成氢
氧化钙溶液沉镁,正确;B项,金属镁为活泼金属,工业上常用电解熔融MgCl 制备金属镁,正确;C
2
项,由流程图知,氯化过程中反应物为C、MgO、Cl,生成物为MgCl 、CO,故发生的反应为:MgO+C
2 2
+Cl====MgCl +CO,正确;D项,没有标明是否在标准状况下,无法算氯气的体积,错误。
2 2
4.空气吹出法是工业规模海水提溴的常用方法,流程如下:
下列说法不正确的是( )
A.获得工业Br 的方法是过滤
2
B.步骤②③的目的是富集溴元素
C.步骤①发生的主要反应为:Cl+2Br-=Br +2Cl-
2 2
D.步骤②发生的主要反应为:3Br +3NaCO=5NaBr+3CO+NaBrO
2 2 3 2 3
【答案】A
【解析】A项,利用溴的挥发性,空气吹出法是获得工业Br 的方法,错误;B项,步骤②③是使溴元
2
素浓度增大,目的是富集溴元素,正确;C项,步骤①是用氯气把溴离子氧化为溴单质,发生的主要反应
为:Cl+2Br-=Br +2Cl-,正确;D项,步骤②是溴和碳酸钠溶液反应生成溴化钠、硝酸镍、二氧化
2 2
碳,发生的主要反应为:3Br +3NaCO=5NaBr+3CO+NaBrO ,正确。
2 2 3 2 3
5.21世纪以来,国与国之间因对海洋权益的争夺引起的摩擦不断,在捍卫主权的同时,人们看重的
是海洋这个巨大的资源宝藏。下列对于海水利用的认识不正确的是( )
A.海水中蕴藏着丰富的铁、锰、钴等金属元素,这些物质可以大量开发,以弥补资源的短缺B.淡化海水的方法主要有蒸馏法、电渗析法、离子交换法
C.晒盐浓缩后得到的苦卤中含有浓度较高的溴离子,向苦卤中通入氯气,可以得到溴单质
D.从海水中可以提取食盐、溴、钾盐、镁及其化合物、铀、重水等
【答案】A
【解析】A.海底的资源非常丰富,蕴藏着丰富的铁、锰、钴等金属元素,在考虑资源、成本、环境
等因素的条件下,提倡合理开发这些物质,以弥补资源的短缺,故A错误;B.海水为盐和水的混合物,
可以利用蒸馏法、电渗析法、离子交换法等方法实现海水的淡化,故B正确;C.晒盐浓缩后得到的苦卤
中含有浓度较高的溴离子,向苦卤中通入氯气,氯气可以与苦卤中的溴离子发生置换反应得到溴单质,故
C正确;D.海水资源的利用主要是指从海水中可以提取食盐、溴、钾盐、镁及其化合物、铀、重水、卤
水等,故D正确;故选A。
6.海水综合利用的工艺流程如图所示(粗盐中的可溶性杂质有MgCl 、CaCl 、NaSO ),下列说法不正
2 2 2 4
确的是( )
A.过程①加入的药品顺序为NaCO 溶液→BaCl 溶液→NaOH溶液→过滤后加盐酸
2 3 2
B.过程②中所加的试剂是盐酸
C.过程④的离子方程式:SO +Br +2H O=SO +2Br-+4H+
2 2 2
D.在过程③或⑤反应中每氧化0.2molBr-需消耗标况下2.24LCl
2
【答案】A
【解析】A.Ca2+用碳酸钠除去,Mg2+用氢氧化钠除去,SO用氯化钡除去,最后加入盐酸酸化。但
用于过量的氯化钡要用碳酸钠来除,所以碳酸钠必需放在氯化钡的后面,而氢氧化钠可以随意调整,A错
误;B.氢氧化镁与盐酸反应生成氯化镁和水,所以过程②中所加的试剂是盐酸,B正确;C.过程④中二
氧化硫和溴反应生成硫酸和氢溴酸,离子方程式:SO +Br +2H O=SO+2Br-+4H+,C正确;D.在过程③或
2 2 2
⑤反应中均是溴离子被氧化为溴单质,根据电子转移守恒每氧化0.2molBr-需0.1mol氯气,标况下
2.24LCl ,D正确; 故选A。
2
7.海水化学资源开发利用中的提碘、提溴的部分过程如图所示。下列说法正确的是( )A.I中操作①用到的玻璃仪器只有烧杯、玻璃棒、胶头滴管
B.I中操作②的苯可用酒精代替
C.Ⅱ中SO 与Br 反应的化学方程式为:
2 2
D.Ⅱ中还原性:
【答案】C
【解析】A.I中操作①为过滤,缺少玻璃仪器漏斗,A错误;B. 酒精与水互溶,不能做萃取剂,I
中操作②的苯不可用酒精代替,B错误;C. Ⅱ中,水参与下,SO 与Br 反应生成硫酸和氢溴酸,化学方
2 2
程式为:SO +Br +2H O=HSO +2HBr,C正确;D.还原剂的还原性强于还原产物的还原性,Ⅱ中2Br-
2 2 2 2 4
+Cl=Br +2Cl-,Br-是还原剂、Cl-是还原产物,则还原性:Br->Cl-,又有反应:Br +SO+2H O=2Br-+4H+
2 2 2 2 2
+SO,二氧化硫是还原剂、Br-是还原产物,则还原性:SO >Br-,综上,还原性:SO >Br->Cl-,D错误;答
2 2
案选C。
8.大海中蕴藏着丰富的资源,部分化学资源获取途径如图:
(1)下列有关说法正确的是_____________________。
A.步骤Ⅰ中除去粗盐中的杂质离子Ca2+、Mg2+、SO ,加入试剂的先后顺序可以是BaCl 、
2
NaCO、NaOH
2 3
B.用澄清的石灰水可鉴别NaHCO 溶液和NaCO 溶液
3 2 3
C.在第Ⅱ、Ⅲ、Ⅳ步骤中,溴元素均被氧化
(2)步骤Ⅳ蒸馏过程中不可能用到的仪器有_______________________。
A.温度计 B.容量瓶 C.直形冷凝管 D.酒精灯
(3)步骤Ⅲ用SO 水溶液吸收Br ,吸收率可达95%,有关反应的化学方程式为
2 2
______________________。
(4)经过步骤Ⅱ已获得Br ,不直接用含Br 的稀溶液进行蒸馏,而要经过“空气吹出、SO 吸收、通
2 2 2
入氯气”后再蒸馏,其目的是____________________________________________________________。(5)根据流程中的反应可判断SO 、Cl、Br 三种物质的氧化性由强到弱的顺序为
2 2 2
___________________。
【答案】(1)A (2)B (3)Br +SO+2H O=HSO +2HBr
2 2 2 2 4
(4)富集Br (直接蒸馏低浓度溴水成本高,经过吸收、氧化后得到浓度较高的Br 溶液)
2 2
(5)Cl>Br >SO
2 2 2
【解析】(1)A.镁离子用氢氧根离子沉淀,加入过量的氢氧化钠可以将镁离子沉淀,硫酸根离子用
钡离子沉淀,加入过量的氯化钡可以将硫酸根离子沉淀,至于是先除镁离子,还是先除硫酸根离子都行,
钙离子用碳酸根离子沉淀,除钙离子加入碳酸钠转化为沉淀,但是加入的碳酸钠要放在加入的氯化钡之
后,这样碳酸钠会除去反应剩余的氯化钡,离子都沉淀了,再进行过滤,最后再加入盐酸除去反应剩余的
氢氧根离子和碳酸根离子,所以加入试剂的先后顺序可以是BaCl 、NaCO、NaOH,A项正确;B.澄清
2 2 3
石灰水的主要成分是氢氧化钙,但氢氧化钙可以与碳酸钠反应生成碳酸钙沉淀,也可以与碳酸氢钠反应生
成碳酸钙沉淀,B项错误;C.步骤II中氯气将母液中的溴离子氧化成溴单质,步骤III中利用空气将溶液
中的溴单质吹出与二氧化硫发生氧化还原反应生成溴离子,这里面的溴元素是被还原的,步骤IV中溶液
中的溴离子又被氯气氧化成溴单质,C项错误;答案选A。
(2)蒸馏时用到的仪器没有容量瓶,容量瓶是在配制一定体积一定浓度溶液时所使用的计量仪器,
答案选B。
(3)二氧化硫和溴单质发生氧化还原反应,其中二氧化硫做还原剂,被氧化成硫酸根,溴单质做氧
化剂,被还原成溴离子,依据得失电子守恒和质量守恒,两者反应的化学方程式为:
Br +SO+2H O=HSO +2HBr。
2 2 2 2 4
(4)由于开始得到的是溴的稀溶液,直接蒸馏低浓度溴水成本高,产率低,经过吸收、氧化后得到
浓度较高的Br 溶液,实现对溴的富集。
2
(5)由题目可知,氯气可以将溴离子氧化成溴单质,说明氯气的氧化性比溴单质强,而溴单质又可
以把二氧化硫氧化成硫酸根,说明溴单质的氧化性比二氧化硫强,因此三者氧化性强弱的顺序为:
Cl>Br >SO。
2 2 2