文档内容
第八章 化学与可持续发展
第一节 自然资源的开发利用
第一课时 金属矿物的开发利用
【学习目标】1.通过联系旧知、归纳总结,认识金属冶炼的原理和冶炼方法,理解氧化还原反应在金
属矿物开发中的应用,构建金属冶炼的思维模型。
2.通过讨论交流、数据分析,以铝的冶炼为例,了解金属冶炼成本的计算方法,认识合理开发和利用
金属资源的重要性和必要性。
3.通过资料收集、阅读思考,能从化学的角度分析从自然资源到产品的转化途径,认识化学方法在实
现物质转中的作用和贡献,感受化学科学在生产、生活中的应用价值。
【学习重点】金属冶炼原理及方法
【学习难点】金属活动性顺序与金属冶炼方法的关系
【课前预习】
旧知回顾:1.金属具有哪些通性?金属单质的还原性及离子的氧化性强弱有何规律?
2.判断元素金属性强弱的方法有哪些?
新知预习:1.金属在自然界的存在有何特点?
2.金属冶炼的实质是什么?
【课中探究】
情景导入:观看视频:拿破仑三世的金属餐具。金属材料是当前乃至未来人类发展与生存的重要物质
基础,你知道拿破仑三世的刀叉具和纽扣为什么都用铝制造吗?筵席上,他为什么为多数客人提供金餐
具,而只让少数客人使用铝餐具呢?(视频见PPT)
一、金属矿物的开发利用活动一、金属矿物与自然资源
任务一、阅读教材P98页第一自然段,结合“资料卡片”内容,思考自然资源与可持续发展有何关
系?
任务二、思考交流:回顾初中所学知识,思考金属在自然界的存在有何特点和规律?
【对应训练】1.中国高铁是一张国家名片,工业中常利用赤铁矿来炼铁,下列说法中正确的是
( )
A.地壳中含量最高的金属元素是铁元素
B.高炉炼铁得到的产品是纯铁
C.炼铁过程中,氧化铁体现了还原性
D.高炉炼铁时加入石灰石可将杂质二氧化硅转化为炉渣
2.化学在生产和日常生活中有重要的应用。下列说法不正确的是( )
A.目前我国流通的硬币是由合金材料制造的
B.合金的熔点一般比其成分金属的熔点高
C.青铜是我国使用最早的合金材料,目前世界上使用量最大的合金材料是钢铁
D.铝比铁活泼,但在空气中铝制品比铁制品耐腐蚀
活动二、探究金属的冶炼
任务一、阅读教材P98页第二自然段,思考什么是金属的冶炼?结合氧化还原反应原理,回答金属冶
炼的实质是什么?
任务二、讨论交流:金属的冶炼方法与金属活泼性有何关系?为什么不同的金属的冶炼方法不同?注意:
任务三、归纳总结:结合金属冶炼的原理,思考如何根据金属的活泼性不同选择不同的金属冶炼方
法?
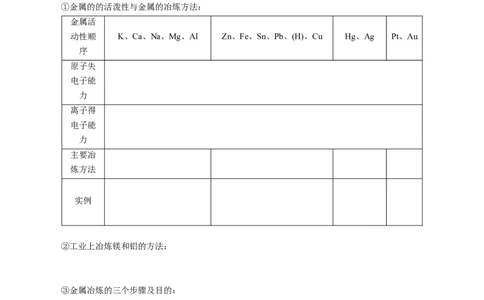
①金属的的活泼性与金属的冶炼方法:
金属活
动性顺 K、Ca、Na、Mg、Al Zn、Fe、Sn、Pb、(H)、Cu Hg、Ag Pt、Au
序
原子失
电子能
力
离子得
电子能
力
主要冶
炼方法
实例
②工业上冶炼镁和铝的方法:
③金属冶炼的三个步骤及目的:
注意:
【对应训练】1.《天工开物》中述及铜的开采与冶炼:凡铜砂……淘洗去土滓,然后入炉煎炼,其
熏蒸旁溢者为自然铜……色似干银泥……凡铜质有数种:有与铅同体者,其煎炼炉法,傍通高低二孔,铅
质先化,从上孔流出。下列有关说法错误的是 ( )
A.“淘洗去土滓”属于原料的富集 B.炼制所得自然铜为合金C.铜与铅混合物的分离过程利用了物质的熔点不同 D.可用热分解法冶炼铜
2.冶炼金属一般有下列四种方法:①焦炭法,②水煤气(或H 或CO)法,③活泼金属置换法,④电
2
解法。四种方法在工业上均有应用。古代有(Ⅰ)火烧孔雀石法炼铜,(Ⅱ)湿法炼铜,现代有(Ⅲ)铝
热法炼铬,(Ⅳ)从光卤石(KCl•MgCl •6H O)中炼镁,对它们的冶炼方法分析不正确的是( )
2 2
A.(Ⅰ)用① B.(Ⅱ)用②
C.(Ⅲ)用③ D.(Ⅳ)用④
二、铝热反应与金属资源的利用
活动一、探究铝热反应的原理及应用
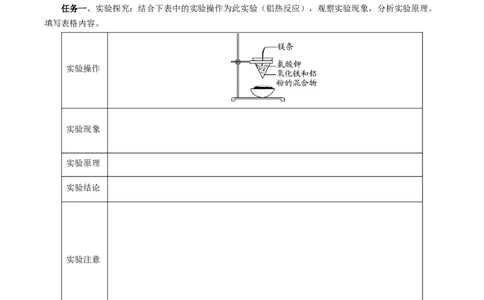
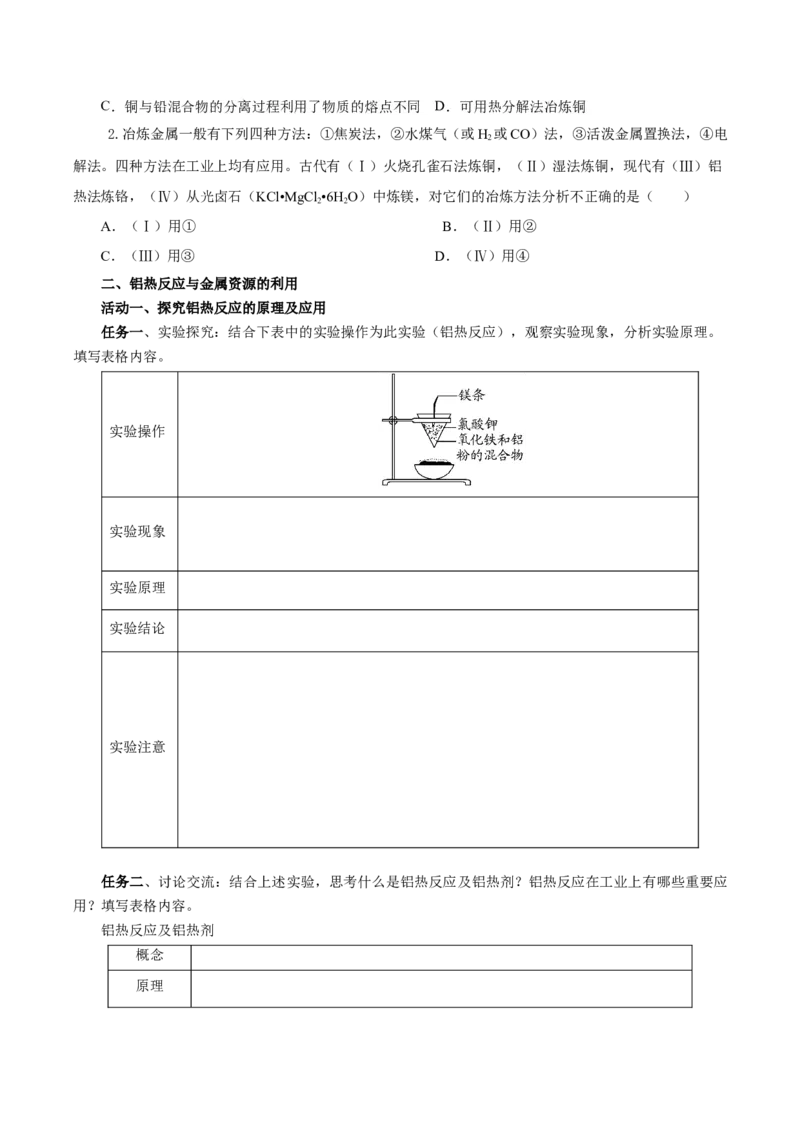
任务一、实验探究:结合下表中的实验操作为此实验(铝热反应),观察实验现象,分析实验原理。
填写表格内容。
实验操作
实验现象
实验原理
实验结论
实验注意
任务二、讨论交流:结合上述实验,思考什么是铝热反应及铝热剂?铝热反应在工业上有哪些重要应
用?填写表格内容。
铝热反应及铝热剂
概念
原理铝热剂
反应特点
应用
【对应训练】1.野外焊接钢轨常用如图所示装置,镁条引燃混合物后,反应非常剧烈,火星四射,
有熔融铁珠落入沙子中。下列叙述错误的是( )
A.该反应属于置换反应
B.有“熔融铁珠”生成说明该反应为放热反应
C.该反应的化学能全部转化为热能
D.该反应中断键吸收的能量小于成键释放的能量
2.下列有关金属冶炼的说法错误的是( )
①金属的冶炼都是把金属单质从其矿物中分离出来
②可以采用加热分解氧化银的方法制取单质银
③可以采用电解熔融氯化铝的方法制取单质铝
④铝热反应的原理是利用铝作还原剂,置换出相对不活泼的金属
A.①② B.①③ C.②④ D.③④
活动二、合理利用金属资源
任务一、阅读教材P99页第一自然段,回答合理开发和利用金属矿物资源的原因及措施是什么?
①原因:
②措施:
任务二、讨论交流:根据教材P99页“思考与讨论”,结合数据及图8-1和图8-2的分析和比较,思考
在利用金属资源的过程中要注意哪些问题?
【对应练习】1.铝曾是比黄金还要贵重的金属。1885年建成的华盛顿纪念碑,其顶端就是一块当时
很昂贵的金属铝。下列关于当时铝的价格高昂的原因分析中,错误的是
A.活泼的金属冶炼难度高B.氧化铝熔点很高,电解需要耗费的热量极其多
C.当时化学家还未尝试采用焦炭冶炼铝的方法
D.还未找到良好的助熔剂
2.下列关于金属的冶炼方法说法不正确的是( )
A.废旧金属的回收利用有利于减轻污染
B.银的金属性弱,用加热Ag O的方法冶炼
2
C.金子比沙子密度大,利用水洗法直接获得
D.金属镁活泼,电解氯化镁溶液可以获取
【课后巩固】1.下列说法不正确的是( )
A.自然界中存在游离态的金属单质
B.金属活动性不同,冶炼方法也有所不同
C.地球上金属矿物资源是取之不尽的,因此,应加大开采金属矿物的速度,以满足经济发展的需要
D.废旧金属的回收利用,有利于环境保护
2.下列关于金属冶炼的说法正确的是( )
A.由于Al的活泼性强,故工业上采用电解熔融AlCl 的方法生产Al
3
B.可以用钠加入氯化镁饱和溶液中制取镁
C.炼铁高炉中所发生的反应都是放热的,故无需加热
D.金属冶炼的本质是将化合态金属还原为游离态,冶炼方法由金属的活泼性决定
3.下列常见金属的冶炼原理不合理的是( )
A.还原法炼铝:3H+Al O=====2Al+3H O
2 2 3 2
B.加热法炼汞:2HgO=====2Hg+O↑
2
C.铝热法炼铁:2Al+Fe O=====2Fe+Al O
2 3 2 3
D.火法炼铜:Cu S+O=====2Cu+SO
2 2 2
4.下列有关金属的冶炼描述错误的是( )
A.电解熔融的NaCl制取Na
B.金属冶炼过程中,被冶炼的金属被还原
C.CO还原Fe O 制取Fe
2 3
D.从自然界中获得金属单质均需要通过化学方法
5.铝热反应有广泛的用途,实验装置如图1所示。下列说法错误的是( )A.铝热反应的能量变化可用图2表示
B. 和铝粉的混合物被称为铝热剂
C.铝热反应只能用于冶炼铁、锰、铬、镁等熔点较高的金属
D.铝热反应可用于焊接铁轨,反应的化学方程式为2Al+Fe O=====2Fe+Al O
2 3 2 3
6.西汉刘安所著的《淮南万毕术》中有“曾青得铁,则化为铜,外化而内不化”,该反应被认为是
现代湿法冶金术之祖。下列说法正确的是( )
A.硫酸铜晶体化学式为CuSO ·5H O,是混合物
4 2
B.“内不化”是因为内部的铁活泼性比表面的铁活泼性差
C.上述反应的离子方程式为2Fe+3Cu2+=2Fe3++3Cu
D.“化为铜”表明发生的是氧化还原反应
7.以铝土矿(主要成分为Al O,含SiO 和Fe O 等杂质)为原料制备铝的一种工艺流程如下:
2 3 2 2 3
下列有关叙述不正确的是( )
A.将铝土矿粉碎有利于加快碱溶速率
B.滤渣的主要成分为SiO 和Fe(OH)
2 3
C.过滤Ⅱ所得滤液中主要存在的离子为Na+、HCO -
3
D.Al O 与冰晶石共熔电解得到单质铝
2 3
8.镁及其合金是用途很广的金属材料。工业上冶炼镁的方法有两种,电解法和皮江法。电解法是电
解熔融的MgCl ,皮江法是Si在高温下还原MgO。
2
已知:相关各物质熔点见下表:
物质 MgO MgCl Mg Si
2
熔点 2852 714 649 1410
Ⅰ.电解法冶炼镁。
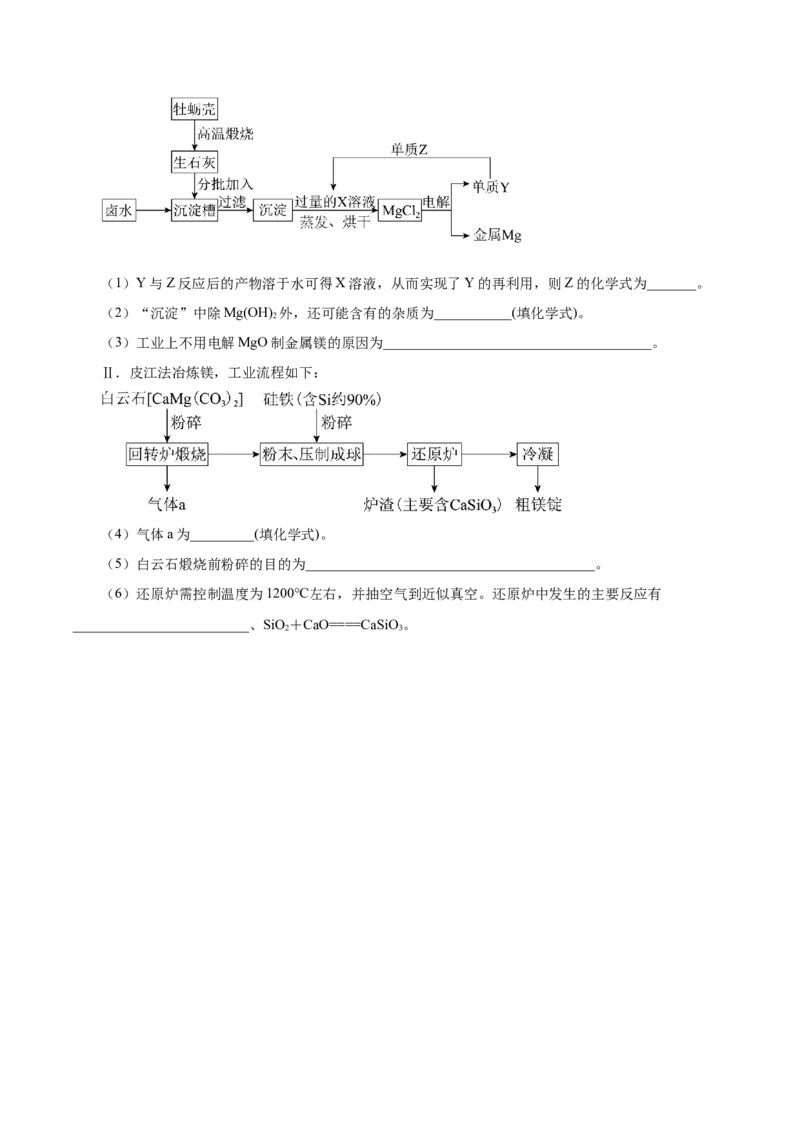
化工厂利用卤水(主要成分为NaCl和MgCl )生产金属镁的一种工艺流程如图所示:
2(1)Y与Z反应后的产物溶于水可得X溶液,从而实现了Y的再利用,则Z的化学式为_______。
(2)“沉淀”中除Mg(OH) 外,还可能含有的杂质为___________(填化学式)。
2
(3)工业上不用电解MgO制金属镁的原因为______________________________________。
Ⅱ.皮江法冶炼镁,工业流程如下:
(4)气体a为_________(填化学式)。
(5)白云石煅烧前粉碎的目的为_________________________________________。
(6)还原炉需控制温度为1200℃左右,并抽空气到近似真空。还原炉中发生的主要反应有
_________________________、SiO+CaO====CaSiO 。
2 3