文档内容
第八章 化学与可持续发展
第一节 自然资源的开发利用 课时作业
第一课时 金属矿物的开发利用
基础达标
1.中华文化如长河,源远流长势不竭。下列国家级文物中,主要成分属于硅酸盐材料的是
( )
A.三星堆青铜人像 B.官窑彩瓷
C.金漆木雕大神龛 D.镶金兽首玛瑙杯
2.目前电动车、手机等使用的新型电池——锂电池,是一种高效、环保电池。已知锂的金
属性介于钠和镁之间,则下列能冶炼出金属锂的方法是( )
A.电解法 B.高温还原法 C.热分解法 D.铝热还原法
3.下列金属的冶炼方法与其他三者不同的是( )
A.Mg B.Al C.Cu D.Na
4.下列反应原理不符合工业上冶炼金属的方法的是( )
A.MgO+H====Mg+HO B.3CO+Fe O====2Fe+3CO
2 2 2 3 2
C.2Ag O====4Ag+O↑ D.2Al O(熔融)=====4Al+3O↑
2 2 2 3 2
5.氧化还原反应广泛应用于金属的冶炼。下列说法正确的是( )
A.冶炼铁的主要原料有铁矿石、焦炭、空气、石灰石等,其中焦炭的作用是氧化剂
B.湿法炼铜与火法炼铜的反应中,铜元素都发生还原反应
C.工业上Mg由电解熔融的MgO制取,Na由电解熔融的NaCl制取
D.越活泼的金属越容易冶炼
6.从石器、青铜器到铁器时代,金属的冶炼体现了人类文明的发展水平。下列有关金属冶
炼的说法正确的是( )
A.工业炼铁的还原剂是CO B.纯铁的硬度比生铁高
C.工业上金属Mg、Al都是用电解熔融的氯化物制得的
D.金属被人类开发利用的时间先后顺序主要取决于金属在地壳中的含量
7.能用铝作原料来冶炼难熔的金属是因为( )A.铝的密度小,熔点较低 B.铝在空气中燃烧放出大量的热
C.铝在金属活动性顺序表中排在较前面 D.铝具有还原性,发生铝热反应时放出大量
热
8.下列说法错误的是( )
A.活泼金属钠的冶炼是通过电解其盐溶液制得
B.对废旧金属的最好处理方法是回收、再利用
C.提炼金属要经过矿石的富集、冶炼、精炼三步
D.热还原法中还原剂有焦炭、一氧化碳、氢气或活泼金属等
9.下列有关金属的说法中,正确的是( )
A.Al是地壳中含量最高的元素
B.Fe是现代工业的基础,铝热法冶炼Fe工艺简单,可以大规模推广
C.纯Cu多应用于电气工业, Cu元素在自然界都是以化合态形式存在
D.Na常应用于制高压钠灯、Na-K合金做原子反应堆的导热剂等
10.下列关于金属冶炼的说法中错误的是( )
A.电解法获得镁时,不可在CO 或N 中降温冷却
2 2
B.热还原法常用的还原剂有CO、H、C、Al等
2
C.金属Na、Mg、Al均能通过电解熔融氯化物的方法获得
D.人类历史上金属被发现的顺序与金属的活泼性有关
能力提升
11.工业上可通过电解 生产金属钠,流程如下。有关说法错误的是( )
A.粗钠中含有金属钙
B.过程I发生的是置换反应
C.过程Ⅱ控制温度可分离出液态粗钠
D.过程Ⅱ的化学方程式为:
NaO+2Ca=2CaO+2Na
2 2
12.工业上以铝土矿(主要成分为Al O,含少量氧化铁和二氧化硅)为原料生产铝的流程如
2 3
图所示,下列叙述不正确的是( )
A.物质a可以是NH 或氨水
3
B.滤渣①的主要成分是SiO
2C.滤液1和滤液2中铝元素的化合价相同
D.步骤Ⅰ发生反应的化学方程式为:2Al O(熔融)=====4Al+3O↑
2 3 2
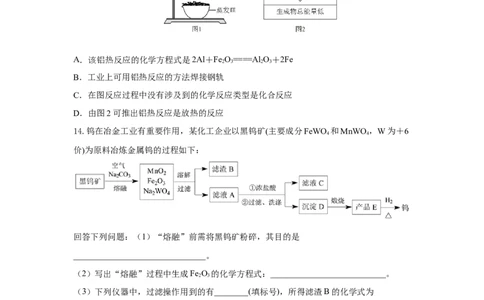
13.铝热反应有广泛的用途,实验装置如下图所示。下列说法不正确的是( )
A.该铝热反应的化学方程式是2Al+Fe O====Al O+2Fe
2 3 2 3
B.工业上可用铝热反应的方法焊接钢轨
C.在图反应过程中没有涉及到的化学反应类型是化合反应
D.由图2可推出铝热反应是放热的反应
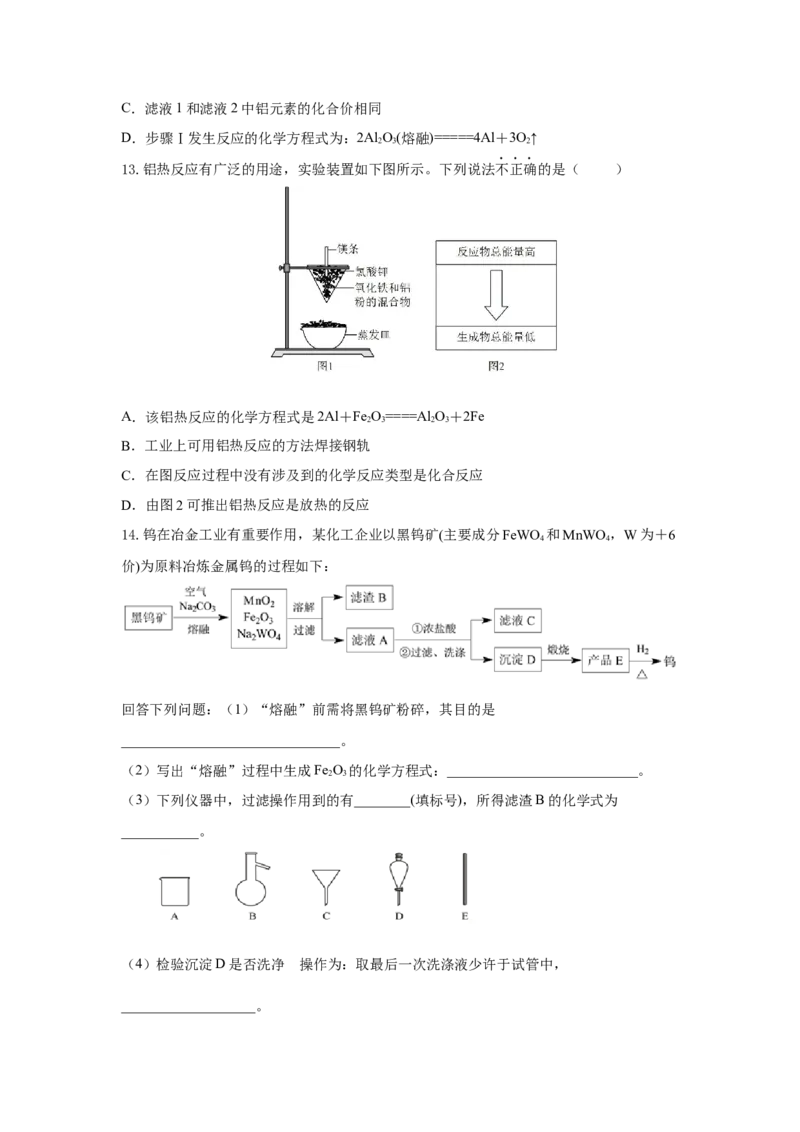
14.钨在冶金工业有重要作用,某化工企业以黑钨矿(主要成分FeWO 和MnWO ,W为+6
4 4
价)为原料冶炼金属钨的过程如下:
回答下列问题:(1)“熔融”前需将黑钨矿粉碎,其目的是
_______________________________。
(2)写出“熔融”过程中生成Fe O 的化学方程式:___________________________。
2 3
(3)下列仪器中,过滤操作用到的有________(填标号),所得滤渣B的化学式为
___________。
的
(4)检验沉淀D是否洗净 操作为:取最后一次洗涤液少许于试管中,
___________________。(5)产品E的化学式为WO ,其中W的化合价有+5和+6两种。若x=0.1,则+5价
3-x
的W(V)占该化合物中钨元素总量的_________;该流程中由产品E冶炼金属钨的方法属于
_____________法。
直击高考
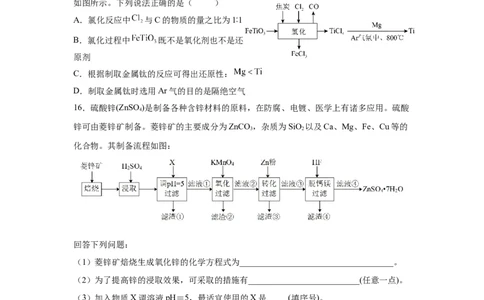
15.钛铁矿( ,其中Ti为 价)在高温下经氯化得到四氯化钛,再制取金属钛的流程
如图所示。下列说法正确的是( )
A.氯化反应中 与C的物质的量之比为1∶1
B.氯化过程中 既不是氧化剂也不是还
原剂
C.根据制取金属钛的反应可得出还原性:
D.制取金属钛时选用Ar气的目的是隔绝空气
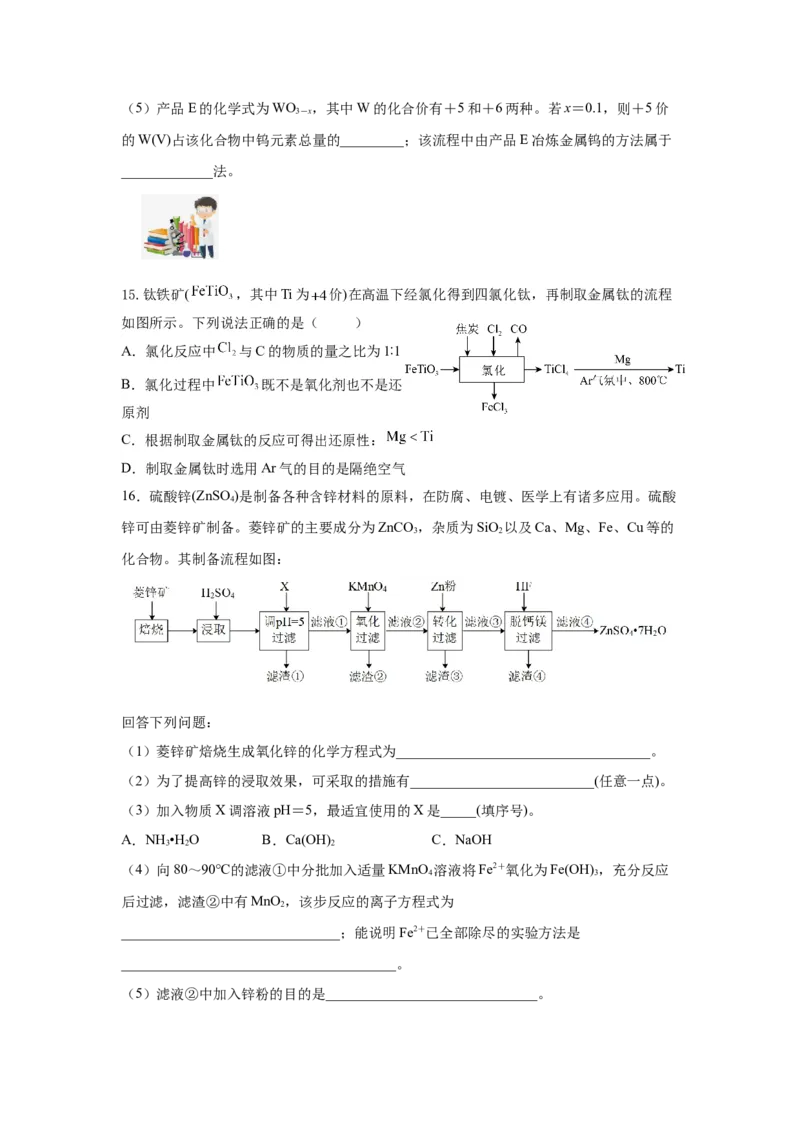
16.硫酸锌(ZnSO)是制备各种含锌材料的原料,在防腐、电镀、医学上有诸多应用。硫酸
4
锌可由菱锌矿制备。菱锌矿的主要成分为ZnCO ,杂质为SiO 以及Ca、Mg、Fe、Cu等的
3 2
化合物。其制备流程如图:
回答下列问题:
(1)菱锌矿焙烧生成氧化锌的化学方程式为____________________________________。
(2)为了提高锌的浸取效果,可采取的措施有__________________________(任意一点)。
(3)加入物质X调溶液pH=5,最适宜使用的X是_____(填序号)。
A.NH •H O B.Ca(OH) C.NaOH
3 2 2
(4)向80~90℃的滤液①中分批加入适量KMnO 溶液将Fe2+氧化为Fe(OH) ,充分反应
4 3
后过滤,滤渣②中有MnO ,该步反应的离子方程式为
2
_______________________________;能说明Fe2+已全部除尽的实验方法是
_______________________________________。
(5)滤液②中加入锌粉的目的是______________________________。