文档内容
第八章 化学与可持续发展
第一节 自然资源的开发利用 课时作业
第二课时 海水资源的开发利用
基础达标
1.下列关于海水资源综合利用的说法中,不合理的是( )
A.从海水中可以得到MgCl ,可电解MgCl 溶液制备Mg
2 2
B.通常以海水提取食盐后的母液为原料制取溴单质
C.海水蒸发制海盐的过程是物理变化
D.海水淡化的方法主要有蒸馏法、电渗析法、离子交换法等
【答案】A
【解析】A.从海水中可以得到MgCl ,可电解熔融MgCl 制备Mg,A错误;B.通常以
2 2
海水提取食盐后的母液中含有大量溴离子,可以作为原料制取溴单质,B正确;C.海水蒸
发制海盐是蒸发结晶的过程,是物理变化,C正确;D.海水淡化可通过蒸馏法、电渗析
法、离子交换法等实现,D正确;故选A。
2.海水是一个巨大的化学资源库,下列有关海水综合利用的说法正确的是( )
A.海水中含有镁元素,只需经过物理变化就可以得到镁单质
B.海水蒸发制海盐的过程中只发生了物理变化
C.从海水中可以得到 ,电解饱和食盐水可制备
D.海水中的溴、碘可用四氯化碳直接萃取得到
【答案】B
【解析】A.海水中镁元素以 Mg2+形式存在,需经过 MgCl →Mg(OH) →MgCl 溶液
2 2 2
→MgCl 6HO→MgCl →Mg等化学反应得到镁单质,故A错误;B.海水蒸发制海盐,溶
2 2 2
剂减少,氯化钠析出,只发生了物理变化,故 B正确;C.电解饱和食盐生成氢氧化钠、
氢气、氯气,电解熔融NaCl制备Na,故C错误;D.海水中的溴、碘以Br-、I-形式存
在,可以先用氯气氧化,再用四氯化碳萃取得到,故D错误;选B。
3.从海水中提取的粗盐主要成分是NaCl,现要除去NaCl中少量的CaCl 、ZnCl 、NaSO
2 2 2 4
杂质,下列选用的试剂及其使用顺序正确的是( )
A.NaCO、BaCl 、HCl B.BaCl 、NaCO、HSO
2 3 2 2 2 3 2 4
C.BaCl 、NaCO、HCl D.Ba(NO )、NaCO、HCl
2 2 3 3 2 2 3
【答案】C
【解析】一般除杂质的试剂,要尽量除去杂质,加入的试剂必须稍过量,加过量试剂时还
应考虑下一步要除去过量未反应的试剂。本题加试剂顺序应是Ba2+→CO→HCl,加稍过量BaCl 可除去NaSO ,稍后加入的NaCO 在除去CaCl 同时也除去了过量的BaCl ,最后再
2 2 4 2 3 2 2
用盐酸除去过量的NaCO,盐酸过量点不要紧,可通过加热挥发而除去。
2 3
4.下列叙述正确的是( )
A.海带提碘时可用HO 将I-还原为碘单质
2 2
B.海水既苦又涩,不能直按利用
C.海水提溴过程中不涉及氧化还原反应
D.海水提溴时吸收塔内SO 、Br 和水之间发生反应生成硫酸和氢溴酸,体现SO 的还原
2 2 2
性
【答案】D
【解析】A.碘离子被过氧化氢氧化为碘单质,发生氧化反应,故A错误;B.海水既苦又
涩,海水可直接利用如用潮水发电,从海水中可直接提取食盐NaCl,提取镁,提取溴等物
质,故B错误;C.海水提溴是利用加入氧化剂氧化溴离子得到溴单质,过程中需要发生
氧化还原反应,故C错误;D.二氧化硫可以和溴单质发生氧化还原反应生成氢溴酸和硫
酸,即SO +Br +2H O=2HBr+HSO ,S元素化合价升高,SO 做还原剂,体现SO 的还原
2 2 2 2 4 2 2
性,故D正确;故选:D。
5.空气吹出法是工业规模海水提溴的常用方法,流程如下:
下列说法不正确的是( )
A.步骤①发生的主要反应为:Cl+2Br-=Br +2Cl-
2 2
B.步骤②③的目的是富集溴元素
C.物质X为HBrO
D.空气吹出法用到了溴易发挥的性质
【答案】C
【解析】A.步骤①发生的主要反应为:Cl+2Br-=Br +2Cl-,生成粗产品溴,选项A正确;
2 2
B.海水中溴离子浓度较低,由上述分析可知,步骤②③的目的是富集溴元素,选项B正
确;C.物质X含硫酸和HBr,选项C错误;D.溴易挥发,可空气吹出,选项D正确;
答案选C。
6.通过海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl 、CaCl 、NaSO ,以及泥沙等
2 2 2 4
杂质,粗盐精制的实验流程如图。下列说法不正确的是( )
A.在第①步中使用玻璃棒搅拌可加速粗盐溶解B.流程图中的系列操作用到的主要仪器有玻璃棒、烧杯、漏斗、蒸发皿
C.在第②③④⑥步通过加入化学试剂除杂,试剂②可能是NaCO 溶液
2 3
D.除去Mg2+的主要离子反应为:Mg2++2OH-=Mg(OH) ↓
2
【答案】C
【解析】粗盐溶解,乙醇加入氢氧化钠、氯化钡、碳酸钠除去MgCl 、CaCl 、NaSO ,过
2 2 2 4
滤后加入盐酸除去氢氧化钠、碳酸钠,蒸发、结晶、烘干得精盐。A.第①步是溶解,使
用玻璃棒搅拌可加速粗盐溶解,故A正确;B.流程图中的系列操作包括过滤、蒸发、结
晶等,用到的主要仪器有玻璃棒、烧杯、漏斗、蒸发皿,故B正确;C.用氢氧化钠除
MgCl 、用氯化钡除NaSO ,用碳酸钠除CaCl 和过量的氯化钡,过滤后用盐酸除去氢氧化
2 2 4 2
钠、碳酸钠,所以要在加入氯化钡溶液后加碳酸钠,试剂②不可能是NaCO 溶液,故C错
2 3
误;D.用氢氧化钠除MgCl ,除去Mg2+的主要离子反应为:Mg2++2OH-=Mg(OH) ↓,故D
2 2
正确;选C。
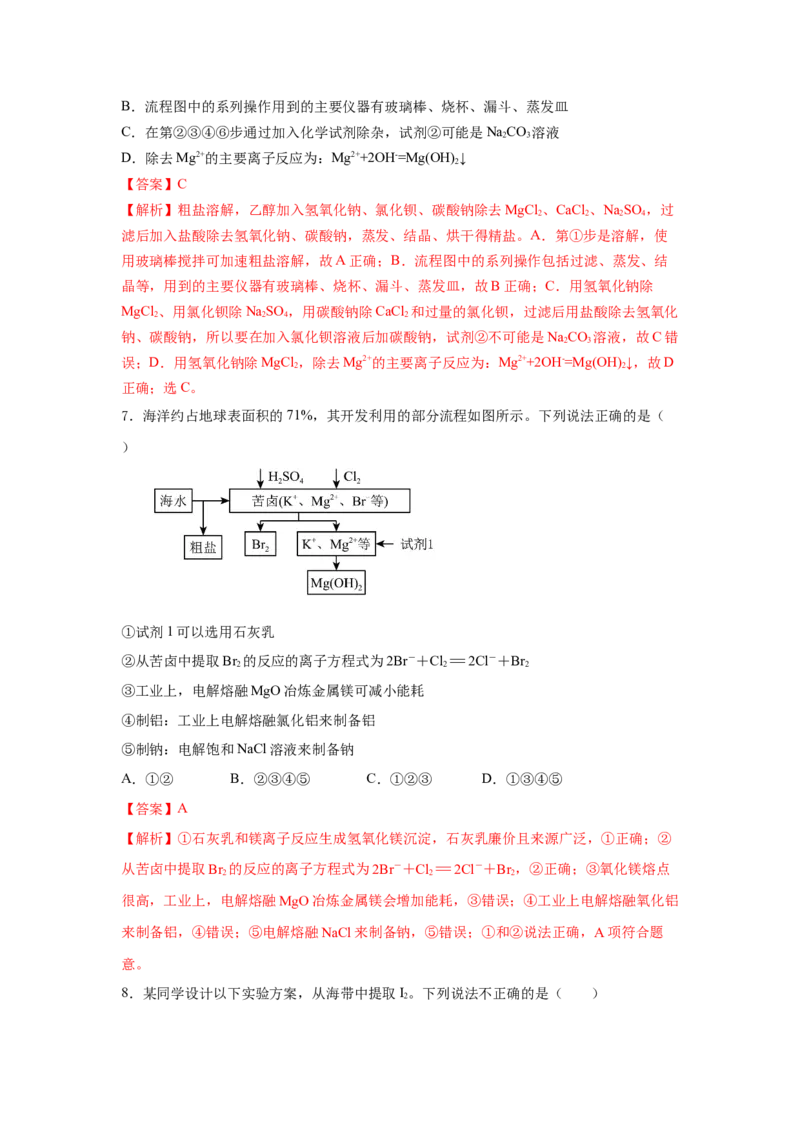
7.海洋约占地球表面积的71%,其开发利用的部分流程如图所示。下列说法正确的是(
)
①试剂1可以选用石灰乳
②从苦卤中提取Br 的反应的离子方程式为2Br-+Cl=2Cl-+Br
2 2 2
③工业上,电解熔融MgO冶炼金属镁可减小能耗
④制铝:工业上电解熔融氯化铝来制备铝
⑤制钠:电解饱和NaCl溶液来制备钠
A.①② B.②③④⑤ C.①②③ D.①③④⑤
【答案】A
【解析】①石灰乳和镁离子反应生成氢氧化镁沉淀,石灰乳廉价且来源广泛,①正确;②
从苦卤中提取Br 的反应的离子方程式为2Br-+Cl=2Cl-+Br ,②正确;③氧化镁熔点
2 2 2
很高,工业上,电解熔融MgO冶炼金属镁会增加能耗,③错误;④工业上电解熔融氧化铝
来制备铝,④错误;⑤电解熔融NaCl来制备钠,⑤错误;①和②说法正确,A项符合题
意。
8.某同学设计以下实验方案,从海带中提取I。下列说法不正确的是( )
2A.操作①是过滤
B.含I 的溶液经3步转化为I 的悬浊液,其目的是富集
2 2
C.③的离子方程式是5I-+IO -+6H+=3I+3HO
3 2 2
D.②中双氧水作还原剂
【答案】D
【解析】由流程可知,热水溶解后,操作①为过滤,滤液含碘离子,加过氧化氢可氧化碘
离子生成碘单质,试剂 a为苯或四氯化碳可萃取碘,分液得到含碘的有机溶液,再加
NaOH与碘反应生成I-和IO -,分液后向含I-和IO -的溶液中加稀硫酸发生反应5I-+IO
3 3 3
-+6H+=3I +3HO,过滤提取得到粗碘。A项,根据以上分析可知操作①是过滤,正
2 2
确;B项,海水中碘含量较低,因此含 I 的溶液经3步转化为I 的悬浊液,其目的是富
2 2
集,正确;C项,反应③是碘酸根离子氧化碘离子,反应的离子方程式是5I-+IO -+6H+
3
=3I+3HO,正确;D项,②中双氧水作氧化剂,氧化碘离子,错误。
2 2
9.海水是一个巨大的化学资源库,下列有关海水综合利用的说法错误的是( )
A.海水中含有溴元素,需经过化学变化才可以得到溴单质
B.无论是海水波浪发电还是潮汐发电,都是将化学能转化为电能
C.从海水中可以得到NaCl,电解熔融NaCl可制备金属钠
D.从海水中提取镁可以采用下列方法:
海水―→苦卤――→Mg(OH) ――→MgCl 溶液―→无水MgCl ―→MgCl (熔融)――→Mg
2 2 2 2
【答案】B
【解析】海水中的溴元素以离子形式存在,需要通过化学反应来转化成溴单质,A项正
确;在波浪发电和潮汐发电过程中机械能转化为电能,而不是化学能转化为电能,B项错
误;从海水中可以得到NaCl固体,电解熔融NaCl可制备金属钠,C项正确;依据海水提
取镁的原理分析,卤水中加入氢氧化钙以沉淀镁离子,生成氢氧化镁,过滤后加盐酸溶
解、蒸发浓缩、冷却结晶析出晶体,然后得到氯化镁固体,电解熔融氯化镁得到金属镁,
该方法合理,D项正确。
10.海水提溴的流程如图所示。下列说法错误的是( )A.步骤②利用了溴的挥发性
B.步骤④可以用双氧水代替Cl
2
C.步骤⑤用到的玻璃仪器只有漏斗和烧杯
D.使用该法处理1m3海水最终得到18gBr ,若提取率为30%,则原海水中Br-的浓度为
2
60mg·L-1
【答案】C
【解析】A.因溴易挥发,可用热空气吹出,所以步骤②利用了溴的挥发性,故A正确;
B.因双氧水氧化性强于溴,且双氧水还原产物为水,所以可用双氧水代替Cl,故B正
2
确;C.步骤⑤为分离溴和水,先用苯或四氯化碳萃取分液的方法得到溴的有机溶液,再
进行蒸馏,用到的玻璃仪器有分液漏斗、烧杯、蒸馏烧瓶、冷凝管等,故C错误;D.使
用该法处理1m3海水最终得到18gBr ,若提取率为30%,则1m3海水中含有Br-的质量为
2
18g 60×1000mg
=60g,原海水中Br-的浓度为 =60mg·L-1,故D正确;故选C;
30% 1000L
能力提升
11.下列从海洋中获取物质的方案不合理的是( )
A.粗盐先通过除杂、精制得到饱和食盐水,然后电解得到氯气,最后和石灰乳反应制得
漂白粉
B.苦卤酸化后通入氯气得到溴水,然后用热空气将其通入到SO 水溶液中,最后通入氯气
2
后蒸馏得粗溴
C.干海带灼烧后加水浸取,然后加入HO 得到碘水,最后通过萃取、分液、蒸馏得到碘
2 2
单质
D.向引入水库中的海水加入明矾,明矾电离后可以与水反应产生胶体,即可获得较为纯
净的饮用水
【答案】D
【解析】A.粗盐中含有泥沙、Ca2+、Mg2+、SO等杂质,先依次加入BaCl2、NaCO、
2 3
NaOH除去SO、Ca2+、Mg2+,再过滤除去泥沙及沉淀,最后加入稀盐酸调节pH,除去过量
的NaCO、NaOH,从而得到精制饱和食盐水,然后电解得到氯气,即:
2 3
2NaCl+2H O\o(\s\up6(_____)2NaOH+H ↑+Cl↑,所得Cl 和石灰乳反应制得漂白粉,即:
2 2 2 22Cl+2Ca(OH) =CaCl +Ca(ClO) +2H O,A正确;B.苦卤中含有Br-,酸化后通入氯气得
2 2 2 2 2
到溴水(Cl+2Br-=2Cl-+Br ),然后用热空气将其通入到SO 水溶液中(Br +SO+2H O
2 2 2 2 2 2
=HSO +2HBr),最后通入氯气后蒸馏得粗溴(2HBr+Cl =2HCl+Br ),B正确;C.干
2 4 2 2
海带灼烧后加水浸取得到含碘离子的溶液,然后加入HO 得到碘水,最后通过萃取、分
2 2
液、蒸馏得到碘单质,C正确;D.明矾电离后可以与水反应产生胶体只是吸附水中的悬
浮杂质沉淀,无法除去海水中的Mg2+、Na+、Br-、Cl-等离子,不能获得较为纯净的饮用
水,D错误;故选D。
12.通过下列实验流程制备少量CaBr ·6H O。下列说法错误的是( )
2 2
A.空气吹出法是海水提溴较成熟的工业方法
B.步骤①可用热水浴加热
C.步骤②中CO(NH) 作氧化剂
2 2
D.步骤④的主要操作是蒸发浓缩,冷却结晶
【答案】C
【解析】石灰乳和液溴在50℃~70℃条件下反应生成溴酸钙、溴化钙,溴酸钙和CO(NH)
2 2
发生氧化还原反应生成CaBr ,加入HBr调节pH至中性,加入活性炭吸附杂质,再将溶液
2
蒸发浓缩、冷却结晶、过滤得到CaBr ·6H O。A.海水提溴较成熟的工业方法是空气吹出
2 2
法,故A正确;B.步骤①用50℃~70℃的温度,因此可用热水浴加热,故B正确;C.
步骤②中CO(NH) 与Ca(BrO) 反应变为CaBr ,说明Br化合价降低,则CO(NH) 中氮化
2 2 3 2 2 2 2
合价升高,应作还原剂,故C错误;D.步骤④是从溶液到晶体的过程,其主要操作是蒸
发浓缩、冷却结晶、过滤,故D正确。综上所述,答案为C。
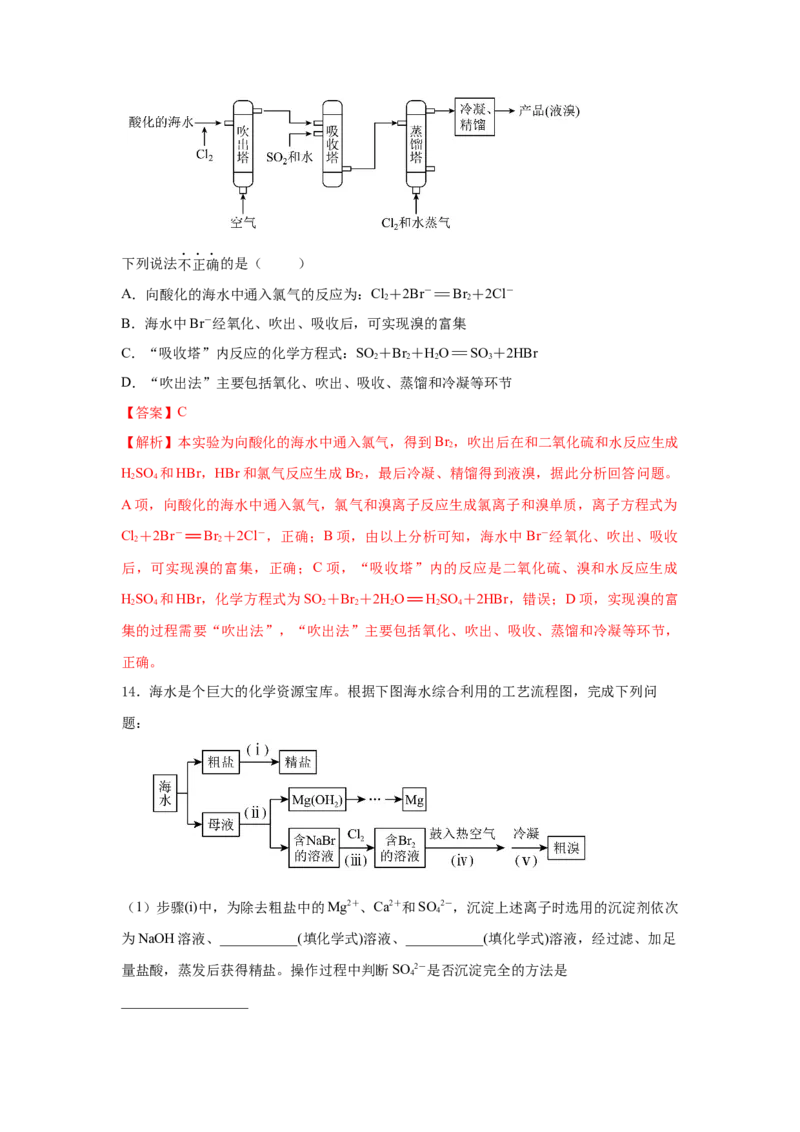
13.溴及其化合物在生产中有广泛应用。工业上常用“吹出法”从海水中提溴,工艺流程
示意图如下:下列说法不正确的是( )
A.向酸化的海水中通入氯气的反应为:Cl+2Br-=Br +2Cl-
2 2
B.海水中Br-经氧化、吹出、吸收后,可实现溴的富集
C.“吸收塔”内反应的化学方程式:SO +Br +HO=SO +2HBr
2 2 2 3
D.“吹出法”主要包括氧化、吹出、吸收、蒸馏和冷凝等环节
【答案】C
【解析】本实验为向酸化的海水中通入氯气,得到Br ,吹出后在和二氧化硫和水反应生成
2
HSO 和HBr,HBr和氯气反应生成Br ,最后冷凝、精馏得到液溴,据此分析回答问题。
2 4 2
A项,向酸化的海水中通入氯气,氯气和溴离子反应生成氯离子和溴单质,离子方程式为
Cl +2Br-=Br +2Cl-,正确;B项,由以上分析可知,海水中Br-经氧化、吹出、吸收
2 2
后,可实现溴的富集,正确;C项,“吸收塔”内的反应是二氧化硫、溴和水反应生成
HSO 和HBr,化学方程式为SO +Br +2HO=HSO +2HBr,错误;D项,实现溴的富
2 4 2 2 2 2 4
集的过程需要“吹出法”,“吹出法”主要包括氧化、吹出、吸收、蒸馏和冷凝等环节,
正确。
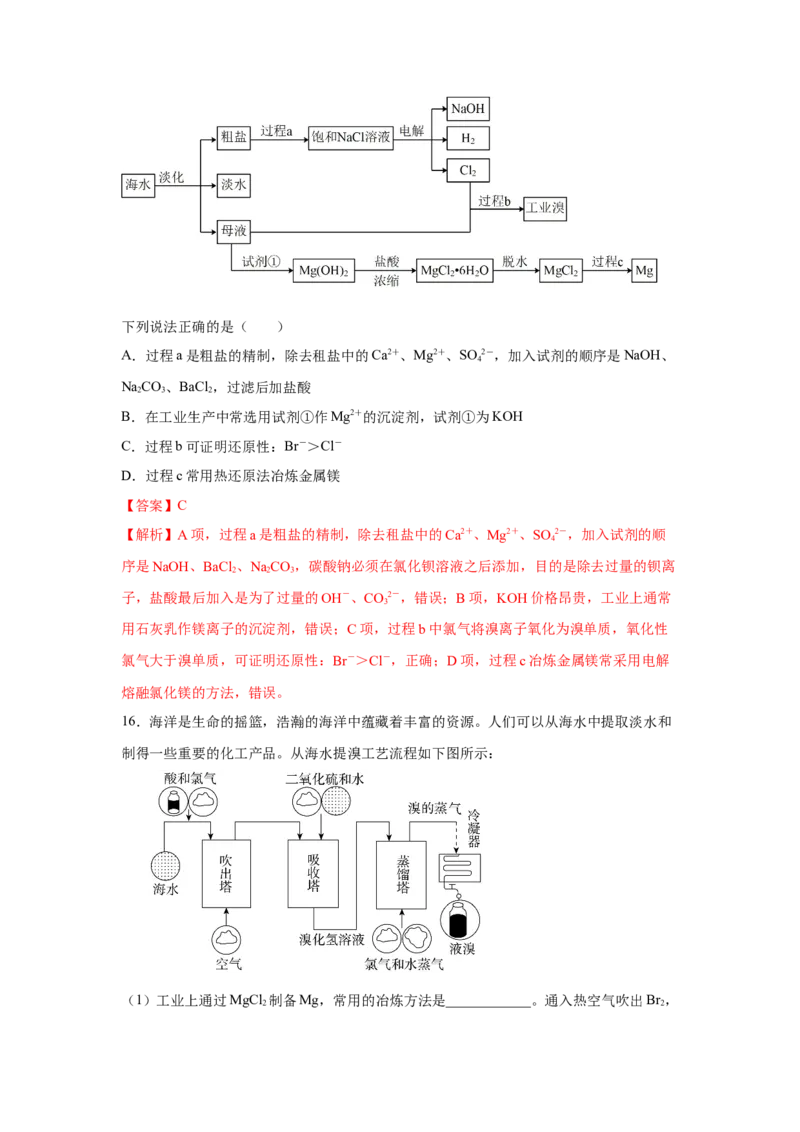
14.海水是个巨大的化学资源宝库。根据下图海水综合利用的工艺流程图,完成下列问
题:
(1)步骤(i)中,为除去粗盐中的Mg2+、Ca2+和SO 2-,沉淀上述离子时选用的沉淀剂依次
4
为NaOH溶液、___________(填化学式)溶液、___________(填化学式)溶液,经过滤、加足
量盐酸,蒸发后获得精盐。操作过程中判断SO 2-是否沉淀完全的方法是
4
___________________________________________________。
(2)步骤(ⅱ)中分离Mg(OH) 与母液的操作名称是___________,工业上通常采用向母液中
2
加入___________的方法来获得Mg(OH) 。
2
(3)写出步骤(ⅲ)主要反应的离子方程式______________________________;步骤(ⅳ)鼓入
热空气可将溴单质分离出来,是利用溴单质的__________性。
【答案】(1)BaCl Na CO 继续加入BaCl 溶液,若没有沉淀生成,说明SO 2-沉淀完
2 2 3 2 4
全 (2)过滤 石灰乳 (3)2Br-+Cl=Br +2Cl- 挥发性
2 2
【解析】海水蒸发、过滤,得到粗盐和母液;粗盐溶解,依次加入氢氧化钠、氯化钡、碳
酸钠除去除去粗盐中的Mg2+、Ca2+和SO 2-,经过滤、加足量盐酸,蒸发后获得精盐;母
4
液中加氢氧化钙,过滤分离出氢氧化镁沉淀;含有 NaBr的溶液中通氯气把NaBr氧化为
Br ,鼓入热空气,挥发出Br 蒸气,冷凝得粗溴。
2 2
(1)步骤(i)中,为除去粗盐中的Mg2+、Ca2+和SO 2-,沉淀上述离子时选用的沉淀剂依次
4
为过量NaOH溶液除Mg2+、加入过量BaCl 溶液除SO 2-、加入过量的NaCO 溶液除Ca2
2 4 2 3
+、Ba2+,经过滤、加足量盐酸,蒸发后获得精盐;继续加入BaCl 溶液,若没有沉淀生
2
成,说明SO 2-沉淀完全;
4
(2)步骤(ⅱ)中分离Mg(OH) 与母液的操作属于固液分离,名称是过滤;氯化镁和氢氧化
2
钙反应生成氢氧化镁沉淀和氯化钙,工业上通常采用向母液中加入石灰乳的方法来获得
Mg(OH) ;
2
(3)步骤(ⅲ)含有NaBr的溶液中通氯气把NaBr氧化为Br ,主要反应的离子方程式2Br-
2
+Cl=Br +2Cl-;溴的沸点低,易挥发,步骤(ⅳ)鼓入热空气可将溴单质分离出来,是利
2 2
用溴单质的挥发性。
直击高考
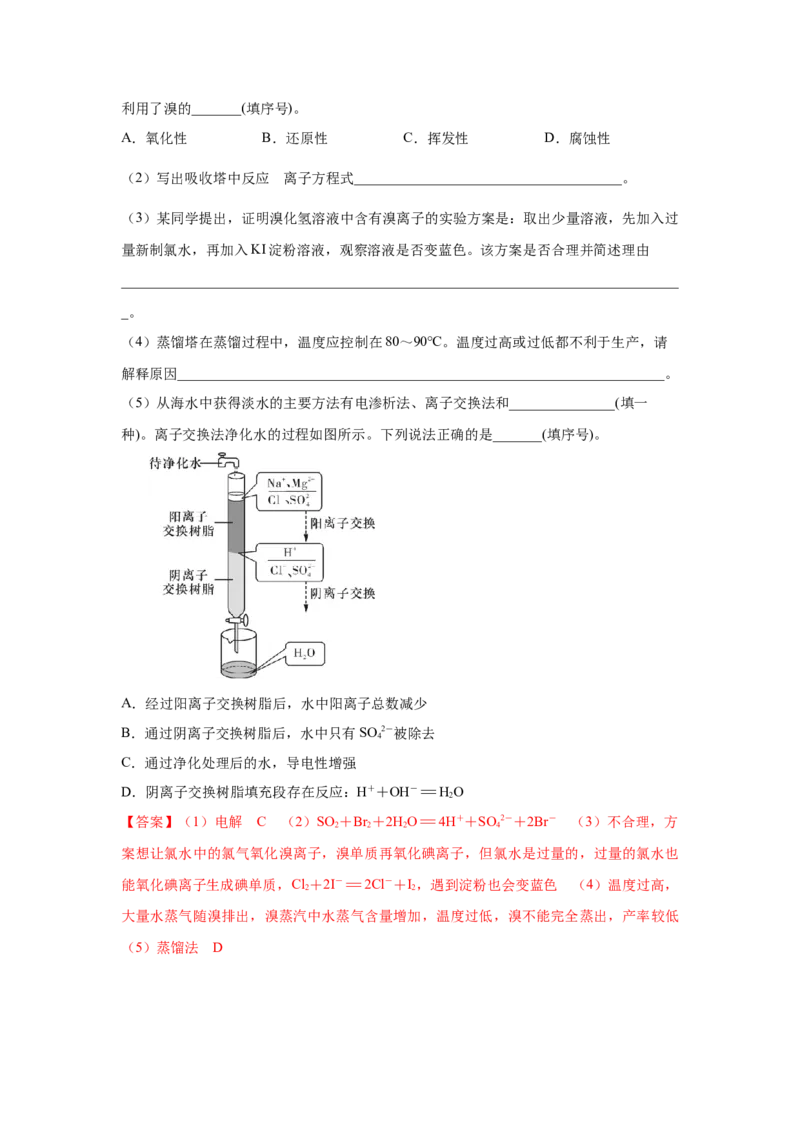
15.下图为海水资源综合开发利用的流程图:下列说法正确的是( )
A.过程a是粗盐的精制,除去租盐中的Ca2+、Mg2+、SO 2-,加入试剂的顺序是NaOH、
4
NaCO、BaCl ,过滤后加盐酸
2 3 2
B.在工业生产中常选用试剂①作Mg2+的沉淀剂,试剂①为KOH
C.过程b可证明还原性:Br->Cl-
D.过程c常用热还原法冶炼金属镁
【答案】C
【解析】A项,过程a是粗盐的精制,除去租盐中的Ca2+、Mg2+、SO 2-,加入试剂的顺
4
序是NaOH、BaCl 、NaCO,碳酸钠必须在氯化钡溶液之后添加,目的是除去过量的钡离
2 2 3
子,盐酸最后加入是为了过量的OH-、CO2-,错误;B项,KOH价格昂贵,工业上通常
3
用石灰乳作镁离子的沉淀剂,错误;C项,过程b中氯气将溴离子氧化为溴单质,氧化性
氯气大于溴单质,可证明还原性:Br->Cl-,正确;D项,过程c冶炼金属镁常采用电解
熔融氯化镁的方法,错误。
16.海洋是生命的摇篮,浩瀚的海洋中蕴藏着丰富的资源。人们可以从海水中提取淡水和
制得一些重要的化工产品。从海水提溴工艺流程如下图所示:
(1)工业上通过MgCl 制备Mg,常用的冶炼方法是____________。通入热空气吹出Br ,
2 2利用了溴的_______(填序号)。
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
的
(2)写出吸收塔中反应 离子方程式______________________________________。
(3)某同学提出,证明溴化氢溶液中含有溴离子的实验方案是:取出少量溶液,先加入过
量新制氯水,再加入KI淀粉溶液,观察溶液是否变蓝色。该方案是否合理并简述理由
_______________________________________________________________________________
_。
(4)蒸馏塔在蒸馏过程中,温度应控制在80~90℃。温度过高或过低都不利于生产,请
解释原因_____________________________________________________________________。
(5)从海水中获得淡水的主要方法有电渗析法、离子交换法和_______________(填一
种)。离子交换法净化水的过程如图所示。下列说法正确的是_______(填序号)。
A.经过阳离子交换树脂后,水中阳离子总数减少
B.通过阴离子交换树脂后,水中只有SO 2-被除去
4
C.通过净化处理后的水,导电性增强
D.阴离子交换树脂填充段存在反应:H++OH-=HO
2
【答案】(1)电解 C (2)SO +Br +2HO=4H++SO 2-+2Br- (3)不合理,方
2 2 2 4
案想让氯水中的氯气氧化溴离子,溴单质再氧化碘离子,但氯水是过量的,过量的氯水也
能氧化碘离子生成碘单质,Cl +2I-=2Cl-+I ,遇到淀粉也会变蓝色 (4)温度过高,
2 2
大量水蒸气随溴排出,溴蒸汽中水蒸气含量增加,温度过低,溴不能完全蒸出,产率较低
(5)蒸馏法 D