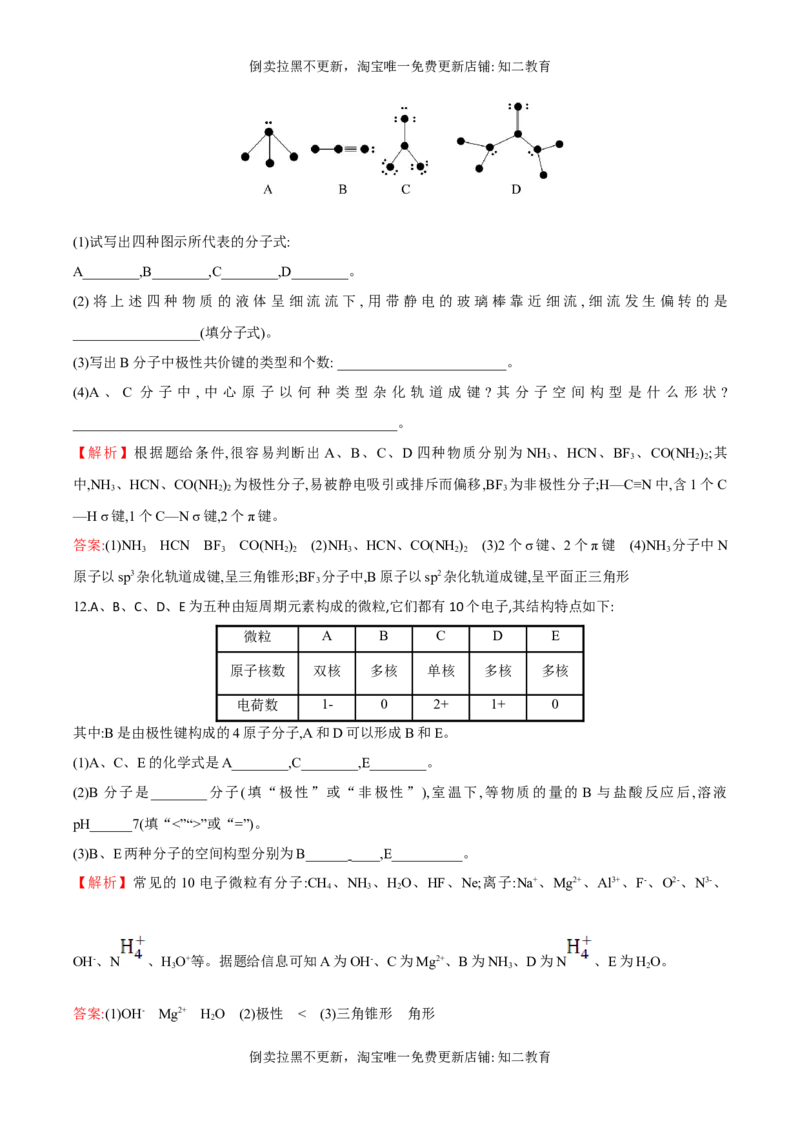
文档内容
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
2021-2022 学年高二化学重难点专题突破
模块二 分子结构与性质
专题 06 分子的空间结构和分子的性质
一、选择题
1.偶极矩是电荷量与正、负电荷重心间的距离的乘积。用偶极矩可判断分子的极性:一般来说极性分子的偶
极矩不为零;非极性分子的偶极矩是零。下列分子中偶极矩不为零的是 ( )
A.BeCl B.BF C.PCl D.CH
2 3 3 4
【答案】选C。
【解析】由题意可知,非极性分子的偶极矩为零,极性分子的偶极矩不为零。在题给四种分子中,只有PCl (结
3
构与NH 相似)是极性分子。
3
2.(双选)下列叙述正确的是 ( )
A.NH 、CO、CO 都是极性分子
3 2
B.CH 、CCl 都是含有极性键的非极性分子
4 4
C.HF、HCl、HBr、HI的稳定性依次减弱
D.CS 、HO、C H 都是直线形分子
2 2 2 2
【答案】选BC。
【解析】A项中CO 属于非极性分子;C项中HF、HCl、HBr、HI的稳定性依次减弱;D项中HO是角形结
2 2
构。
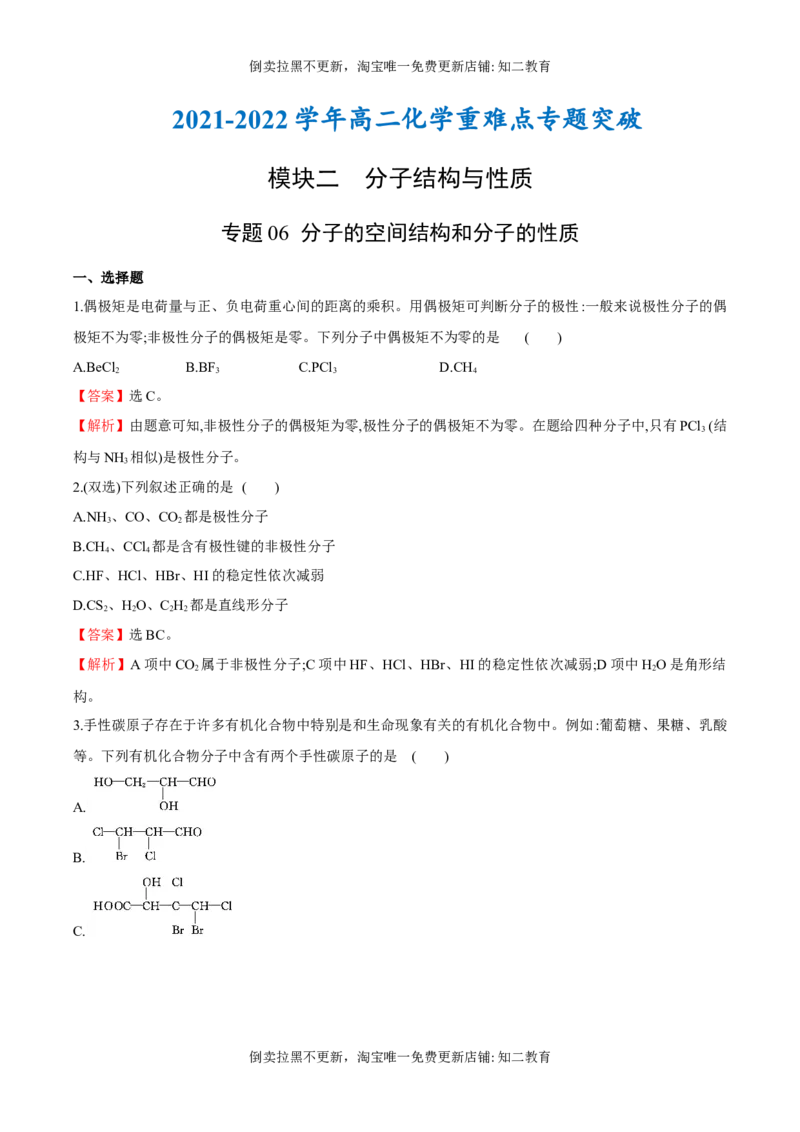
3.手性碳原子存在于许多有机化合物中特别是和生命现象有关的有机化合物中。例如:葡萄糖、果糖、乳酸
等。下列有机化合物分子中含有两个手性碳原子的是 ( )
A.
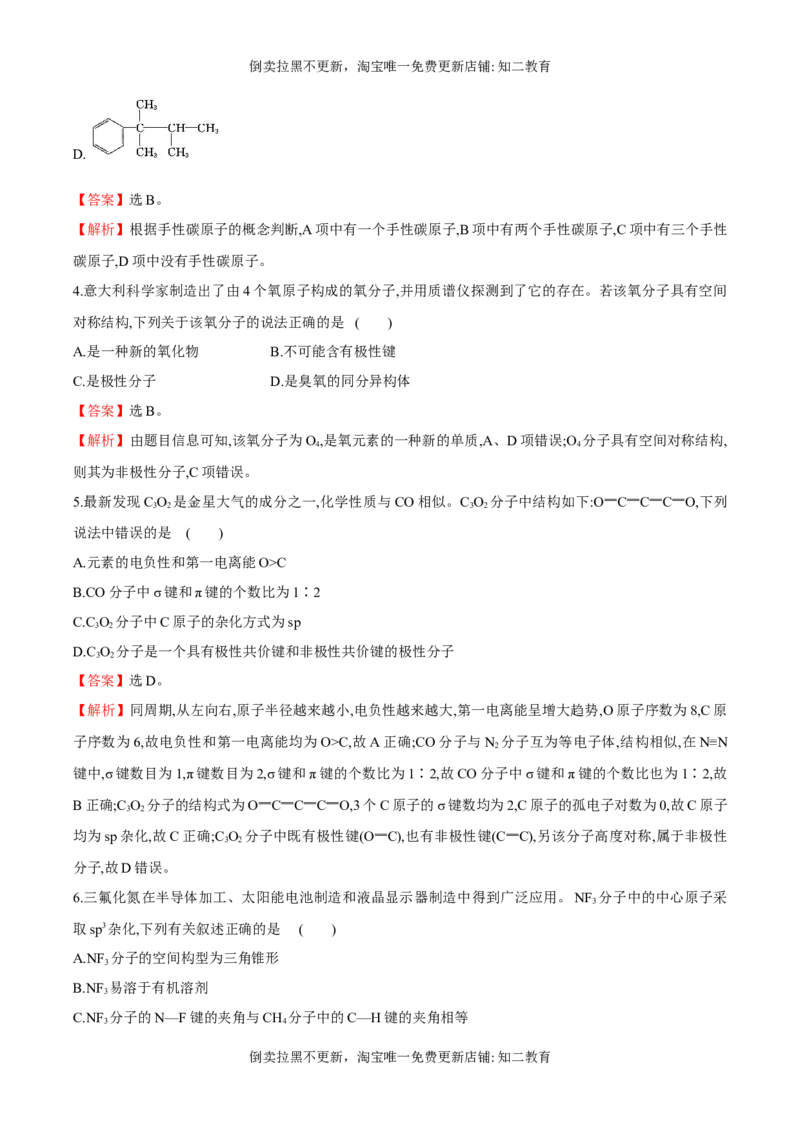
B.
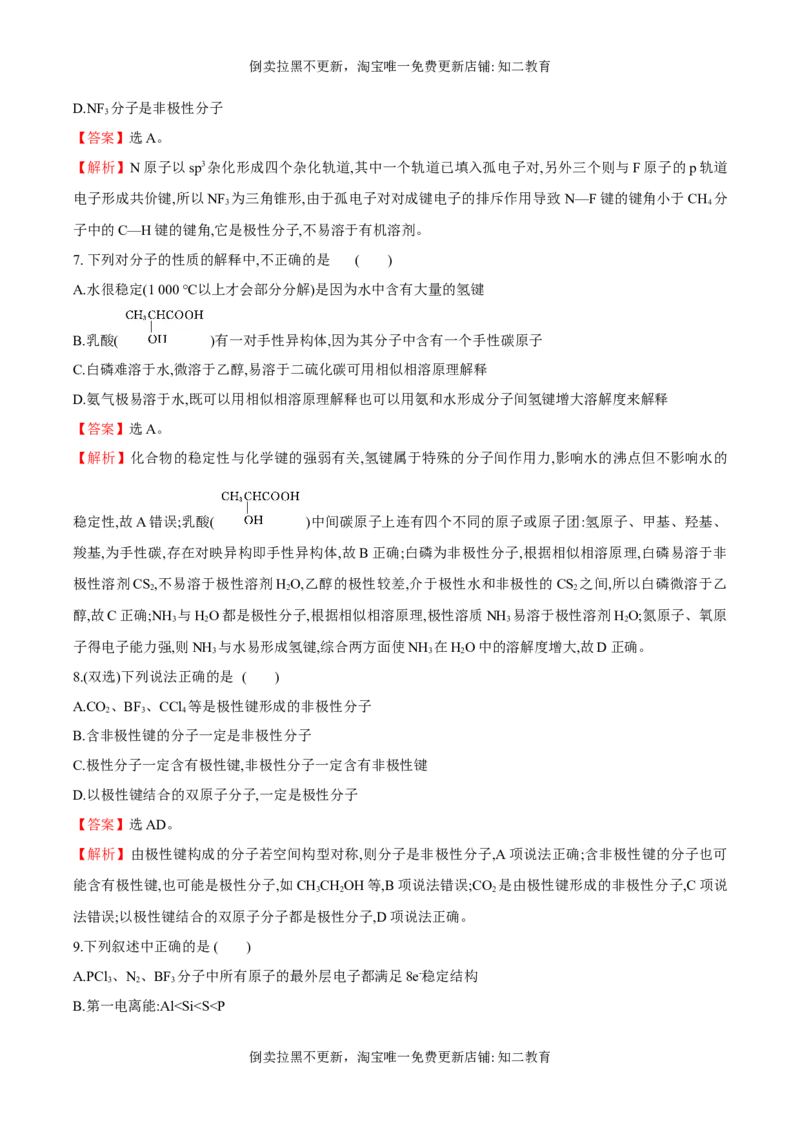
C.
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
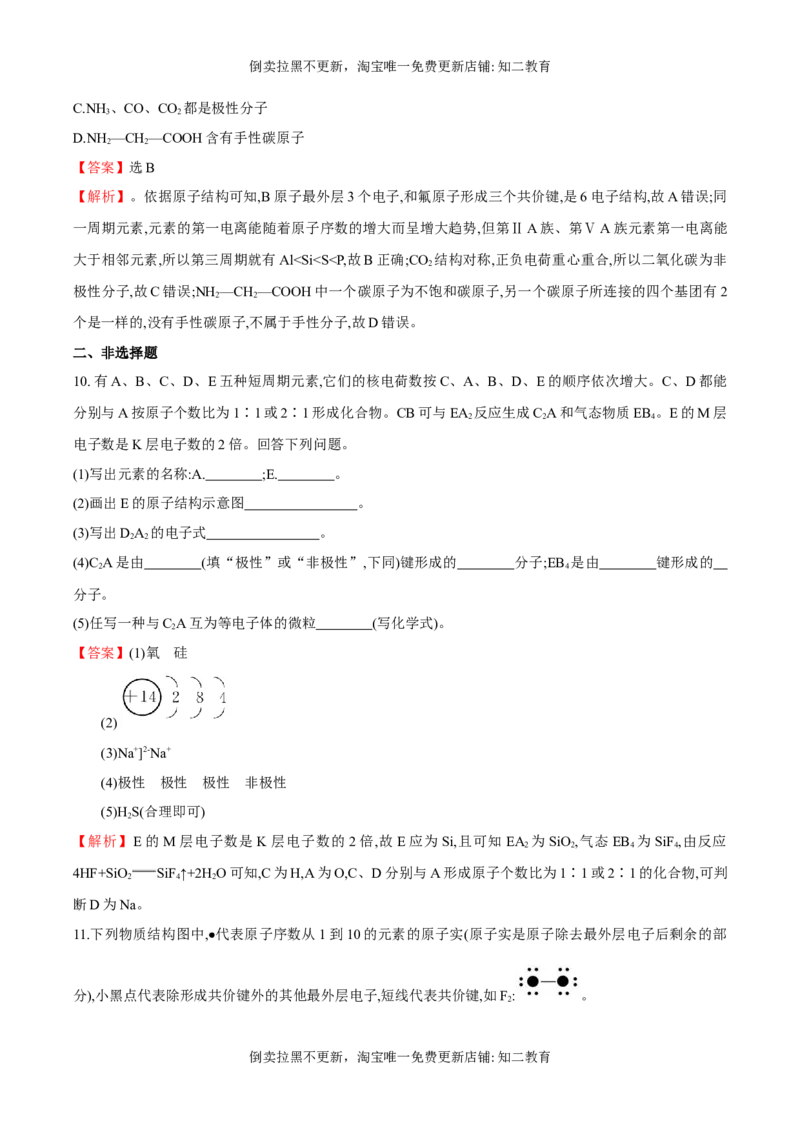
D.
【答案】选B。
【解析】根据手性碳原子的概念判断,A项中有一个手性碳原子,B项中有两个手性碳原子,C项中有三个手性
碳原子,D项中没有手性碳原子。
4.意大利科学家制造出了由4个氧原子构成的氧分子,并用质谱仪探测到了它的存在。若该氧分子具有空间
对称结构,下列关于该氧分子的说法正确的是 ( )
A.是一种新的氧化物 B.不可能含有极性键
C.是极性分子 D.是臭氧的同分异构体
【答案】选B。
【解析】由题目信息可知,该氧分子为O,是氧元素的一种新的单质,A、D项错误;O 分子具有空间对称结构,
4 4
则其为非极性分子,C项错误。
5.最新发现C O 是金星大气的成分之一,化学性质与CO相似。C O 分子中结构如下:O C C C O,下列
3 2 3 2
说法中错误的是 ( )
A.元素的电负性和第一电离能O>C
B.CO分子中σ键和π键的个数比为1∶2
C.C O 分子中C原子的杂化方式为sp
3 2
D.C O 分子是一个具有极性共价键和非极性共价键的极性分子
3 2
【答案】选D。
【解析】同周期,从左向右,原子半径越来越小,电负性越来越大,第一电离能呈增大趋势,O原子序数为8,C原
子序数为6,故电负性和第一电离能均为O>C,故A正确;CO分子与N 分子互为等电子体,结构相似,在N≡N
2
键中,σ键数目为1,π键数目为2,σ键和π键的个数比为1∶2,故CO分子中σ键和π键的个数比也为1∶2,故
B正确;C O 分子的结构式为O C C C O,3个C原子的σ键数均为2,C原子的孤电子对数为0,故C原子
3 2
均为sp杂化,故C正确;C O 分子中既有极性键(O C),也有非极性键(C C),另该分子高度对称,属于非极性
3 2
分子,故D错误。
6.三氟化氮在半导体加工、太阳能电池制造和液晶显示器制造中得到广泛应用。NF 分子中的中心原子采
3
取sp3杂化,下列有关叙述正确的是 ( )
A.NF 分子的空间构型为三角锥形
3
B.NF 易溶于有机溶剂
3
C.NF 分子的N—F键的夹角与CH 分子中的C—H键的夹角相等
3 4
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
D.NF 分子是非极性分子
3
【答案】选A。
【解析】N原子以sp3杂化形成四个杂化轨道,其中一个轨道已填入孤电子对,另外三个则与F原子的p轨道
电子形成共价键,所以NF 为三角锥形,由于孤电子对对成键电子的排斥作用导致 N—F键的键角小于CH 分
3 4
子中的C—H键的键角,它是极性分子,不易溶于有机溶剂。
7. 下列对分子的性质的解释中,不正确的是 ( )
A.水很稳定(1 000 ℃以上才会部分分解)是因为水中含有大量的氢键
B.乳酸( )有一对手性异构体,因为其分子中含有一个手性碳原子
C.白磷难溶于水,微溶于乙醇,易溶于二硫化碳可用相似相溶原理解释
D.氨气极易溶于水,既可以用相似相溶原理解释也可以用氨和水形成分子间氢键增大溶解度来解释
【答案】选A。
【解析】化合物的稳定性与化学键的强弱有关,氢键属于特殊的分子间作用力,影响水的沸点但不影响水的
稳定性,故A错误;乳酸( )中间碳原子上连有四个不同的原子或原子团:氢原子、甲基、羟基、
羧基,为手性碳,存在对映异构即手性异构体,故B正确;白磷为非极性分子,根据相似相溶原理,白磷易溶于非
极性溶剂CS,不易溶于极性溶剂HO,乙醇的极性较差,介于极性水和非极性的CS 之间,所以白磷微溶于乙
2 2 2
醇,故C正确;NH 与HO都是极性分子,根据相似相溶原理,极性溶质NH 易溶于极性溶剂HO;氮原子、氧原
3 2 3 2
子得电子能力强,则NH 与水易形成氢键,综合两方面使NH 在HO中的溶解度增大,故D正确。
3 3 2
8.(双选)下列说法正确的是 ( )
A.CO、BF、CCl 等是极性键形成的非极性分子
2 3 4
B.含非极性键的分子一定是非极性分子
C.极性分子一定含有极性键,非极性分子一定含有非极性键
D.以极性键结合的双原子分子,一定是极性分子
【答案】选AD。
【解析】由极性键构成的分子若空间构型对称,则分子是非极性分子,A项说法正确;含非极性键的分子也可
能含有极性键,也可能是极性分子,如CHCHOH等,B项说法错误;CO 是由极性键形成的非极性分子,C项说
3 2 2
法错误;以极性键结合的双原子分子都是极性分子,D项说法正确。
9.下列叙述中正确的是( )
A.PCl 、N、BF 分子中所有原子的最外层电子都满足8e-稳定结构
3 2 3
B.第一电离能:Al”或“=”)。
(3)B、E两种分子的空间构型分别为B______ ____,E__________。
【解析】常见的10电子微粒有分子:CH 、NH 、HO、HF、Ne;离子:Na+、Mg2+、Al3+、F-、O2-、N3-、
4 3 2
OH-、N 、HO+等。据题给信息可知A为OH-、C为Mg2+、B为NH 、D为N 、E为HO。
3 3 2
答案:(1)OH- Mg2+ HO (2)极性 < (3)三角锥形 角形
2
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
13.在极性分子中,正电荷重心与负电荷重心间的距离称为偶极长,通常用d表示。极性分子的极性强弱与偶
极长和电荷量(q)有关,一般用偶极矩(μ)来衡量。分子的偶极矩是偶极长和电荷量的乘积,即μ=dq。在非极性
分子中,其正、负电荷重心重合,故μ为0。试回答下列问题:
(1)HCl、CS、HS、SO 四种分子中μ=0的有___________________。
2 2 2
(2)实验测得:μ(PF )=1.03、μ(BCl )=0。
3 3
①由此可知,PF 分子的空间构型为________________;
3
②BCl 分子的空间构型为________________,
3
中心原子的杂化方式为________________。
(3)治癌药物Pt(NH )Cl 具有平面四边形结构,Pt处在四边形中心, NH 和Cl分别处在四边形的4个顶点。已
3 2 2 3
知该化合物有两种同分异构体,棕黄色化合物的μ>0,淡黄色化合物的μ=0。试写出两种同分异构体的结构简
式:________________、
______________________________, 在水中溶解度较大的是_______________(填结构简式)。
【解析】(1)HCl是由极性键形成的双原子极性分子;根据价电子对互斥理论可知,CS 是直线形分子,正、负
2
电荷重心重合,为非极性分子,其偶极矩为0;H S、SO 都是角形结构,是极性分子,其μ>0。(2)①μ(PF )=1.03说
2 2 3
明PF 是极性分子,则PF 是三角锥形结构。②μ(BCl )=0说明BCl 是非极性分子,其正、负电荷重心重合,应
3 3 3 3
该是平面正三角形结构;中心原子B与3个Cl原子形成3个共价键(没有孤电子对),即B的杂化方式是sp2杂
化。(3)根据题意,Pt(NH)Cl 具有平面四边形结构,若μ=0,则为非极性分子,NH 和Cl分别对称分布在四边形
3 2 2 3
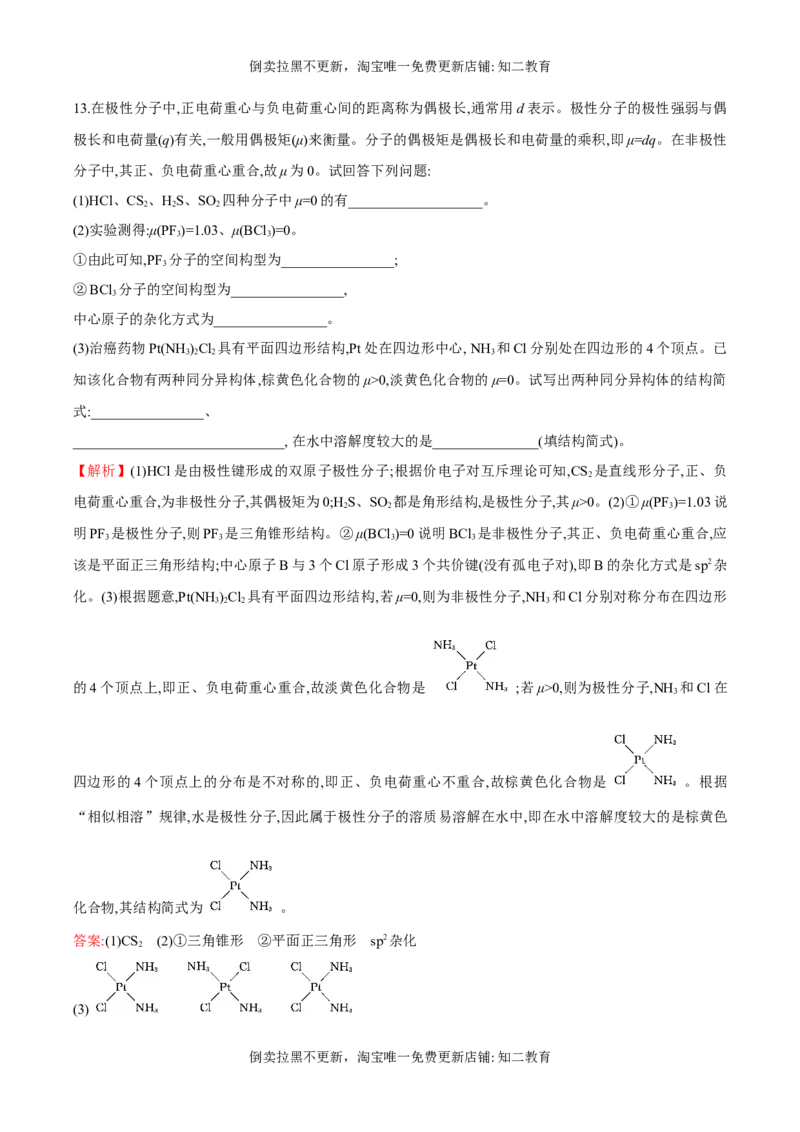
的4个顶点上,即正、负电荷重心重合,故淡黄色化合物是 ;若μ>0,则为极性分子,NH 和Cl在
3
四边形的4个顶点上的分布是不对称的,即正、负电荷重心不重合,故棕黄色化合物是 。根据
“相似相溶”规律,水是极性分子,因此属于极性分子的溶质易溶解在水中,即在水中溶解度较大的是棕黄色
化合物,其结构简式为 。
答案:(1)CS (2)①三角锥形 ②平面正三角形 sp2杂化
2
(3)
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
14.W、X、Y、Z四种短周期元素的原子序数依次增大。其中X原子的价电子排布式为2s22p2,Y原子的L电
子层中有三个未成对电子,且无空轨道;W、Z的原子序数相差10,且Z原子的第一电离能在同周期中最低。
回答下列问题:
(1)写出Y元素基态原子的最外层电子轨道表示式: ________________________;
(2)WXY分子中的三个原子除W原子外均为8电子结构,写出该分子的结构式:__ ___________, 根据电子云
重叠方式的不同,该分子里共价键的主要类型有___________________________________;
(3)YW 分子是一种常见气体,分子中Y原子的杂化方式是____________________,为________性分子,空间构
3
型为________形;
(4)液态的 YW 也是一种重要的溶剂,其性质与 HO 相似,Z 的单质与液态 YW 反应的化学方程式为
3 2 3
______________________________________________。
【解析】(1)X原子的核外电子排布式为1s22s22p2,则X为碳元素。Y原子的核外电子排布式为1s22s22p3,则Y
为氮元素。W、Z原子序数相差10,且Z原子的第一电离能在同周期中最低,则在短周期中只能为第1、3周
期,则W为氢元素,Z为钠元素。
(2)WXY为HCN,结构式为H—C≡N,三键中有一个σ键和两个π键。
(3)YW 为NH ,N的杂化方式为sp3杂化,NH 分子的空间构型为三角锥形。
3 3 3
(4)Na与液态NH 反应置换出其中的氢。
3
答案:(1)
(2)H—C≡N σ键、π键 (3)sp3杂化 极 三角锥
(4)2Na+2NH (l) 2NaNH +H ↑
3 2 2
15.回答下列问题:
(1)根据“相似相溶”原理,极性溶质能溶于极性溶剂,非极性溶质一般能溶于非极性溶剂。
①在a.苯、b.CH OH、c.HCHO、d.CS 、e.CCl 五种分子中,碳原子采取sp2杂化的分子有 (填字
3 2 4
母)。CS 分子的空间结构是 ,是 (填“极性”或“非极性”)分子。
2
②CrOCl 常温下为深红色液体,能与CCl 、CS 等互溶,据此可判断CrOCl 是 (填“极性”或“非
2 2 4 2 2 2
极性”)分子。
③金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO) ,Ni(CO) 分子呈正四面体结构。Ni(CO) 易
4 4 4
溶于下列 (填字母)。
a.水 b.CCl c.C H(苯) d.NiSO 溶液
4 6 6 4
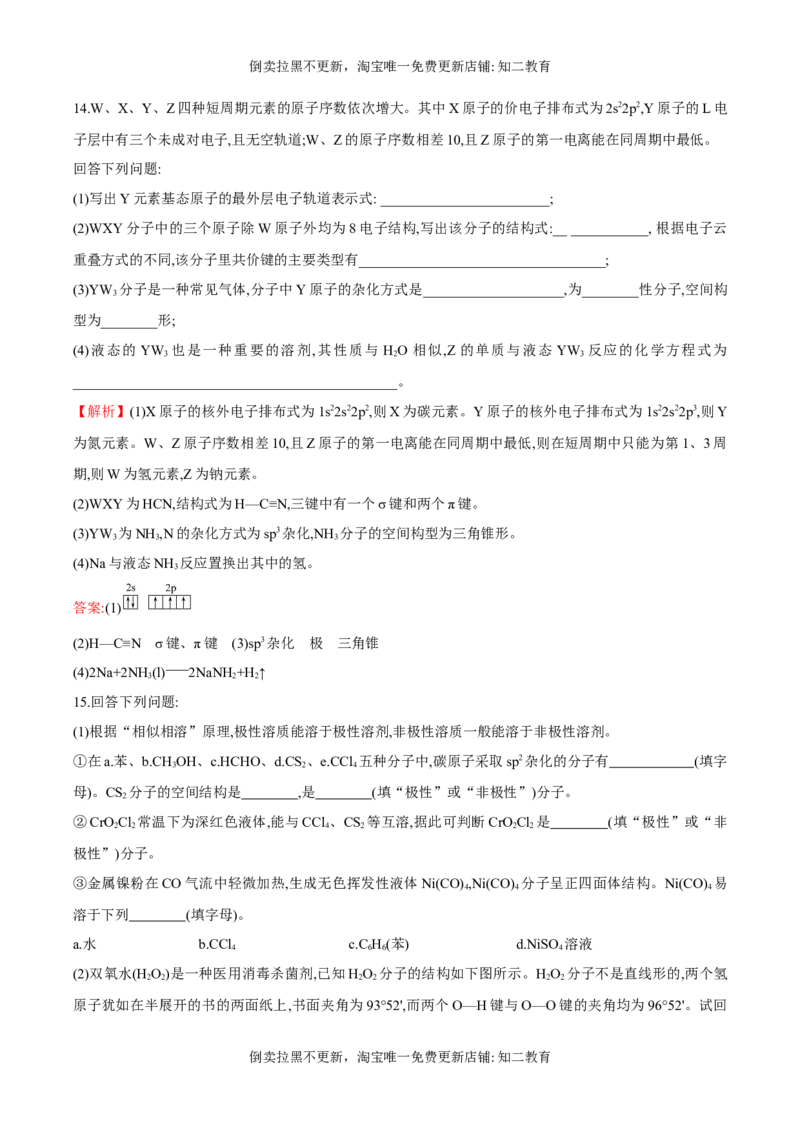
(2)双氧水(H O)是一种医用消毒杀菌剂,已知HO 分子的结构如下图所示。HO 分子不是直线形的,两个氢
2 2 2 2 2 2
原子犹如在半展开的书的两面纸上,书面夹角为93°52',而两个O—H键与O—O键的夹角均为96°52'。试回
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
答:
①下列关于HO 的说法中正确的是 (填字母)。
2 2
a.分子中有极性键
b.分子中有非极性键
c.氧原子的轨道发生sp2杂化
d.分子是非极性分子
②HO 分子的电子式为 。
2 2
③HO 分子中氧元素的化合价为 ,原因是 。
2 2
④HO 难溶于CS,主要原因是 。
2 2 2
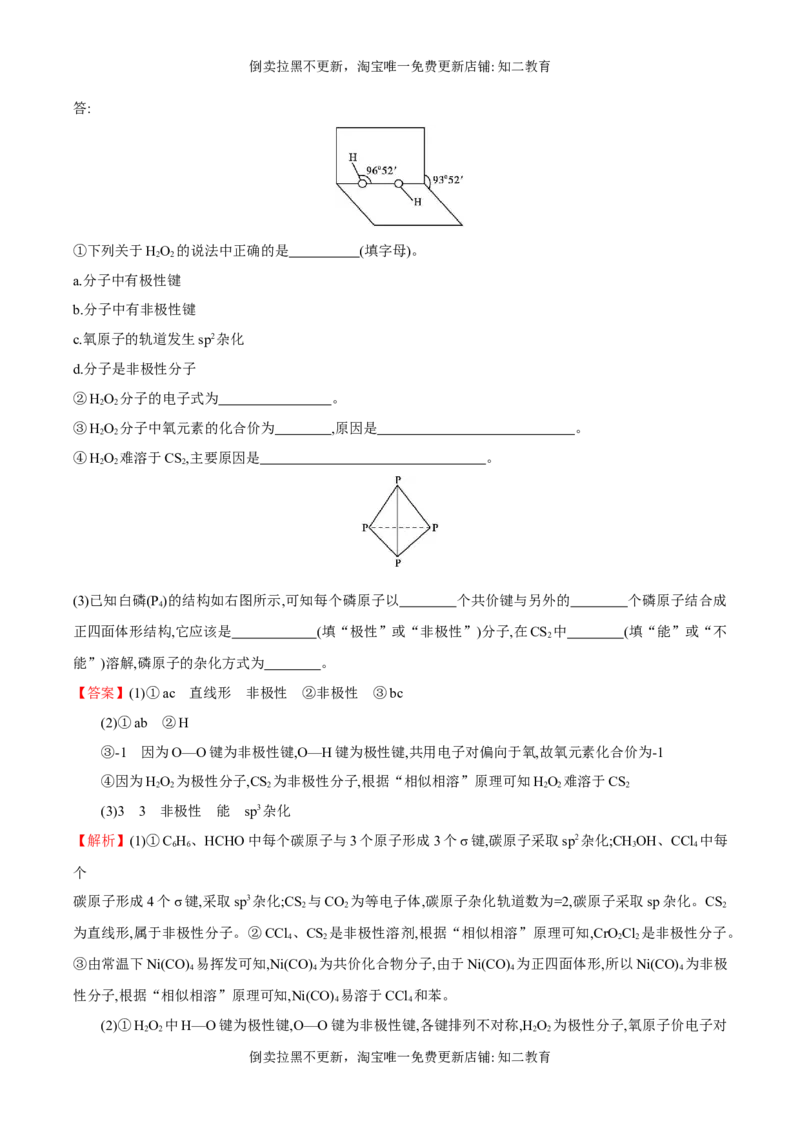
(3)已知白磷(P )的结构如右图所示,可知每个磷原子以 个共价键与另外的 个磷原子结合成
4
正四面体形结构,它应该是 (填“极性”或“非极性”)分子,在CS 中 (填“能”或“不
2
能”)溶解,磷原子的杂化方式为 。
【答案】(1)①ac 直线形 非极性 ②非极性 ③bc
(2)①ab ②H
③-1 因为O—O键为非极性键,O—H键为极性键,共用电子对偏向于氧,故氧元素化合价为-1
④因为HO 为极性分子,CS 为非极性分子,根据“相似相溶”原理可知HO 难溶于CS
2 2 2 2 2 2
(3)3 3 非极性 能 sp3杂化
【解析】(1)①C H 、HCHO中每个碳原子与3个原子形成3个σ键,碳原子采取sp2杂化;CH OH、CCl 中每
6 6 3 4
个
碳原子形成4个σ键,采取sp3杂化;CS 与CO 为等电子体,碳原子杂化轨道数为=2,碳原子采取sp杂化。CS
2 2 2
为直线形,属于非极性分子。②CCl 、CS 是非极性溶剂,根据“相似相溶”原理可知,CrO Cl 是非极性分子。
4 2 2 2
③由常温下Ni(CO) 易挥发可知,Ni(CO) 为共价化合物分子,由于Ni(CO) 为正四面体形,所以Ni(CO) 为非极
4 4 4 4
性分子,根据“相似相溶”原理可知,Ni(CO) 易溶于CCl 和苯。
4 4
(2)①HO 中H—O键为极性键,O—O键为非极性键,各键排列不对称,H O 为极性分子,氧原子价电子对
2 2 2 2
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
数为=4,氧原子采取sp3杂化。②由HO 的分子结构可知,其电子式为H。③通过共用电子对发生的偏移可判
2 2
断元素在化合物中的化合价。④HO 为极性分子,CS 为非极性分子,根据相似相溶原理可知HO 难溶于
2 2 2 2 2
CS。
2
(3)P 分子中每个磷原子与3个磷原子以3个共价键结合成正四面体形结构,各键排列对称,属非极性分
4
子,CS 是直线形分子,属非极性分子,故P 易溶于CS 。磷原子形成3个σ键,且有一对孤电子对,所以磷原子
2 4 2
采取sp3杂化。
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育