文档内容
第 14 讲 氯气的实验室制法、氯离子的检验
知识导航
课前引入
自然界中是否存在氯气?
氯气是被谁发现的?怎样发现的?
知识精讲
一、氯气的实验室制法
1. 基本原理与装置
试剂
浓盐酸+强氧化性物质(如MnO 、KMnO 、KClO 等)
选择 2 4 3
实
实
方 验
验
程 装
原
式 置
理
图
装置
固液加热型发生装置/固液不加热型发生装置
选择
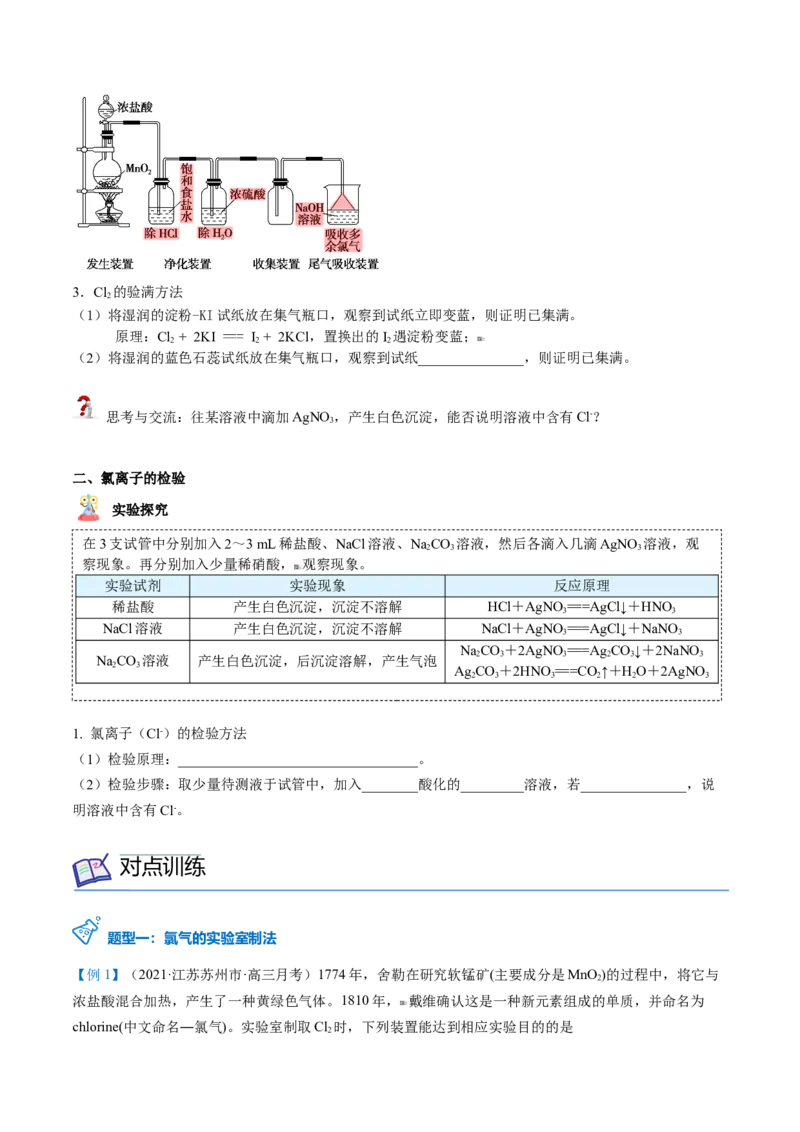
2. 制备氯气的优化装置3.Cl 的验满方法
2
(1)将湿润的淀粉-KI试纸放在集气瓶口,观察到试纸立即变蓝,则证明已集满。
原理:Cl + 2KI === I + 2KCl,置换出的I 遇淀粉变蓝;
2 2 2
(2)将湿润的蓝色石蕊试纸放在集气瓶口,观察到试纸_______________,则证明已集满。
思考与交流:往某溶液中滴加AgNO,产生白色沉淀,能否说明溶液中含有Cl-?
3
二、氯离子的检验
实验探究
在3支试管中分别加入2~3 mL稀盐酸、NaCl溶液、NaCO 溶液,然后各滴入几滴AgNO 溶液,观
2 3 3
察现象。再分别加入少量稀硝酸, 观察现象。
实验试剂 实验现象 反应原理
稀盐酸 产生白色沉淀,沉淀不溶解 HCl+AgNO===AgCl↓+HNO
3 3
NaCl溶液 产生白色沉淀,沉淀不溶解 NaCl+AgNO===AgCl↓+NaNO
3 3
NaCO+2AgNO===Ag CO↓+2NaNO
NaCO 溶液 产生白色沉淀,后沉淀溶解,产生气泡 2 3 3 2 3 3
2 3 Ag CO+2HNO===CO ↑+HO+2AgNO
2 3 3 2 2 3
1. 氯离子(Cl-)的检验方法
(1)检验原理:__________________________________。
(2)检验步骤:取少量待测液于试管中,加入________酸化的_________溶液,若_______________,说
明溶液中含有Cl-。
对点训练
题型一:氯气的实验室制法
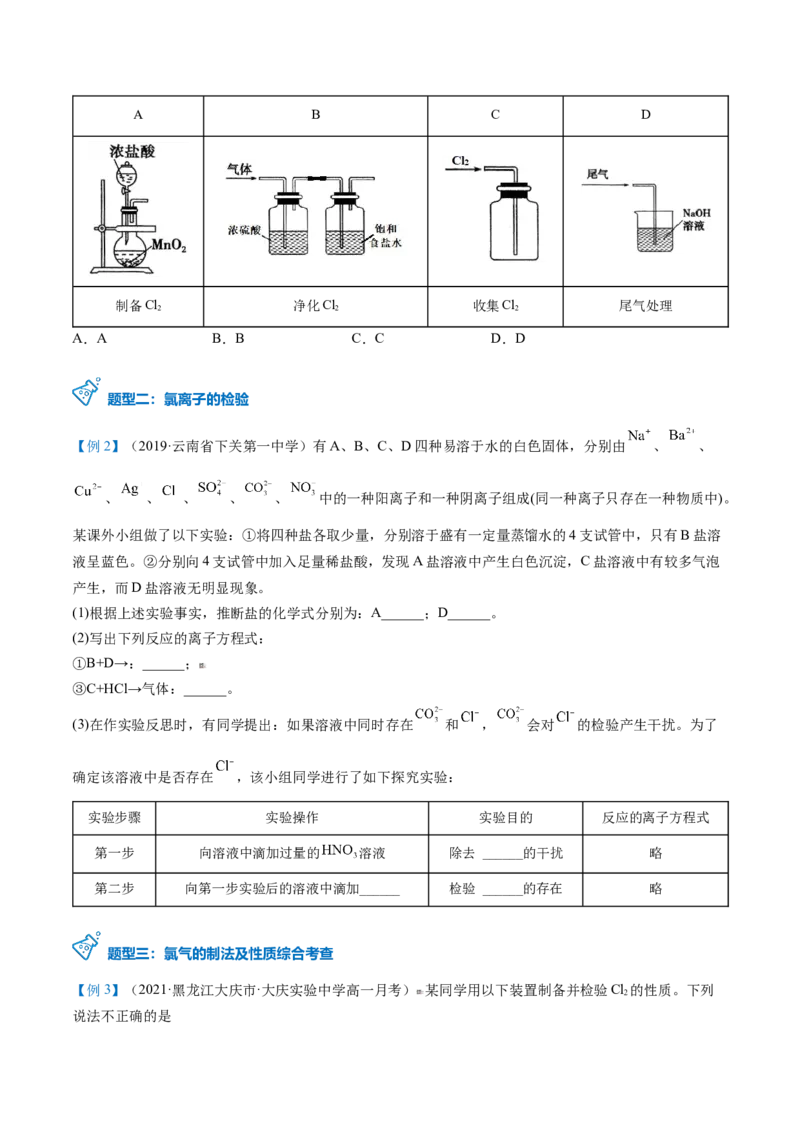
【例1】(2021·江苏苏州市·高三月考)1774年,舍勒在研究软锰矿(主要成分是MnO )的过程中,将它与
2
浓盐酸混合加热,产生了一种黄绿色气体。1810年, 戴维确认这是一种新元素组成的单质,并命名为
chlorine(中文命名―氯气)。实验室制取Cl 时,下列装置能达到相应实验目的的是
2A B C D
制备Cl 净化Cl 收集Cl 尾气处理
2 2 2
A.A B.B C.C D.D
题型二:氯离子的检验
【例2】(2019·云南省下关第一中学)有A、B、C、D四种易溶于水的白色固体,分别由 、 、
、 、 、 、 、 中的一种阳离子和一种阴离子组成(同一种离子只存在一种物质中)。
某课外小组做了以下实验:①将四种盐各取少量,分别溶于盛有一定量蒸馏水的4支试管中,只有B盐溶
液呈蓝色。②分别向4支试管中加入足量稀盐酸,发现A盐溶液中产生白色沉淀,C盐溶液中有较多气泡
产生,而D盐溶液无明显现象。
(1)根据上述实验事实,推断盐的化学式分别为:A______;D______。
(2)写出下列反应的离子方程式:
①B+D→:______;
③C+HCl→气体:______。
(3)在作实验反思时,有同学提出:如果溶液中同时存在 和 , 会对 的检验产生干扰。为了
确定该溶液中是否存在 ,该小组同学进行了如下探究实验:
实验步骤 实验操作 实验目的 反应的离子方程式
第一步 向溶液中滴加过量的 溶液 除去 ______的干扰 略
第二步 向第一步实验后的溶液中滴加______ 检验 ______的存在 略
题型三:氯气的制法及性质综合考查
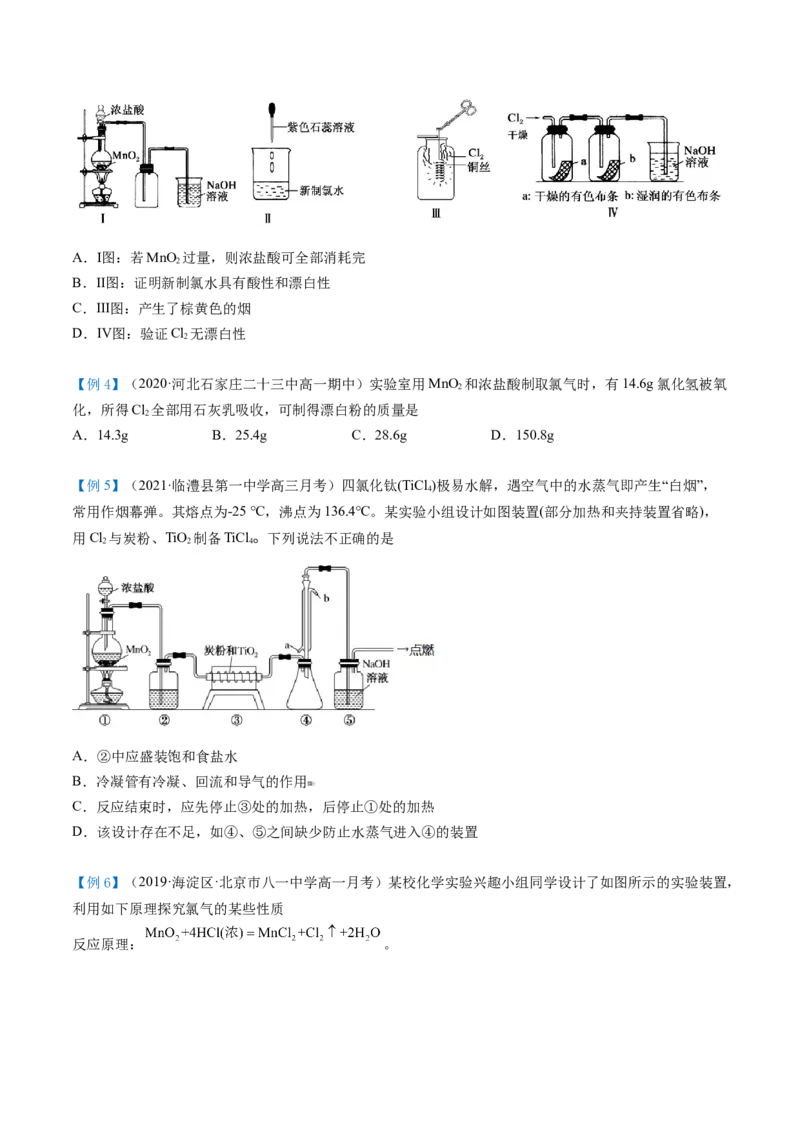
【例3】(2021·黑龙江大庆市·大庆实验中学高一月考) 某同学用以下装置制备并检验Cl 的性质。下列
2
说法不正确的是A.Ⅰ图:若MnO 过量,则浓盐酸可全部消耗完
2
B.Ⅱ图:证明新制氯水具有酸性和漂白性
C.Ⅲ图:产生了棕黄色的烟
D.Ⅳ图:验证Cl 无漂白性
2
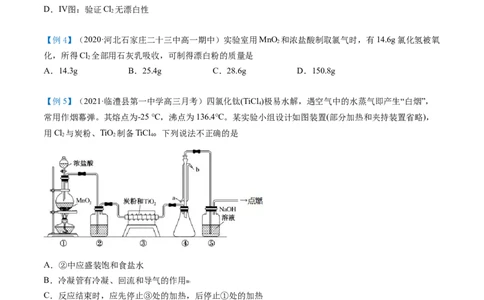
【例4】(2020·河北石家庄二十三中高一期中)实验室用MnO 和浓盐酸制取氯气时,有14.6g氯化氢被氧
2
化,所得Cl 全部用石灰乳吸收,可制得漂白粉的质量是
2
A.14.3g B.25.4g C.28.6g D.150.8g
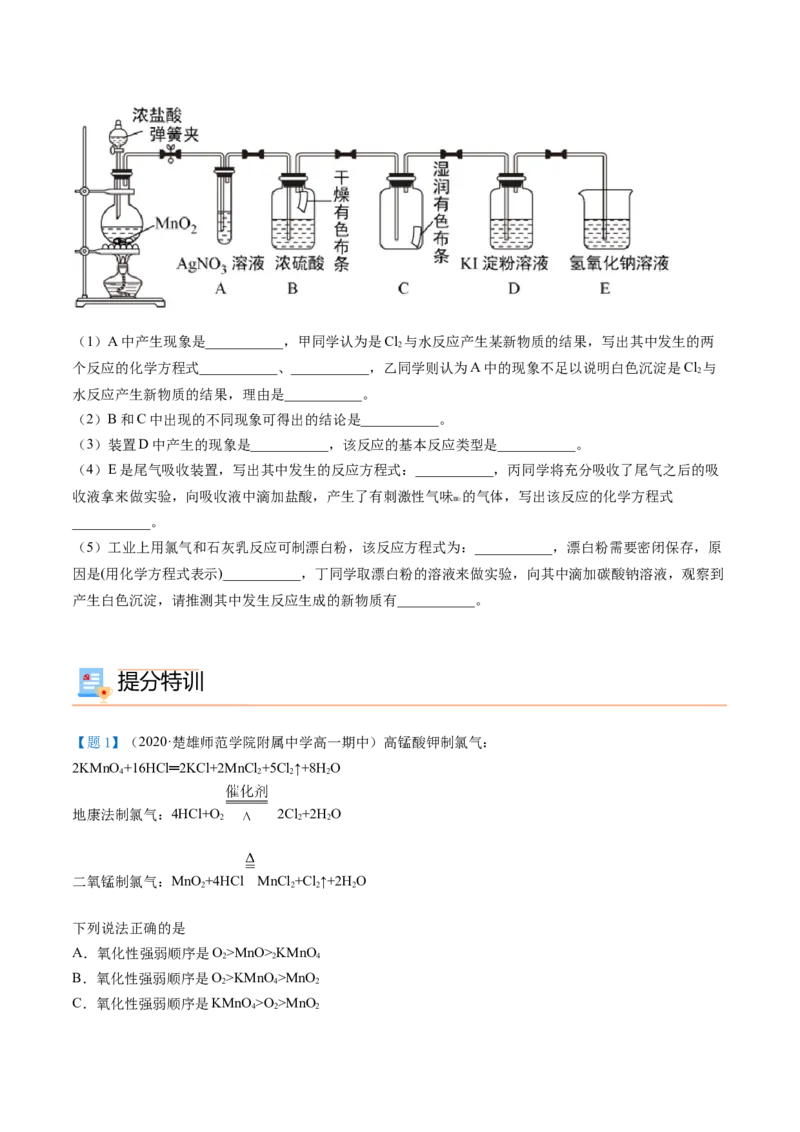
【例5】(2021·临澧县第一中学高三月考)四氯化钛(TiCl )极易水解,遇空气中的水蒸气即产生“白烟”,
4
常用作烟幕弹。其熔点为-25 ℃,沸点为136.4℃。某实验小组设计如图装置(部分加热和夹持装置省略),
用Cl 与炭粉、TiO 制备TiCl 。下列说法不正确的是
2 2 4
A.②中应盛装饱和食盐水
B.冷凝管有冷凝、回流和导气的作用
C.反应结束时,应先停止③处的加热,后停止①处的加热
D.该设计存在不足,如④、⑤之间缺少防止水蒸气进入④的装置
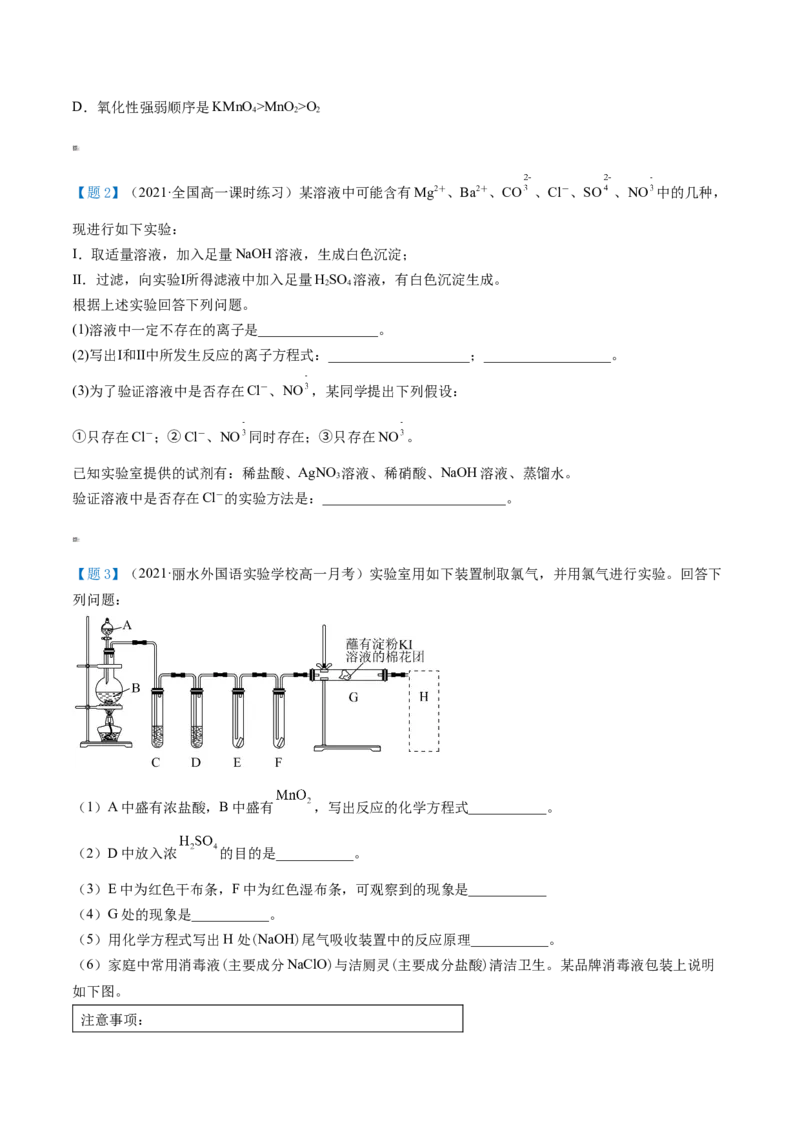
【例6】(2019·海淀区·北京市八一中学高一月考)某校化学实验兴趣小组同学设计了如图所示的实验装置,
利用如下原理探究氯气的某些性质
反应原理: 。(1)A中产生现象是___________,甲同学认为是Cl 与水反应产生某新物质的结果,写出其中发生的两
2
个反应的化学方程式___________、___________,乙同学则认为A中的现象不足以说明白色沉淀是Cl 与
2
水反应产生新物质的结果,理由是___________。
(2)B和C中出现的不同现象可得出的结论是___________。
(3)装置D中产生的现象是___________,该反应的基本反应类型是___________。
(4)E是尾气吸收装置,写出其中发生的反应方程式:___________,丙同学将充分吸收了尾气之后的吸
收液拿来做实验,向吸收液中滴加盐酸,产生了有刺激性气味 的气体,写出该反应的化学方程式
___________。
(5)工业上用氯气和石灰乳反应可制漂白粉,该反应方程式为:___________,漂白粉需要密闭保存,原
因是(用化学方程式表示)___________,丁同学取漂白粉的溶液来做实验,向其中滴加碳酸钠溶液,观察到
产生白色沉淀,请推测其中发生反应生成的新物质有___________。
提分特训
【题1】(2020·楚雄师范学院附属中学高一期中)高锰酸钾制氯气:
2KMnO +16HCl═2KCl+2MnCl +5Cl↑+8H O
4 2 2 2
地康法制氯气:4HCl+O 2Cl +2H O
2 2 2
二氧锰制氯气:MnO +4HCl MnCl +Cl↑+2H O
2 2 2 2
下列说法正确的是
A.氧化性强弱顺序是O>MnO> KMnO
2 2 4
B.氧化性强弱顺序是O>KMnO >MnO
2 4 2
C.氧化性强弱顺序是KMnO >O >MnO
4 2 2D.氧化性强弱顺序是KMnO >MnO>O
4 2 2
【题2】(2021·全国高一课时练习)某溶液中可能含有Mg2+、Ba2+、CO 、Cl-、SO 、NO 中的几种,
现进行如下实验:
Ⅰ.取适量溶液,加入足量NaOH溶液,生成白色沉淀;
Ⅱ.过滤,向实验Ⅰ所得滤液中加入足量HSO 溶液,有白色沉淀生成。
2 4
根据上述实验回答下列问题。
(1)溶液中一定不存在的离子是_________________。
(2)写出Ⅰ和Ⅱ中所发生反应的离子方程式:____________________;__________________。
(3)为了验证溶液中是否存在Cl-、NO ,某同学提出下列假设:
①只存在Cl-;②Cl-、NO 同时存在;③只存在NO 。
已知实验室提供的试剂有:稀盐酸、AgNO 溶液、稀硝酸、NaOH溶液、蒸馏水。
3
验证溶液中是否存在Cl-的实验方法是:__________________________。
【题3】(2021·丽水外国语实验学校高一月考)实验室用如下装置制取氯气,并用氯气进行实验。回答下
列问题:
(1)A中盛有浓盐酸,B中盛有 ,写出反应的化学方程式___________。
(2)D中放入浓 的目的是___________。
(3)E中为红色干布条,F中为红色湿布条,可观察到的现象是___________
(4)G处的现象是___________。
(5)用化学方程式写出H处(NaOH)尾气吸收装置中的反应原理___________。
(6)家庭中常用消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)清洁卫生。某品牌消毒液包装上说明
如下图。
注意事项:1、本品对棉织品有漂白脱色作用,对金属制品有腐蚀作用。
2、密封保存,请勿与洁厕灵同时使用。
3、保质期为一年。
消毒液与洁厕灵不能同时使用,原因是(可用文字说明,也可用离子方程式表示)___________。
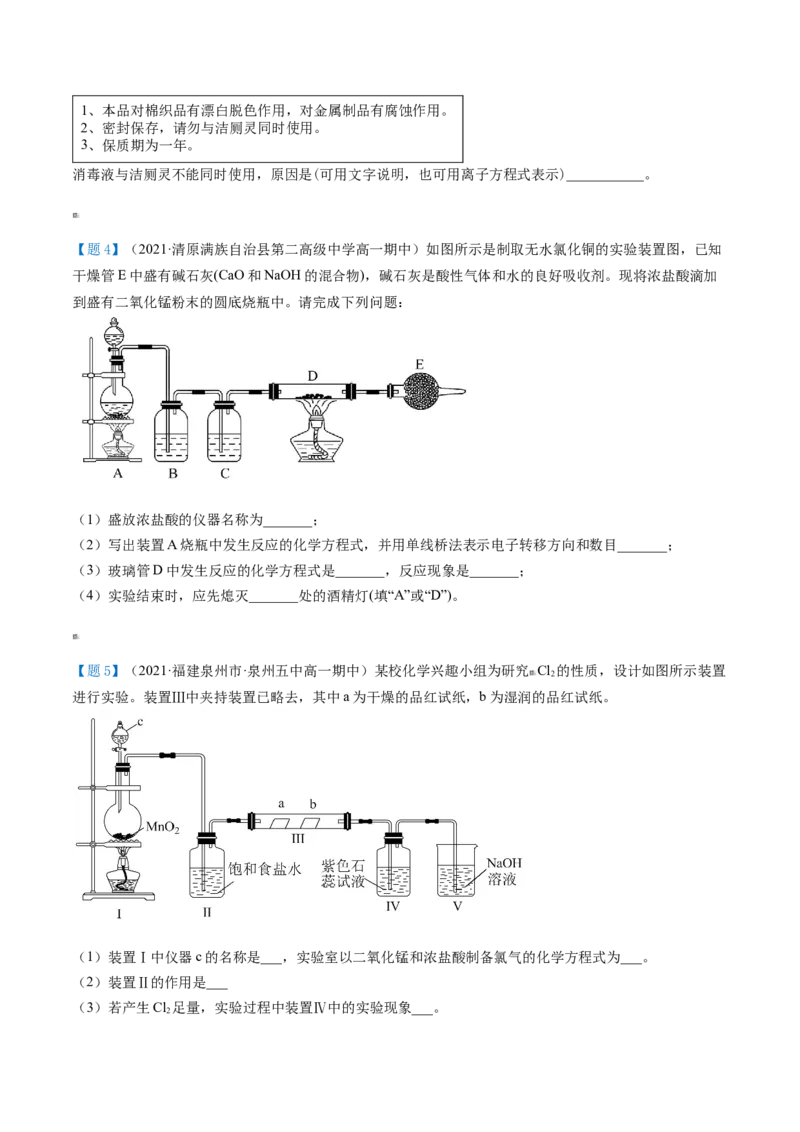
【题4】(2021·清原满族自治县第二高级中学高一期中)如图所示是制取无水氯化铜的实验装置图,已知
干燥管E中盛有碱石灰(CaO和NaOH的混合物),碱石灰是酸性气体和水的良好吸收剂。现将浓盐酸滴加
到盛有二氧化锰粉末的圆底烧瓶中。请完成下列问题:
(1)盛放浓盐酸的仪器名称为_______;
(2)写出装置A烧瓶中发生反应的化学方程式,并用单线桥法表示电子转移方向和数目_______;
(3)玻璃管D中发生反应的化学方程式是_______,反应现象是_______;
(4)实验结束时,应先熄灭_______处的酒精灯(填“A”或“D”)。
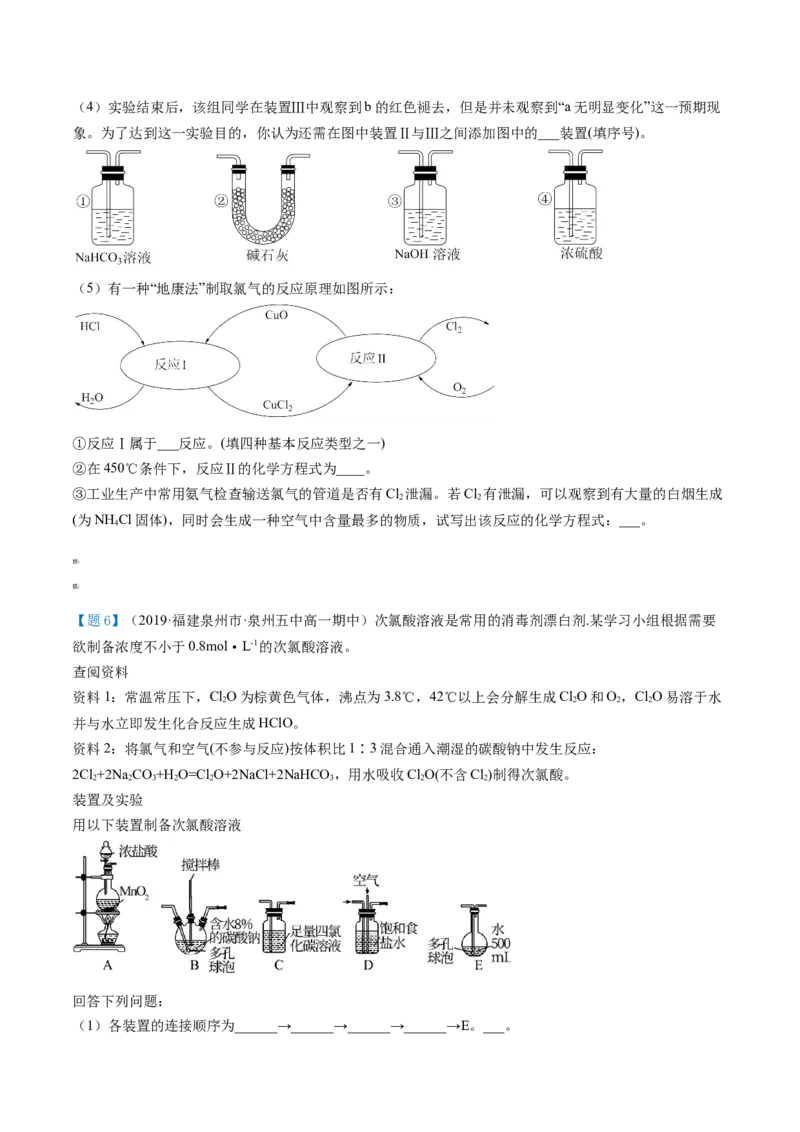
【题5】(2021·福建泉州市·泉州五中高一期中)某校化学兴趣小组为研究 Cl 的性质,设计如图所示装置
2
进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
(1)装置Ⅰ中仪器c的名称是___,实验室以二氧化锰和浓盐酸制备氯气的化学方程式为___。
(2)装置Ⅱ的作用是___
(3)若产生Cl 足量,实验过程中装置Ⅳ中的实验现象___。
2(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现
象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的___装置(填序号)。
(5)有一种“地康法”制取氯气的反应原理如图所示:
①反应Ⅰ属于___反应。(填四种基本反应类型之一)
②在450℃条件下,反应Ⅱ的化学方程式为____。
③工业生产中常用氨气检查输送氯气的管道是否有Cl 泄漏。若Cl 有泄漏,可以观察到有大量的白烟生成
2 2
(为NH Cl固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式:___。
4
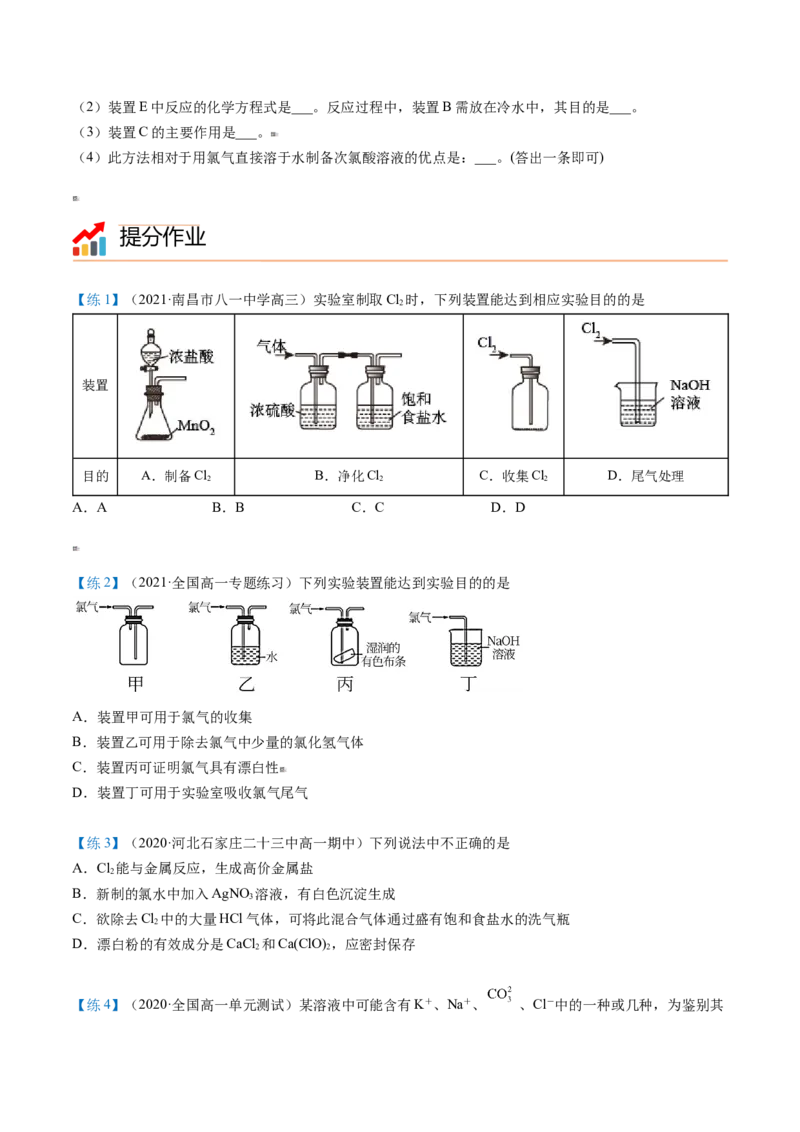
【题6】(2019·福建泉州市·泉州五中高一期中)次氯酸溶液是常用的消毒剂漂白剂.某学习小组根据需要
欲制备浓度不小于0.8mol·L-1的次氯酸溶液。
查阅资料
资料1:常温常压下,ClO为棕黄色气体,沸点为3.8℃,42℃以上会分解生成ClO和O,ClO易溶于水
2 2 2 2
并与水立即发生化合反应生成HClO。
资料2:将氯气和空气(不参与反应)按体积比1∶3混合通入潮湿的碳酸钠中发生反应:
2Cl+2Na CO+H O=Cl O+2NaCl+2NaHCO ,用水吸收ClO(不含Cl)制得次氯酸。
2 2 3 2 2 3 2 2
装置及实验
用以下装置制备次氯酸溶液
回答下列问题:
(1)各装置的连接顺序为______→______→______→______→E。___。(2)装置E中反应的化学方程式是___。反应过程中,装置B需放在冷水中,其目的是___。
(3)装置C的主要作用是___。
(4)此方法相对于用氯气直接溶于水制备次氯酸溶液的优点是:___。(答出一条即可)
提分作业
【练1】(2021·南昌市八一中学高三)实验室制取Cl 时,下列装置能达到相应实验目的的是
2
装置
目的 A.制备Cl B.净化Cl C.收集Cl D.尾气处理
2 2 2
A.A B.B C.C D.D
【练2】(2021·全国高一专题练习)下列实验装置能达到实验目的的是
A.装置甲可用于氯气的收集
B.装置乙可用于除去氯气中少量的氯化氢气体
C.装置丙可证明氯气具有漂白性
D.装置丁可用于实验室吸收氯气尾气
【练3】(2020·河北石家庄二十三中高一期中)下列说法中不正确的是
A.Cl 能与金属反应,生成高价金属盐
2
B.新制的氯水中加入AgNO 溶液,有白色沉淀生成
3
C.欲除去Cl 中的大量HCl气体,可将此混合气体通过盛有饱和食盐水的洗气瓶
2
D.漂白粉的有效成分是CaCl 和Ca(ClO) ,应密封保存
2 2
【练4】(2020·全国高一单元测试)某溶液中可能含有K+、Na+、 、Cl-中的一种或几种,为鉴别其中所含离子,现进行如下实验:
序号 实验操作及现象
步骤① 取原溶液,进行焰色反应,显黄色,透过蓝色钴玻璃观察无紫色
步骤② 取原溶液,向溶液中加入盐酸,有气体产生
请回答下列问题:
(1)原溶液中一定存在的离子是______(填离子符号,下同),一定不存在的离子是______________,可能存
在的离子是__________________。
(2)为进一步确定原溶液中可能存在的离子是否存在,应进行的实验操作及判断依据是_________
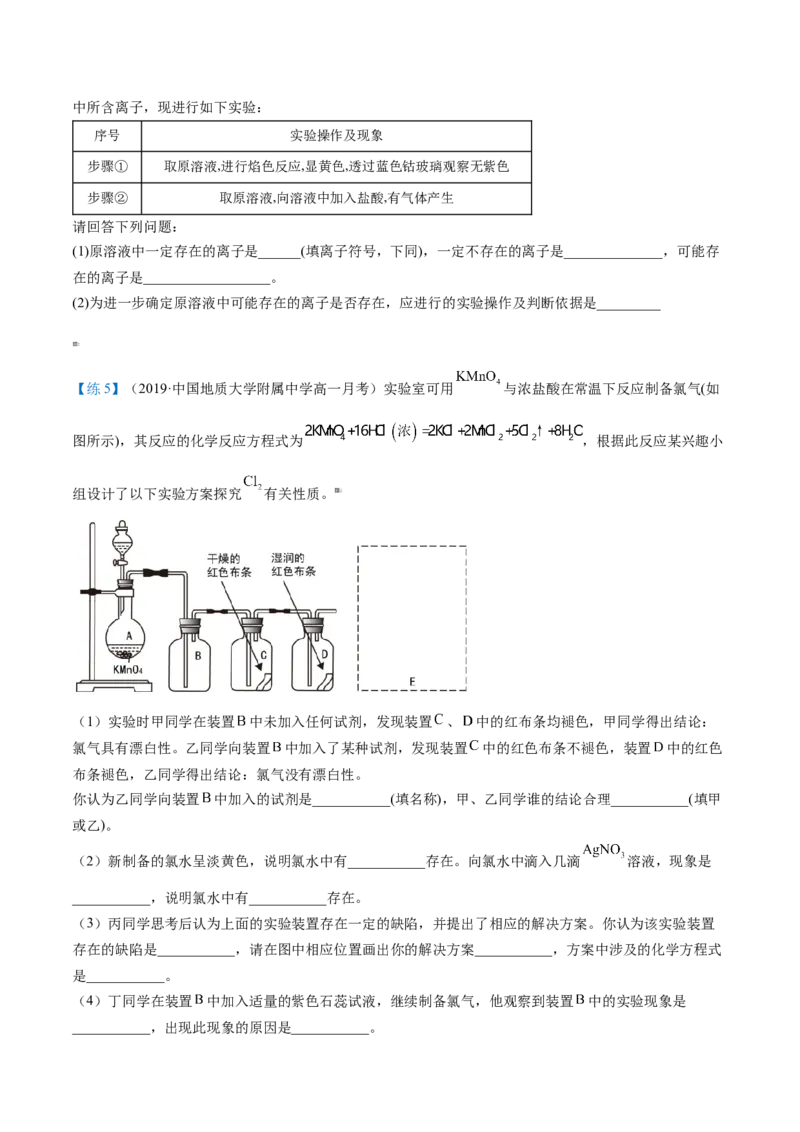
【练5】(2019·中国地质大学附属中学高一月考)实验室可用 与浓盐酸在常温下反应制备氯气(如
图所示),其反应的化学反应方程式为 ,根据此反应某兴趣小
组设计了以下实验方案探究 有关性质。
(1)实验时甲同学在装置 中未加入任何试剂,发现装置 、 中的红布条均褪色,甲同学得出结论:
氯气具有漂白性。乙同学向装置 中加入了某种试剂,发现装置 中的红色布条不褪色,装置 中的红色
布条褪色,乙同学得出结论:氯气没有漂白性。
你认为乙同学向装置 中加入的试剂是___________(填名称),甲、乙同学谁的结论合理___________(填甲
或乙)。
(2)新制备的氯水呈淡黄色,说明氯水中有___________存在。向氯水中滴入几滴 溶液,现象是
___________,说明氯水中有___________存在。
(3)丙同学思考后认为上面的实验装置存在一定的缺陷,并提出了相应的解决方案。你认为该实验装置
存在的缺陷是___________,请在图中相应位置画出你的解决方案___________,方案中涉及的化学方程式
是___________。
(4)丁同学在装置 中加入适量的紫色石蕊试液,继续制备氯气,他观察到装置 中的实验现象是
___________,出现此现象的原因是___________。关注更新免费领取,淘宝唯一每月更新店铺:知二教育