文档内容
第一章 章末测试(基础)
满分100分,考试用时75分钟
一、选择题:本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。在每小
题给出的四个选项中,只有一项是符合题目要求的
1.乙烷燃烧热为Q kJ·mol-1,则下列热化学方程式中正确的是
A.2C H(g)+7O(g)=4CO (g)+6HO(g) H=-2Q kJ·mol-1
2 6 2 2 2
B.2C
2
H
6
(g)+7O
2
(g)=4CO
2
(g)+6H
2
O(l) △H=+2Q kJ·mol-1
△
C.C H(g)+ O(g)=2CO (g)+3HO(g) H=-Q kJ·mol-1
2 6 2 2 2
△
D.2C H(g)+7O(g)=4CO (g)+6HO(l) H=-2Q kJ·mol-1
2 6 2 2 2
【答案】D △
【解析】A.燃烧热是指:在25℃、101KPa时,1mol纯净物完全燃烧生成稳定的氧化物放出的热量,水
应该为液态,故A错误,A错误;
B.该反应为放热反应, H为负值,故B错误;
C.燃烧热是指:在25℃△、101KPa时,1mol纯净物完全燃烧生成稳定的氧化物放出的热量,水应该为液
态,故C错误;
D.由于化学计量数增大2倍,所以反应的焓变变为原来的2倍, H =-2Q kJ·mol-1,故D正确;
故选D。 △
2.下列关于化学反应与能量变化的说法正确的是
A.燃烧属于放热反应
B.中和反应是吸热反应
C.断裂化学键放出能量
D.反应物总能量与生成物总能量可能相等
【答案】A
【解析】A.物质燃烧时向外界释放能量,属于放热反应,A项正确;
B.中和反应都是放热反应,B项错误;
C.化学键断裂吸收能量,化学键形成放出能量,C项错误;
D. 化学反应中的物质变化一定伴随着能量变化,反应物总能量与生成物总能量一定不相等,D项错误。
故选A。
3.燃烧热与反应热的关系是
A.燃烧热是反应热的一种类型B.当一个反应是燃烧反应时,该燃烧反应的反应热就是燃烧热
C.燃烧热不属于反应热,反应热是在25 ℃、101 kPa下测定的,而燃烧反应的温度要高
D.反应热有正负之分,燃烧反应的焓变全部是正值
【答案】A
【解析】A.燃烧热是1mol纯物质完全燃烧生成指定产物时放出的热量,反应热是化学反应过程中放出或
吸收的热量,燃烧热是反应热的一种,故A正确;
B.燃烧热是燃烧1mol可燃物时放出的热量,故B错误;
C.燃烧热属于反应热,故C错误;
D.燃烧反应是放热的,所以焓变为负值,故D错误;
故选A。
4.下列有关中和反应反应热测定实验的说法正确的是
A.强酸与强碱反应生成 释放的热量都约为
B.温度计能代替环形玻璃搅拌器,用于搅拌反应物
C.一组完整的实验数据需要测三次温度
D.测定中和反应反应热的实验中,读取的混合溶液不再变化的温度为终止温度
【答案】C
【解析】A.当酸、碱浓度过大时,溶于水时会放热,则生成 1molH O(l) 释放的热量大于 57.3kJ,A错
2
误;
B.温度计易断裂,不能代替环形玻璃搅拌器,用于搅拌反应物,B错误;
C.一组完整的实验数据需要测①反应前酸溶液的温度②反应前碱溶液的温度③反应后混合溶液的最高温
度,C正确;
D.中和反应为放热反应,恰好反应完全时温度最高,应读取混合溶液最高温度为终止温度,D错误;
故答案选C。
5.金刚石和石墨是碳元素的两种结构不同的单质 同素异形体 ,在 时, 石墨 转化为金刚
石,要吸收 的热能。据此,试判断在 压强下,下列结论正确的是
A.金刚石比石墨稳定
B.石墨比金刚石稳定
C.金刚石与石墨不能相互转化
D. 石墨 比 金刚石 的总能量高【答案】B
【解析】A.石墨转化为金刚石是吸热反应,石墨的能量较低,所以石墨比金刚石稳定,A错误;
B.石墨转化为金刚石是吸热反应,石墨的能量较低,所以石墨比金刚石稳定,B正确;
C.在100kPa时,1mol石墨转化为金刚石,要吸收1.895kJ的热量,金刚石能转化为石墨,C错误;
D.在100kPa时,1mol石墨转化为金刚石,要吸收1.895kJ的热量,1mol金刚石比1mol石墨的总能量高,
D错误。
本题选B。
6.为了测定酸碱反应的反应热,计算时至少需要的数据是
①酸的浓度和体积②碱的浓度和体积③比热容④反应后溶液的质量⑤反应前后溶液温度变化⑥操作所需的
时间
A.①②③⑤ B.①③④⑥ C.③④⑤⑥ D.全部
【答案】A
【解析】由反应热的计算公式ΔH= 可知,酸碱反应的中和热计算时,至少需要的数据有:比热容c,
酸的浓度和体积、碱的浓度和体积,反应前后温度变化ΔT,然后计算出反应后溶液的质量、生成水的物质
的量;故选A。
7.下列反应既属于氧化还原反应,又属于放热的是
A.氢氧化钠与稀硫酸反应 B.灼热的木炭与 反应
C.铁与稀硫酸反应 D.石灰石高温分解
【答案】C
【解析】A.氢氧化钠与稀硫酸反应放热,但该反应不是氧化还原反应,A不选;
B.碳与二氧化碳反应生成一氧化碳是氧化还原反应,但属于吸热反应,B不选;
C.铁与稀硫酸反应生成硫酸亚铁和氢气,是放热反应,且是氧化还原反应,C选;
D.石灰石分解生成氧化钙和二氧化碳是吸热反应,且不是氧化还原反应,D不选;
答案选C。
8. 和 反应可转化为无毒气体: 。已知该反应分两
步进行,反应进程中能量变化如图所示。下列说法正确的是
A.
B.使用催化剂可降低 的值
C. ,故反应无需加热即可发生
D.反应①的焓变 小于反应②的焓变
【答案】D
【解析】A.根据图像可知E 是第一步正反应的活化能,E 是第二步逆反应的活化能,因此 ,
1 2
A错误;
B.使用催化剂可降低活化能,但不能改变焓变即 的值,B错误;
C. ,反应放热,但反应条件与反应是放热还是吸热没有关系,C错误;
D.根据图像可知反应①放出的热量多,由于焓变小于0,所以反应①的焓变 小于反应②的焓变 ,
D正确;
答案选D。
9.下列反应既属于氧化还原反应,又是吸热反应的是
A.钠和水的反应 B.锌片和稀硫酸的反应
C. 与 的反应 D.灼热的碳与 的反应
【答案】D
【解析】A.钠与水反应是氧化还原反应,也是常见的放热反应,A不符合题意;
B.锌片和稀硫酸的反应是氧化还原反应,也是常见的放热反应,B不符合题意;
C. 与 反应是吸热反应,属于复分解反应,复分解一定不是氧化还原反应,C不符
合题意;D. ,C元素化合价改变,属于氧化还原反应且是吸热反应,D符合题意。
答案选D。
10.已知2H(g)+O(g)=2HO(l) ΔH=-571.6 kJ·mol-1,则下列关于方程式2HO(l)=2H(g)+O(g)的ΔH的说
2 2 2 2 2 2
法中正确的是
A.方程式中的化学计量数表示分子数
B.该反应ΔH大于零
C.该反应ΔH=-571.6 kJ·mol-1
D.该反应可表示36 g水分解时的热效应
【答案】B
【解析】A.方程式中的化学计量数表示该物质的物质的量,A错误;
B.在书写热化学方程式时,若反应物和生成物对换,则ΔH的符号相反,数值不变,B正确;
C.该反应ΔH=+571.6 kJ·mol-1,C错误;
D.未注明水的状态,应该为液态水,D错误;
故选B。
11.盖斯定律认为能量总是守恒的,不管化学反应过程是一步完成或分几步完成,整个过程的热效应是相
同的。
已知:①HO(g)=H O(l) ΔH=-Q kJ·mol-1
2 2 1 1
②C HOH(g)=C HOH(l) ΔH=-Q kJ·mol-1
2 5 2 5 2 2
③C HOH(g)+3O (g)=2CO (g)+3HO(g) ΔH=-Q kJ·mol-1
2 5 2 2 2 3 3
若使23g液态无水酒精完全燃烧,最后恢复到室温,则放出的热量为(单位:kJ)
A.Q+Q +Q B.1.5Q -0.5Q +0.5Q
1 2 3 1 2 3
C.0.5Q -1.5Q +0.5Q D.0.5(Q +Q +Q )
1 2 3 1 2 3
【答案】B
【解析】液态无水酒精完全燃烧生成液态水的方程式为:C HOH(l)+3O (g)=2CO (g)+3HO(l),根据盖斯定
2 5 2 2 2
律,此方程式可由③-②+①×3得到,焓变ΔH=-(Q -Q +3Q )kJ·mol-1,23 g酒精的物质的量为 =0.5
3 2 1
mol,完全燃烧放出的热量为(0.5Q -0.5Q +1.5Q )kJ,
3 2 1
答案选B。
12.已知:2H(g)+O(g)= 2H O(l) ΔH=-571.6kJ·mol-1,2CO(g)+O(g)= 2CO (g) ΔH=-565.8kJ·mol-1。某
2 2 2 2 2
H 和CO的混合气体完全燃烧时放出113.74kJ热量,同时生成8.8gCO ,则原混合气体中H 和CO的物质
2 2 2的量之比为
A.2﹕1 B.1﹕2 C.1﹕1 D.2﹕3
【答案】C
【解析】由8.8gCO ,可得原CO为0.2mol,反应中放热为56.58kJ,其余的热量113.74kJ-56.58kJ=57.16kJ
2
是H 燃烧放出的,由此可根据反应2H(g)+O(g)= 2H O(l) ΔH=-571.6kJ·mol-1求出H 也是0.2mol;
2 2 2 2 2
答案选C。
13.科学家提出的碘硫热化学循环是由Ⅰ、Ⅱ、Ⅲ三步反应组成的(如图所示),下列有关说法正确的是
A.该循环总的结果是放热反应
B.整个循环过程中产生1molO 的同时产生44.8LH
2 2
C.若反应Ⅰ、Ⅱ、Ⅲ的反应热分别为ΔH、ΔH、ΔH,则ΔH+ΔH+ΔH>0
1 2 3 1 2 3
D.图中反应Ⅰ、Ⅱ、Ⅲ均可在常温常压下进行
【答案】C
【解析】该循环是在SO 和I 参与情况的水的分解反应。
2 2
【详解】A.总反应是水的分解,是吸热反应,选项A错误;
B.反应不一定是在标准状况下进行的,不能确定是44.8LH ,选项B错误;
2
C.ΔH+ΔH+ΔH 就是该反应的总焓变,由于总反应是水的分解,ΔH>0,选项C正确;
1 2 3
D.反应II是HSO 的分解,常温常压下不能进行,反应III是HI的分解,常温常压下是可逆反应,选项D
2 4
错误;
答案选C。
14.下列依据热化学方程式得出的结论正确的是
A. ,则
B.已知 ; ;则C.已知31 g白磷比31 g红磷能量多b kJ,则 (白磷,s) (红磷,s)
D.已知 ,则氢气燃烧热
【答案】C
【解析】A. ,由于
反应有硫酸钡固体生成, ,故A错
误;
B.碳完全燃烧放热多, ;
;则 ,故B错误;
C.已知31 g白磷比31 g红磷能量多b kJ,白磷变为红磷放热,则 (白磷,s) (红磷,
s) ,故C正确;
D.已知 ,氢气燃烧热是1mol氢气完全燃烧生成液态水
放出的能量,则氢气燃烧热 ,故D错误;
选C。
15.在常温常压时,充分燃烧一定量的丁烷(C H )气体,放出热量QkJ(Q>0),将生成的二氧化碳全部通入
4 10
足量NaOH溶液中,发生的反应为CO+2NaOH=Na CO+HO,共消耗了4mol·L-1的NaOH溶液200mL。
2 2 3 2
则此条件下,下列热化学方程式正确的是
A.C H (g)+ O(g)=4CO (g)+5HO(l) ΔH=-QkJ·mol-1
4 10 2 2 2
B.C H (g)+ O(g)=4CO (g)+5HO(l) ΔH=-10QkJ·mol-1
4 10 2 2 2
C.C H (g)+ O(g)=4CO (g)+5HO(l) ΔH=10QkJ·mol-1
4 10 2 2 2
D.C H (g)+ O(g)=4CO (g)+5HO(l) ΔH=-10QkJ
4 10 2 2 2【答案】B
【解析】消耗氢氧化钠的物质的量是0.2Lx0.4mol/L=0.8mol,则需要的二氧化碳的物质的量是0.4mol,说
明0.1mol C H (g)完全燃烧生成0.4mol的二氧化碳放出QkJ的热量,则1mol C H (g)完全燃烧放出的热量
4 10 4 10
是10QkJ;热化学反应方程式为:C H (g)+ O(g)=4CO (g)+5HO(l) ΔH=-10QkJ·mol-1。
4 10 2 2 2
故答案选B。
16.已知丙烷的燃烧热 , ,若一定量的丙烷
完全燃烧后生成18g水蒸气,则放出的热量为
A.2039kJ B.509.75kJ C.553.75kJ D.597.75kJ
【答案】B
【解析】已知丙烷的燃烧热 , ,则C H(g)+
3 8
5O(g)=3CO(g)+4HO(g) ,若一定量的丙烷完全燃烧后生成18g水蒸气(即物质的
2 2 2
量为1mol),则放出的热量为 ,故B符合题意。
综上所述,答案为B。
二、非选择题:共56分。
17.(14分)生产生活中的化学反应都伴随着能量的变化,请根据有关知识回答下列问题:
(1)S(单斜)和S(正交)是硫的两种同素异形体。已知:
①S(单斜,s) ;
②S(正交,s) 。
则S(单斜)和S(正交)中更稳定的是_______。
(2)常温常压下,几种共价键的键能如下表:
共价键 S-S F-F H-F H-Br Br-Br
键能 266 159 565 363 193
① 单质的分子结构如图所示。 全部转化成S(g)时要吸收或放出的热量为_______kJ。②写出HBr(g)和 反应生成HF(g)和 的热化学方程式_______。
(3)已知: ,甲烷完全燃烧与不完全燃烧的热效应如下图所示。
①写出表示甲烷燃烧热的热化学方程式_______。
②CO的燃烧热 _______ 。
【答案】(1)S(正交)
(2) 2128
(3) -283
【解析】(1)根据盖斯定律,反应①-②得S(单斜,s)=S(正交,s)ΔH=(-297.16kJ•mol-1)-
(-296.83kJ•mol-1)=-0.33kJ/mol,则单斜硫的能量比正交硫的能量高,能量越低越稳定,所以S(单斜)和 S(正
交)中更稳定的是 S(正交),故答案为:S(正交);
(2)①断裂化学键吸收热量,1个S 分子含8个S-S键,1molS (g)全部转化成S(g)时要吸收的热量为
8 8
266kJmol-1×8mol=2128kJ,故答案为:2128;
②ΔH⋅=反应物的总键能-生成物的总键能,即2HBr(g)+F
2
(g)=2HF(g)+Br
2
(g)ΔH=(363×2+159-565×2-
193)kJmol-1=-438kJmol-1,故答案为: ;
⋅ ⋅
(3)①燃烧热是1mol可燃物完全燃烧产生稳定的氧化物时放出的热量,由图可知,1mol甲烷燃烧生成二
氧化碳气体和水蒸气放出802.3kJ能量,又有 ,则表示甲烷燃烧热的热化学方程式为 ,故答案为:
;
②设a. ,b.
,根据盖斯定律,将a-b得到CO燃烧热的热化学方
程式为CO(g)+ O(g)=CO (g) ΔH=(-890.3+607.3)kJ•mol-1=-283kJ•mol-1,故答案为:-283。
2 2
18.(12分)化学反应伴随能量变化,获取反应能量变化有多条途径。
(1)下列反应中,属于吸热反应的是___________(填字母)。
A.NaO与水反应
2
B.铝和氧化铁反应
C.CaCO 受热分解
3
D.锌与盐酸反应
(2)获取能量变化的途径
①通过化学键的键能计算。已知:
化学键 H—H O=O O—H
键能(kJ·mol-1) 436 496 463.4
则2H(g)+O(g)=2HO(g)ΔH=___________kJ·mol-1
2 2 2
②通过物质所含能量计算。已知反应A+B=C+D中A、B、C、D所具有的能量依次可表示为E 、E 、E 、
A B C
E ,该反应ΔH=___________。
D
③通过盖斯定律计算。已知在25℃、101kPa时,2Na(s)+ O(g)=Na O(s) ΔH=-414kJ·mol-1;2Na(s)
2 2 1
+O (g)=Na O(s) ΔH=-511kJ·mol-1
2 2 2 2
写出NaO 与Na反应生成NaO的热化学方程式:___________。
2 2 2
④利用实验装置测量。测量盐酸与NaOH溶液反应的热量变化的过程中,若取50mL0.50mol·L-1的盐酸,则
还需加入___________(填字母)。
A.50mL0.50mol·L-1NaOH溶液B.50mL0.55mol·L-1NaOH溶液C.1.0gNaOH固体
【答案】(1)C(2) ① -483.6 ② E +E -(E +E ) ③NaO(s)+2Na(s)=2Na O(s) ΔH=-317kJ·mol-1 ④B
C D A B 2 2 2
【解析】(1)常见的吸热反应有:大多数的分解反应、C或氢气作还原剂的氧化还原反应、氯化铵与氢氧
化钡的反应等,A、B、D均为放热反应,只有C为吸热反应,故答案为C;
(2)2H(g)+O(g)=2HO(g)ΔH=(2×436+498-463.4×2×2) kJ·mol-1=-483.6kJ·mol-1;
2 2 2
反应A+B=C+D中A、B、C、D所具有的能量依次可表示为E 、E 、E 、E ,该反应ΔH= E +E -
A B C D C D
(E +E ),故答案为E +E -(E +E );
A B C D A B
2Na(s)+ O(g)=Na O(s) ΔH=-414kJ·mol-1;2Na(s)+O (g)=Na O(s) ΔH=-511kJ·mol-1结合盖斯定律可知
2 2 1 2 2 2 2
I×2-II得到NaO(s)+2Na(s)=2Na O(s) ΔH=-317kJ·mol-1;故答案为NaO(s)+2Na(s)=2Na O(s)
2 2 2 2 2 2
ΔH=-317kJ·mol-1;
测定中和热,因盐酸易挥发,需加稍过量的NaOH,保证盐酸完全反应,且固体溶解放热,只有B合理,
故答案为B。
19.(14分)氢能是一种极具发展潜力的清洁能源。
(1)氢能是一种既高效又干净的新能源,发展前景良好,用氢能作能源的燃料电池汽车是研究的重点方向之
一、下列说法正确的是___________(填字母)。
A.氢燃料电池中H 在正极反应,O 在负极反应
2 2
B.理论上氢能源汽车使用时不会产生污染物
C.氢燃料电池可以将化学能完全转化为电能
D.水分解产生氢气的同时放出热量供汽车使用
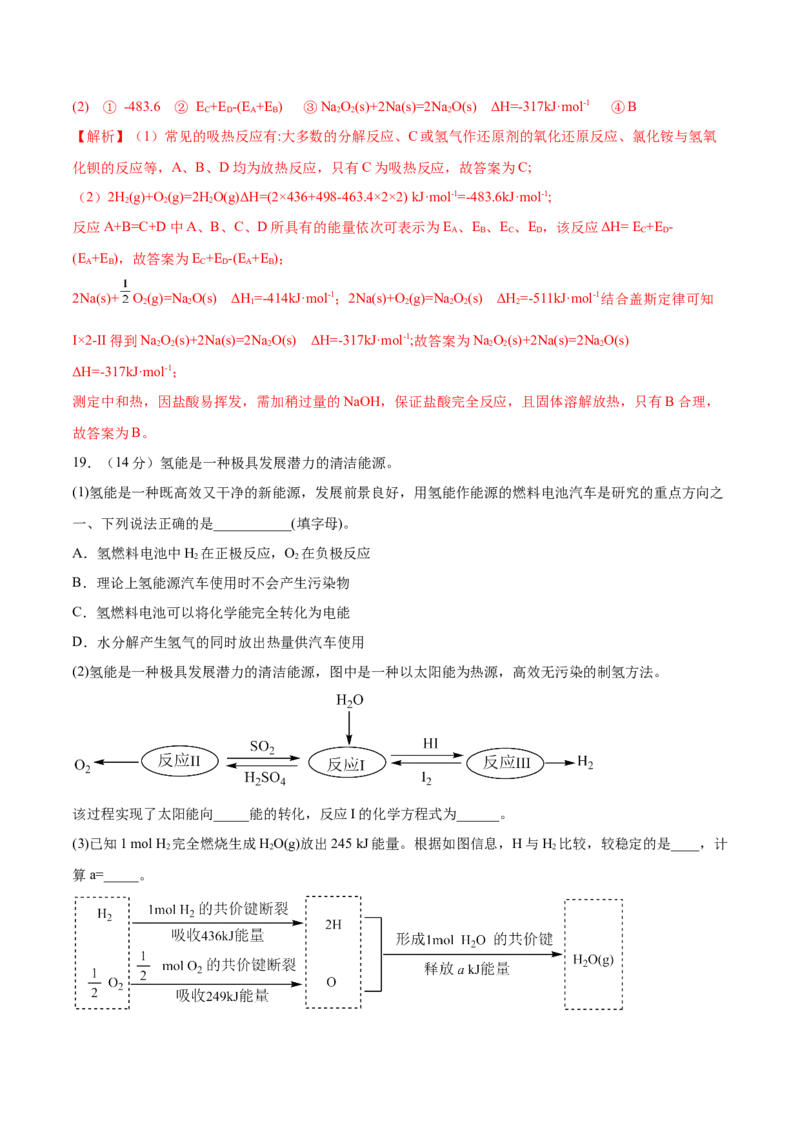
(2)氢能是一种极具发展潜力的清洁能源,图中是一种以太阳能为热源,高效无污染的制氢方法。
该过程实现了太阳能向_____能的转化,反应I的化学方程式为______。
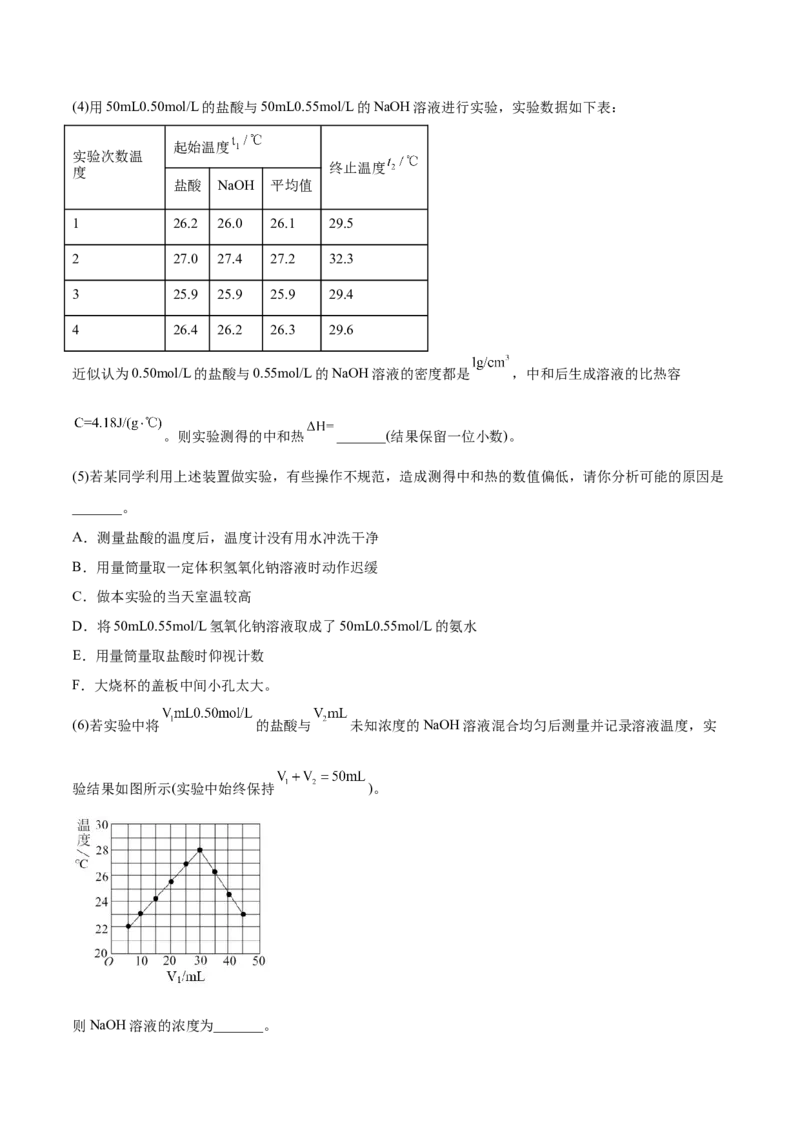
(3)已知1 mol H 完全燃烧生成HO(g)放出245 kJ能量。根据如图信息,H与H 比较,较稳定的是____,计
2 2 2
算a=_____。(4)已知:Fe O(s) + 3C(石墨)=2Fe(s) + 3CO(g) H
2 3 1
△
CO(g)+ O(g)=CO (g) H
2 2 2
△
C(石墨)+O (g)=CO (g) H
2 2 3
2Fe
2
O
3
(s)=4Fe(s)+3O
2
(g)△ H
4
请写出△H
4
与△H
1
、△H△2 、 △H
3
的关系___________。
【答案】(1)B
(2) 化学 2HO+I +SO=2HI+H SO
2 2 2 2 4
(3) H 930
2
(4) H=2 H-6 H+6 H
4 1 3 2
【解△析】(△1)A△. 氢燃料△电池中H
2
在负极反应,O
2
在正极反应,A错误;B.氢燃料燃烧产物是水,理论
上氢能源汽车使用时不会产生污染物,B正确;C.氢燃料电池可以将化学能部分转化为电能,C错误;
D.水分解产生氢气的同时吸收热量,D错误;
(2)该过程实现了太阳能向化学能的转化;由图知反应I的反应物为HO、SO 、I,生成物为HSO 和
2 2 2 2 4
HI,则其化学方程式为2HO+I +SO=2HI+H SO ;
2 2 2 2 4
(3)由图知,1 mol H 变成2molH时需要吸收436kJ的能量,故H原子的能量高,能量越高越不稳定,所
2
以较稳定的是H;1 mol H 完全燃烧生成HO(g)放出245 kJ能量,245kJ=akJ-436kJ-249kJ,则a=930kJ;
2 2 2
(4)由盖斯定律知, H=2 H-6 H+6 H。
4 1 3 2
20.(16分)某实验小△组用△50mL0△.50mol/L△的盐酸与50mL0.55mol/L的NaOH溶液在图所示的装置中进行
中和热的测定。
(1)从实验装置上看,图中缺少的仪器是_______。
(2)烧杯间填满碎纸条的作用是_______,若大烧杯上不盖硬纸板,求得的反应热数值将_______(填“偏
大”“偏小”或“无影响”)。
(3)若实验中用60mL0.50mol/L的盐酸与50mL0.55mol/L的NaOH溶液进行反应,与上述实验相比,放出的
热量_______(填“相等”或“不相等”),所得中和热的数值_______(填“相等”或“不相等”)。(4)用50mL0.50mol/L的盐酸与50mL0.55mol/L的NaOH溶液进行实验,实验数据如下表:
起始温度
实验次数温
终止温度
度
盐酸 NaOH 平均值
1 26.2 26.0 26.1 29.5
2 27.0 27.4 27.2 32.3
3 25.9 25.9 25.9 29.4
4 26.4 26.2 26.3 29.6
近似认为0.50mol/L的盐酸与0.55mol/L的NaOH溶液的密度都是 ,中和后生成溶液的比热容
。则实验测得的中和热 _______(结果保留一位小数)。
(5)若某同学利用上述装置做实验,有些操作不规范,造成测得中和热的数值偏低,请你分析可能的原因是
_______。
A.测量盐酸的温度后,温度计没有用水冲洗干净
B.用量筒量取一定体积氢氧化钠溶液时动作迟缓
C.做本实验的当天室温较高
D.将50mL0.55mol/L氢氧化钠溶液取成了50mL0.55mol/L的氨水
E.用量筒量取盐酸时仰视计数
F.大烧杯的盖板中间小孔太大。
(6)若实验中将 的盐酸与 未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实
验结果如图所示(实验中始终保持 )。
则NaOH溶液的浓度为_______。【答案】(1)环形玻璃搅拌棒
(2) 防止热量散失 偏大
(3) 不相等 相等
(4)-56.8kJ/mol
(5)ADF
(6)0.75mol/L
【解析】(1)由量热计的构造可知该装置缺少的一种仪器是环形玻璃搅拌棒;
(2)碎纸条可以起到保温隔热的作用,如果没有碎纸条,会有热量的流失,该反应为放热反应,反应热
会偏大,故答案为:防止热量散失;偏大;
(3)反应放出的热量和所用酸以及碱的量的多少有关,用60mL0.50mol/L的盐酸与50mL0.55mol/L的
NaOH溶液进行反应,生成水的量增多,所放出的热量偏高,但是中和热的均是强酸和强碱反应生成1mol
水时放出的热,与酸碱的用量无关,所以用60mL0.50mol/L的盐酸与50mL0.55mol/L的NaOH溶液进行反
应测得中和热数值相等;故答案为:不相等;相等;
(4)第2组温度差为5.1℃,除第二组,其余3次温度差分别为:3.4℃,3.5℃,3.3℃
第2组数据明显有误,所以删掉,其余4次温度差平均值为 ,该反应中,氢氧化
钠过量,按照盐酸的量计算水的量,水的物质的量为: ,溶液的质量为:
,则生成0.025mol水放出的热量为: ,
所以实验测得的中和热 ;
(5)通过对比数据可知,该反应放出热量的计算值较小,则根据选项可以分析,
A.测量盐酸的温度后,温度计没有用水冲洗干净,则在测量氢氧化钠温度时,会放热,从而起始温度会
较高,计算出的热量较小,A正确;
B.用量筒量取一定体积氢氧化钠溶液时,没有温度变化,动作迟缓,不会影响反应热,B错误;
C.本题需要的是温度差,故做本实验的当天室温较高,没有影响,C错误;
D.一水合氨是弱电解质,其电离的时候要放热,故换成氨水后,测得的热量会变小,D正确;
E.用量筒量取盐酸时仰视计数,则盐酸的试剂体积,大于量取的数值,放热较多,E错误;
F.大烧杯的盖板中间小孔太大,实验时,会有热量流失,热量偏小,F正确;
故选ADF;
(6)V=30mL时溶液温度最高、酸碱恰好完全反应,则V=20mL,此时有n(HCl)=n(NaOH),即30×10-
1 23×0.5mol/L=c(NaOH)×20×10-3L,c(NaOH)=0.75mol/L。倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育