文档内容
第七章 有机化合物
单元知识清单
【知识导引】
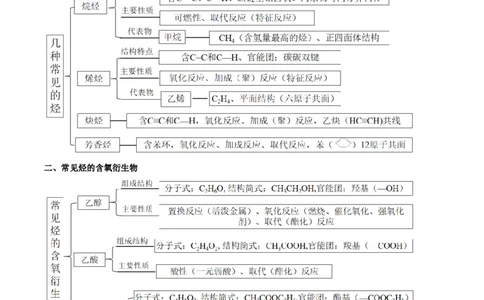
一、几种常见的烃
二、常见烃的含氧衍生物
三、基本营养物质【知识清单】
一、认识有机化合物
知识点一、烷烃的结构
1.碳原子的成键特点—有机物种类繁多的原因
(1)原子结构:碳原子有四个未成对电子,可形成四个价键;碳原子可与其他原子成键,碳原子间也可
成键。
(2)成键特点:①碳原子间成键方式的多样性:碳原子之间形成碳碳单键( )、碳碳双键(
)、碳碳三键(—C≡C—)。
②碳原子间连接方式的多样性:多个碳原子之间可结合成碳链或碳环,如下图所示。
③碳原子数目灵活性:有机物分子可能只含有一个或几个碳原子,也可能是成千上万个碳原子
④碳原子还可以和H、O、N、S、P、卤素等多种非金属原子形成共价键。
2.烷烃的结构特点
(1)结构特点:C—C单键、饱和(碳原子剩余的价键全部与H结合,每个碳原子均形成4条价键)、链
状(碳原子结合形成的碳链可以是直链,也可以含有支链)。
(2)通式:C H
n 2n+23.烷烃的命名
若碳原子数不多于10时,依次用天干表示,碳原子数大于10时,以汉字数表示;若碳原子相同,结构不
同时,用正、异、新表示。
4.甲烷的组成与结构特点
分子式 电子式 结构式 球棍模型 空间填充模型 键角
CH 109028′
4
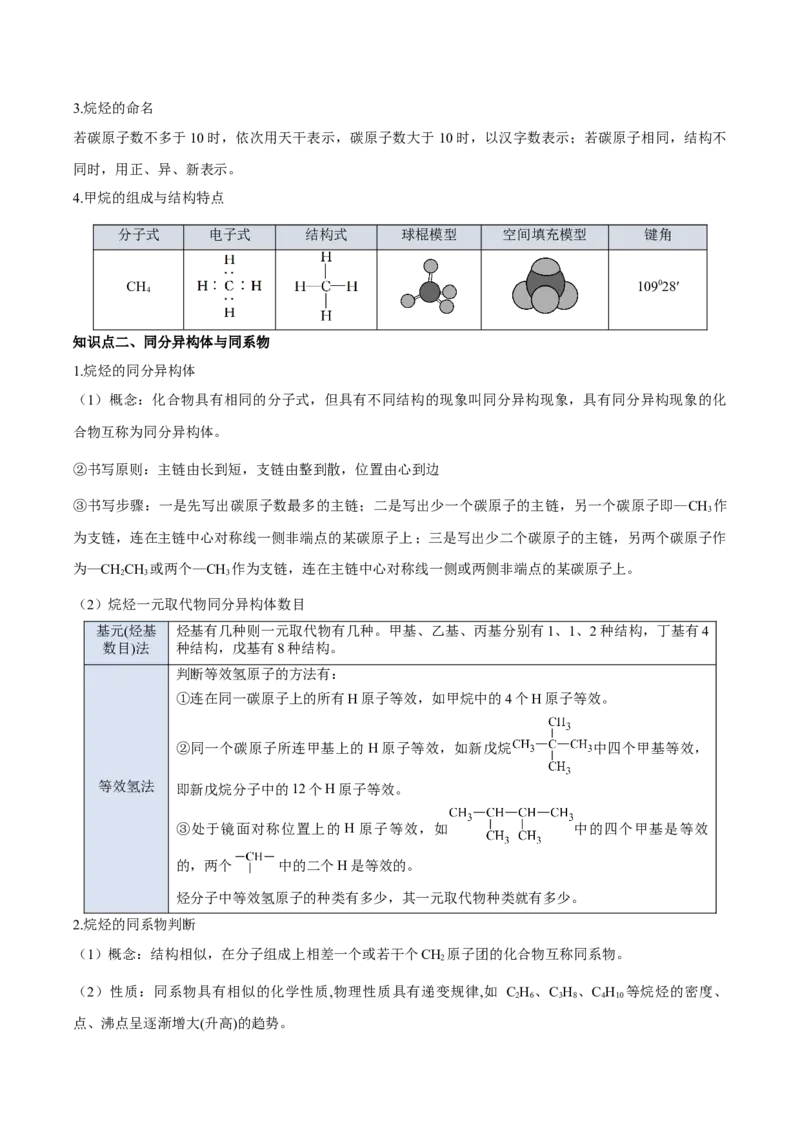
知识点二、同分异构体与同系物
1.烷烃的同分异构体
(1)概念:化合物具有相同的分子式,但具有不同结构的现象叫同分异构现象,具有同分异构现象的化
合物互称为同分异构体。
②书写原则:主链由长到短,支链由整到散,位置由心到边
③书写步骤:一是先写出碳原子数最多的主链;二是写出少一个碳原子的主链,另一个碳原子即—CH 作
3
为支链,连在主链中心对称线一侧非端点的某碳原子上;三是写出少二个碳原子的主链,另两个碳原子作
为—CHCH 或两个—CH 作为支链,连在主链中心对称线一侧或两侧非端点的某碳原子上。
2 3 3
(2)烷烃一元取代物同分异构体数目
基元(烃基 烃基有几种则一元取代物有几种。甲基、乙基、丙基分别有1、1、2种结构,丁基有4
数目)法 种结构,戊基有8种结构。
判断等效氢原子的方法有:
①连在同一碳原子上的所有H原子等效,如甲烷中的4个H原子等效。
②同一个碳原子所连甲基上的 H原子等效,如新戊烷 中四个甲基等效,
等效氢法 即新戊烷分子中的12个H原子等效。
③处于镜面对称位置上的 H原子等效,如 中的四个甲基是等效
的,两个 中的二个H是等效的。
烃分子中等效氢原子的种类有多少,其一元取代物种类就有多少。
2.烷烃的同系物判断
(1)概念:结构相似,在分子组成上相差一个或若干个CH 原子团的化合物互称同系物。
2
(2)性质:同系物具有相似的化学性质,物理性质具有递变规律,如 C H 、C H 、C H 等烷烃的密度、
2 6 3 8 4 10
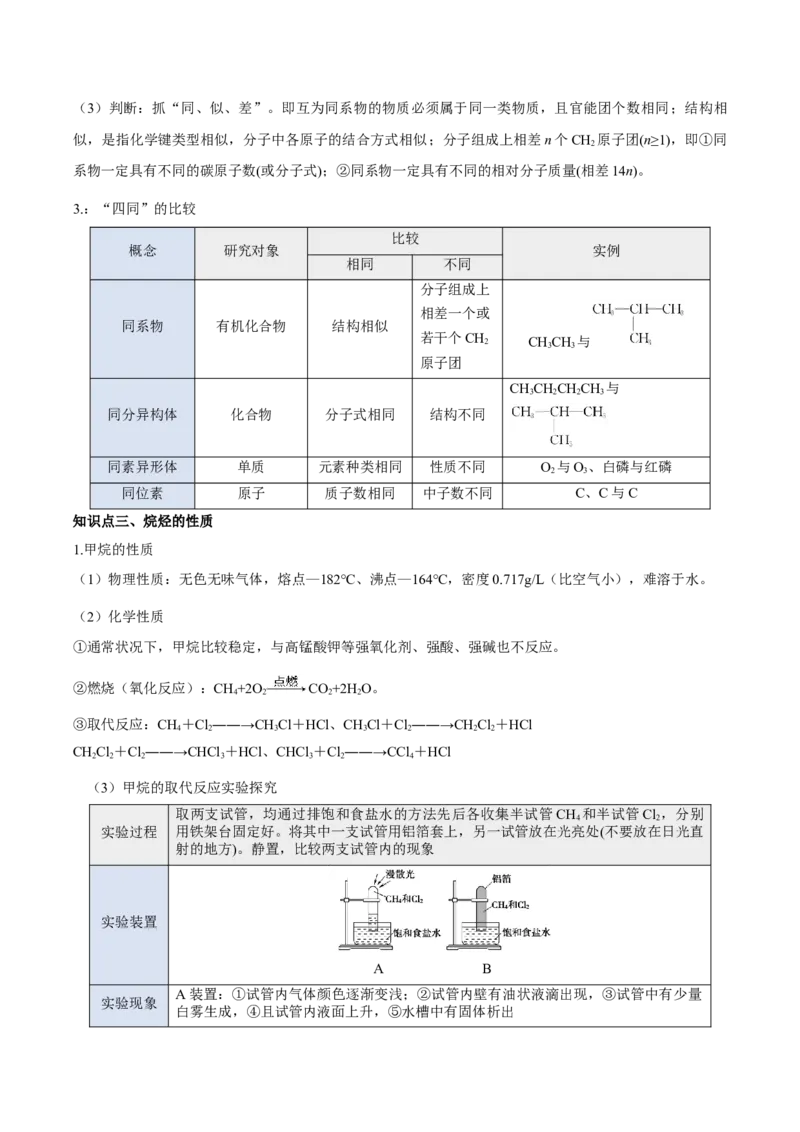
点、沸点呈逐渐增大(升高)的趋势。(3)判断:抓“同、似、差”。即互为同系物的物质必须属于同一类物质,且官能团个数相同;结构相
似,是指化学键类型相似,分子中各原子的结合方式相似;分子组成上相差n个CH 原子团(n≥1),即①同
2
系物一定具有不同的碳原子数(或分子式);②同系物一定具有不同的相对分子质量(相差14n)。
3.:“四同”的比较
比较
概念 研究对象 实例
相同 不同
分子组成上
相差一个或
同系物 有机化合物 结构相似
若干个CH 2 CH 3 CH 3 与
原子团
CHCHCHCH 与
3 2 2 3
同分异构体 化合物 分子式相同 结构不同
同素异形体 单质 元素种类相同 性质不同 O 与O、白磷与红磷
2 3
同位素 原子 质子数相同 中子数不同 C、C与C
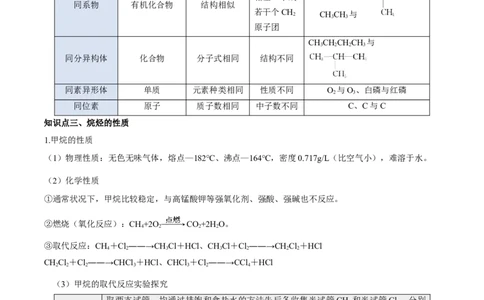
知识点三、烷烃的性质
1.甲烷的性质
(1)物理性质:无色无味气体,熔点—182℃、沸点—164℃,密度0.717g/L(比空气小),难溶于水。
(2)化学性质
①通常状况下,甲烷比较稳定,与高锰酸钾等强氧化剂、强酸、强碱也不反应。
②燃烧(氧化反应):CH+2O CO+2HO。
4 2 2 2
③取代反应:CH+Cl――→CHCl+HCl、CHCl+Cl――→CHCl+HCl
4 2 3 3 2 2 2
CHCl+Cl――→CHCl +HCl、CHCl +Cl――→CCl +HCl
2 2 2 3 3 2 4
(3)甲烷的取代反应实验探究
取两支试管,均通过排饱和食盐水的方法先后各收集半试管CH 和半试管Cl ,分别
4 2
实验过程 用铁架台固定好。将其中一支试管用铝箔套上,另一试管放在光亮处(不要放在日光直
射的地方)。静置,比较两支试管内的现象
实验装置
A B
A装置:①试管内气体颜色逐渐变浅;②试管内壁有油状液滴出现,③试管中有少量
实验现象
白雾生成,④且试管内液面上升,⑤水槽中有固体析出B装置:无明显现象
A 装置中①气体颜色变浅说明氯气与甲烷发生了反应,②反应后试管内壁有油状液
滴,说明有难溶于水的有机物生成,③出现白雾说明生成了 HCI,④试管内液面上升说明
实验分析 反应后气体体积减小,⑤水槽中析出的固体为 NaCI 晶体
B装置中无明显现象说明氯气与甲烷的反应需要在光照条件下进行
实验结论 CH 与Cl 在光照时才能发生化学反应
4 2
2.烷烃的物理性质:无色、难溶于水、碳原子数越多,熔沸点越高(通常情况下碳原子数≤4的烷烃为气
体),碳原子数相同的烷烃,含支链越多熔沸点越低。
3.烷烃的化学性质
稳定性 通常情况下,比较稳定——与强酸、强碱或KMnO 等强氧化剂不发生反应
4
可燃性 在空气中完全燃烧,发生氧化反应,生成CO 和HO
2 2
分解反应 在较高温度下会发生分解——用于制备基本的化工原料和燃料
反应条件 光照(室温下在暗处不发生反应)
取代反应
反应产物 可生成多种有机生成物(化合物)
连锁反应—逐步取代,各步反应同时进行取代1 mol H原子,消耗1 mol X ,生
反应特点 2
成1 mol HX
反应模型 A—B+C—D光照—\s\up 4()A—D+C—B 有进有出,取而代之
—→
二、乙烯与有机高分子材料
知识点一、乙烯(烯烃)的结构与性质
1.乙烯与乙烷、乙炔分子结构的比较
分子 结构简 空间填充模 结构
烃 电子式 结构式 球棍模型 键角
式 式 型 特点
空间
乙 109°28
C H H : ¿ CHCH 四面
烷 2 6 3 3 ′
¿ 体
六原
乙 CH=
烯 C 2 H 4 H ¿ CH 2 120° 子共
¿ 2 面
四原
乙
C H H—C≡C—H HC≡CH 180° 子共
炔 2 2
线
2.乙烯与乙烷的化学性质的比较
乙烷 乙烯
O 2C H+7O点燃—\s\up 4()4CO+6HO C H+3O点燃—\s\up 4()2CO+2HO
氧化 2 2 6 2—→ 2 2 2 4 2—→ 2 2
反应 KMnO /H+ 不反应 乙烯被氧化
4
取代反应 加成反应
特征反应
C H+Cl光照—\s\up 4()C HCl+HCl CH=CH+Br ―→BrCHCHBr
2 6 2—→ 2 5 2 2 2 2 2
加聚反应 不反应 nCH=CH催化剂\s\up 4()
2 2———3.取代反应与加成反应比较
取代反应 加成反应
反应物结构特征 含有易被取代的原子或原子团 含有不饱和键
生成物数目 一般相等,常为两种 减少为一种
反应特点 取而代之,有进有出 加之而成,有进无出
碳碳键变化 无变化 不饱和键断裂
等量替换 开键加合
结构变化举例
C H+Cl光照—\s\up 4()C HCl+HCl CH=CH+HBr催化剂\s\up 4()CHCHBr
2 6 2—→ 2 5 2 2 ——— 3 2
4.乙烯的物理性质与应用
物理性质 无色 稍有气味 难溶于水 比空气略轻
重要的化工原料,用来制聚乙烯塑料、聚乙烯纤维、乙醇等(乙烯的产量可以用来衡
应用
量一个国家的石油化工发展水平);在农业生产中用作植物生长调节剂
5.加聚反应的特点
nCHCH=CH催化剂Δ
3 2———
实例
单体 形成高分子化合物的有机小分子 CHCH=CH
3 2
链节 高分子化合物中不断重复的基本结构单元
聚合度 高分子化合物中链节的数目 n
知识点二、烃 有机高分子材料
1.烃
(1)定义:仅含碳和氢两种元素的有机化合物称为碳氢化合物,也称为烃。
(2)烃的分类及性质
依据 分类 通式 官能团 代表物 主要化学性质
饱和烃 烷烃 C H n≥1 —— CH 取代反应
n 2n+2 4
碳碳双键 加成反应 加聚反应
烯烃 C H n≥2 C H
n 2n 2 4
碳原子 (>C=C<) 氧化反应
成键方 碳碳三键 加成反应 加聚反应
不饱和烃 炔烃 C H n≥2 C H
式 n 2n-2 2 2
(—C≡C—) 氧化反应
芳香烃 C H n≥6 (苯环) 取代反应
n 2n-6
链状烃 烷烃 烯烃 —— —— —— ——
碳的骨
环烷烃 C H n≥3 —— 取代反应
架 n 2n
环状烃
芳香烃 —— —— —— ——2.有机高分子材料
(1)分类
①天然高分子材料:天然纤维——棉花、羊毛;天然橡胶。
②合成高分子材料:塑料、合成纤维、合成橡胶、黏合剂、涂料。
(2)高分子化合物的结构
①线型结构:成千上万个链节以共价键连成长链,长链之间相互缠绕,以分子间作用力结合;如聚乙烯、
聚氯乙烯中以C—C键连成长链;淀粉、纤维素中以C—C键和C—O键连成长链。
②体型结构:高分子链上的某些基团与另的物质反应后,高分子链之间从而形成新的化学键,产生了交
联,形成了体型网状结构。如硫化橡胶中,长链与长链间形成化学键,产生网状结构而交联在一起。
(3)三大合成材料
概述 实例 主要用途
合成树脂(聚乙烯、聚丙烯、
聚氯乙烯、酚醛树脂)+添加
组成 聚 乙 烯 、 聚 丙 制作食品包装袋、
剂(增塑剂、防老剂、着色
烯、聚氯乙烯、 管道、包装材料、
塑料
剂) 聚苯乙烯、有机 电器开关、日常用
玻璃 品
强度高、密度小、耐腐蚀,
性能
易加工
天然橡胶 主要成分是聚异戊二烯 橡胶树获得
制造飞机、汽车轮
合成天然橡胶单体是异戊二烯;其他橡 丁苯橡胶、顺丁 胎和各种密封材料
合成橡胶
胶单体是二种不同的烯烃 橡胶、氯丁橡胶
橡胶
耐热和耐酸、碱腐蚀 氟橡胶 用于航空、航天和
特种橡胶 国防等尖端领域
耐高温和严寒 硅橡胶
天然纤维 取自棉花、羊毛、蚕丝、麻 天然纤维纺纱织布
供人类穿着,制成
化学纤维 将纤维素、蛋白质等天然高分子再加工
人造丝、真丝 绳索、渔网、工业
纤维 (再生纤维 成纤维
用滤布,飞机、船
与合成纤 以石油、天然气为原料制成小分子单 丙纶、氯纶、腈 舶的结构材料
维)
体,再聚合成纤维 纶、涤纶、锦纶
3.有机物共线与共面
有机化合物 H—C≡C—H
键角 109º28′ 约120º 180º 120º 109º28′
空间构型 正四面体 平面形 直线形 平面正六边形 立体
共面的点数 3点共面 6点共面 4点共线(面) 12点共面 4点共面
4.烃(CH)燃烧规律
x y
(1)气态烃完全燃烧体积变化的规律
CH+(x+)O ――→xCO+HO ΔV=V -V
x y 2 2 2 后 前
1 x+ x若反应后水为气态,ΔV=-1。
当y>4,ΔV>0,气体总体积变大;
当y=4,ΔV=0,气体总体积不变,CH、C H、C H 符合;
4 2 4 3 4
当y<4,ΔV<0,气体总体积变小,只有C H 符合。
2 2
若反应后水为液态,ΔV=-(1+),反应后气体体积始终减小,且减小量只与氢原子数有关。
(2)烃完全燃烧耗氧量判断
①等质量时:越大,耗氧量越多。
②等物质的量时:(x+)越大,耗氧量越多。
三、乙醇与乙酸
知识点一、乙醇
1.物理性质:通常情况下是具有特殊香味的无色透明液体,能与水以任意比互溶,密度比水小,易挥发。
2.分子结构
分子 官能团 分子模型
结构式 结构简式
式 名称 化学式 球棍模型 填充模型
CHCHOH
3 2
C HO 羟基 —OH
2 6
或C HOH
2 5
3.化学性质
分子结构 反应类型 断键部位 化学方程式
2Na+2CHCHOH—→2CHCHONa+H↑
3 2 3 2 2
置换反应 ①
钠沉在底部,有无色气泡在钠粒表面生成后逸出液
面,最终钠粒消失
CHCHOH+3O点燃—\s\up 4()2CO+3HO
3 2 2—→ 2 2
可燃性 ①②③④⑤
氧 产生淡蓝色火焰,燃烧能产生大量的热
化
反 2CH 3 CH 2 OH+O 2 催 — 化 — 剂 — Δ2CH 3 CHO+2H 2 O
催化氧
应 ①③
化 乙醇分子脱去羟基上的氢原子以及与羟基直接相连的
碳原子上的氢原子形成碳氧双键
强氧化 乙醇酸性K\s\up 4()乙酸
③ MnO
剂
① CHCHOH+CHCOOH CHCOOC H+HO
取代反应 3 2 3 3 2 5 2
4.—OH与OH-的区别:
羟基 氢氧根离子
电子式
不
同 电子数 9 10
点
电性 不显电性或电中性 显负电性
稳定程度 不稳定 较稳定存在 不能独立存在,必须与其他基团结合在一起 能独立存在
书写方法 —OH OH-
相同点 组成元素相同;质子数相同,均为9
知识点二、乙酸
1.物理性质:俗称冰醋酸,具有刺激性气味的无色透明液体,易溶于水和乙醇,易挥发,熔点16.6℃。
2.分子结构
分子 官能团 分子模型
结构式 结构简式
式 名称 化学式 球棍模型 填充模型
C HO CHCOOH 羧基 —COOH
2 4 2 3
3.化学性质
分子结构 反应类型 断键部位 化学方程式
CHCOOH+NaOH—→CHCOONa+HO
3 3 2
中和反应 ① 醋酸是弱酸:CHCOOH H++CHCOO-
3 3
其酸性比碳酸的酸性强
CHCHOH+CHCOOH CHCOOC H+HO
3 2 3 3 2 5 2
反应类型 反应速率 反应规律 反应特点
酯化反应 ②
酸脱羟基,醇脱
取代反应 较慢 反应可逆
氢
取代反应 ④ CHCOOH+Br 催化剂\s\up 4()CHBrCOOH+HBr
3 2——— 2
4.乙酸乙酯制备
实验装置 饱和NaCO 溶液的作用 浓硫酸的作用
2 3
①与挥发出来的乙酸发生反应,生成可溶于水
的乙酸钠,便于闻乙酸乙酯的香味 ①催化剂:加快反应速率
②溶解挥发出来的乙醇 ②吸水剂:提高乙酸、乙
③减小乙酸乙酯在水中的溶解度,使液体分 醇的转化率
层,便于得到酯
5.分子中羟基氢原子的活泼性比较
乙醇 水 碳酸 乙酸
羟基氢原子的活泼性 ―――――――――――――――――→
电离程度 不电离 部分电离 部分电离 部分电离
酸碱性 - 中性 弱酸性 弱酸性
与Na 反应 反应 反应 反应与NaOH 不反应 不反应 反应 反应
与NaHCO 不反应 不反应 不反应 反应
3
6.酯
概念 羧酸分子羧基中的羟基(—OH)被—OR取代后的生成物,简写为RCOOR
官能团
酯基( )
物理性质 低级酯(如乙酸乙酯)密度比水小,难溶于水,易溶于有机溶剂,具有芳香气味
化学性质 与HO发生取代反应也叫水解反应
2
①用作香料,如作饮料、香水等中的香料。
用途
②用作溶剂,如作指甲油、胶水的溶剂。
知识点三、官能团与有机物的分类
1.烃的衍生物
(1)定义:烃分子的氢原子被其他原子或原子团所代替的一系列物质称为烃的衍生物。
(2)官能团:决定有机化合物的化学特性的原子或原子团叫作官能团。
2.常见官能团与物质类别及性质
>C=C< —C≡C— —OH —CHO —COOH —COOR
官能团
碳碳双键 碳碳三键 羟基 醛基 羧基 酯基
类别 烯烃 炔烃 醇 醛 羧酸 酯
加成、氧 加成、氧
置换、取代、
性质 化、 化、 氧化 中和、取代 取代
氧化
加聚 加聚
代表物 CH=CH CH≡CH CHCHOH CHCHO CHCOOH CHCOOC H
2 2 3 2 3 3 3 2 5
3.判断陌生有机物性质的一般方法
分析—\s\up 4()联想—\s\up 4()结论—\s\up 4()
——→ ——→ ——→
4.常见有机物的转化关系
5.常见有机物与液溴、溴水、溴的四氯化碳溶液、酸性KMnO 溶液反应的比较
4
液溴 溴水 溴的四氯化碳溶液 KMnO 酸性溶液
4
光照条件下发生取代反 不反应,互溶不褪
甲烷 不反应 不反应
应 色
乙烯 常温加成褪色 常温加成褪色 常温加成褪色 氧化褪色不反应,互溶不褪
乙醇 不反应,互溶不褪色 不反应,互溶不褪色 氧化褪色
色
不反应,互溶不褪
乙酸 不反应,互溶不褪色 不反应,互溶不褪色 不反应
色
四、基本营养物质
知识点一.糖类
1.组成和分类
(1)组成:由C、H、O三种元素组成,大多数糖类符合通式C (H O) 。
n 2 m
(2)分类:糖类根据其能否水解以及水解产物的不同来分类。
类别 单糖 低聚糖(以双糖为例) 多糖
不能再水解成更小的糖分 1 mol双糖能水解成2 1 mol 多糖能水解成n mol(n>10)
特点
子 mol单糖 单糖
化学式 C H O C H O (C H O)
6 12 6 12 22 11 6 10 5 n
常见物质 葡萄糖、果糖 蔗糖、麦芽糖 淀粉、纤维素
关系 互为同分异构体 互为同分异构体 不属于同分异构体
淀粉可用于制造葡萄糖和酒精;纤
用途 可用于制造药品、糖果等 可用作甜味剂
维素可用于制造无烟火药、纸张等
注意:根据糖有无还原性,可分为还原性糖如葡萄糖、果糖、麦芽糖;非还原性糖如蔗糖、淀粉、纤维
素。
2.葡萄糖的结构与性质
(1)结构特点
最简式 分子式 结构简式 官能团
CHO C H O CHOH(CHOH) CHO —OH、—CHO
2 6 12 6 2 4
(2)主要化学性质
官能团 反应 应用
与新制的Cu(OH) 浊液加热产生砖红色沉淀 可用于尿糖的检测
2
—CHO 氧化反应
与银氨溶液加热,产生光亮的银镜 水瓶胆镀银
与金属钠反应 ——
—OH 发生催化氧化反应 ——
与乙酸发生酯化反应 ——
体内氧化 在人体组织中发生氧化反应,C H O+6O―→6CO+6HO 为生命活动提供能量
6 12 6 2 2 2
3.蔗糖、淀粉、纤维素的性质及应用
(1)存在及主要性质
物质 在自然界的存在 主要性质
C H O +HO催化剂ΔC H O+C H O
12 22 11 2 ——— 6 12 6 6 12 6
蔗糖 甘蔗、甜菜等植物体内
蔗糖 葡萄糖 果糖植物种子和块根、大米、小 (C H O)+HO催化剂ΔnC H O
6 10 5 n 2 ——— 6 12 6
淀粉
麦 淀粉 葡萄糖
植物的红细胞壁、棉花、木 C H O)+HO催化剂ΔnC H O
6 10 5 n 2 ——— 6 12 6
纤维素
材 纤维素 葡萄糖
(2)淀粉的特征反应:淀粉溶液遇I 变蓝色。
2
(3)淀粉水解及水解程度的检验
实验步骤
情况 现象A 现象B 结论
① 溶液呈蓝色 未产生砖红色沉淀 未水解
实验现象及结论
② 溶液呈蓝色 出现砖红色沉淀 部分水解
③ 溶液不呈蓝色 出现砖红色沉淀 完全水解
(4)糖类在生产、生活中的应用
淀粉 为人体提供能量淀粉:[(C H O)]酶—\s\up 4()糊精[(C H O) ,m<n]酶—\s\up 4()麦芽糖
6 10 5 n → 6 10 5 m →
(C H O )酶—\s\up 4()葡萄糖(C H O)缓慢氧\s\up 4()CO 和HO
12 22 11 → 6 12 6 化—— 2 2
食草动物的体内有纤维素水解酶,可将纤维素水解生成葡萄糖;人体内,食物中的
纤维素
纤维素能刺激肠道蠕动,促进消化和排泄。
工业原料,二者水解生成的葡萄糖在酶的作用下转化为乙醇,用于酿酒和生产燃料
淀粉和纤维素
乙醇:C H O(葡萄糖)酶—\s\up 4()2C HOH+2CO↑
6 12 6 → 2 5 2
知识点二、蛋白质
1.存在和组成
广泛存在于生物体内,是组成细胞的基础物质。动物的肌肉、皮肤、毛发等的主要成分都是
存在
蛋白质
由C、H、O、N、S等元素组成,是一类结构非常复杂、相对分子质量很大(几万到几千万)
组成
的有机化合物
2.物理性质:有的蛋白质能能溶于水,如鸡蛋清;有的不溶于水,如丝、毛等。
3.化学性质
水解 蛋白质水解生成各种氨基酸
概念 浓的盐溶液使蛋白质的溶解度降低而使蛋白质从溶液中析出的过程
条件 浓的轻金属盐溶液或铵盐溶液(或轻金属盐固体或铵盐固体)
盐析
特点 是可逆过程,继续加水时能使沉淀溶解,不影响蛋白质的生理活性
实质 溶解度降低,物理变化
概念 蛋白质在加热、酸、碱等条件下性质发生改变而聚沉
紫外线照射、加热或加入某些有机化合物(如甲醛、乙醇等)、强酸、强
条件
变性
碱、重金属盐(如铅盐、铜盐、汞盐等)
特点 不可逆过程,蛋白质失去生理活性
实质 结构性质改变,化学变化显色反应 某些蛋白质遇浓硝酸显黄色
蛋白质的灼烧 蛋白质灼烧时有烧焦羽毛的气味,常用此性质来鉴别蛋白质
4.氨基酸
组成元素 官能团 化学性质
氨基(—NH ) 与酸、碱均可以发生反应
2
C、H、N、O
羧基(—COOH) 自身发生聚合反应:氨基酸―→多肽―→蛋白质
5.主要用途
作为人体必需的营养物质。
食用
蛋白质――――――――→氨基酸―――→蛋白质(如激素、酶等)―→尿素
纺织业 动物的毛和蚕丝织成的丝绸制作服装
医药业 从动物皮、骨中提取的明胶生产胶囊,用驴皮制阿胶(中药材)
工业
从动物皮、骨中提取的明胶用作食品增稠剂,从牛奶和大豆中提取酪素可制作食
食品业
用途 品
从动物皮、骨中提取的明胶生产摄影用感光材料,从牛奶和大豆中提取的酪素可
化工业
制作涂料
酶 一类特殊的蛋白质,是生物体内重要的催化剂,应用于医药、食品、纺织等领域
知识点三、油脂
1.分类、组成和结构
分类 概念 组成元素 结构
植物油脂通常呈液态,
油
如:豆油、花生油等
油脂是一类特殊的酯,可以
C、H、O 看作是高级脂肪酸与甘油(丙
脂肪
动物油脂通常呈固态, 三醇)经酯化反应生成的酯
如:牛、羊等的脂肪
2.物理性质:油脂都难溶于水,易溶于乙醇、乙醚等有机溶剂,密度一般比水小。
3.常见高级脂肪酸及甘油
饱和脂肪酸酸 不饱和脂肪酸酸
名称 甘油
硬脂酸 软脂酸 油酸 亚油酸
结构简式 C H COOH C H COOH C H COOH C H COOH C H(OH)
17 35 15 31 17 33 17 31 3 5 3
4.化学性质
酸性水解
+3HO R COOH+R COOH+R COOH+
2 1 2 3
水解反应
碱性水解
(皂化反
应) +3NaOH→R COONa+R COONa+R COONa+
1 2 3加成反应 液态植物油(含碳碳不饱和键)H2—\s\up 4()固态脂肪(人造脂肪)
—→
5.生产、生活中的应用
(1)油脂是产生能量最高的营养物质:人体中的脂肪是维持生命活动的一种备用能源;油脂能保持体温
和保护内脏器官。
(2)油脂能促进脂溶性维生素(如维生素A、D、E、K)的吸收,并为人体提供亚油酸等必需脂肪酸。
(3)油脂能增加食物的滋味,增进食欲,保证机体的正常生理功能