文档内容
第一章 章末测试(提升)
满分100分,考试用时75分钟
一、选择题:本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。在每小
题给出的四个选项中,只有一项是符合题目要求的
1.下列反应中生成物的总能量高于反应物的总能量的是
A.碳酸钙受热分解 B.乙醇燃烧 C.钠与水反应 D.氧化钙溶于水
【答案】A
【解析】A.碳酸钙受热分解属于吸热反应,生成物总能量高于反应物总能量,故A正确;
B.乙醇燃烧属于放热反应,生成物的总能量小于反应物的总能量,故B错误;
C.钠与水反应属于放热反应,生成物的总能量小于反应物的总能量,故C错误;
D.氧化钙溶于水与水发生化合反应,属于放热反应,生成物的总能量小于反应物的总能量,故D错误;
故选A。
2.(2022河南省)石墨在一定条件下可转化为金刚石,已知12g石墨完全转化为金刚石时,要吸收QkJ
的热量,下列说法正确的是
A.石墨不如金刚石稳定
B.金刚石与石墨的结构是相同的
C.等物质的量的石墨与金刚石完全燃烧,金刚石放出的热量多
D.等物质的量的石墨与金刚石完全燃烧,石墨放出的热量多
【答案】C
【解析】A.由题给信息,判断出石墨能量比金刚石低,能量越低越稳定,所以石墨比金刚石稳定,故A
错误;
B.金刚石和石墨是同种元素形成的两种不同单质,结构不同。金刚石是立体网状结构,石墨是片层状结
构,故B错误;
C.石墨、金刚石都是碳单质,由于金刚石能量高于石墨,等物质的量的金刚石和石墨燃烧时,金刚石燃
烧放热多,故C正确;
D.由C选项可知,金刚石燃烧放热多,故D错误;
答案选C。
3.人体内葡萄糖的消耗可用下列热化学方程式表示:C H O(s)+6O(g)=6CO (g)+6HO(l) ΔH=-2800.6
6 12 6 2 2 2
kJ·mol-1;如果某人每天消耗12540 kJ热量,则他每天至少要摄入葡萄糖的质量为
A.806 g B.1000 g C.1250 g D.1500 g【答案】A
【解析】根据葡萄糖热化学方程式可知每天需要摄入葡萄糖的物质的量为: ,葡萄糖的质量
为 ×180 g/mol=806 g,综上所述故选A。
4.已知:N(g)+3H(g)=2NH (g) ΔH=-92.4 kJ /mol 。若断裂1molH-H键、1molN-H需要吸收的能量分别为
2 2 3
436kJ、391kJ,则断裂1molN≡N需要吸收的能量为
A.431 kJ B.945.6 kJ C.649 kJ D.869 kJ
【答案】B
【解析】设 键能为 ,则 ,解得 ,
故断裂1 mol 键需要能量为945.6 kJ;
故选B。
5.氢氟酸是一种弱酸,可用来刻蚀玻璃。
①HF(aq)+OH-(aq) = F-(aq)+H O(l) ΔH=a kJ·mol-1
2
②HO+(aq)+OH-(aq) = 2H O(l) ΔH=b kJ·mol-1
3 2
③HF(aq)+HO(l) HO+(aq)+F-(aq) ΔH=c kJ·mol-1
2 3
④F-(aq)+H
2
O(l) ⇌HF(aq)+OH-(aq) ΔH=d kJ·mol-1
已知:a<b<0,⇌下列说法正确的是
A.HF的电离过程吸热 B.c=a-b,c<0
C.c>0,d<0 D.d=b+c,d<0
【答案】B
【解析】A.根据③式是电离方程式,③=①-②,ΔH=c=a-b,由于a0。故C不正确。
D.反应④是反应①的逆过程,故d=-a>0。故不正确。
故选答案B。
6.已知:25℃、101kPa时,1g H 完全燃烧生成液态水放出142.9kJ的热量,下列热化学方程式中书写正
2
确的是
A.2H(g) + O(g) = 2HO(l) ΔH = -142.9kJ/mol
2 2 2
B.H(g)+ O(g)= H O(l) ΔH = -285.8kJ/mol
2 2 2C.2H(g) + O(g) = 2HO(g) ΔH = -571.6kJ/mol
2 2 2
D.H(g) + O(g) = HO(g) ΔH = +285.8kJ/mol
2 2 2
【答案】B
【解析】已知:25℃、101kPa时,1g H 完全燃烧生成液态水放出142.9kJ的热量,因此1mol氢气即2g氢
2
气完全燃烧生成液态水放出285.8kJ的热量,所以热化学方程式为H(g)+ O(g)=HO(l) ΔH=-285.8kJ/
2 2 2
mol。
答案选B。
7.已知:(1)H (g)+ O(g)═H O(g) ΔH=akJ/mol
2 2 2
(2)2H (g)+O(g)═2H O(g) ΔH=bkJ/mol
2 2 2
(3)H (g)+ O(g)═H O(l) ΔH=ckJ/mol
2 2 2
(4)2H (g)+O(g)═2H O(l) ΔH=dkJ/mol
2 2 2
下列关系式中正确的是( )
A.a<c<0 B.b>d>0 C.2a=b<0 D.2c=d>0
【答案】C
【解析】A.(1)式和(3)式中水的状态不同,(3)中生成的是液态水,放出的热量多,生成液态水的焓变数值
小于生成气态水的焓变,所以c<a<0,故A错误;
B.(2)式和(4)式中水的状态不同,(4)中生成的是液态水,放出的热量多,生成液态水的焓变数值小于生成
气态水的焓变,所以d<b<0,故B错误;
C.燃烧反应为放热反应,ΔH<0,热化学方程式的焓变与化学计量数成正比,(2)式化学计量数为(1)式化
学计量数的两倍,(2)式的焓变也是(1)的两倍,故b=2a<0,故C正确;
D.燃烧反应为放热反应,ΔH<0,热化学方程式的焓变与化学计量数成正比,(4)式化学计量数为(3)式化
学计量数的两倍,(4)式焓变也是(3)的两倍,d=2c<0,故D错误;
答案选C。
8.已知: ; ;
、 和 键的键能( )分别为436、496和462,则a为
A. B. C. D.
【答案】A【解析】①
②
根据盖斯定律①×2-②得 ,断裂旧键需要吸热,形成新
键需要放热,根据吸热为正,放热为负,可得+ ×4-436×2-496= ,
a=+130;
故选A。
9.在1200℃时,天然气脱硫工艺中会发生下列反应
①HS(g)+ O(g)=SO(g)+HO(g) H
2 2 2 2 1
△
②2HS(g)+SO (g)= S(g)+2HO(g) H
2 2 2 2 2
△
③HS(g)+ O(g)=S(g)+H O(g) H
2 2 2 3
△
④2S(g) =S (g) H
2 4
则△H
4
的正确表△达式为( )
A.△H=2/3(△H+ H-3 H)
4 1 2 3
B.△H
4
=2/3(3 H
3
-△H
1
- △H
2
)
C.△H
4
=3/2(△△H
1
+△H
2
-3△ H
3
)
D.△H
4
=3/2(△H
1
-△H
2
-3△H
3
)
【答案】A △ △
【解析】根据盖斯定律,①× -③× 得⑤: S(g)+ O(g)= SO (g) H= (△H- H);根据盖斯
2 2 5 1 3
△ △
定律,②× -③× 得⑥: SO (g)+ S(g)= O(g) + S (g) H= (△H-2 H);⑤+⑥得:2S(g)
2 2 2 6 2 3
△ △
=S (g) H= (△H+ H-3 H),答案为A。
2 4 1 2 3
△ △ △
10.白磷与氧可发生如下反应:P+5O =P O 。已知断裂下列化学键需要吸收的能量分别为:P—P akJ·mol
4 2 4 10
—1、P—O bkJ·mol—1、P=O ckJ·mol—1、O=O dkJ·mol—1。根据图示的分子结构和有关数据估算该反应的△H,其中正确的是
A.(6a+5d-4c-12b)kJ·mol—1
B.(4c+12b-6a-5d)kJ·mol—1
C.(4c+12b-4a-5d)kJ·mol—1
D.(4a+5d-4c-12b)kJ·mol—1
【答案】A
【解析】反应热等于断键吸收的总能量与形成化学键所放出的能量的差值,由图可以看出:P 中有6mol的
4
P-P,5mol的O 中含有5molO=O,1mol的PO 中含有4mol的P=O,12mol的P-O,所以根据方程式
2 4 10
可知反应热△H=(6a+5d-4c-12b)kJ·mol-1。答案选A。
11.氢卤酸的能量关系如图所示,下列说法正确的是( )
A.已知 气体溶于水放热,则 的△H<0
1
B.相同条件下, 的△H2比 的小
C.相同条件下, 的( H+ H4)比 的大
3
D.一定条件下,气态原子△生成△ 键放出 能量,则该条件下△H
2
=+akJ/mol
【答案】D
【解析】A.△H1代表的是HX气体从溶液中逸出过程的焓变,因为 气体溶于水放热,则 气体溶于
水的逆过程吸热,即HF的△H>0,A错误;
1
B.由于 比 稳定,所以相同条件下 的△H2比 的大,B错误;
C.( H3+ H4)代表 的焓变,与是 的还是 的H原子无关,C错误;
△ △
D.一定条件下,气态原子生成 键放出 能量,则断开 键形成气态原子吸收 的能量,即△H2=+akJ/mol,D正确;
故选D。
12.下列关于热化学方程式的说法正确的是
A.若H 的燃烧热为 ,则热化学方程式为
2
B.若 和 完全反应放热98.3 kJ,则热化学方程式为
C.若 ,则稀硫酸与稀Ba(OH) 反应的热化学方程式为
2
D.若31 g白磷的能量比31 g红磷多b kJ,则白磷转化为红磷的热化学方程式为
【答案】D
【解析】A.反应热的多少与物质的存在状态有关,未注明物质的存在状态,因此不能表示该反应的反应
热,A错误;
B.反应热与反应的物质多少相对应,由于该反应为可逆反应,求不出生成的三氧化硫的物质的量,写不
出其热化学方程式 ,B错误;
C.稀硫酸与Ba(OH) 发生中和反应时除产生2 mol的HO放出热量外,反应产生BaSO 沉淀时也会放出热
2 2 4
量,反应放出热量越多,则反应热越小,故稀硫酸与稀Ba(OH) 反应的热化学方程式为
2
D.1 mol的白磷质量是124 g,若31 g白磷的能量比31 g红磷多b kJ,则1 mol白磷的能量比等质量的红
磷的能量多4b kJ,故白磷转化为红磷的热化学方程式为 ,D正确;
故合理选项是D。
13.已知部分化学键的键能数据如表所示:
化学键键能 413 347 614 436
则下列有关反应 的说法正确的是
A.生成1mol乙烷气体时放出热量123 kJ
B.生成1mol乙烷气体时吸收热量123 kJ
C.该反应的热化学方程式为
D.该反应为放热反应,无需加热即可发生该反应
【答案】A
【解析】A.根据反应方程式可知,该反应的反应焓变为
,则生成1mol乙烷气体时放出的热量为123 kJ,A
正确;
B.根据A选项可知,B错误;
C.该反应的热化学方程式 ,C错误;
D.该反应需在催化剂且加热条件下才能实现,D错误;
答案选A。
14.在实验室进行中和热测定实验,下列有关叙述错误的是
A.大小烧杯之间塞满碎泡沫,目的是减少热量损失
B.测量终止温度时,应当记录混合溶液的最高温度
C.为了使酸碱充分反应,应当缓慢分次倒入 溶液并搅拌
D.可用塑料材质的环形搅拌棒代替环形玻璃搅拌棒
【答案】C
【解析】A. 大小烧杯之间塞满碎泡沫,目的是减少热量损失,减小测量误差,故A正确;
B. 充分反应,放出热量最多时,温度最高,测量终止温度时,应当记录混合溶液的最高温度,故B正确;
C. 为了使酸碱充分反应,应当快速一次倒入 溶液并搅拌,防止热量散失,故C错误;
D. 塑料材质的环形搅拌棒导热能力差,可用塑料材质的环形搅拌棒代替环形玻璃搅拌棒,故D正确;
故选C。
15.用CH 催化还原NO 可以消除氮氧化物的污染,例如:
4 2
①CH(g)+4NO (g)=4NO(g)+CO (g)+2HO(g) H=-574kJ·mol-1
4 2 2 2
②CH
4
(g)+4NO(g)=2N
2
(g)+CO
2
(g)+2H
2
O(g) △H=-1160kJ·mol-1
△下列说法不正确的是
A.由反应①可知CH(g)+4NO (g)=4NO(g)+CO (g)+2HO(l) H<-574kJ·mol-1
4 2 2 2
B.反应①②转移的电子数相同 △
C.若用标准状况下4.48LCH 还原NO 至N,放出的热量为173.4kJ
4 2 2
D.若用标准状况下4.48LCH 还原NO 至N,整个过程中转移的电子总物质的量为0.80mol
4 2 2
【答案】D
【解析】A.根据反应①可知,当生成液态水时,由于气体转化为液体时放热,所以生成液态水放出的热
量更多,放热越多,焓变越小,A正确;
B.物质的量相等的甲烷分别参加反应①、②,C元素的化合价均是从-4价升高到+4价,所以转移电子数
相同,B正确;
C.标准状况下4.48L甲烷的物质的量是0.2mol,还原NO 至N,放出的热量为 kJ/
2 2
mol×0.2mol=173.4kJ,C正确;
D.0.2mol甲烷还原NO 至N,C元素的化合价从-4价升高到+4价,所以转移电子总数是
2 2
0.2mol×8=1.6mol,D错误;
答案选D。
16.室温下,将1molCuSO ·5H O(s)溶于水会使溶液温度降低,热效应为ΔH,将1mol的CuSO (s)溶于水
4 2 1 4
会使溶液温度升高,热效应为ΔH;将1molCuSO ·5H O加热到45℃时,失去两分子水、热效应为ΔH;
2 4 2 3
继续加热113℃时,再失去两分子水、热效应为ΔH;最后加热到258℃以上,能脱去最后一分子水、热效
4
应为ΔH。下列判断一定正确的是
5
A.ΔH<ΔH+ΔH +ΔH B.ΔH=ΔH
1 3 4 5 2 3
C.ΔH+ΔH +ΔH +ΔH =ΔH D.ΔH+ΔH =ΔH+ΔH +ΔH
1 3 4 5 2 1 2 3 4 5
【答案】A
【解析】根据题干信息可知:
①CuSO ·5H O(s)=CuSO (aq)+5H O(l)ΔH >0
4 2 4 2 1
②CuSO (s)=CuSO (aq)ΔH<0
4 4 2
③CuSO ·5H O(s)=CuSO ·3H O(s)+2H O(l)ΔH >0
4 2 4 2 2 3
④CuSO ·3H O(s)=CuSO ·H O(s)+2H O(l)ΔH >0
4 2 4 2 2 4
⑤CuSO ·H O(s)=CuSO (s)+HO(l)ΔH >0
4 2 4 2 5
根据盖斯定律可知②+③+④+⑤即得到①,则ΔH=ΔH+ΔH +ΔH +ΔH ,因此ΔH<ΔH+ΔH +ΔH 一定是
1 2 3 4 5 1 3 4 5
正确的。答案选A。二、非选择题:共56分。
17.(14分)Ⅰ.已知下列热化学方程式:①H(g)+ O(g)=HO(l) ∆H=-285kJ·mol-1,
2 2 2
②H(g)+ O(g)=HO(g) ∆H=-241.8kJ·mol-1,
2 2 2
③C(s)+ O(g)=CO(g) ∆H=-110.5kJ·mol-1,
2
④C(s)+O(g)=CO (g)ΔH=-393.5kJ·mol-1,回答下列问题:
2 2
(1)C燃烧热的热化学方程式为___________;(填序号)
(2)燃烧1gH 生成气态水,放出的热量为___________。
2
Ⅱ.中和热是一类重要的反应热,也是化学研究的重要课题。已知强酸稀溶液与强碱稀溶液发生反应的热
化学方程式为H+(aq)+OH-(aq)=H O(l) ∆H =-57.3kJ•mol-1。
2 1
(3)下列各组试剂混合发生反应的离子方程式为H++OH-=H O的是___________(填序号)。
2
A.盐酸与氢氧化钠溶液
B.稀硫酸与氢氧化钡溶液
C.醋酸与氢氧化钠固体
D.硫酸氢钠溶液与氢氧化钠溶液
E.氢氧化镁溶于稀盐酸
(4)若稀硫酸与氢氧化钠固体反应生成1molH O(l),则反应放出的热量___________(填“大于”“等于”或
2
“小于”)57.3kJ,原因是___________。
Ⅲ.如图所示,某反应在不同条件下的反应历程分别为a、b。
(5)据图可判断出反应物的总键能___________(填“>”“<”或“=”,下同)生成物的总键能,则该反
应的反应热∆H ___________0。
【答案】(1) ④
(2)142.5kJ
(3)AD(4)大于 氢氧化钠固体溶解放热
(5)< <
【解析】Ⅰ.(1) 燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的热量,C的稳定氧化物为CO,所
2
以C的燃烧热的热化学方程式为④;
(2)根据热化学方程式①可知1mol氢气,即2g氢气燃烧生成液态水放出的热量为285kJ,则燃烧1g氢气液
态水放出的热量为285kJ÷2=142.5kJ;
Ⅱ.A.HCl和NaOH均为强电解质,反应生成强电解质NaCl和水,可以用H++OH-=H O表示,A符合题
2
意;
B.稀硫酸和氢氧化钡反应时除了生成水还生成硫酸钡沉淀,不能用H++OH-=H O表示,B不符合题意;
2
C.醋酸为弱酸,不能写成离子,故不能用H++OH-=H O表示,C不符合题意;
2
D.硫酸氢钠在水溶液中电离得到SO 、H+和Na+,与氢氧化钠反应生成水和强电解质硫酸钠,可以用H+
+OH-=H O表示,D符合题意;
2
E.氢氧化镁难溶于水,不能写成离子,故不能用H++OH-=H O表示,E不符合题意;
2
综上所述答案为AD;
(2)氢氧化钠固体溶于水时也会放热,所以稀硫酸与氢氧化钠固体反应生成1molH O(l),反应放出的热量大
2
于57.3kJ;
Ⅲ.据图可知反应物的总能量高于生成物的总能量,所以为放热反应,则反应物的总键能<生成物的总键
能,反应热∆H=生成物的总能量-反应物的总能量<0。
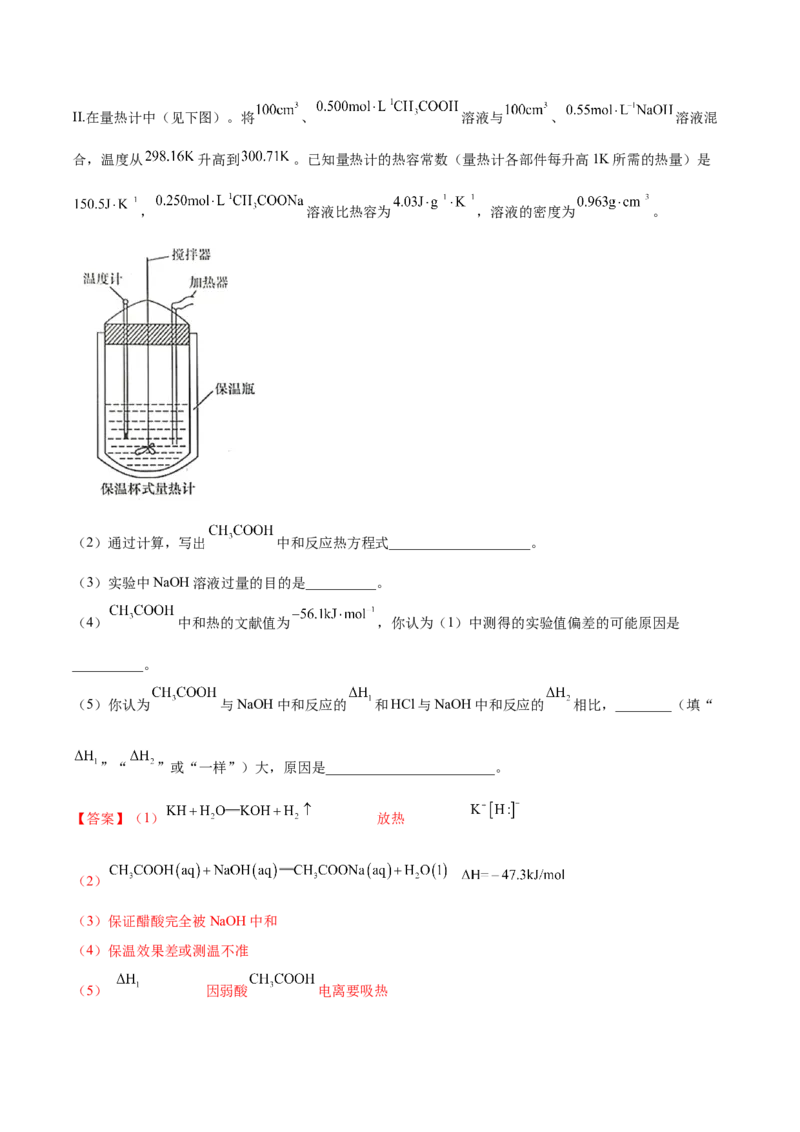
18.(12分)Ⅰ.将 与 混合在一起放入小烧杯中,将烧杯放在滴有3~4滴水
的玻璃片上,用玻璃棒迅速搅拌。
(1)实验中玻璃棒的作用___________。
(2)写出有关反应的化学方程式:___________。
(3)实验中观察到的现象有___________,能闻到刺激性气味,反应混合物成糊状。
(4)实验中的现象说明该反应为___________ (填“吸热”或“放热”)反应,反应中反应物的总能量
___________(填“大于”或“小于”)生成物的总能量。
Ⅱ.某化学反应中,设反应物的总能量为E,生成物的总能量为E
1 2。(5)若E>E,则该反应为__________(填“放热”或“吸热”)反应。该反应可用图__________(填“A”或
1 2
“B”)表示。
(6)若E