文档内容
2018年中考化学一轮复习·《质量守恒定律和化学方程式》真题练习
一、选择题
1.(2017济南)宏观辨识与微观探析是化学学科的重要核心素养。如图为某化学
反应的微观模拟示意图,下列说法中,正确的是( )
A.反应前后氧元素的化合价没有改变
B.生成的丙、丁两物质的分子个数比为2:1
C.该反应属于复分解反应
D.参加反应的甲、乙两物质的质量比为13:16
【答案】B
【解析】反应的化学方程式为2C H +5O 4CO +2H O.A选项,反应前氧元素
2 2 2 2 2
的化合价为0价,反应后氧元素的化合价为﹣2价,故A错误.B选项,由化学方
程式可知,生成的丙、丁两物质的分子个数比为2:1,故B正确.C选项,反应物为
一种单质和一种化合物,所以该反应不是复分解反应,故C错误.D选择,参加反
应的甲、乙两物质的质量比为(26×2):(32×5)=13:40,故D错误.
2.(2017南宁)下列关于化学方程式H SO +2H ==S↓+3H O的理解,错误的是(
2 3 2 2
)
A.生成物有沉淀
B.反应物是H SO 和H ,生成物是S和H O
2 3 2 2
C.该反应中,反应前后原子的种类和数目都不变
D.每1份质量的H SO 和2份质量的H 完全反应,生成1份质量的S和3份
2 3 2
质量的H O
2
【答案】D
【解析】 A.在化学方程式中有“↓”表示有沉淀产生,故A选项正确;B.在化学
方程式中,等号前面表示反应物,等号后面表示生成物,故 B正确;C.根据质量
1守恒定律,在化学反应前后原子的种类和数目都不变,故 C正确;D.根据质量守
恒定律,反应物的总质量和生成物的总质量相等,正确的表述应为:82份质量的
H SO 和4份质量的H 完全反应,生成32份质量的S和54份质量的H O,故D
2 3 2 2
错误。
3.(2017衢州)质量守恒定律是自然界基本的规律之一。下列装置及实验(天平未
画出)能用来验证质量守恒定律的是( )
【答案】A
【解答】A、反应无物质跑出也无物质进入可以验证质量守恒定律,A正确;
B、这是扩散现象未出现化学反应,B错误;
C、镁条燃烧生成的氧化镁因氧来自空气所以质量增加不能验证质量守恒定律,C
错误;
D、反应生成的氧气跑出容器内质量减小不能验证质量守恒定律,D错误。
4.(2017内蒙古呼和浩特市)下图表示某化学反应的微观示意图,依据图分析判
断,下列说法正确的是( )
A.甲物质由5个原子构成
B.化学变化前后硅元素的化合价不变
C.参加反应的乙的质量和生成的丁中氢元素的质量相等
D.参加反应的甲、乙两种物质的分子个数比为1:1
【答案】C
【解析】本题考查化学变化中的微观示意图。由图知,甲为SiCl ,乙为H ,丙为Si,
4 2
丁为HCl,即该反应为:SiCl +2H 一定条件 Si+4HCl.
4 2
甲物质由SiCl 分子构成,每个SiCl 分子由1个Si原子和4个Cl原子构成,A错
4 4
2误;
在该反应前后,Si元素化合价由+4价变为0价,B错误;
由化学反应中的元素守恒可知,参加反应的氢气的质量等于反应后生成氯化氢中
氢元素的质量,C正确;
在该反应中,参加反应的甲、乙两种物质的分子个数比为1:2,D错误。
5.(2017湖南省永州市)为避免汽车尾气的有害气体对大气的污染,目前最有效的方
法是给汽车安装尾气净化装置。其净化原理是2NO+2CO N +xCO ,下列说法不
2 2
正确的是( )
A.x=2
B.最终排放的汽车尾气是混合物
C.反应中氮元素的化合价由+2价变为0价
D. 该反应生成的N 和CO 的质量比为1:2
2 2
【答案】D
【解析】本题考查质量守恒定律及其应用、纯净物和混合物的判别、有关元素化合
价的计算。A.根据反应的化学方程式可知,反应物中碳、氮、氧原子个数分别为
2、2、4,反应后的生成物中碳、氮、氧原子个数分别为x、2、2x,根据化学反应前后
原子种类、数目不变,则x=2,所以该选项不符合题意;
B.根据化学方程式可知生成物是氮气和二氧化碳两种物质,属于混合物,所以该
选项不符合题意;
C.反应前氮元素存在于一氧化氮中,化合价为+2;反应后氮元素存在于氮气中,
化合价为0,所以该选项不符合题意;
D.该反应生成的氮气和二氧化碳的质量比为28:2×44=7:22,所以该选项符合题
意。
6.(2017长春市)银器变黑的原理是:4Ag+2H S+O = 2X+2H O。下列说法中,正确
2 2 2
的是
A.X的化学式为AgS B.反应中H S和O 的质量比为17:16
2 2
C.该反应属于置换反应 D.反应中氧元素的化合价由0变为-2
【答案】D
【解析】此题主要考查质量守恒定律的运用及相关知识。
3A、由质量守恒定律可知X的化学式为Ag S,故A错误;
2
B、根据化学方程式的意义可得:反应中 H S和O 的质量比=2×(1×2+32):
2 2
(16×2)=17:8,故B错误;
C、置换反应是指单质与化合物反应生成另外的单质和化合物的化学反应,说明
参加反应物质只有两种,而从此反应中知参加反应物质有三种,故C错误;
D、此反应中参加反应的氧气是单质,则O 中氧元素化合价为0,生成的水中因H
2
为+1价,在化合物中正负化合价代数和为0,则氧元素为-2价,故D正确;故选D。
7.(2017四川省绵阳市)120℃时,取3g有机物R在氧气中完全燃烧,产物只有
CO 和H O。将其燃烧产物全部通入足量的浓硫酸和足量的澄清石灰水中,最终
2 2
浓硫酸增重1.8g,澄清石灰水中产生10g沉淀。下列判断正确的是( )
A.R的化学式一定是CH O B.6g R完全燃烧消耗氧气6.4g
2
C.R中碳元素的质量分数约为85.7% D.R仅由C、H两种元素组成,其质量
比为6:1
【答案】B
【解析】本题考查根据化学方程式的简单计算。由题知,浓硫酸增重的质量即反应
生成水的质量,澄清石灰水中产生沉淀的质量为二氧化碳与氢氧化钙反应生成碳
酸钙的质量。
1.8g水中含氢元素的质量为:1.8g×2/18=0.2g
生成10g碳酸钙所需二氧化碳的质量为:10g×44/100=4.4g;其中碳元素的质量
为:10g×12/100=1.2g
由此可知,3g R中含0.2g H元素和1.2g C元素,还含有O元素1.6g,则R中
C、H、O三种元素的原子个数比为1:2:1,即R的化学式为(CH O) ,(n≥1),A错
2 n
误;
由上述计算可知,3g R完全燃烧生成1.8g水和4.4g 二氧化碳,同时消耗氧气
的质量为3.2g;则6g R完全燃烧消耗氧气的质量为6.4g,B正确;
R中碳元素的质量分数=1.2g/3g×100%=40%,C错误;
由上述计算可知,R由C、H、O三种元素组成,D错误。
8.(2017四川省绵阳市)工业上常用空气中的氮气生产硝酸,其反应的化学方程
式如下:
①N +3H 高温、高压、催化剂 2NH ②4NH +5O 催化剂 4NO+6H O
2 2 3 3 2 2
4③2NO+O =2NO ④3NO +H O=2HNO +NO(NO难溶于水)
2 2 2 2 3
下列有关说法错误的是( )
A.上述①②③④中反应前后均有元素化合价的变化
B.用H O吸收NO 的过程中通入过量的O 可以提高硝酸的产量
2 2 2
C.反应②④都不属于四种基本反应类型中的任何一种,反应①③均属于化合反
应
D.在密闭容器中,将46g NO 溶于64g H O中形成HNO 溶液,其溶质的质量分
2 2 3
数为38.2%
【答案】D
【解析】本题考查化学方程式的意义及根据化学方程式的简单计算。
反应①由两种单质反应生成一种化合物,元素化合价分别由0价变为-3、+1价;
反应②氧元素化合价由0价变为-2价,N元素化合价由-3变为+2价;反应③N元
素化合价由+2变为+4价,氧元素化合价由0价变为-2价;反应④中N元素化合
价由+4分别变为+5、+2价,A正确;
由反应③④可知,当用H O吸收NO 的过程中通入过量的O 时,氧气可将反应
2 2 2
生成的NO气体再次转化为NO ,可以提高硝酸的产量,B正确;
2
反应②④都是由两种物质发生反应生成另外两种物质的反应,但不属于置换反应
或复分解反应,也不属于化合反应或分解反应;反应①③均由两种物质发生反应
生成另一种物质的反应,属于化合反应,C正确;
由反应④可知,46g NO 溶于64g H O中生成10g NO和42g HNO ,共形成硝酸
2 2 3
溶液的质量为100g,则形成硝酸溶液溶质的质量分数为42%,D错误。
9.(2017 怀化市,题号 13,分值 2) 某纯净物 X 燃烧的化学方程式为
,则X的化学式是()
A.C H B.C H C.C H O D.C H
2 2 2 4 2 6 2 6
【答案】B
【解析】此题考察质量守恒定律的应用,反应前后原子的种类数目不变。从题目可
以看出,反应后有两个碳原子,四个氢原子,所以反应物中也应该有两个碳原子,
四个氢原子,而氧原子反应前后相同,所以该物质含有两个碳原子,四个氢原子,
不含氧原子,所以选择B.
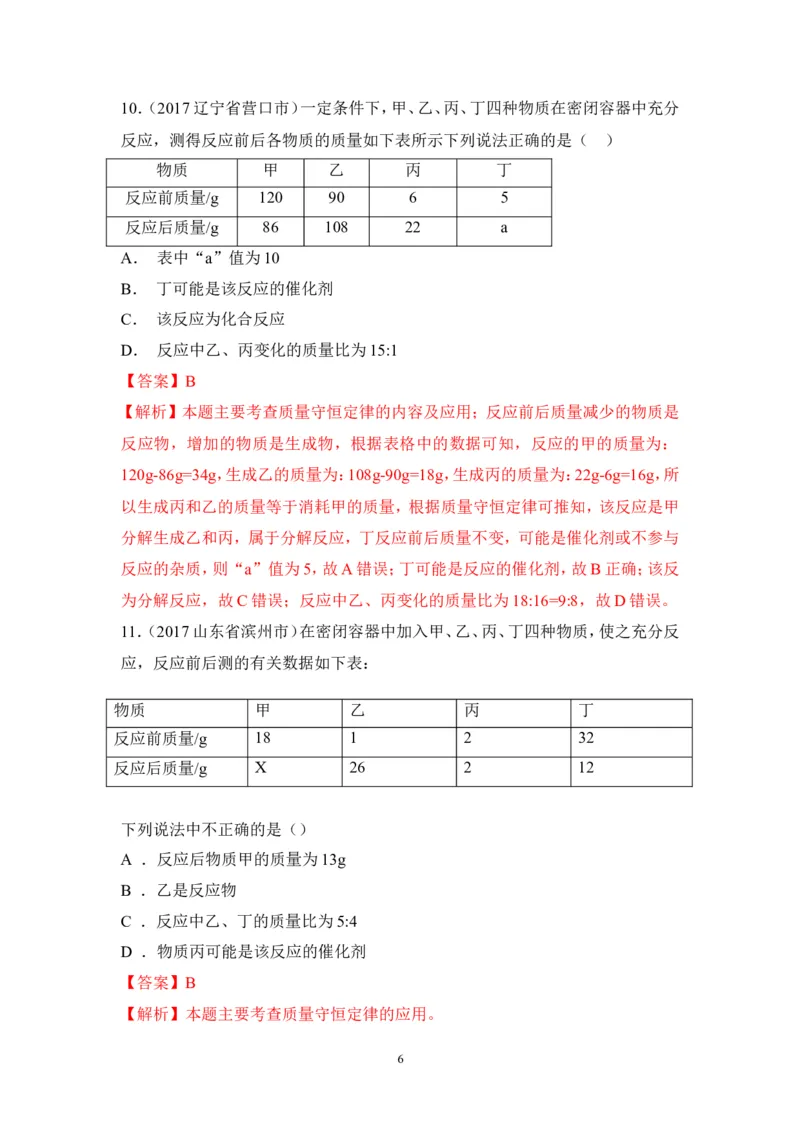
510.(2017辽宁省营口市)一定条件下,甲、乙、丙、丁四种物质在密闭容器中充分
反应,测得反应前后各物质的质量如下表所示下列说法正确的是( )
物质 甲 乙 丙 丁
反应前质量/g 120 90 6 5
反应后质量/g 86 108 22 a
A. 表中“a”值为10
B. 丁可能是该反应的催化剂
C. 该反应为化合反应
D. 反应中乙、丙变化的质量比为15:1
【答案】B
【解析】本题主要考查质量守恒定律的内容及应用;反应前后质量减少的物质是
反应物,增加的物质是生成物,根据表格中的数据可知,反应的甲的质量为:
120g-86g=34g,生成乙的质量为:108g-90g=18g,生成丙的质量为:22g-6g=16g,所
以生成丙和乙的质量等于消耗甲的质量,根据质量守恒定律可推知,该反应是甲
分解生成乙和丙,属于分解反应,丁反应前后质量不变,可能是催化剂或不参与
反应的杂质,则“a”值为5,故A错误;丁可能是反应的催化剂,故B正确;该反
为分解反应,故C错误;反应中乙、丙变化的质量比为18:16=9:8,故D错误。
11.(2017山东省滨州市)在密闭容器中加入甲、乙、丙、丁四种物质,使之充分反
应,反应前后测的有关数据如下表:
物质 甲 乙 丙 丁
反应前质量/g 18 1 2 32
反应后质量/g X 26 2 12
下列说法中不正确的是()
A .反应后物质甲的质量为13g
B .乙是反应物
C .反应中乙、丁的质量比为5:4
D .物质丙可能是该反应的催化剂
【答案】B
【解析】本题主要考查质量守恒定律的应用。
6A . 由 质 量 守 恒 定 律 可 知 , 化 学 反 应 前 后 物 质 的 总 质 量 不 变 , 即
18+1+2+32=x+26+2+12,求得x=13
B.反应前乙物质的质量为1g,反应后乙物质的质量为26g,乙的质量在增加,故
乙是生成物;
C.反应中乙、丁的质量比=(26-1):(32-12)=5:4
D.催化剂是能改变其他物质的化学反应速率,而本身的质量和化学性质在反应
前后不变的物质。物质丙反应前后质量不变,但其能否改变该反应的化学反应速
率,化学性质在反应前后是否改变无法判断,故丙可能是该反应的催化剂,但不
能说物质丙一定是该反应的催化剂。
12.(2017上海市) 根据化学方程式: ,无法获取的信
息是( )
A. 反应所需条件
B. 生成物的状态
C. 生成物的物质的量之比
D. 氧气可助燃
【答案】D
【解析】本题主要考查化学方程式表示的意义;由方程式可知该反应的反应条件
是通电,故A不符合题意;反应后生成的氢气和氧气为气态,“↑”表示物质为
气体,故B不符合题意;方程式中的化学计量数之比等于物质的量之比,故C不
符合题意;氧气是一种生成物,通过方程式不能获取氧气助燃的信息,故D符合
题意。
13.(2017年湖北省鄂州市)煤油中含有噻吩(用X表示),噻吩有令人不愉快的
气味,其燃烧时发生反应的化学方程式可表示为:X + 6O 4CO + SO +
2 2 2
2H O ,则噻吩的化学式为
2
A.C H S B.C H S C.C H S D.C H S
4 6 4 4 4 4 2 6 6
【答案】B
【解析】此题考查了质量守恒定律:在化学反应前后物质的总质量、元素的种类、
原子的种类、原子数目接原子的质量都不发生改变
7A 反应物C H S分子中有6个氢原子,反应后只有 2H O含4个氢原子,故错
4 6 2
误
B根据化学反应前后各元素原子个数相等可得X为C H S ,故正确。
4 4
C生成物中只有SO 中有一个硫原子而C H S 分子中有两个硫原子,故错误。
2 4 4 2
D反应物C H S中有6个碳原子而生成物只有4CO 含有4个碳原子,故错误。
6 6 2
14.(2017广西省来宾市)关于2H +O 2H O的读法不正确的是
2 2 2
A.氢气与氧气在点燃的条件下生成水
B.每2个氢分子与1个氧分子完全反应,生成2个水分子
C.常温下,每2体积的氧气与l体积的氧气完全反应,生成2体积的水
D.每4份质量的氢气与32份质量的氧气完全反应,生成36份质量的水
【答案】C
【解析】此题考查化学方程式的含义与读法;
A.化学方程式可以表示反应物、生成物及反应条件,因此,该反应方程式可读作
氢气和氧气在点燃的条件下生成水,A正确;
B.从微观的角度看,该化学方程式可读作:每2个氢气分子和1个氧气分子完全
反应,生成2个水分子,B正确;
C.常温下,当反应物、生成物都是气体时,化学方程式可以表示反应物、生成物之
间的体积关系,如果不是气体就不能表示体积关系,水在常温下是液体,所以C
错误;
D.化学方程式可以表示出反应物、生成物之间的关系,因此,该反应方程式为读
作:每4份质量的氢气与32份质量的氧气完全反应,生成36份质量的水,D正确;
15.(2017辽宁省沈阳市) 一种焰火火药中所含的Cu(NO ) 在燃放时产生绿色火
3 2
焰,发生如下反应:2Cu(NO ) 2CuO+O ↑+4X↑,其中X是一种污染空气的
3 2 2
有毒气体,依据质量守恒定律,推测X 应是( )
A.NO B.NO C.N O D.N O
2 2 5 2
【答案】A
【解析】本题考查质量守恒定律及其应用。根据反应的化学方程式可知,反应物中
铜、氮、氧原子个数分别为2、4、12,反应后的生成物中铜、氮、氧原子个数分别为
2、0、4,根据化学反应前后原子种类、数目不变,则4X含有4个氮原子和8个氧原
8子,则每个X子由1个氮原子和2个氧原子构成,则物质X化学式为NO ,所以选
2
A。
16.(2017陕西省)从陶瓷、玻璃、水泥到电子芯片,硅元素的用途非常广泛。工业
制取高纯硅的部分反应原理的微观示意图如下,有关说法不正确的是( )
高温
+ 4 X 硅原子
氯原子
甲 乙 丙 丁
氢原子
A.该反应属于置换反应 B.反应后硅元素的化合价升高
C.X的化学式是HCl D.图甲所示物质中硅、氯元素的质量比是14:71
【答案】B
【解析】此题主要考查化学反应的微观示意图。
A. 由图可知乙是氢气,氢气在高温的条件下具有还原性,把四氯化硅还原出硅
单质,故正确;
B. 反应前硅元素存在于四氯化硅中,化合价为+4,反应后被还原,化合价为0,化
合价降低,故错误;
C. 根据质量守恒定律,化学反应前后原子的种类和数目不变,可得X的化学式
是HCl,故正确;
D. 由图可知甲物质是四氯化硅,化学式为SiCl ,其硅、氯元素的质量比是28:35.
4
5×4=14:71,故正确;
17.(2017福建省) 炼铁炉中某反应的微观示意图(不同的球代表不同原子)如下
所示,下列说法正确的是( )
A.该反应属于化合反应
B.反应前后原子数目发生变化
C.反应前后各元素化合价均不变
D.反应前后元素种类发生变化
【答案】A
【解析】本题主要考查微观模型示意图表示的意义及质量守恒定律的应用;由图
示反应可知该反应是一种单质和一种化合物反应生成一种化合物,属于化合反应
9故A选项正确;化学反应都遵循质量守恒定律,化学反应前后原子个数、种类都
不变,故B错误;反应前后由单质转化为化合物中的元素一定有化合价改变,另
一种元素的化合价不一定改变,故C错误;根据质量守恒定律可知,化学反应前
后元素的种类不变,故D错误。
18.(2017年江苏省徐州市).甲、乙、丙、丁4种物质在密闭容器中充分反应,测
得反应前后各物质的质量如下表。下列说法正确的是
物质 甲 乙 丙 丁
反应前的质量/g 4 31 21 10
反应后的质量/g m 40 6 16
A.甲一定是该反应的催化剂 B.该反应一定是化合反应
C.丙物质一定属于化合物 D.乙、丁在反应中的质量比为5︰2
【答案】C
【解析】根据质量守恒定律,可计算出m=4,甲质量不变,可能是该反应的催化剂,
也可能是杂质,因此A错误;由于丙质量减少,乙、丁质量增加,所以发生的是分
解反应,丙一定是化合物,因此B错误,C正确;乙在反应中质量增加9、丁在反应
中质量增加6,因此二者反应中的质量比为3︰2,所以D错误。所以选C。
19.(2017黑龙江绥化市)地质人员考察时发现一种带螺纹的矿石。研究发现该矿
石能氧气中燃烧,主要反应是4X+11O 2Fe O +8SO ,下列说法正确的是(
2 2 3 2
)
A.该物质的化学式是FeS B.该物质由铁、硫、氧三种元素组成
2
C.氧气由两个氧原子构成 D.SO 中硫、氧元素质量比为1:2
2
【答案】A
【解析】本题考查的质量守恒定律和化学式。化学反应前后原子的种类和个数
不变,根据提供的反应方程式可以看出,反应前还少4个Fe、8个S,而X前
的化学计量数是4,故X的化学式是FeS ,故A正确;X的化学式是FeS ,根
2 2
据其化学式可以看出,该物质由铁、硫两种元素组成,故B错误;氧气由氧分
子构成,故C错误;SO 中硫、氧元素的质量比=32:(16×2)=1:1,故D错误。
2
20.(2017广西省来宾市)关于2H +O 2H O的读法不正确的是( )
2 2 2
A.氢气与氧气在点燃的条件下生成水
10B.每2个氢分子与1个氧分子完全反应,生成2个水分子
C.常温下,每2体积的氧气与l体积的氧气完全反应,生成2体积的水
D.每4份质量的氢气与32份质量的氧气完全反应,生成36份质量的水
【答案】C
【解析】此题考查化学方程式的含义与读法;
A.化学方程式可以表示反应物、生成物及反应条件,因此,该反应方程式可读作:
氢气和氧气在点燃的条件下生成水,A正确;
B.从微观的角度看,该化学方程式可读作:每2个氢气分子和1个氧气分子完全
反应,生成2个水分子,B正确;
C.常温下,当反应物、生成物都是气体时,化学方程式可以表示反应物、生成物之
间的体积关系,如果不是气体就不能表示体积关系,水在常温下是液体,所以C
错误;
D.化学方程式可以表示出反应物、生成物之间的关系,因此,该反应方程式为读
作:每4份质量的氢气与32份质量的氧气完全反应,生成36份质量的水,D正确;
二、填空题
1.(2017遂宁市)汽车尾气是导致酸雨的重要原因之一,为减少有害气体的排放,
人们在汽车排气管上安装“催化转换器",发生反应的微观示意图如下:
(1)写出乙图中物质的化学式__________。
(2)该反应中化合价有改变的两种元素是________________(填元素符号)。
【答案】(1)N (2分) ;(2)C、N(2分)
2
【解析】此题考察微粒的结构示意图和质量守恒定律及化合价的相关知识,在化
学反应前后原子的种类和数目不变。
(1)反应前后原子种类和个数不变,所以生成物中少两个氮原子,所以该物质
为氮气,化学式为N ;
2
11(2)反应物为一氧化碳和一氧化氮,碳元素和氮元素的化合价都为+2价,生成
物中氮气是单质,化合价为0价,二氧化碳中碳元素为+4价,而氧元素在反应前
后都是-2价,所以化合价改变的元素是C和N两种元素。
2.(2017年湖南省株州市)黑火药是我国古代四大发明之一,它的组成是“一硫
(硫粉)二硝(硝石,即KNO 固体)三碳(木炭粉)”。点燃黑火药发生爆炸,生成硫
3
化钾(K S)和空气中含量最多的气体及一种无毒的氧化物气体。请回答下列问题:
2
(1)黑火药爆炸时产生白烟,白烟是由于______(填化学式)分散到空气中形
成的。
(2)请写出黑火药爆炸时的化学方程式:___________________。
【答案】(1)K S;(1分)(2)S+3C+2KNO K S+N ↑+3CO ↑。(2分)
2 3 2 2 2
【解析】此题主要考查根据信息写化学方程式的相关知识。(1)烟是指物质燃烧产
生的固体小颗粒物浮在空中形成的,故是硫化钾(K S);(2)黑火药发生爆炸,
2
生成硫化钾(K S)和空气中含量最多的气体及一种无毒的氧化物气体;空气
2
中含量最多的气体是氮气;由于反应物中有木炭粉,则生成物中含碳元素,则
一种无毒的氧化物气体为二氧化碳;故化学方程式为:S+3C+2KNO3
K2S+N2↑+3CO2↑。
3.(2017山东省临沂市)下图为某化学反应在催化剂作用下的微观模拟示意图,
其中“●”和“○”分别表示氢原子和氧原子。
(1)虚线框内应填的微观图示是 (填序号)
(2)结合上图,从原子、分子的角度分析,在化学反应过程中, 可分,
12而______不能再分。
(3)请写出该反应的化学方程式:
【答案】(1)D;(2)分子; 原子;(3)2H O 2H O+O ↑。
2 2 2 2
【解析】本题主要考查分子和原子的区别及化学方程式的书写。
(1)图中“●”和“○”分别表示氢原子和氧原子,故 表示H O ,
2 2
表示H O,过氧化氢分解生成水和氧气,故应选D。
2
(2)在化学反应过程中,分子可以再分成原子,原子不能再分,原子是化学变化中
的最小粒子;
(3)过氧化氢在催化剂作用下反应的化学方程式为2H O 2H O+O ↑。
2 2 2 2
4.(2017山东省青岛市,题号25,分值5分)为了探究化学反应前后物质的总质
量是否发生改变, 甲同学和乙同学分别设计了下面两个实验, 请根据图示回答
问题:
(1)甲同学设计的实验如图 A 所示,反应前,托盘天平的指针指向刻度盘的
中间;两种物质反应后, 托盘天平的指针______(选填“向左”、 “向右”
或“不”)偏转, 原因是______。
(2)乙同学设计的实验如图B所示,通过实验得出结论:化学反应前后物质
的总质量______。
(3)两位同学通过交流反思得到启示: 在探究化学反应前后物质的总质量是
否发生改变时, 对于有气体参加或有气体生成的反应一定要在______装置
中进行。
(4)从微观角度分析, 在化学反应前后一定不变的是______(选填序号)。
①原子种类 ②分子种类 ③原子数目 ④分子质量 ⑤分子数目 ⑥原子质量
13【答案】(1)向左(1分);反应生成的氢气逸出(1分);
(2)相等(1分);
(3)密闭(1分);
(4)①③⑥(1分)。
【解析】(1)锌和稀硫酸反应生成硫酸锌和氢气,由于在敞口容器中进行反应,生
成的氢气逸出,使反应后烧杯中的物质总质量减小,托盘天平的指针偏向左边;
(2)硝酸银溶液和氯化钠溶液反应生成氯化银沉淀和硝酸钠,反应过程中既没有
气体参加,又没有气体生成,反应前后烧杯中的物质总质量不变;
(3)在做验证质量守恒定律实验时,应选择无气体参加或生成的反应,对于有气
体参加或生成的反应一定要在密闭的装置中进行;
(4)从微观的角度看,在化学反应前后原子的种类不变、原子的数目不变、每个原
子的质量不变,所以,反应前后物质的总质量不变;在化学反应前后,一定发生变
化的是分子的种类,可能发生变化的是分子的数目;因此,本题的正确选项是
①③⑥。
5.(2017浙江省杭州市)小金进行如图所示实验来验证质量守恒定律。在实验中
用电子天平和量筒准确测量出表中m 、m 、m 、m 和V。(实验操作正确,O 的密
1 2 3 4 2
度为ρg/cm3)
实验序号 1 2 ……
m (MnO )/g
1 2
m (KClO )/g
2 3
m (试管)/g
3
m (试管+加热后剩余固体)/g
4
量筒内收集气体的体积V/cm3
(1)装置中试管口略向下倾斜的原因是__________________。
14(2)根据质量守恒定律,m 、m 、m 、m 、V和ρ之间应存在的等量关系是
1 2 3 4
_______________。
(3)每次实验结束后,小金在拆卸装置时总能闻到刺激性气味。他将加热后剩余
固体中的MnO 分离并测量其质量,发现总小于加热前MnO 的质量。查阅资料后
2 2
发现,一般认为加热KClO 和MnO 混合物的反应过程如下;
3 2
第1步:2 MnO +2KClO 2KMnO +Cl ↑+O ↑;(其中Cl 有刺激性气味)
2 3 4 2 2 2
第2 步:2KMnO K MnO +MnO +O ↑;
4 2 4 2 2
第3步:K MnO +Cl 2KCl+ MnO +O ↑。
2 4 2 2 2
写出加热后剩余固体中MnO 质量小于加热前MnO 质量的原因
2 2
__________________________。
【答案】(1)防止冷凝水倒流使试管炸裂(2分);(2)m +m +m =m +ρV(2分);
1 2 3 4
(3)有部分MnO 转化成了K MnO (2分);
2 2 4
【解析】本题主要考查了催化剂及其应用;
(1)给固体加热时,试管口略向下倾斜的原因是防止冷凝水倒流使试管炸裂;
(2)根据质量守恒定律可知,参加反应的各物质的质量总和等于生成物的各物质
的质量总和,故有m +m +m =m +ρV。
1 2 3 4
(3)根据三个化学方程式可知,MnO 在反应中转化成KMnO →K MnO →MnO ,
2 4 2 4 2
在最后一步转化的过程中需要和Cl 反应,但是,生成的Cl 大部分随着生成的氧
2 2
气导出了,不能够将生成的K MnO 全部在转化成MnO ,所以加热后剩余固体中
2 4 2
MnO 质量小于加热前MnO 质量。
2 2
6.(2017湖北省随州市))小李用盐酸与碳酸钙粉末反应验证质量守恒定律,实验
装置如图
15(1)根据实验目的,小李必须测量的数据是______。
A.锥形瓶质量
B.气球质量
C.反应前整个反应装置(包括里边的物质)质量
D.反应后整个反应装置(包括里边的物质)质量
(2)将反应装置放在天平左盘,使天平平衡后,再将碳酸钙粉末倒入锥形瓶中。反
应结束后,气球鼓起,天平向右倾斜。小李按规范操作重新实验,得到相同结果。
请你帮他分析原因_。
(3)反应结束后,锥形瓶中无固体剩余,则生成气体质量____g,所得溶液中生成
物的溶质质量分数(只需写出最终的计算表达式)_____。
【答案】(1)CD(1分);(2)气球受到浮力增大(1分);(3)0.88(1分);
。
【解析】本题考查的是质量守恒定律及化学方程式的计算,探究质量守恒定律时
有气体参加或者气体产生的反应要选择密闭容器,但同时要考虑浮力对实验的
影响。
(1)要验证质量守恒定律,就是验证反应前后物质的质量总和是否相同,故实验
中要称量反应前后整个装置的质量,故选择CD;
(2)碳酸钙和盐酸反应会生成气体二氧化碳,气球鼓起,则气球受到的浮力增大,
故可以观察到天平向右倾斜;
(3)参加反应的碳酸钙的质量为2g,设生成的氯化钙的质量为x
CaCO +2HCl=CaCl +H O+CO ↑
3 2 2 2
100 111
2g x
x=2.22g
溶质质量分数是溶质质量与溶液质量之比,故反应后溶质质量分数表示为:
16。
17