文档内容
综合测试题
(满分:100分 时间:90分钟)
相对原子质量:H—1 C—12 O—16 K—39 Fe—56
一、选择题(每小题3分,共45分)
1.(2017·郴州)下列说法涉及到化学变化的是(B)
A.酒香不怕巷子深 B.野火烧不尽,春风吹又生
C.泥菩萨过河,自身难保 D.只要功夫深,铁杵磨成针
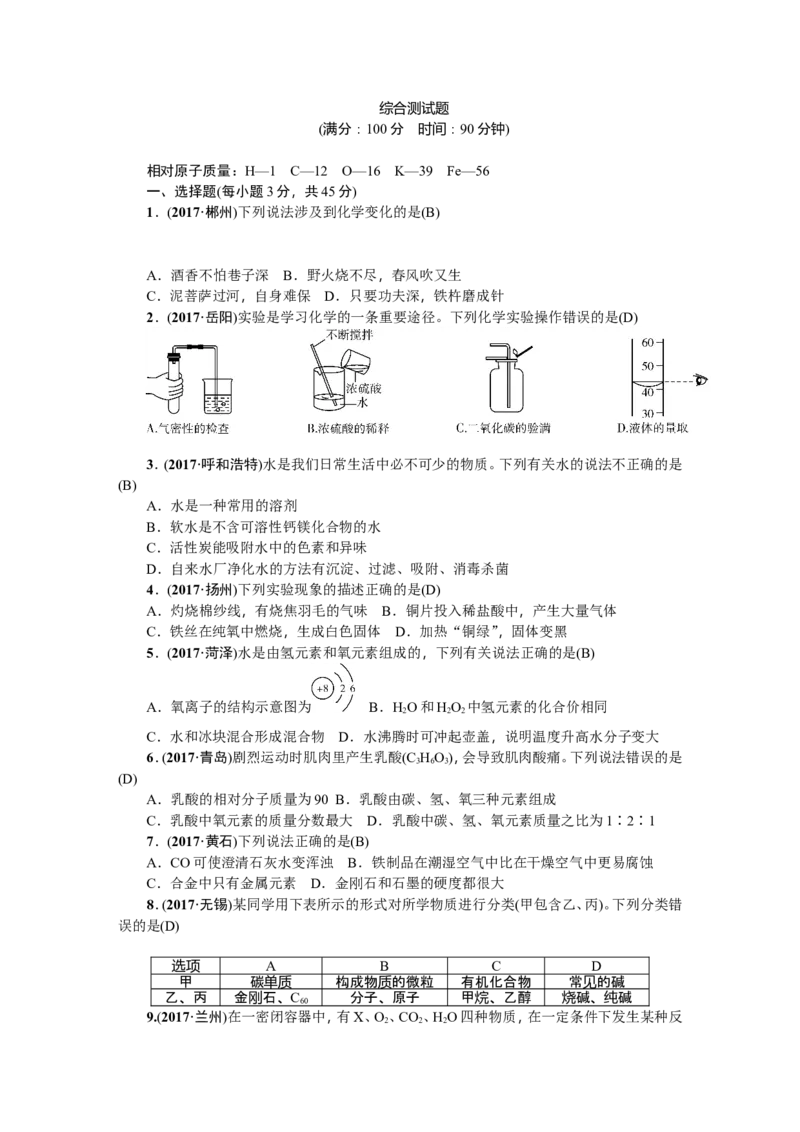
2.(2017·岳阳)实验是学习化学的一条重要途径。下列化学实验操作错误的是(D)
3.(2017·呼和浩特)水是我们日常生活中必不可少的物质。下列有关水的说法不正确的是
(B)
A.水是一种常用的溶剂
B.软水是不含可溶性钙镁化合物的水
C.活性炭能吸附水中的色素和异味
D.自来水厂净化水的方法有沉淀、过滤、吸附、消毒杀菌
4.(2017·扬州)下列实验现象的描述正确的是(D)
A.灼烧棉纱线,有烧焦羽毛的气味 B.铜片投入稀盐酸中,产生大量气体
C.铁丝在纯氧中燃烧,生成白色固体 D.加热“铜绿”,固体变黑
5.(2017·菏泽)水是由氢元素和氧元素组成的,下列有关说法正确的是(B)
A.氧离子的结构示意图为 B.HO和HO 中氢元素的化合价相同
2 2 2
C.水和冰块混合形成混合物 D.水沸腾时可冲起壶盖,说明温度升高水分子变大
6.(2017·青岛)剧烈运动时肌肉里产生乳酸(C HO),会导致肌肉酸痛。下列说法错误的是
3 6 3
(D)
A.乳酸的相对分子质量为90 B.乳酸由碳、氢、氧三种元素组成
C.乳酸中氧元素的质量分数最大 D.乳酸中碳、氢、氧元素质量之比为1∶2∶1
7.(2017·黄石)下列说法正确的是(B)
A.CO可使澄清石灰水变浑浊 B.铁制品在潮湿空气中比在干燥空气中更易腐蚀
C.合金中只有金属元素 D.金刚石和石墨的硬度都很大
8.(2017·无锡)某同学用下表所示的形式对所学物质进行分类(甲包含乙、丙)。下列分类错
误的是(D)
选项 A B C D
甲 碳单质 构成物质的微粒 有机化合物 常见的碱
乙、丙 金刚石、C 分子、原子 甲烷、乙醇 烧碱、纯碱
60
9.(2017·兰州)在一密闭容器中,有X、O、CO、HO四种物质,在一定条件下发生某种反
2 2 2应,反应一段时间后,测得反应前后各物质的质量如下表,下列说法正确的是(D)
物质 X O CO HO
2 2 2
反应前的质量/g 19 34 6 2
反应后的质量/g 11 待测 28 20
A.表中的待测值为32 B.X中一定含有C、H、O元素
C.该反应是置换反应 D.反应中CO 和HO的质量比为11∶9
2 2
10.(2017·达州)某纯净物3 g在氧气中完全燃烧,生成8.8 g二氧化碳和5.4 g水。下列说
法不正确的是(D)
A.该纯净物中含有C、H元素,不含O元素 B.该反应中O 和CO 的质量比为14∶11
2 2
C.该反应中O 和HO的分子数之比为7∶6 D.该纯净物中C、H原子的个数比为1∶4
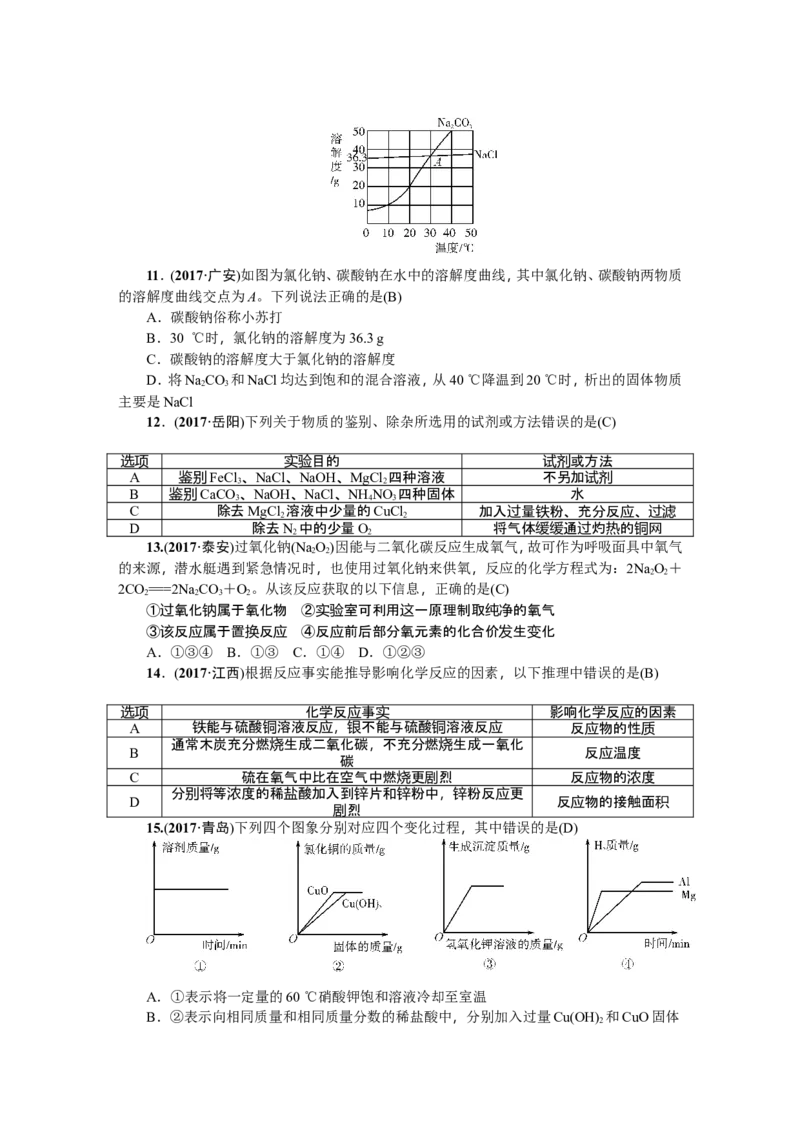
2 211.(2017·广安)如图为氯化钠、碳酸钠在水中的溶解度曲线,其中氯化钠、碳酸钠两物质
的溶解度曲线交点为A。下列说法正确的是(B)
A.碳酸钠俗称小苏打
B.30 ℃时,氯化钠的溶解度为36.3 g
C.碳酸钠的溶解度大于氯化钠的溶解度
D.将NaCO 和NaCl均达到饱和的混合溶液,从40 ℃降温到20 ℃时,析出的固体物质
2 3
主要是NaCl
12.(2017·岳阳)下列关于物质的鉴别、除杂所选用的试剂或方法错误的是(C)
选项 实验目的 试剂或方法
A 鉴别FeCl 、NaCl、NaOH、MgCl 四种溶液 不另加试剂
3 2
B 鉴别CaCO 、NaOH、NaCl、NH NO 四种固体 水
3 4 3
C 除去MgCl 溶液中少量的CuCl 加入过量铁粉、充分反应、过滤
2 2
D 除去N 中的少量O 将气体缓缓通过灼热的铜网
2 2
13.(2017·泰安)过氧化钠(Na O)因能与二氧化碳反应生成氧气,故可作为呼吸面具中氧气
2 2
的来源,潜水艇遇到紧急情况时,也使用过氧化钠来供氧,反应的化学方程式为:2NaO+
2 2
2CO===2Na CO+O。从该反应获取的以下信息,正确的是(C)
2 2 3 2
①过氧化钠属于氧化物 ②实验室可利用这一原理制取纯净的氧气
③该反应属于置换反应 ④反应前后部分氧元素的化合价发生变化
A.①③④ B.①③ C.①④ D.①②③
14.(2017·江西)根据反应事实能推导影响化学反应的因素,以下推理中错误的是(B)
选项 化学反应事实 影响化学反应的因素
A 铁能与硫酸铜溶液反应,银不能与硫酸铜溶液反应 反应物的性质
通常木炭充分燃烧生成二氧化碳,不充分燃烧生成一氧化
B 反应温度
碳
C 硫在氧气中比在空气中燃烧更剧烈 反应物的浓度
分别将等浓度的稀盐酸加入到锌片和锌粉中,锌粉反应更
D 反应物的接触面积
剧烈
15.(2017·青岛)下列四个图象分别对应四个变化过程,其中错误的是(D)
A.①表示将一定量的60 ℃硝酸钾饱和溶液冷却至室温
B.②表示向相同质量和相同质量分数的稀盐酸中,分别加入过量Cu(OH) 和CuO固体
2C.③表示向一定量的氯化铁和氯化钾的混合溶液中,逐滴加入过量的氢氧化钾溶液
D.④表示向相同质量和相同质量分数的稀硫酸中,分别加入过量的镁粉和铝粉
二、填空题(共27分)
16.(4分)(2017·贵港)请用数字和化学符号填空:
(1)2个硅原子2Si (2)保持氢气化学性质的粒子H
2
(3)3个铁原子3Fe (4)海水中含量最多的离子Na+、Cl-
17.(8分)(2017·扬州)能源和环境一直受到人们关注。
(1)太阳能和天然气中属于可再生能源的是太阳能,属于不可再生能源的是天然气。天然
气的主要成分是CH,CH 中H的质量分数为25%。CH 燃烧主要是将化学能转化为热能。
4 4 4
(2)造成大气中CO 含量增加的主要原因是c(填字母)。
2
a.动植物的呼吸作用 b.实验室逸出CO c.化石燃料的大量燃烧
2
(3)汽车尾气中的CO和NO,在催化剂作用下能转化为CO 和N,该反应中CO和NO的
2 2
分子个数比为1∶1。
(4)下列可用来改良酸性土壤的是a(填字母)。
a.熟石灰 b.氯化钠 c.稀硫酸
(5)下列做法会导致“白色污染”的是b(填字母)。
a.丢弃废旧电池 b.随意丢弃废旧塑料 c.使用含铅汽油
18.(6分)(2017·重庆)2017年“全国生态文化村”遴选工作已开启。为了保护环境,我市
某村办企业需对含硫酸的废水处理呈中性后排放。
(1)若用pH试纸检测废水,其pH<(填“>”、“<”或“=”)7。若要达到排放标准,可以向
废水里加入C(填字母)。
A.氯化钠 B.氯化钡 C.生石灰
(2)某同学欲利用该村的赤铁矿(杂质不溶于水,也不与酸反应)来处理废水,并制取红色颜
料(Fe O)从而变废为宝。他设计了如下方案,试回答相关问题。
2 3
溶液A中一定含有的金属阳离子是Fe3+(填符号),写出反应②的化学方程式Fe (SO ) +
2 4 3
6NaOH===2Fe(OH) ↓+3NaSO ,反应③是分解反应,另外一种产物的名称是水(已知:不溶
3 2 4
于水的碱受热易分解为两种氧化物,且化合价不变)。
19.(9分)(2017·天津)金属材料广泛应用于生产生活中。
(1)铝块能制成铝箔是利用了铝的延展(填“导电”或“延展”)性。
(2)为探究铝、铜的金属活动性顺序,某同学选用了下列药品进行实验,其中可行的是
B(填字母)。
A.铝丝、铜丝、氯化镁溶液 B.铝丝、铜丝、硫酸铜溶液
(3)A~G是初中化学常见的物质。已知A为黑色固体单质,B为红棕色粉末,G为紫红色
固体单质,它们的转化关系如图所示,回答问题。①写出化学式:AC;BFe O。
2 3
②反应Ⅱ的化学方程式为CO+C=====2CO。
2
③反应Ⅲ的化学方程式为Fe+CuSO ===FeSO+Cu。
4 4
(4)用 1600 t 含氧化铁 80%的赤铁矿石,理论上可以炼出含铁 96%的生铁的质量为
933.3t。(结果保留至0.1)
三、实验探究题(共20分)
20.(10分)(2017·湘潭)根据下列实验装置图填空:
(1)写出图中仪器a的名称:锥形瓶。
(2)实验室可用上图中的装置来制备和收集一些常见的气体,请用化学方程式和上图中字
母填写下表空白。
反应原理(用化学方程式表
制取的气体 发生装置 收集装置
示)
2KMnO =====KMnO +
O 4 2 4 A D或F
2 MnO +O↑
2 2
CaCO +2HCl===CaCl +
CO 3 2 B或C D
2 HO+CO↑
2 2
H Zn+HSO ===ZnSO +H↑ B或C E或F
2 2 4 4 2
(3)汽车尾气中的一氧化氮是一种无色有毒气体,难溶于水,密度略大于空气。实验室中制
取一氧化氮可采用的收集装置是F(填字母)。
(4)某同学取一定浓度的盐酸与石灰石反应,将生成的气体通入新制澄清石灰水中,始终
未见浑浊,可能的原因是所用盐酸为浓盐酸(写出一条即可)。
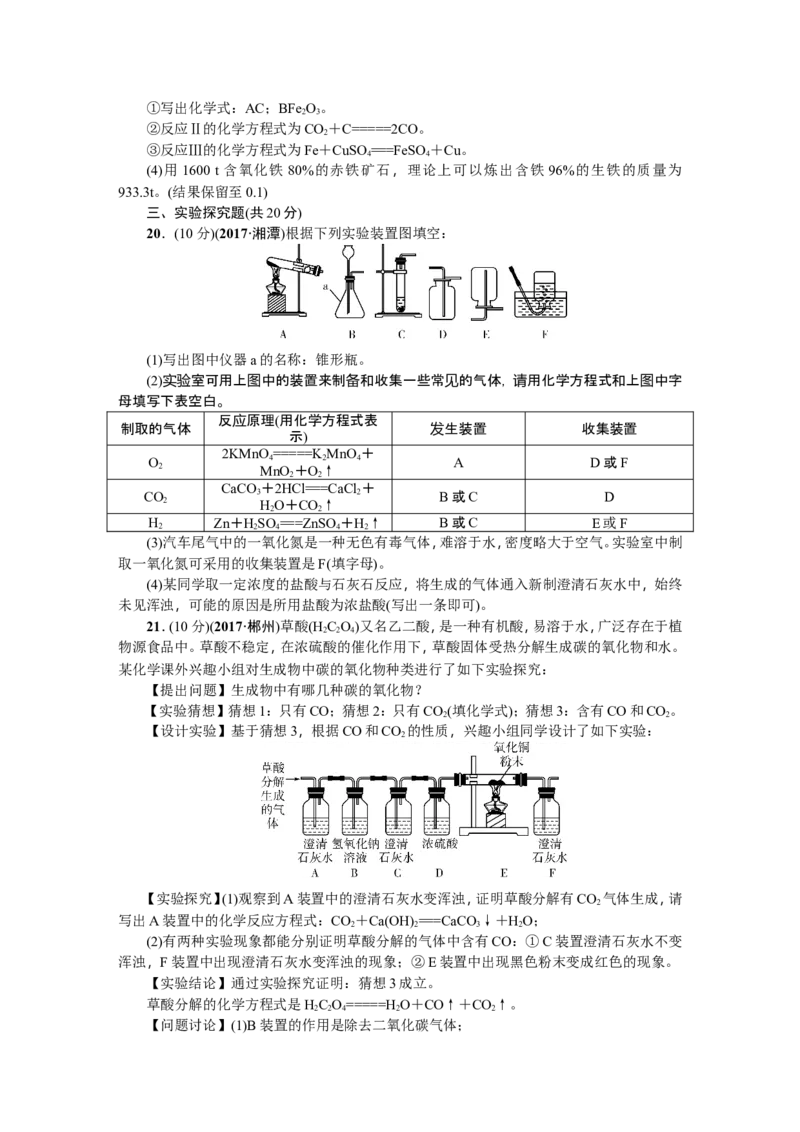
21.(10分)(2017·郴州)草酸(H C O)又名乙二酸,是一种有机酸,易溶于水,广泛存在于植
2 2 4
物源食品中。草酸不稳定,在浓硫酸的催化作用下,草酸固体受热分解生成碳的氧化物和水。
某化学课外兴趣小组对生成物中碳的氧化物种类进行了如下实验探究:
【提出问题】生成物中有哪几种碳的氧化物?
【实验猜想】猜想1:只有CO;猜想2:只有CO(填化学式);猜想3:含有CO和CO。
2 2
【设计实验】基于猜想3,根据CO和CO 的性质,兴趣小组同学设计了如下实验:
2
【实验探究】(1)观察到A装置中的澄清石灰水变浑浊,证明草酸分解有CO 气体生成,请
2
写出A装置中的化学反应方程式:CO+Ca(OH) ===CaCO ↓+HO;
2 2 3 2
(2)有两种实验现象都能分别证明草酸分解的气体中含有CO:①C装置澄清石灰水不变
浑浊,F装置中出现澄清石灰水变浑浊的现象;②E装置中出现黑色粉末变成红色的现象。
【实验结论】通过实验探究证明:猜想3成立。
草酸分解的化学方程式是HC O=====HO+CO↑+CO↑。
2 2 4 2 2
【问题讨论】(1)B装置的作用是除去二氧化碳气体;(2)C装置的作用是检验二氧化碳气体是否除尽;
(3)该实验装置的设计还有一处明显不足(实验前已排尽装置内的空气),请提出改进措施
在F装置后设置尾气处理装置(合理即可)(任写一条)。
四、计算题(8分)
22.(2017·重庆)合成氨工业中,常用碳酸钾溶液吸收产生的二氧化碳得到碳酸氢钾,反应
的化学方程式为:KCO+CO+HO===2KHCO 。现向碳酸钾溶液中通入二氧化碳,恰好完
2 3 2 2 3
全反应,得到溶质的质量分数为10%的溶液50 g。试计算:
(1)碳酸钾中钾元素、碳元素、氧元素的质量比为39∶6∶24。
(2)若把该50 g溶液,稀释为溶质的质量分数为4%的溶液,需要加入水的质量。
(3)原碳酸钾溶液中溶质的质量分数(计算结果精确到0.1%)。
解:(1)碳酸钾(K CO)中钾元素、碳元素、氧元素的质量比(39×2)∶12∶(16×3)=
2 3
39∶6∶24。
(2)若把该50 g 溶液,稀释为溶质的质量分数为4%的溶液,设加入的水的质量为x。
50 g×10%=(50 g+x)×4% x=75 g
(3)设溶液中碳酸钾的质量为y,参加反应的二氧化碳的质量为z。
溶质的质量分数为10%的溶液50 g中碳酸氢钾的质量为100%×50 g=5 g。
KCO+CO+HO===2KHCO
2 3 2 2 3
138 44 200
y z 5 g
== y=3.45 g z=1.1 g
原碳酸钾溶液中溶质的质量分数为×100%≈7.1%