文档内容
第四、五单元测试题
(满分:100分 时间:90分钟)
相对原子质量:H—1 C—12 N—14 O—16 F—19 Cl—35.5 K—39 Ca—40
一、选择题(每小题3分,共45分)
1.(2017·淮安)焦亚硫酸钠在食品加工中常用作防腐剂、漂白剂和疏松剂。焦亚硫酸钠
(Na SO)中硫元素的化合价为(C)
2 2 5
A.-2 B.+3 C.+4 D.+5
2.(2017·广东)现有反应:2Cu(NO )=====2CuO+O↑+4X↑,则X的化学式为(B)
3 2 2
A.NO B.NO C.NH D.NO
2 3 2 3
3.(2017·来宾)关于2H+O=====2HO的读法不正确的是(C)
2 2 2
A.氢气与氧气在点燃的条件下生成水
B.每2个氢分子与1个氧分子完全反应,生成2个水分子
C.常温下,每2体积的氢气与1体积的氧气完全反应,生成2体积的水
D.每4份质量的氢气与32份质量的氧气完全反应,生成36份质量的水
4.(2017·绍兴)下列属于置换反应的是(A)
A.H+CuO=====Cu+HO B.2KMnO =====KMnO +MnO +O↑
2 2 4 2 4 2 2
C.HCl+NaOH===NaCl+HO D.2Mg+O=====2MgO
2 2
5.(2017·重庆)自然界的水都不是纯净水,下列有关水的净化的说法不正确的是(D)
A.过滤不能使硬水转化为软水 B.净水时活性炭起吸附作用
C.蒸馏可将海水淡化 D.电解水是一种常用的净水方法
6.(2017·湘潭)2017年中国水周的宣传主题为“落实绿色理念,全面推行河长制”。下列
有关说法中不正确的是(A)
A.硬水经过吸附、过滤可变成软水 B.净化水程度最高的方法是蒸馏
C.水是一种常见的溶剂 D.为爱护水资源,既要节约用水,又要防止水污染
7.(2017·泸州)分类是科学研究的重要方法,下列物质对应的类别不正确的是(A)
选项 A B C D
物质 熟石灰 小苏打 氨气 硅
类别 氧化物 盐 化合物 单质
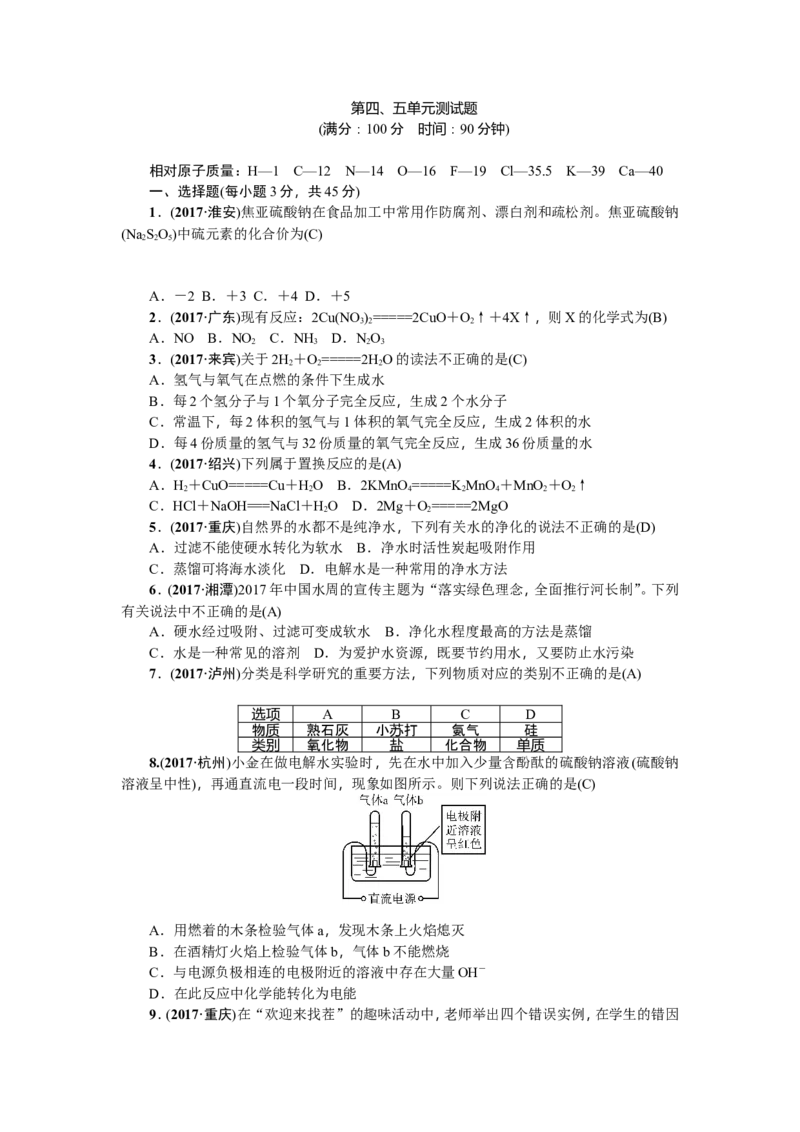
8.(2017·杭州)小金在做电解水实验时,先在水中加入少量含酚酞的硫酸钠溶液(硫酸钠
溶液呈中性),再通直流电一段时间,现象如图所示。则下列说法正确的是(C)
A.用燃着的木条检验气体a,发现木条上火焰熄灭
B.在酒精灯火焰上检验气体b,气体b不能燃烧
C.与电源负极相连的电极附近的溶液中存在大量OH-
D.在此反应中化学能转化为电能
9.(2017·重庆)在“欢迎来找茬”的趣味活动中,老师举出四个错误实例,在学生的错因分析中错误的是(B)
选项 错误实例 错因分析
A 铁与稀硫酸反应生成硫酸铁 反应产物不正确
B FeCl +3NaOH===Fe(OH) +NaCl 只缺少沉淀符号
3 3
C 2KMnO ===K MnO +MnO +O↑ 反应条件不正确
4 2 4 2 2
D 氢氧化钠俗名烧碱或纯碱 俗名中的纯碱不正确
10.(2017·泸州)下列有关反应方程式正确,且反应前后有元素化合价升高和降低的是(D)
A.铁和盐酸混合:2Fe+6HCl===2FeCl +3H↑
3 2
B.碳酸铵与硫酸反应:(NH )CO+HSO ===(NH )SO +HO+CO↑
4 2 3 2 4 4 2 4 2 2
C.石英和纯碱高温:SiO+NaCO=====NaSiO+CO↑
2 2 3 2 3 2
D.磁铁矿(Fe O)高温下通CO:Fe O+4CO=====3Fe+4CO
3 4 3 4 2
11.(2017·临沂)豆腐是人们喜爱的食物,营养丰富,能为人体提供所需的多种氨基酸,其
中含量最多的是亮氨酸(C H NO )。关于亮氨酸的说法正确的是(C)
6 13 2
A.亮氨酸是氧化物
B.亮氨酸中碳元素的质量分数为27.3%
C.一个亮氨酸分子由22个原子构成
D.亮氨酸中碳、氢、氮、氧四种元素的质量比为6∶13∶1∶2
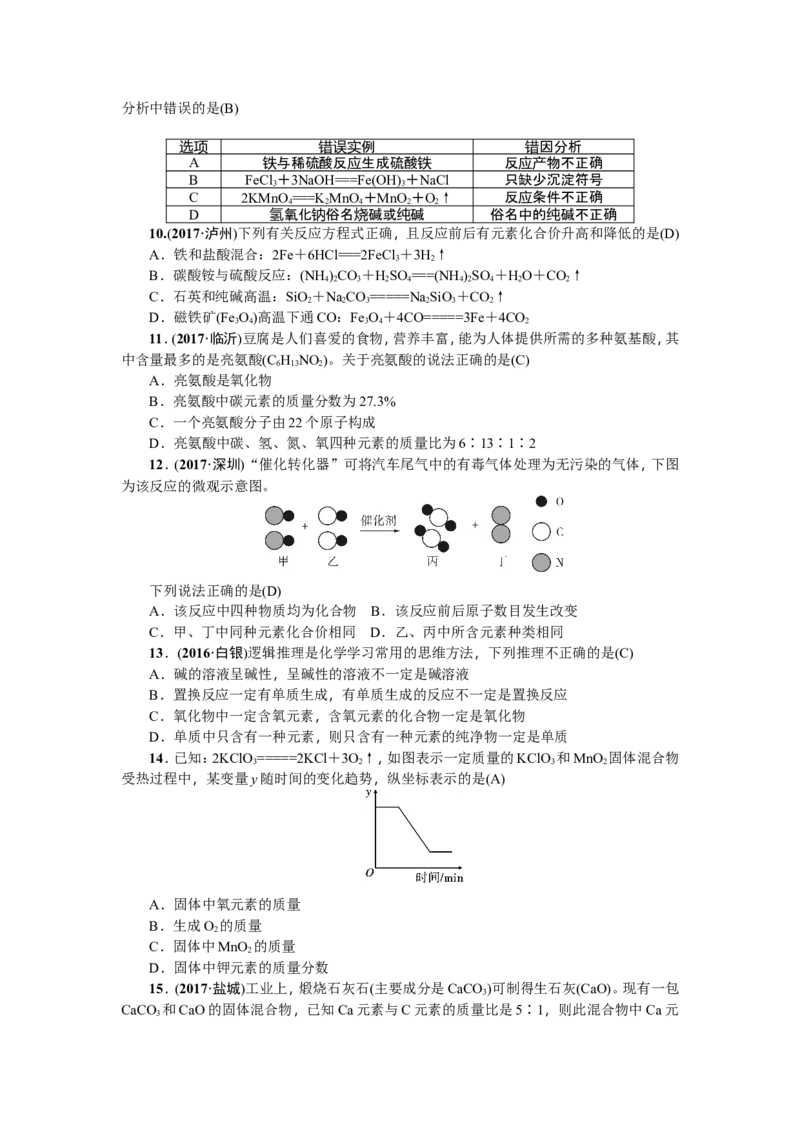
12.(2017·深圳)“催化转化器”可将汽车尾气中的有毒气体处理为无污染的气体,下图
为该反应的微观示意图。
下列说法正确的是(D)
A.该反应中四种物质均为化合物 B.该反应前后原子数目发生改变
C.甲、丁中同种元素化合价相同 D.乙、丙中所含元素种类相同
13.(2016·白银)逻辑推理是化学学习常用的思维方法,下列推理不正确的是(C)
A.碱的溶液呈碱性,呈碱性的溶液不一定是碱溶液
B.置换反应一定有单质生成,有单质生成的反应不一定是置换反应
C.氧化物中一定含氧元素,含氧元素的化合物一定是氧化物
D.单质中只含有一种元素,则只含有一种元素的纯净物一定是单质
14.已知:2KClO=====2KCl+3O↑,如图表示一定质量的KClO 和MnO 固体混合物
3 2 3 2
受热过程中,某变量y随时间的变化趋势,纵坐标表示的是(A)
A.固体中氧元素的质量
B.生成O 的质量
2
C.固体中MnO 的质量
2
D.固体中钾元素的质量分数
15.(2017·盐城)工业上,煅烧石灰石(主要成分是CaCO )可制得生石灰(CaO)。现有一包
3
CaCO 和CaO的固体混合物,已知Ca元素与C元素的质量比是5∶1,则此混合物中Ca元
3素与O元素的质量比是(B)
A.15∶16 B.15∶14 C.5∶4 D.15∶8
二、填空题(共33分)
16.(5分)(2017·乌鲁木齐)建立“宏观—微观—符号”之间的联系是化学学科的重要特
点。
(1)用化学符号和数字表示下列微粒。
2个氢原子2H;2个二氧化硫分子2SO ;2个硝酸根离子2NO -。
2 3
(2)“水循环”和“碳循环”是自然界中存在的两大重要循环。
①从微观的角度看:水分子是由氢原子和氧原子构成的。
②从宏观的角度看:二氧化碳是由碳元素和氧元素组成的。
17.(8分)(2016·荆州)用适当的化学方程式说明或解释下列问题:
(1)铜的金属活动性比铁弱:Fe+CuSO ===FeSO+Cu。
4 4
(2)工业上煅烧石灰石制生石灰:CaCO =====CaO+CO↑。
3 2
(3)用石灰浆粉刷墙面,干燥后变得坚硬:CO+Ca(OH) ===CaCO ↓+HO。
2 2 3 2
(4)服用含Al(OH) 的药丸治疗胃酸过多症:Al(OH) +3HCl===AlCl +3HO。
3 3 3 2
18.(4分)(2017·重庆)食盐是维持人体正常生理活动必不可少的物质。低钠盐能预防高血
压,碘盐能补充人体所需碘元素,工业上盐使用不当易使人中毒。
(1)氯化钠中质量分数较大的是氯(填名称)元素。
(2)硫酸镁可以改变钠盐的“口味”,硫酸镁的化学式为MgSO 。
4
(3)碘盐中加了碘酸钾(KIO ),则KIO 中碘元素的化合价为+5。
3 3
(4)工业用盐含NaNO ,NaNO 的名称为C(填字母)。
2 2
A.磷酸钠 B.硝酸钠 C.亚硝酸钠
19.(8分)(2017·黄石)水是生命之源,人类的日常生活和工农业生产都离不开水。
(1)生活中常用肥皂水来区分硬水和软水。
(2)小液滴分散到液体里形成的混合物叫做乳浊液。
(3)下列做法有利于节约水资源或减少水体污染的是①③(填序号,多选)。
①农业和园林漫灌改为喷灌、滴灌 ②工业废水直接排入江河中
③生活污水集中处理和排放 ④为提高农作物产量,大量使用化肥农药
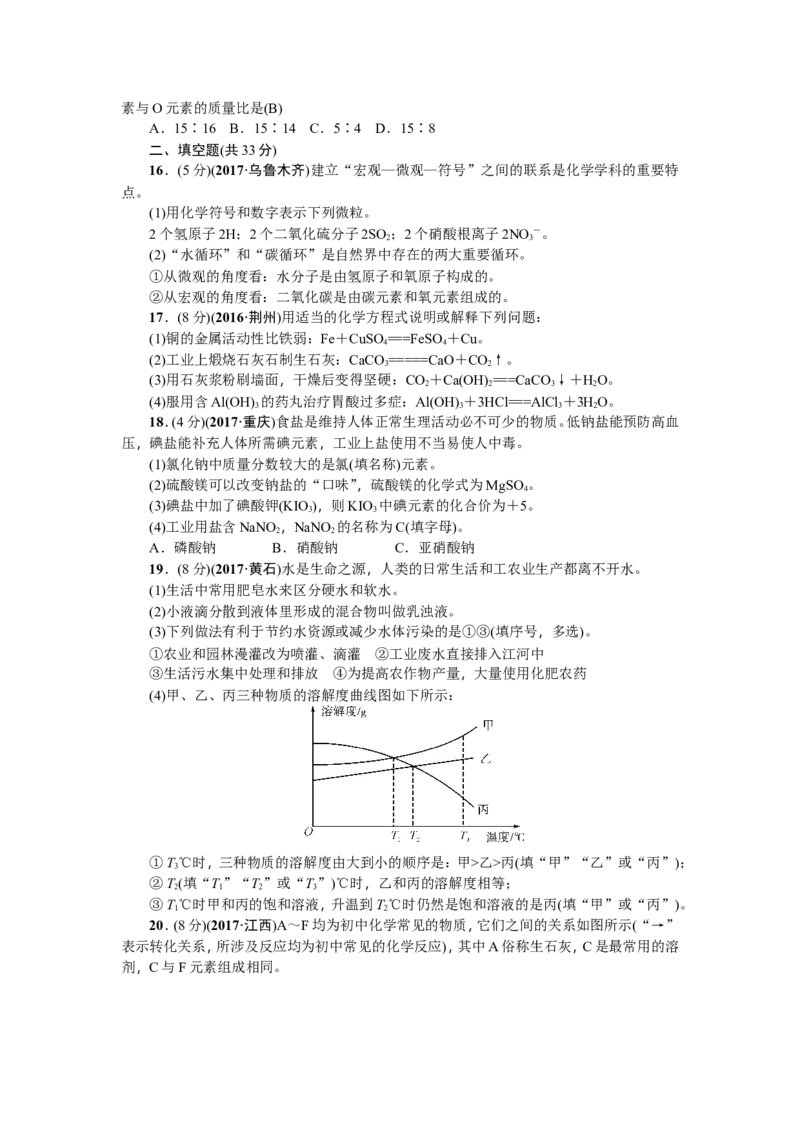
(4)甲、乙、丙三种物质的溶解度曲线图如下所示:
①T℃时,三种物质的溶解度由大到小的顺序是:甲>乙>丙(填“甲”“乙”或“丙”);
3
②T(填“T”“T”或“T”)℃时,乙和丙的溶解度相等;
2 1 2 3
③T℃时甲和丙的饱和溶液,升温到T℃时仍然是饱和溶液的是丙(填“甲”或“丙”)。
1 2
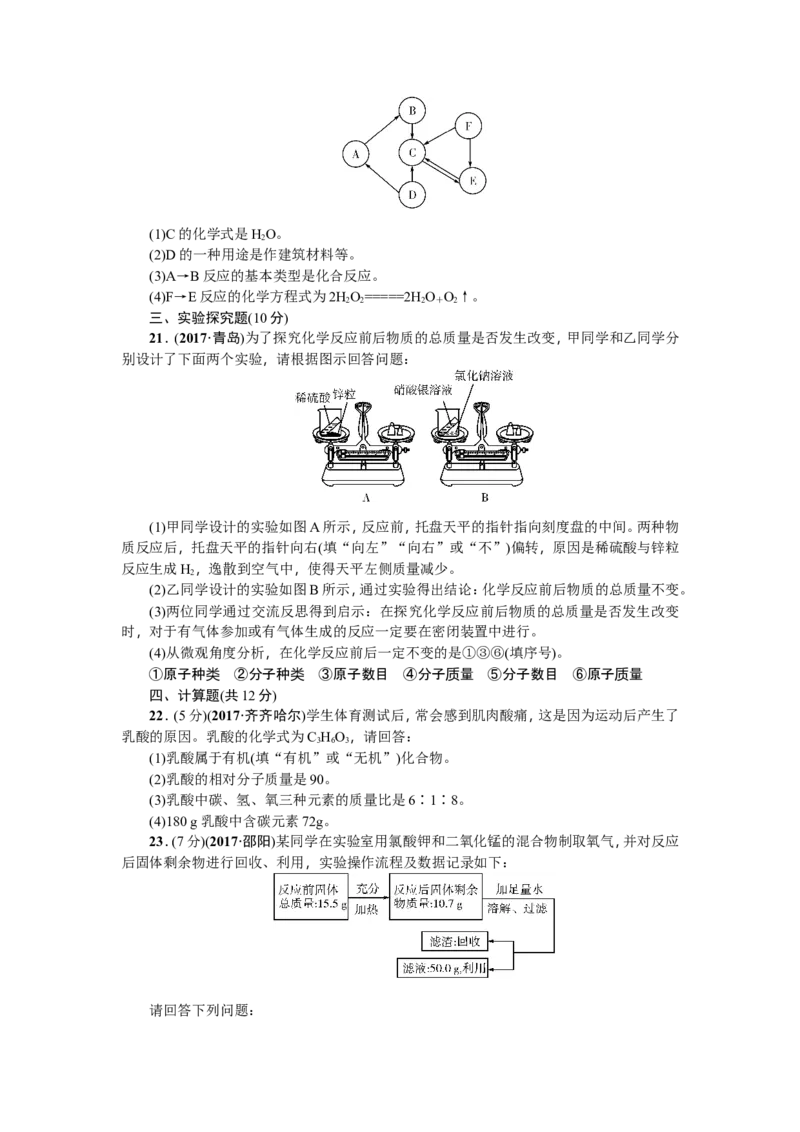
20.(8分)(2017·江西)A~F均为初中化学常见的物质,它们之间的关系如图所示(“→”
表示转化关系,所涉及反应均为初中常见的化学反应),其中A俗称生石灰,C是最常用的溶
剂,C与F元素组成相同。(1)C的化学式是HO。
2
(2)D的一种用途是作建筑材料等。
(3)A→B反应的基本类型是化合反应。
(4)F→E反应的化学方程式为2HO=====2HO O↑。
2 2 2 + 2
三、实验探究题(10分)
21.(2017·青岛)为了探究化学反应前后物质的总质量是否发生改变,甲同学和乙同学分
别设计了下面两个实验,请根据图示回答问题:
(1)甲同学设计的实验如图A所示,反应前,托盘天平的指针指向刻度盘的中间。两种物
质反应后,托盘天平的指针向右(填“向左”“向右”或“不”)偏转,原因是稀硫酸与锌粒
反应生成H,逸散到空气中,使得天平左侧质量减少。
2
(2)乙同学设计的实验如图B所示,通过实验得出结论:化学反应前后物质的总质量不变。
(3)两位同学通过交流反思得到启示:在探究化学反应前后物质的总质量是否发生改变
时,对于有气体参加或有气体生成的反应一定要在密闭装置中进行。
(4)从微观角度分析,在化学反应前后一定不变的是①③⑥(填序号)。
①原子种类 ②分子种类 ③原子数目 ④分子质量 ⑤分子数目 ⑥原子质量
四、计算题(共12分)
22.(5分)(2017·齐齐哈尔)学生体育测试后,常会感到肌肉酸痛,这是因为运动后产生了
乳酸的原因。乳酸的化学式为C HO,请回答:
3 6 3
(1)乳酸属于有机(填“有机”或“无机”)化合物。
(2)乳酸的相对分子质量是90。
(3)乳酸中碳、氢、氧三种元素的质量比是6∶1∶8。
(4)180 g乳酸中含碳元素72g。
23.(7分)(2017·邵阳)某同学在实验室用氯酸钾和二氧化锰的混合物制取氧气,并对反应
后固体剩余物进行回收、利用,实验操作流程及数据记录如下:
请回答下列问题:(1)滤液可作化肥使用,你认为它属于钾肥。
(2)该同学制得氧气的质量为4.8g。
(3)计算滤液中溶质质量分数。
解:设生成KCl的质量为x。
2KClO=====2KCl+3O↑
3 2
149 96
x 4.8 g
149∶96=x∶4.8 g
x=7.45 g
溶质的质量分数=×100%=14.9%
答:滤液中溶质质量分数为14.9%。