文档内容
备战2017年中考二轮讲练测
专题 10 碳及其氧化物(讲案)
☆ 考点梳理 ☆
一、碳的几种单质
1、金刚石(C)是自然界中最硬的物质,可用于制钻石、刻划玻璃、钻探机的钻头等。
2、石墨(C)是最软的矿物之一,有优良的导电性,润滑性。可用于制铅笔芯、干电池的电极、电车的滑块
等。
3、无定形碳:由石墨的微小晶体和少量杂质构成.主要有:焦炭,木炭,活性炭,炭黑等。活性炭、木炭具有强
烈的吸附性,但活性炭的吸附作用比木炭要强,如制糖工业利用其来脱色,防毒面具里的滤毒罐也是
利用活性炭来吸附毒气。焦炭用于冶铁,炭黑加到橡胶里能够增加轮胎的耐磨性。
4、C 是一种由60个碳原子构成的分子,形似足球,性质很稳定。
60
注意:
1、铅笔里面其实不含铅,是石墨和黏土混合而成的混合物。H代表Hard,坚硬的;B代表Black,黑的。6B
最软,颜色最深;6H最硬,HB软硬适中。
2、金刚石和石墨的物理性质有很大差异的原因是:碳原子的排列不同。
二、碳单质的化学性质
各种单质碳的物理性质差异很大,但它们的化学性质是完全相同。
1、常温下的化学性质稳定
⑴原因:碳原子的最外层有4个电子,既不容易得电子,也不容易失去电子,因此常温下碳的化学性质
比较稳定。
⑵应用:①档案材料一般用碳素墨水书写;②古代书画历经百年也安然无恙;③木质电线杆埋入地下部
分用火烧焦可防腐都是利用这个原理。
2、可燃性:
完全燃烧(氧气充足),生成CO : C+O CO
2 2 2
不完全燃烧 (氧气不充足),生成CO:2C+O 2CO
2
3、还原性:C+2CuO 2Cu+CO ↑ (置换反应) 应用:冶金工业
2
现象:黑色粉末逐渐变成光亮红色,澄清的石灰水变浑浊。
1注意:
1、:碳在常温下的化学性质稳定。碳参与的反应条件一般为点燃、高温或加热。
2、:可利用碳的还原性将其应用在冶金工业上。
三、二氧化碳
1、物理性质:常温下是无色,无味的气体,密度比空气大,能溶于水。高压低温下可得固体----干冰。
[来源:学.科.网]
2、化学性质:
1)一般情况下不能燃烧,也不支持燃烧,不能供给呼吸
2)与水反应生成碳酸,反应的化学方程式为:CO+H O==H CO。生成的碳酸能使紫色的石蕊试液变红。
2 2 2 3
碳酸不稳定,易分解。HCO == H O+ CO ↑
2 3 2 2
3)能和碱反应生成碳酸盐和水。
①能使澄清的石灰水变浑浊:CO+Ca(OH) ==CaCO↓+H O 本反应可用于检验二氧化碳。
2 2 3 2
②能和氢氧化钠反应生成碳酸钠和水。2NaOH+CO =Na CO+H O 反应无明显现象,可用于吸收大量
2 2 3 2
的二氧化碳。
4)二氧化碳能与炽热的碳反应,生成一氧化碳。该反应的化学方程式为:CO+C 2CO
2
5)二氧化碳与水被绿色植物利用,而进行光合作用的反应,合成有机物(主要是淀粉)。
该反应的化学方程式为:6CO+6H O======C H O+6O 。
2 2 6 12 6 2 [来源:学§科§网]
3、用途:①灭火(依据:二氧化碳不燃烧也不支持燃烧,密度比空气大)既利用其物理性质,又利用其化学
性质。②干冰用于人工降雨、制冷剂利用其物理性质。
③温室肥料。④作制碳酸氢铵、碳酸钠(纯碱)的工业原料。
4、二氧化碳对环境的影响
二氧化碳对环境的影响,客观地说是两方面的。
(1)有利的方面是:它能促进绿色植物进行光合作用,满足人和动物所需的有机物的合成和对氧气的需
求;以及空气中氧气含量的相对稳定和自然界的碳、氧的循环。
(2)不利的方面是:二氧化碳含量猛增,导致温室效应。温室效应的危害:①全球变暖;②地球上的病虫害
增加;③海平面上升;④气候反常;⑤土地沙漠化等。
2(3)对策:
①减少使用煤、石油、天然气等化石燃料
②开发新能源如、太阳能、风能、地热等清洁能源。
③大力植树造林、严禁乱砍滥伐森林。
注意:
1、灭火既利用其物理性质(密度比空气大),又利用其化学性质(不燃烧也不支持燃烧)。
2、二氧化碳在与碱时,先与水反应生成碳酸;碳酸再与碱反应。所以反应中二氧化碳会转化为碳酸根。反
应的类型判断为复分解反应。
3、二氧化碳过多排放会引起温室效应,但不是空气污染物。
四、一氧化碳的性质
1、物理性质:常温下是无色,无味的气体,密度比空气略小,难溶于水
2、化学性质: (H、CO、C具有相似的化学性质:①可燃性 ②还原性)
2
1)可燃性:2CO+O 2CO ( 可燃性气体点燃前一定要检验纯度)实验现象:发出蓝色的火焰;生
2 2
成的气体能使澄清的石灰水变浑浊。
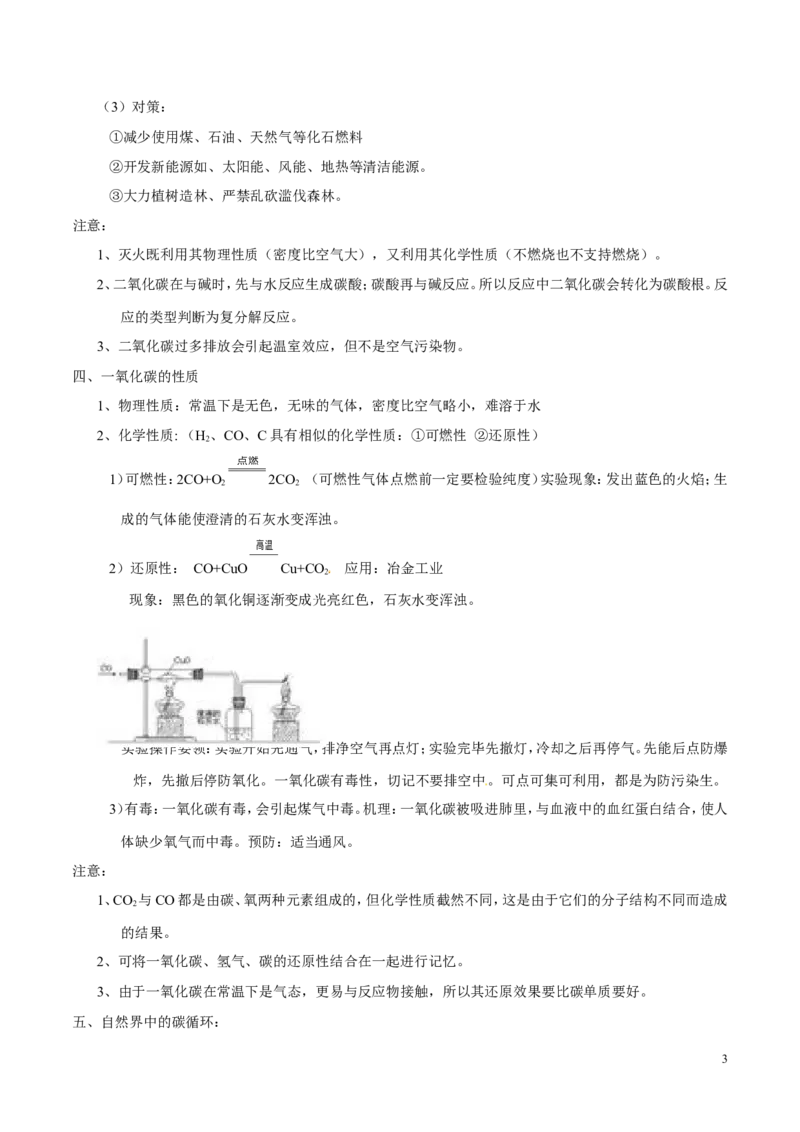
2)还原性: CO+CuO Cu+CO 应用:冶金工业
2
现象:黑色的氧化铜逐渐变成光亮红色,石灰水变浑浊。
实验操作要领:实验开始先通气,排净空气再点灯;实验完毕先撤灯,冷却之后再停气。先能后点防爆
炸,先撤后停防氧化。一氧化碳有毒性,切记不要排空中。可点可集可利用,都是为防污染生。
3)有毒:一氧化碳有毒,会引起煤气中毒。机理:一氧化碳被吸进肺里,与血液中的血红蛋白结合,使人
体缺少氧气而中毒。预防:适当通风。
[来源:学科网]
注意:
1、CO 与CO都是由碳、氧两种元素组成的,但化学性质截然不同,这是由于它们的分子结构不同而造成
2
的结果。
2、可将一氧化碳、氢气、碳的还原性结合在一起进行记忆。
3、由于一氧化碳在常温下是气态,更易与反应物接触,所以其还原效果要比碳单质要好。
五、自然界中的碳循环:
3过程:
☆ 考点典析 ☆
【题型一】温室效应、低碳生活
氧循环和碳循环密不可分,其中属于二氧化碳转化为氧气的变化的是( )
A.海水吸收二氧化碳 B.动植物的呼吸作用
C.绿色植物的光合作用 D.化石燃料的燃烧
【解题方法】根据自然界中的碳循环和氧循环的主要方法和途径进行分析和回答。
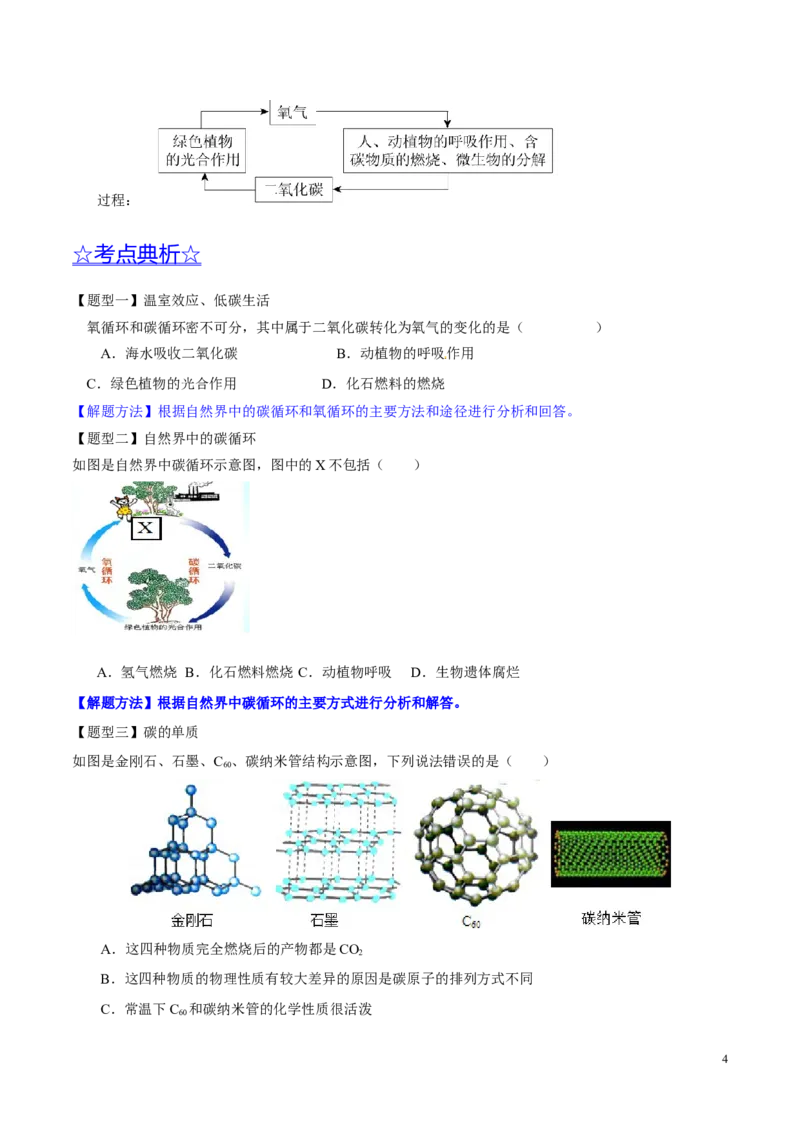
【题型二】自然界中的碳循环
如图是自然界中碳循环示意图,图中的X不包括( )
A.氢气燃烧 B.化石燃料燃烧 C.动植物呼吸 D.生物遗体腐烂
【解题方法】根据自然界中碳循环的主要方式进行分析和解答。
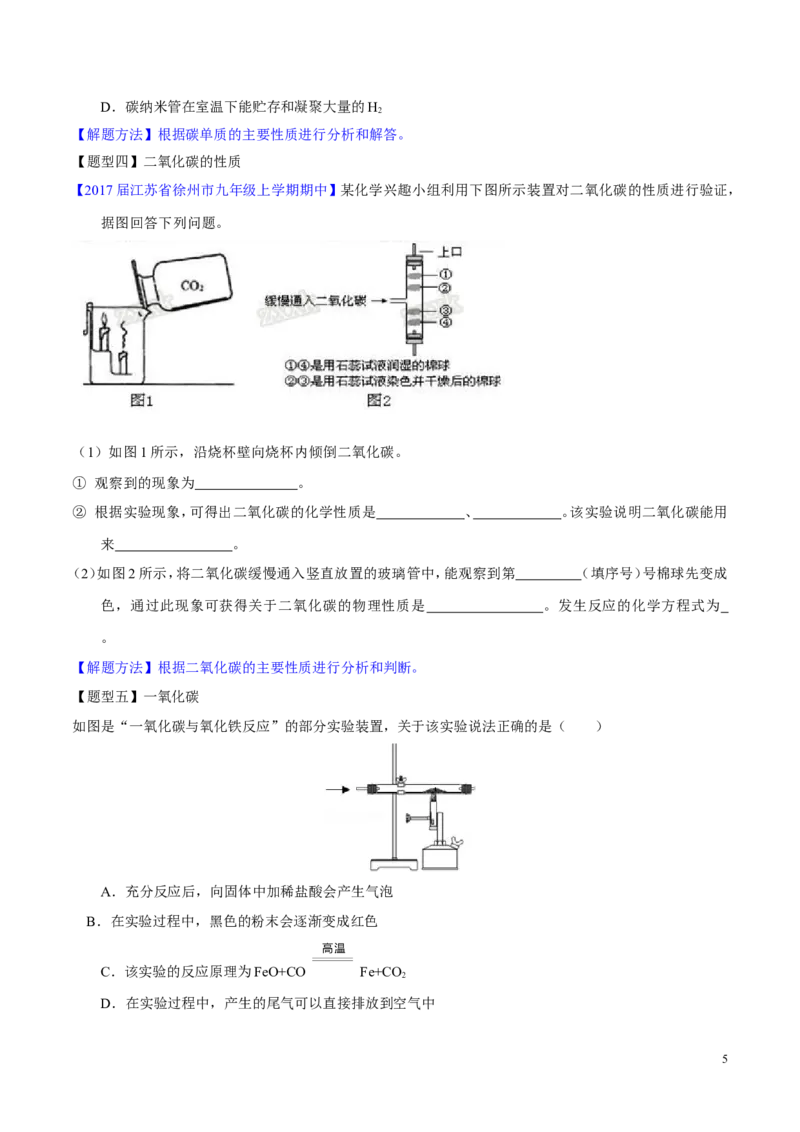
【题型三】碳的单质
如图是金刚石、石墨、C 、碳纳米管结构示意图,下列说法错误的是( )
60
A.这四种物质完全燃烧后的产物都是CO
2
B.这四种物质的物理性质有较大差异的原因是碳原子的排列方式不同
C.常温下C 和碳纳米管的化学性质很活泼
60
4D.碳纳米管在室温下能贮存和凝聚大量的H
2
【解题方法】根据碳单质的主要性质进行分析和解答。
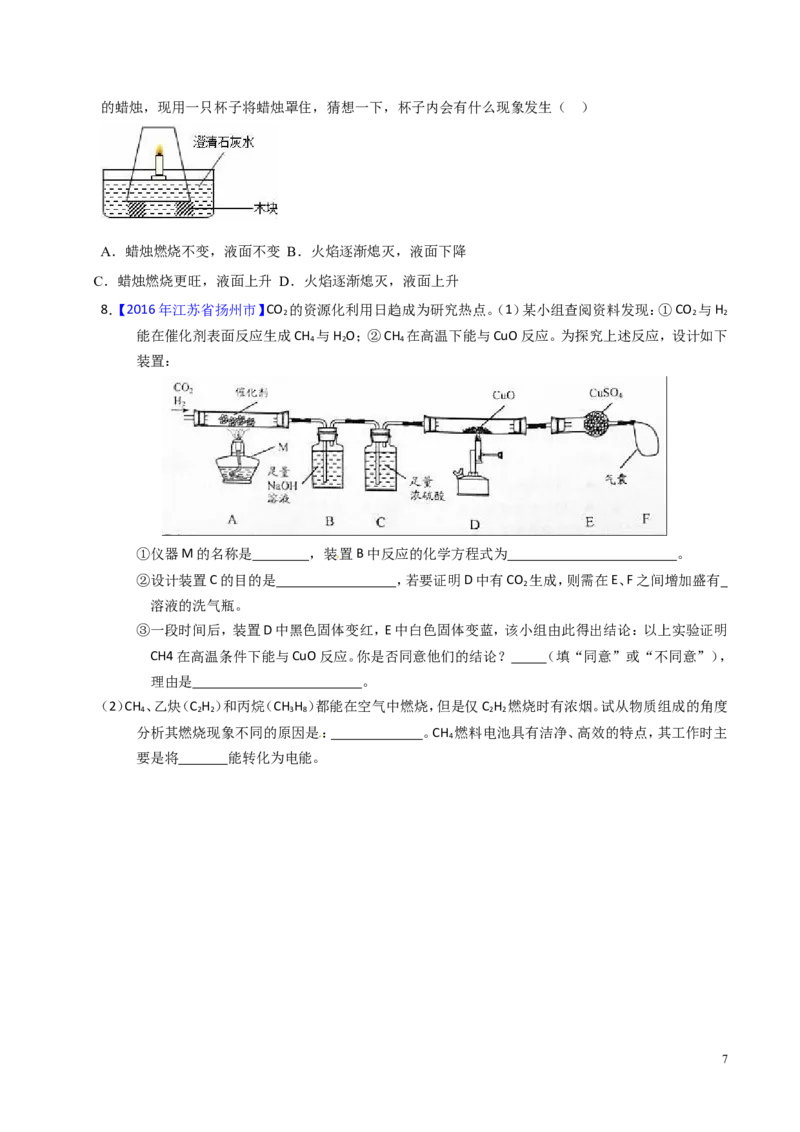
【题型四】二氧化碳的性质
【2017届江苏省徐州市九年级上学期期中】某化学兴趣小组利用下图所示装置对二氧化碳的性质进行验证,
据图回答下列问题。
(1)如图1所示,沿烧杯壁向烧杯内倾倒二氧化碳。
[来源:Z,xx,k.Com]
① 观察到的现象为 。
② 根据实验现象,可得出二氧化碳的化学性质是 、 。该实验说明二氧化碳能用
来 。
(2)如图2所示,将二氧化碳缓慢通入竖直放置的玻璃管中,能观察到第 ( 填序号)号棉球先变成
色,通过此现象可获得关于二氧化碳的物理性质是 。发生反应的化学方程式为
。
【解题方法】根据二氧化碳的主要性质进行分析和判断。
【题型五】一氧化碳
如图是“一氧化碳与氧化铁反应”的部分实验装置,关于该实验说法正确的是( )
A.充分反应后,向固体中加稀盐酸会产生气泡
B.在实验过程中,黑色的粉末会逐渐变成红色
C.该实验的反应原理为FeO+CO Fe+CO
2
D.在实验过程中,产生的尾气可以直接排放到空气中
5【解题方法】根据一氧化碳的性质进行分析和解答。
☆ 方法点拨 ☆
1、由于碳原子排列方式不同,几种碳单质的物理各异;但是,由于它们都是由碳元素组成的单质,所以其
化学性质是相同的。
2、关于碳单质的化学性质及用途,可以根据“性质用途”这个相互关系来互推巧记和理解。
3、结合典型的实验、归纳和对比等方法,来掌握二氧化碳和一氧化碳的性质,可进行记忆。
☆ 随堂小练 ☆
1.自然界中有几千万种含碳物质,并循环转化。下列说法正确的是( )
A.人的生命活动离不开碳循环 B.森林的减少对碳的循环没有影响
C.金刚石中碳原子间没有间隔 D.地下的煤中碳原子是静止不动的
2.下列说法中,正确的是( )
A.海底蕴藏着大量“可燃冰”,以它为燃料不会对自然界中的碳循环产生影响
B.夜间发现液化气泄漏应立即开灯并开窗通风
C.限制化工发展,关停化工企业,消除污染源头
D.扑灭电器、图书档案等火灾最适宜的灭火器是液体二氧化碳灭火器
3.下列做法会加剧温室效应的是( )
A.大力植树造林 B.鼓励私人使用小汽车代替公交车
C.骑自行车上下班 D.大量利用太阳能、风能和氢能等新能源
[来源:学科网]
4.【2017届内蒙古鄂尔多斯市鄂托克旗九年级上期末】下列有关碳和碳的氧化物的说法中不正确的是
A.一氧化碳能使澄清的石灰水变浑浊 B.CO 是植物光合作用的重要原料
2
C.木炭和一氧化碳都能作燃料 D.金刚石、石墨和C 都是由碳元素组成的单质
60
5.下列关于一氧化碳和二氧化碳的说法正确的是( )
A.都比空气重 B.都能和澄清石灰水发生反应
C.都有还原性 D.都可以用碳和氧气反应得到
6.【2016届新人教版九年级下3月月考】“两型”社会,提倡“低碳”生活,下列有关碳及化合物的说法正
确的是( )
A.二氧化碳是导致酸雨的主要气体 B.室内放一盆水能防止一氧化碳中毒
C.大气中二氧化碳消耗的途径主要是绿色植物的光合作用
D.金刚石、石墨是碳的单质,而C 则是碳的化合物
60
7.【2017届江苏省东台第六教育联盟九年级上月考二】如图,在一个盛有澄清石灰水的容器中有一枝燃着
6的蜡烛,现用一只杯子将蜡烛罩住,猜想一下,杯子内会有什么现象发生( )
A.蜡烛燃烧不变,液面不变 B.火焰逐渐熄灭,液面下降
C.蜡烛燃烧更旺,液面上升 D.火焰逐渐熄灭,液面上升
8.【2016年江苏省扬州市】CO 的资源化利用日趋成为研究热点。(1)某小组查阅资料发现:①CO 与H
2 2 2
能在催化剂表面反应生成CH 与H O;②CH 在高温下能与CuO反应。为探究上述反应,设计如下
4 2 4
装置:
①仪器M的名称是 ,装置B中反应的化学方程式为 。
②设计装置C的目的是 ,若要证明D中有CO 生成,则需在E、F之间增加盛有
2
溶液的洗气瓶。
③一段时间后,装置D中黑色固体变红,E中白色固体变蓝,该小组由此得出结论:以上实验证明
CH4在高温条件下能与CuO反应。你是否同意他们的结论? (填“同意”或“不同意”),
理由是 。
(2)CH 、乙炔(C H )和丙烷(CH H )都能在空气中燃烧,但是仅C H 燃烧时有浓烟。试从物质组成的角度
4 2 2 3 8 2 2
分析其燃烧现象不同的原因是: 。CH 燃料电池具有洁净、高效的特点,其工作时主
4
要是将 能转化为电能。
7