文档内容
夯实双基
1、【2016届四川省遂宁市射洪外国语学校九年级上第16周周考】一定质量的镁条在氧气中完全燃烧后生成
氧化镁.固体质量随时间的变化关系如图所示.下列说法不正确的是( )
A.生成MgO的质量:mg B.参加反应的Mg的质量:m g
2 1
C.参加反应的O 的质量:(m﹣m)g D.参加反应的镁和氧气的质量比:m:(m﹣m)=3:1
2 2 1 1 2 1
【答案】D
2.【2017届黑龙江省哈尔滨第六十九中学九年级上11月月考】实验室有10g不锈钢样品(假设除铁外,其他
成分不参加反应),与100g氢元素质量分数为10%的稀硫酸恰好完全反应,则该样品中铁的质量分数为
( )
A.56% B.12.5% C.30% D.70%
【答案】D
【解析】:稀硫酸溶液中氢元素占10%,其它元素占90%,质量比为1:9,HSO 中H和剩余元素的质量比为
2 4
(1×2):(32+16×4)=1:48,HO中H和O两种元素的质量比为1×2:16=1:8,设HSO 分子在溶液中占
2 2 4
的分子个数比为x,则48x+8×(1-x)=9,解得x= ,所以HSO 分子与HO分子个数比为1:39,故稀硫酸
2 4 2
1溶液中溶质的质量分数为 ×100%=12.25%,设样品中铁的质量分数为x,100g稀硫酸中硫酸
的质量是100g×12.25%=12.25g
Fe+H SO =FeSO+H ↑
2 4 4 2
56 98
56x 12.25 g
则 = ,解得x=70% 学科*网
3.【2017届黑龙江省大庆市杜蒙县九年级上学期第一次月考】下列物质分别与100克7.3%的盐酸恰好完全
反应,反应后所得的溶液中溶质的质量分数大小关系正确的是( )
A.Mg>MgO=MgCO >Mg(OH) B.Mg=MgO>MgCO =Mg(OH)
3 2 3 2
C.Mg(OH) >MgO=MgCO >Mg D.Mg>MgO>MgCO >Mg(OH)
2 3 3 2
【答案】A
4.【2016届四川省遂宁市射洪外国语学校九年级上第13周周考】已知化学反应A+B═C+D,A和B参加反应
时质量比为3:2,若反应后生成C和D共10g,则反应掉的A的质量为( )
[来源:学+科+网]
A.4g B.6g C.1g D.2g
【答案】B
【解析】由质量守恒定律,生成C和D共10g,则参加反应的A和B的质量之和也为10g,而A、B两物质完全
2反应时的质量比为3:2,故反应消耗A的质量是10g× =6g.故选B.学科*网
5.【2017届山东省临沂市兰陵县九年级上期末】为测定某石灰石样品中碳酸钙的含量,取10.0g石灰石放于
烧杯中,再向其中加入稀盐酸50.0g,恰好完全反应(石灰石中的杂质不溶于水,也不与稀盐酸反应),反
应后烧杯中物质总质量为56.7g。
(1)生成二氧化碳的质量为 ;
(2)求石灰石样品中碳酸钙的质量分数(写出计算过程)。
【答案】(1)3.3g;(2)75%
6.【2017届四川省富顺县童寺学区九年级上学期第三次月考】某实验小组同学为测定实验室中用KClO 样品
3
的纯度,取一定量样品与1gMnO 混合,其总质量为6g。依次加热该混合物T1、T2、T3、T4时间后,分别
2
冷却称剩余固体质量,记录的有关数字如下表(杂质不参加化学反应):
①完全反应后产生的O 质量为 。
2
②计算氯酸钾样品中KClO 的质量分数。(写出计算过程)
3
【答案】①1.92g ②98%.
[来源:学.科.网Z.X.X.K]
【解析】∶由题中信息知,①完全反应后产生的O 质量为6g-4.08g=1.92g.
2
②解∶设氯酸钾样品中KClO 的质量为xg
3
2KClO 2KCl+3O ↑
3 2
245 96
[来源:学§科§网Z§X§X§K]
X 1.92g
245/x=96/1.92g
3x=4.9g
氯酸钾样品中KClO 的质量分数为 4.9g/﹙6g-1g﹚×100%=98%.
3
答∶氯酸钾样品中KClO 的质量分数为98%·学&科*网
3
能力提升
1.在天平的两个托盘上各放一只烧杯,烧杯中都盛有足量的盐酸,此时天平保持平衡.如果一边投入少许锌
粒,另一边投入相同质量的铁粉,两者都完全溶解后,天平指针将( )
A.偏向放锌粒的烧杯一边 B.不发生偏转
C.偏向放铁粉的烧杯一边 D.无法判断
【答案】A
【解析】由于投入等质量的锌和铁,所以关键看谁产生氢气多,哪一边就轻,由于铁产生的氢气比锌多,所以
最后偏向于锌.故选:A.
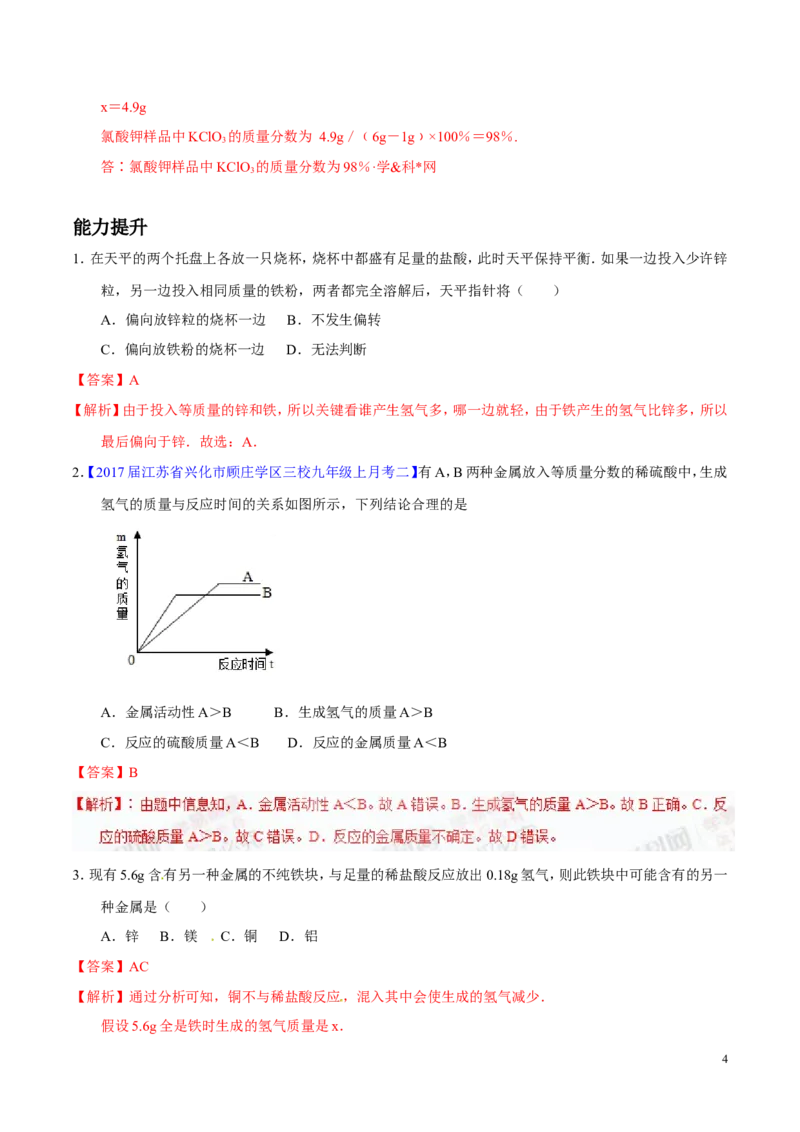
2.【2017届江苏省兴化市顾庄学区三校九年级上月考二】有A,B两种金属放入等质量分数的稀硫酸中,生成
氢气的质量与反应时间的关系如图所示,下列结论合理的是
A.金属活动性A>B B.生成氢气的质量A>B
C.反应的硫酸质量A<B D.反应的金属质量A<B
【答案】B
3.现有5.6g含有另一种金属的不纯铁块,与足量的稀盐酸反应放出0.18g氢气,则此铁块中可能含有的另一
种金属是( )
A.锌 B.镁 C.铜 D.铝
[来源:学科网ZXXK]
【答案】AC
【解析】通过分析可知,铜不与稀盐酸反应,混入其中会使生成的氢气减少.
[来源:Z#xx#k.Com]
假设5.6g全是铁时生成的氢气质量是x.
4Fe+H SO =FeSO+H ↑
2 4 4 2
56 2
5.6g x
则 ,解得 x=0.2g.
由以上计算可知,纯铁5.6g与盐酸反应生成的氢气0.2g比实际生成的氢气0.18g多,可推出掺入的金属
同质量时生成的氢气要比铁少,或者掺入不与盐酸反应的金属,而6.5克锌会生成0.2克的氢气,2.4克
的镁会生成0.2克的氢气,1.8克的铝会生成0.2克的氢气,通过平均值法比较可知,混入的金属可能是
锌,不可能是镁、铝.铜不与盐酸反应,故选AC.
4.有元素化合价为+2价的A、B两种金属.取等质量的大小形状相同的A、B与足量盐酸反应时,产生氢气的
质量与反应时间的函数关系如图所示,从图示说明的函数关系,可以得出的正确结论是( )
A.与酸反应速率:A<B,相对原子质量A<B B.与酸反应速率:A<B,相对原子质量A>B
C.与酸反应速率:A>B,相对原子质量 A>B D.与酸反应速率:A>B,相对原子质量 A<B
【答案】C
5.【2017届黑龙江省大庆市肇源县五四制九年级上学期期中】杯中加入10.2g碳酸镁和氧化镁的混合物,右
边烧杯中加入8g铜,充分反应后,天平重新平衡,则所加入混合物中氧化镁的质量为 ( )
A.1.8g B.2.2g C.6g D.8g
【答案】C
56.【2017届山东省威海市乳山市九年级12月月考】将铁粉和铜粉的混合物7g,加入到盛有58.1g稀盐酸的烧
杯中,恰好完全反应。此时烧杯内各物质的总质量为64.9g。试计算:
(1)原混合物中铁粉的质量分数;
(2)反应后所得溶液中溶质的质量分数;
【答案】(1)80%(2)20%
【解析】:解:生成氢气的质量为7g+58.1g-64.9g=0.2g
设原混合物中Fe的质量为x,生成FeCl 的质量为y,参加反应的HCl的质量为z
2
Fe+2HCl===FeCl +H ↑
2 2
56 73 127 2
x z y 0.2g
56:2=x:0.2g得x=5.6g
127:2=y:0.2g得y=12. 7g
73:2=z:0.2g得z=7.3g
(1) 原混合物中铁粉的质量分数为:5.6g÷7g×100%=80%
(2) 反应后所得溶液中溶质的质量分数为:12.7g÷(5.6g+58.1g-0.2g)×100%=20%
7.【2017届山东省新泰市翟镇中学九年级上学期期末】鸡蛋壳的主要成分是碳酸钙,为了测定某鸡蛋壳中碳
酸钙的含量,小群同学进行了如下实验:将鸡蛋壳洗净、干燥并捣碎后,称取10g放在烧杯里,然后往烧
杯中加入足量的稀盐酸90g,充分反应后,称得烧杯中物质的总质量为97.8g.(假设鸡蛋壳中的其他物
质不与盐酸反应)
(1)产生二氧化碳气体 g.
(2)计算10g该鸡蛋壳中碳酸钙的质量,要求写出完整的解题步骤.
6【答案】(1)2.2;(2)5g.
7