文档内容
夯实双基
1.下列叙述不适合用质量守恒定律解释的是( )。
A.水加热变成水蒸气,变化前后质量相等
B.要得到18 g水,则参加反应的氢气和氧气的总质量一定为18 g
C.1 g硫与1 g氧气化合生成2 g二氧化硫
D.在分解反应中,反应物的质量一定大于任意一种生成物的质量
【答案】A
【解析】质量守恒定律是化学变化普遍遵循的一个规律,而水加热变成水蒸气是物理变化不属于化学变化。
2.【2016年广西省贺州市】某有机物与氧气充分反应,产物只有二氧化碳和水,则该有机物一定含有的元素
是( )
A.C、O B.H、O C.C、H D.C、H、O
【答案】C
3.【2016年福建省厦门市】三种物质在密闭容器中发生反应,反应前后质量比例的变化关系如图所示,下列
说法正确的是( )
A.反应中CaO为催化剂 B.该反应是复分解反应
C.反应后容器中固体质量减少 D.反应后容器中氧元素质量分数增大
【答案】C
【解析】由三种物质在密闭容器这个反应前后质量比例的变化,确定是反应物还是生成物。反应后二氧化碳和
氧化钙的质量都增加了,是生成物,碳酸钙的质量减小了,是反应物,该反应是碳酸钙高温分解成二氧化
碳和氧化钙的反应。A、氧化钙在反应中不是催化剂,是生成物,该选项说法不正确;B、该反应中反应物
为一种,生成物为两种,符合分解反应的定义,该选项说法不正确;C、该反应是一种固体反应物生成一种
固体和一种气体的反应,故反应后固体质量减少,该选项说法正确;D、根据质量守恒定律,反应前后元素
1的种类和质量不变可知,反应后容器中的氧元素质量分数不变,该选项说法不正确。
4.【2016年湖南省衡阳市】FeS 常用于在接触法制硫酸过程中产生CO ,其化学方程式为:4FeS +11O
2 2 2 2
2X+8SO ,则X的化学式为( )
2
A.FeO B.Fe O C.Fe O D.FeSO
2 3 3 4 4
【答案】B
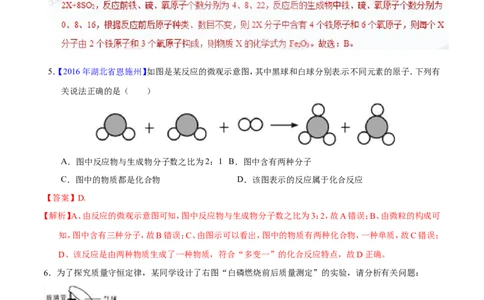
5.【2016年湖北省恩施州】如图是某反应的微观示意图,其中黑球和白球分别表示不同元素的原子.下列有
关说法正确的是( )
[来源:Zxxk.Com]
A.图中反应物与生成物分子数之比为2:1 B.图中含有两种分子
C.图中的物质都是化合物 D.该图表示的反应属于化合反应
【答案】D
[来源:学科网ZXXK]
【解析】A、由反应的微观示意图可知,图中反应物与生成物分子数之比为3:2,故A错误;B、由微粒的构成可
知,图中含有三种分子,故B错误;C、由图示可以看出,图中的物质有两种化合物,一种单质,故C错误;
D、该反应是由两种物质生成了一种物质,符合“多变一”的化合反应特点,故D正确。
[来源:学科网]
6.为了探究质量守恒定律,某同学设计了右图“白磷燃烧前后质量测定”的实验,请分析有关问题:
(1)装置:锥形瓶的底部铺有一层细沙,其作用是 ____________________________
(2)实验现象:白磷燃烧产生________________,气球先变大又变小。气球先变大后又变小的原因
____________________________
2(3)燃烧后称量:发现托盘天平指针偏向右边,造成的原因可能是_________________。
(4)反思:白磷燃烧_________(填“遵守”或“不遵守”)质量守恒定律,理由是_____________。
【答案】(1)防止锥形瓶底部局部受热炸裂。(2) 大量白烟 白磷燃烧放热,锥形瓶内气体膨胀,气球变大;燃烧
消耗氧气,冷却至室温,瓶内压强减小,气球变小。(3) 装置漏气(4)遵守 参加反应的各物质质量总和与
生成的各物质质量总和相等。学科*网
【解析】(1)、为防止锥形瓶底部局部受热炸裂,要在锥形瓶的底部铺有一层细沙;(2)、白磷燃烧产生大量白
烟,放出热量,锥形瓶内气体膨胀,气球变大;燃烧消耗氧气,冷却至室温,瓶内压强减小,气球变小;
(3)、若装置漏气,则燃烧后称量,会发现托盘天平指针偏向右边;(4)、白磷燃烧遵守质量守恒定律;因
为参加反应的各物质质量总和与生成的各物质质量总和相等。
[来源:学&科&网]
能力提升
1.【2016年四川省绵阳市】 液化石油气的成分中含有丙烯(C H)和丁烯(C H),将二者的混合气体14g在
3 6 4 8
足量氧气中充分燃烧,产生二氧化碳44g,下列判断中不正确的是
A.混合气体中碳与氢的质量之比一定是6:1 B.消耗O 的质量一定为48g
2
C.混合气体中丙烯(C H)的质量分数一定为50% D.混合气体燃烧生成HO的质量一定为18g
3 6 2
【答案】D
2.【2016年新疆】现有32g某可燃物在密闭容器中完全燃烧后,测得生成88g二氧化碳和72g水,关于该可
燃物的说法正确的是( )
A.一定是氧化物 B.只含有碳、氢两种元素
C.一定含有碳、氢、氧三种元素 D.一定含有碳、氢元素,可能含有氧元素
【答案】B
【解析】参加反应的氧气质量为:88g+72g﹣32g=128g,88g二氧化碳中碳元素的质量为:88g× ×100% =24g,
3氧元素的质量为:88g﹣24g=64g,72g水中氢元素的质量为:72g× ×100%=8g,氧元素的质量为:72g﹣
8g=64g,二氧化碳中的碳元素和水中的氢元素来自于该可燃物,该可燃物中氧元素的质量为:64g+64g﹣
128g=0,则该可燃物只含有碳、氢两种元素;故选B。学科*网
3.【2016年甘肃省兰州市】把一定质量的甲、乙、丙、丁四种物质放入一密闭容器中,在一定条件下反应一段
时间,测得反应后各物质的质量如下,则下列说法中错误的是( )
物质 甲 乙 丙 丁
反应前的质量(g) 7.6 2.0 0.2 0
[来源:学科网ZXXK]
反应后的质量(g) 3.2 X 5.8 0.4
A.X=0.4 B.丁一定是单质
C.甲和乙是反应物 D.反应中的甲、丙发生改变的质量比是11:14
【答案】B
【解析】A、X=7.6+2+0.2﹣3.2﹣5.8﹣0.4=0.4,正确;B、甲乙质量减少,是反应物,丙丁质量增加,是生成物,丁
不一定为单质,错误;C、甲乙质量减少,是反应物,正确;D、反应中的甲、丙发生改变的质量比是:(7.6﹣
3.2):(5.8﹣0.2)=11:14,正确;故选B。
4.、【2016年广东省梅州市】工业上用甲和乙反应制备丙和丁,其反应的微观示意图如下:
(1)该化学变化中没有发生改变的粒子是______________(填“分子”或“原子”)
(2)写出该反应的化学方程式______________.
(3)该反应中含氢元素的化合物有______________种;反应前后化合价发生可变化的元素是
______________(填元素符号)
【答案】(1)原子;(2)CH+H O CO+3H;(3)2;C、H。
4 2 2
5.【2016年福建省漳州市】如图是某反应的微观粒子示意图.
4(1)根据化学反应的本质,反应物的方框内还应补充的粒子及数目是_________.
A.一个 B.两个 C.一个 D.两个
(2)两种生成物分子的共同之处是_________,该反应属于基本反应类型中的_________反应.
【答案】(1)C;(3)含有两个相同的原子;分解
【解析】(1)在化学反应前后原子种类、数目不变,生成物共有两种原子共6个,对比反应前后原子种类和个
数可知还应补充的粒子为C;(2)由微观结构图可以看出两种生成物的共同之处是:每个分子都含有两个
相同的原子;该反应的反应物是一种,生成物是两种,属于分解反应。学科&网
6.【2016年浙江省衢州市】 以下是俄国化学家罗蒙诺索夫曾开展的实验:
①先用天平称取质量为m 的金属锡粉。
1
②将这些锡粉放在密闭容器里进行完全燃烧,生成了白色固体物质,称量容器的总质量为m 。
2
③打开容器,听到了空气进入容器发出的“丝丝的声响”,称量所得白色物质的质量为m 。
3
④把白色物质放回原容器里(容器中空气的组成恢复到初始状态),重新称量容器的总质量为m 。
4
(1)根据所学知识判断,锡的燃烧是 变化。
(2)罗蒙诺索夫分析数据后发现,生成白色物质的质量m = ,于是提出了“参加反应的物质的总质量,
3
等于反应后产物的总质量”的观点。
(3)后经多位科学家的共同努力,最终确立了质量守恒定律,请从微观角度解释该定律 :
。
【答案】(1)化学 (2)m ﹣m +m( 3)因为化学反应的过程是原子的重新组合过程,反应前后原子的种类不变,
4 2 1
总个数不变,原子质量不变,所以化学反应前后物质的总质量相等
5