文档内容
姓名: 班级: 成绩:
基础过关检测(50分)
(1——8小题每小题4分,共50分)
1.【2017届江苏省扬州市杨寿学校九年级12月月考】铜能被加工成厚度仅为7微米的超薄铜箔,说明铜具有
良好的
A.导电性 B.延展性 C.导热性 D.抗腐蚀性
【答案】B
【解析】∶铜能被加工成厚度仅为7微米的超薄铜箔,说明铜具有良好的B.延展性。学科*网
2.【2017届黑龙江省鸡西十九中九年级上学期期中考试】下列物质的物理性质中,钛、铜、铝三种金属都具有
的是:( )
银白色金属 延展性 导热性 导电性 被磁铁吸引
A.①②③ B.②③④ C.③④⑤ D.①⑤
【答案】B
【解析】:钛、铜、铝三种金属都具有良好的导热性、导电性、延展性,铜是紫红色金属,铁能被磁铁吸引。
3.回收废旧电池最主要的目的是( )
A.回收碳棒 B.回收金属锌 C.防止汞、镉等金属造成的污染 D.为了收藏爱好
【答案】C
4.等质量的氧化铁分别和碳和一氧化碳充分反应后,所得铁的质量为( )
A.一样多 B.CO还原出来的多 C.碳还原出来的多 D.不能确定
【答案】A
【解析】等质量的氧化铁分别和碳和一氧化碳充分反应,根据质量守恒定律,最终都是把氧化铁中的铁完全
还原出来,因此得到的铁的质量一样.故选A.
5.【2017届山东省威海市乳山市九年级12月月考】金属材料在人类活动中已得到越来越广泛的应用。下列属
于金属共性的是:( )
A.很高的熔点 B.良好的导电性 C.很大的硬度 D.银白色的光泽
【答案】B
1【解析】:金属材料有很多共同点,如:都有良好的导电性、导热性、延展性;大多数金属为银白色固体,但是铜
为紫红色,金为黄色;熔点、沸点较高,但是汞常温下为液态,熔点较低;
6.【2017届江苏省泰州市姜堰区实验初级中学九年级上学期12月月考】下列解释错误的是
A.铝制品不用涂任何保层来防腐,因为铝不与空气反应
B.铁丝在空气不能被点燃与空气中氧气的体积分数有关
C.生铁和钢的性能不同与它们的组成中含碳量不同有关
D.新轿车中常弥漫着皮革气味。从分子角度看,这是构成物质的分子大小不同的结果
【答案】AD
7.【2017届山东省威海市乳山市九年级12月月考】向AgNO、Cu(NO )、Zn(NO ) 的混合溶液中加入一些铁
3 3 2 3 2
粉,反应完成后过滤,下列情况不可能存在的是( )
A、滤纸上有Ag、Cu、Fe,滤液中有Zn2+、Fe2+ B、滤纸上有Ag、Cu,滤液中有Zn2+、Fe2+
C、滤纸上有Ag、Cu,滤液中有Cu2+、Zn2+、Fe2+ D、滤纸上有Ag、Cu、Fe,滤液中有Cu2+、Zn2+、Fe2+
【答案】D
【解析】:金属活动顺序表:K Ca Na Mg Al Zn Fe Sn Pb H Cu Hg Ag Pt Au在金属活动顺序表中,排在氢前边
的金属能和酸发生置换反应生成盐和氢气。金属的位置越靠前,金属的活动性越强。位置靠前的金属能
将位于其后的金属从它的盐溶液中置换出来。向AgNO、Cu(NO )、Zn(NO ) 的混合溶液中加入一些铁
3 3 2 3 2
粉,铁先与硝酸银反应生成硝酸亚铁和银,然后与硝酸铜反应生成硝酸亚铁和铜;与硝酸锌不反应,所以
溶液中一定有Zn2+,固体中一定有银;当铁的质量会剩余时,滤纸上有Ag、Cu、Fe,滤液中有Zn2+、Fe2+;
当铁的质量刚好与硝酸银和硝酸铜反应完时,滤纸上有Ag、Cu,滤液中有Zn2+、Fe2+,当铁的质量能将硝
酸银反应完,但剩余铁只能与部分硝酸铜反应时,滤纸上有Ag、Cu,滤液中有Cu2+、Zn2+、Fe2+;硝酸银和
硝酸铜有任何一种物质没有反应完,铁都不会剩余。学科*网
8.【2017届山东省东营市育才学校九年级11月质检】某化学小组在AgNO 和Cu(NO ) 的混合溶液中加入一
3 3 2
定质量的锌粉,充分反应后过滤,得到滤液和滤渣。他们对所得滤液和滤渣有如下描述:
①滤液中一定含有Zn(NO ) ②滤渣中一定含有Ag,可能含有Cu和Zn ③若滤液呈蓝色,则向滤渣
3 2
中滴加稀盐酸无明显现象 ④若向滤渣中滴加稀盐酸有气泡产生,则滤液中一定没有 AgNO 和Cu
3
(NO ) 上述四种描述中正确的个数为( )
3 2
A.1个 B.2个 C.3个 D.4个
2【答案】D
9.【2017届山东省武城二中九年级12月月考】铬(Cr)是重要的金属材料,越来越受到人们的关注。某化学兴
趣小组对Cr、Al、Cu的金属活动性顺序进行探究,过程如下:
【提出假设】对三种金属的活动性顺序提出三种可能的假设:
a.Al>Cr>Cu b.Cr>Al>Cu c.________________
【设计实验】同温下,取大小相同的打磨过的金属薄片,分别投入到等体积等浓度的足量稀盐酸中,观察现象,
记录如下:
金属 Cr Al Cu
与盐酸反应的现 气泡产生缓慢,金 气泡产生剧烈,金 无气泡产生,金属
象 属逐渐溶解 属迅速溶解 无变化
【控制实验条件】打磨三种金属的目的是 ;
[来源:学科网]
【得出结论】原假设中正确的是 (填假设中a、b或c)。写出铬(铬与盐酸反应后显+2价)与盐酸反应
的化学方程式 。
【结论应用】根据探究结果,在CuCl 和AlCl 的混合液中加入一定量的金属铬,充分反应后过滤.向滤出的固
2 3
体中加入盐酸,无明显现象,则滤液中一定有的物质是 。
【答案】 【提出假设】Al﹥Cu﹥Cr; 【控制实验条件】除去金属表面的其他物; 【得出结论】a;
Cr+2HCl=CrCl +H ↑; 【结论应用】CrCl 、AlCl
2 2 2 3
【解析】:三种金属的活动性顺序提出三种可能的假设:a.Al>Cr>Cu ;b.Cr>Al>Cu;c.Al﹥ Cu﹥Cr ;打磨三种
金属的目的是除去金属表面的其他物;原假设中正确的是a,因为铝和酸反应的速度最快,其次是铬。铬
(铬与盐酸反应后显+2价)与盐酸反应的化学方程式Cr + 2HCl= CrCl + H ↑;根据探究结果,在CuCl 和
2 2 2
AlCl 的混合液中加入一定量的金属铬,充分反应后过滤.向滤出的固体中加入盐酸,无明显现象,说明
3
固体中没有铬,铬和氯化铜发生了反应,则滤液中一定有的物质是CrCl ;AlCl ,可能含有氯化铜溶液。
2 3
学&科*网
3中考面对面(50分)
(1—8小题每小题4分,共50分)
1.【2016年辽宁省锦州市】下列不是合金的是( )
A.生铁 B.铁锈C.青铜 D.焊锡
【答案】B
【解析】A、生铁是铁碳合金;B、氧化铁是氧化物,属于纯净物,不属于合金;C、青铜是铜锡合金;D、焊锡是合
金;故选B。
2.【2016年福建省漳州市】下列情况中,铁钉容易生锈的是( )
A.在干燥的空气中 B.浸没在蒸馏水中
C.部分浸入食盐水中 D.浸没在植物油中
【答案】C
【解析】A.在干燥的空气中,铁不与水接触,不易生锈,错误;B.浸没在蒸馏水中,铁不与氧气接触,不易生锈,
错误;C.铁钉浸泡在食盐水中,铁与水和氧气充分接触,容易生锈;且食盐水能促进铁生锈的速率,最易生锈,
正确;D.铁钉浸泡在植物油中,铁钉与氧气和水隔绝,不容易生锈,错误
3.【2016年云南省昆明市】消除铁制品表面的锈可用( )
A.水 B.稀盐酸 C.洗涤剂 D.食盐水
【答案】B
【解析】铁锈的成分是氧化铁,可以与盐酸反应,故可以用稀盐酸除去,故选B。
4.【2016年广西省贺州市】下列有关说法正确的是( )
A.铁在潮湿的环境中比在干燥的环境中更容易生锈
B.铝制品不用涂任何保层来防腐,因为铝不与空气反应
C.镁在氧气中燃烧,发出耀眼白光,生成黑色固体
D.我国的矿物储量比较丰富,所以废旧金属直接扔掉,没有必要回收
【答案】A
5.【2016年甘肃省天水市】将一定质量金属X的粉末放入盛有Fe(NO )溶液的烧杯中,充分反映后溶液呈
3 2
无色;继续向烧杯中加入一定量的AgNO 溶液,待充分反应后过滤,得浅绿色滤液和滤渣。根据实验分析,
3
以下结论错误的是( )
A.金属活动性顺序:X>Fe>Ag B.滤液中一定含有X的阳离子和Fe2+
C.滤渣中一定含有Ag和Fe D.向滤液中滴加稀盐酸,可能产生白色沉淀
【答案】C
46、【2016年贵州省黔东南州】在Cu(NO ) 、AgNO 混合溶液中加入一定量的铁粉,充分反应后过滤,向滤渣中
3 2 3
滴加稀硫酸时无气泡产生,下列说法正确的是( )
A.滤渣中一定有Ag和Cu B.滤渣中一定有Ag
C.滤液中一定有Cu(NO ) D.滤液中一定没有AgNO
3 2 3
【答案】B
【解析】由金属的活动性强弱是:铁>铜>银,在Cu(NO )、AgNO 混合溶液中加入一定量的铁粉,铁先与硝
3 2 3
酸银反应生成硝酸亚铁和银,当硝酸银完全反应后,铁能与硝酸铜反应生成硝酸亚铁和铜,充分反应后过
滤,向滤出的固体中滴加稀硫酸,没有气泡产生,说明无铁剩余,则一定能置换出银,可能含有铜,溶液中
可能含有Cu(NO )、AgNO.A、滤渣中一定有Ag,可能有Cu,故A错误;B、滤渣中一定有Ag,故B正确;
3 2 3
C、滤液中可能有Cu(NO ),故C错误;D、滤液中可能有AgNO,故D错误。
3 2 3
7、【2016年湖南省衡阳市】将适量的铜粉和镁粉的混合物放入一定量的硝酸银溶液中,充分反应后过滤,得
到固体物质和无色滤液,则关于滤出的固体和无色滤液的下列判断正确的是( )
A.滤出的固体中一定含有银和铜,一定不含镁
B.滤出的固体中一定含有银,可能含有铜和镁
C.滤液中一定含有硝酸银和硝酸镁,一定没有硝酸铜
D.滤液中一定含有硝酸镁,一定没有硝酸银和硝酸铜
【答案】D
【解析】由金属活动性顺序的应用及题意可知,充分反应后溶液为无色,此现象可说明铜和硝酸银没有发生反
应,因为镁活动性大于铜,可知硝酸银只与镁发生反应,镁可能刚好完全反应,也可能镁过量,则滤出的
固体中一定含银、铜,可能含有镁,而滤液中一定含硝酸镁,一定没有硝酸铜、硝酸银.综合以上分析可
知:A、滤出的固体中一定含有银、铜,可能含镁,故A错误;B、滤出的固体中一定含有银、铜,可能含镁,
故B错误;C、滤液中一定含有硝酸镁,一定没有硝酸铜,故C错误;D、滤液中一定含有硝酸镁,一定没有
硝酸银和硝酸铜,故D正确。故选:D。
8、【2016年内蒙古包头市】向一定质量的AgNO 和Fe(NO )的混合溶液中加入m克Zn粉,充分反应后过
3 3 2
滤,将滤渣洗涤、干燥后称量,得到的固体质量为m克.据此,下列说法不正确的是( )
A.滤渣中的物质至少有两种 B.取反应后的滤液滴加稀盐酸,有白色沉淀产生
C.物滤渣滴加稀盐酸,一定有气泡产生 D.取反应后的滤液观察,滤液可能呈浅绿色
5【答案】B
9.【2016年宁夏省】M是生活中常见的金属,MSO 溶液是无色液体,某化学兴趣小组的同学欲探究M与铜、
4
铝的活动性顺序,请你和他们一起进行以下探究活动.
【提出问题】M、铜、铝的金属活动性顺序是怎样的?
【猜想与假设】小敏的猜想是Al>Cu>M;小强的猜想是Al>M>Cu;你的猜想是 。
【设计与实验一】小莉取M丝、铜丝、铝丝和编号为①、②、③的3支试管,进行如表的实验(试管中均盛
有体积相同、溶质质量分数也相同的稀盐酸);
M丝插入试管① 钢丝插入试管② 铝丝插入试管③
实验操作 实验结论
中 中 中
刚开始的现象 有少量气泡产生 无气泡 无气泡 M>Cu:
几分钟后的现象 有少量气泡产生 无气泡 有大量气泡产生
【交流与表达】同学们对同一实验得出两种不同结论的现象进行了讨论,明白了实验刚开始时试管③中
无气泡产生的原因,该原因是 。
【设计与实验二】为了进一步探究三种金属的活动性顺序,同学们取粗细相同,打磨干净的M丝、铝丝及
相关溶液,又进行了如图所示的实验:
(1)试管乙中观察到的现象是 。 (2)试管丙中反应的化学方程式为 。
6【交流与表达】同学们经讨论后认为该实验可以优化,去掉试管 (填试管编号)中的实验,也可以得
出正确的结论。
【解释与结论】通过以上实验,同学们得出了三种金属的活动性顺序。
【评价与反思】实验结束后,同学们对实验过程进行了如下反思:
(1)影响金属与酸反应速率快慢的因素,除了相互反应的金属和酸的性质外,还有 (任写一种)
(2)探究金属活动性顺序时,除了上述实验中已经用到的两种方法外,还可以根据 进行判断(任写一
种)
【答案】M>Al>Cu;M>Al;Al>M>Cu;铝表面有一层氧化膜;(1)M表面出现一层红色物质;(2)
2Al+3CuSO=Al(SO )+3Cu;丙;【评价与反思】(1)反应物接触面积、温度等;(2)与氧气反应的剧
4 2 4 3
烈程度
以试管乙中观察到的现象是:M表面出现一层红色物质;(2)铝和硫酸铜反应生成硫酸铝和铜,化学方程式
为:2Al+3CuSO=Al(SO )+3Cu;【交流与表达】甲实验可以验证铝比M活泼,乙实验可以证明M比铜活泼,
4 2 4 3
所以三种金属的活动性顺序是Al>M>Cu,所以去掉试管丙中的实验,也可以得出正确的结论;【评价与反
思】(1)影响金属与酸反应速率快慢的因素,除了相互反应的金属和酸的性质外,还有反应物接触面积、温度
等;(2)金属会与酸、盐、氧气等物质反应,所以除了上述实验中已经用到的两种方法外,还可以根据与氧气
反应的剧烈程度进行判断。
10.【2016年黑龙江省齐齐哈尔市】铁是目前世界年产量最多的金属
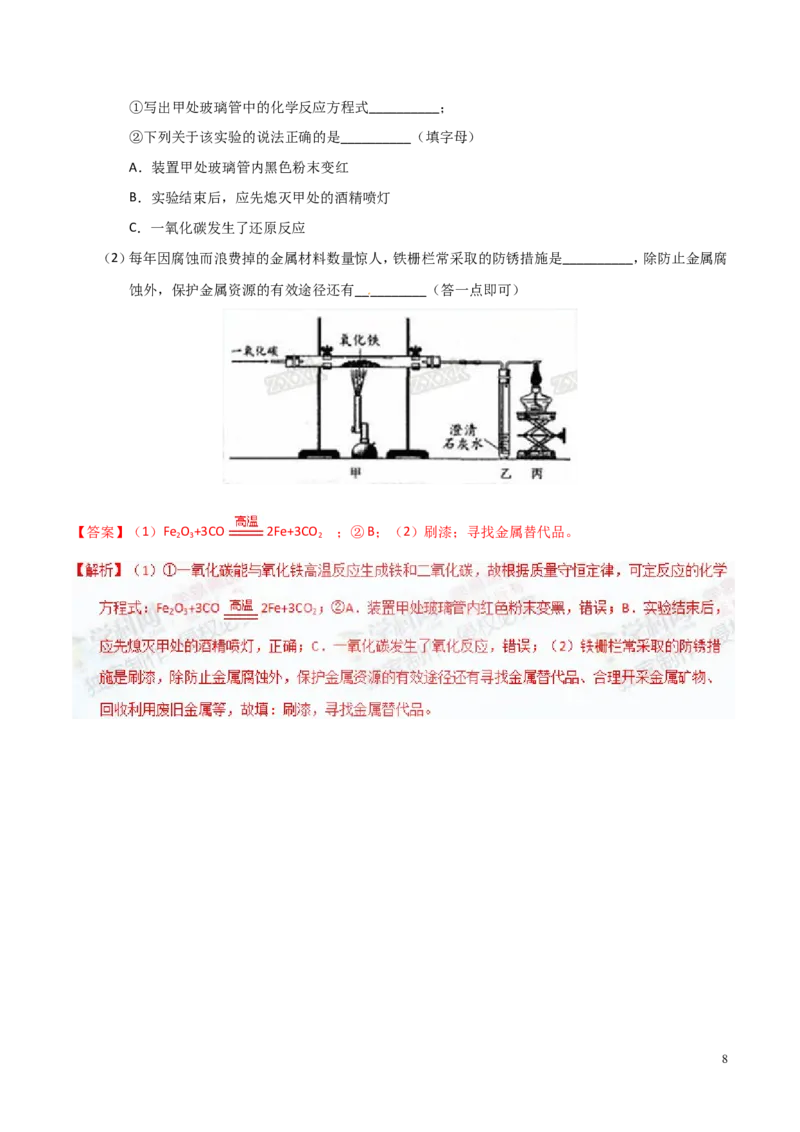
(1)如图是一氧化碳还原氧化铁实验装置图,回答下列问题:
7①写出甲处玻璃管中的化学反应方程式__________;
②下列关于该实验的说法正确的是__________(填字母)
A.装置甲处玻璃管内黑色粉末变红
B.实验结束后,应先熄灭甲处的酒精喷灯
C.一氧化碳发生了还原反应
(2)每年因腐蚀而浪费掉的金属材料数量惊人,铁栅栏常采取的防锈措施是__________,除防止金属腐
蚀外,保护金属资源的有效途径还有__________(答一点即可)
【答案】(1)Fe O +3CO 2Fe+3CO ;②B;(2)刷漆;寻找金属替代品。
2 3 2
8