文档内容
备战2017年中考二轮讲练测
专题 11 金属及金属材料(讲案)
☆ 考点梳理 ☆
一、金属材料
(一)、纯金属材料:纯金属(90多种)
黑色金属:通常指铁、锰、铬及它们的合金。
纯金属
有色金属:通常是指除黑色金属以外的其他金属。
(二)、合金(几千种):由一种金属跟其他一种或几种金属(或金属与非金属)一起熔合而成的具有金属特
性的物质。
1、合金的优点:一般说来,合金的熔点比各成分低,硬度比各成分大,抗腐蚀性能更好。
2、常见的合金:
(1)铁的合金:①生铁:含碳量2%~4.3% ②钢:含碳量0.03%~2%③不锈钢:含铬、镍的钢具有抗腐蚀
性能
(2)铜的合金:①黄铜(铜锌)②青铜(铜锡)
(3)钛的合金:如钛镍合金。具有“记忆”能力,可记住某个特定温度下的形状,只要复回这个温度,就会
恢复到这个温度下的形状,又被称为“记忆金属”。此外,钛还可制取超导材料,美国生产的超导材
料中的90%是用钛铌合金制造的。
(4)焊锡(铅锡):熔点低,广泛应用于电子工业、家电制造业、汽车制造业、维修业和日常生活中。
3:合金的优点:(1)熔点高、密度小;(2)可塑性好、易于加工、机械性能好;(3)抗腐蚀性能好;
注意:
1、钛和钛合金:被认为是21世纪的重要金属材料,钛合金与人体有很好的“相容性”,因此可用来制造
人造骨等。
2、青铜是人类历史上使用最早的合金;生铁和钢是人类利用最广泛的合金.
3、合金都属于混合物。
二、金属的物理性质:
1、金属的物理性质:①常温下一般为固态(汞为液态),有金属光泽;②大多数呈银白色(铜为紫红色,金
为黄色);③密度和硬度较大,熔、沸点高;④有良好的导热性、导电性、延展性。
12、金属之最:①铝:地壳中含量最多的金属元素;②钙:人体中含量最多的金属元素;③铁:目前世界年产
量最多的金属(铁>铝>铜);④银:导电、导热性最好的金属(银>铜>铝);⑤铬:硬度最高的金属;⑥钨:
熔点最高的金属;⑦汞:熔点最低的金属 ;⑧锇:密度最大的金属;⑨锂:密度最小的金属。
注意:
1、有些金属处于粉末状态时,就会呈现不同的颜色;例如,粉末状的铁粉都是呈黑色的,这主要是由于颗
粒太小,光不容易反射。
2、生活中使用的铁制品表面一般有镀金层或油漆,不是其真正颜色。可观察其断面的颜色。
三、金属的化学性质
(一)、大多数金属可与氧气的反应,生成金属氧化物;
1.铁与氧气的反应:常温下,干燥的空气中铁很难与氧气反应.在潮湿的空气中,铁与氧气发生缓慢氧化
而生成铁锈(主要成分:Fe O);在纯氧中,铁丝能够被点燃,剧烈燃烧,火星四射,生成黑色固体,放出
2 3
大量的热,生成四氧化三铁(Fe O)。
3 4
2.镁与氧气的反应:镁条被点燃后,剧烈燃烧,产生耀眼的白光,形成白烟,放出大量的热;生成白色的氧
化镁(MgO)。
3.铝与氧气的反应:铝在空气容易形成致密的氧化物,故其抗腐蚀性能很好.铝箔在纯氧中能够剧烈燃
烧,生成白色的氧化铝(Al O)。
2 3
4.铜与氧气的反应:在加热的情况下,铜能与氧气反应,生成黑色的物质(氧化铜);
(二)、活泼金属与酸的反应:
活泼金属会与酸发生置换反应生成盐和氢气,金属 + 酸 → 盐 + H ↑(置换反应)。如:
2
①锌和稀硫酸Zn+H SO ==ZnSO +H ↑
2 4 4 2
②铁和稀盐酸Fe+2HCl==FeCl +H ↑
2 2
(三)、金属与盐溶液的反应
排在前面的金属能把排在后面的金属从它的盐溶液中置换出来。反应规律:金属 + 盐 → 另一金属 +
另一盐。(置换反应)如:
Fe + CuSO == Cu + FeSO (“湿法冶金”原理)
4 4
注意:
1、金即使在高温时也不与氧气反应;
2、大多数金属一般都能与氧气反应,只是难易及剧烈程度不同而已。
3、同种物质,在不同的反应条件下,现象可能不同,生成物有可能不同.
4、单质铁与酸发生置换反应时生成亚铁盐;
四、常见金属活动性顺序:
[来源:Zxxk.Com]
21、常见金属的活动性顺序:
K Ca Na Mg Al Zn Fe Sn Pb(H)Cu Hg Ag Pt Au
金属活动性由强逐渐减弱
2、意义:①H代表酸中的氢元素;②金属的位置越靠前,它的活动性就越强;③在金属活动性顺序里,位
于氢前面的金属能置换出盐酸、稀硫酸中的氢(不可用浓硫酸、硝酸);④位于前面的金属能把位于后
面的金属从它们的盐溶液中置换出来。(除K、Ca、Na)
3、应用:①用于判断金属是否与酸发生置换反应;②用于判断金属与酸发生化学反应的剧烈程度;③用
于判断金属与盐能否发生置换反应。
注意:
1、金属与盐的反应必须在“盐溶液”中进行,否则不能反应,如:Cu可以与AgNO 溶液反应置换出Ag,
3
但不能与AgCl反应。
2、也可根据反应是否发生及反应剧烈程度来判断金属的活动性强弱。
3、K、Ca、Na 三种金属的活动性太强,除与酸反应外,还能与水在常温下发生置换反应(如
2Na+2HO=2NaOH+H ↑),其余金属则不能。
2 2 [来源:Z。xx。k.Com]
五、铁的冶炼
1、炼铁的基本原理是:在高温条件下,利用焦炭与氧气反应生成的一氧化碳把铁从铁矿石里还原出来。
3CO + Fe O 高温 2Fe + 3CO
2 3 2
2、炼铁的原料:铁矿石[常见的铁矿石有磁铁矿(主要成分是Fe O)和赤铁矿(主要成分是Fe O)]、焦
3 4 2 3
炭、石灰石和空气,主要设备是高炉。
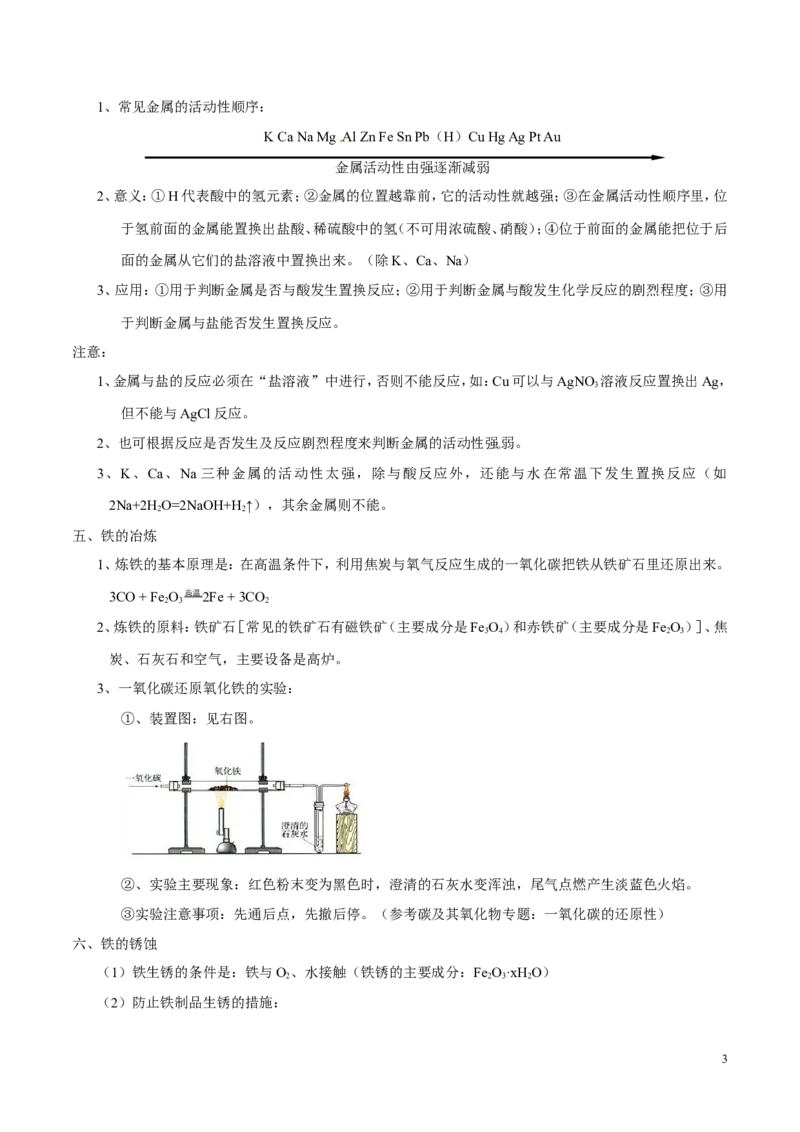
3、一氧化碳还原氧化铁的实验:
①、装置图:见右图。
②、实验主要现象:红色粉末变为黑色时,澄清的石灰水变浑浊,尾气点燃产生淡蓝色火焰。
③实验注意事项:先通后点,先撤后停。(参考碳及其氧化物专题:一氧化碳的还原性)
六、铁的锈蚀
(1)铁生锈的条件是:铁与O、水接触(铁锈的主要成分:Fe O·xH O)
2 2 3 2
(2)防止铁制品生锈的措施:
3①保持铁制品表面的清洁、干燥
②表面涂保护膜:如涂油、刷漆、电镀、烤蓝等
③制成不锈钢
(3)铁锈很疏松,不能阻碍里层的铁继续与氧气、水蒸气反应,因此铁制品可以全部被锈蚀。因而铁锈应
及时除去。
(4)铝与氧气反应生成致密的氧化铝薄膜,从而阻止铝进一步氧化,因此,铝具有很好的抗腐蚀性能。
注意:
1、铜生铜绿的条件:铜与O、水、CO 接触。铜绿的化学式:Cu (OH) CO)。
2 2 2 2 3
2、镁、铝、锌等金属活动性较强。
七、金属资源的保护和利用
1、金属资源的保护:①防止金属腐蚀;②回收利用废旧金属;③合理开采矿物;④寻找金属的代用。
2、金属回收再利用的意义:①防止污染环境;②节约能源;③节约资源。
☆ 考点典析 ☆
【题型一】 金属及金属材料性质和用途
【2017届黑龙江省哈尔滨三中九年级上11月月考】金属是人类生活和生产中的重要材料,下列图示所体现金
属的用途与金属材料不相匹配的是( )
【题型二】炼铁的原理
工业上将赤铁矿炼成铁是一个复杂的过程,炼铁高炉中发生的主要反应有( )
①C+O 点燃 CO ②Fe O+3H 高温 2Fe+2H O ③Fe O+3CO高温 2Fe+3CO
2 2 2 3 2 2 2 3 2
④2Fe O+3C高温 4Fe+3CO ↑ ⑤CO+C高温 2CO
2 3 2 2
A.②③⑤ B.①③⑤ C.①④⑤ D.②③
【解题方法】根据炼铁的原理进行分析和解答。
4【题型三】金属的化学性质
【2017届江苏省泰州中学附中九年级12月月考】将某稀硫酸分为等体积的两份,放入两个烧杯中,分别加入
等质量的甲、乙两种金属,反应后金属都没有剩余。产生H 的质量随时间变化的关系如图所示。下列说
2
法中错误的是
A.乙的活动性比甲强 B.甲的相对原子质量一定比乙小
C.反应消耗等质量的硫酸D.反应消耗等质量的金属
【解题方法】根据不同的金属与酸反应时的特点、图像的特点进行分析和解答。
【题型四】金属的锈蚀及防护及金属资源的保护
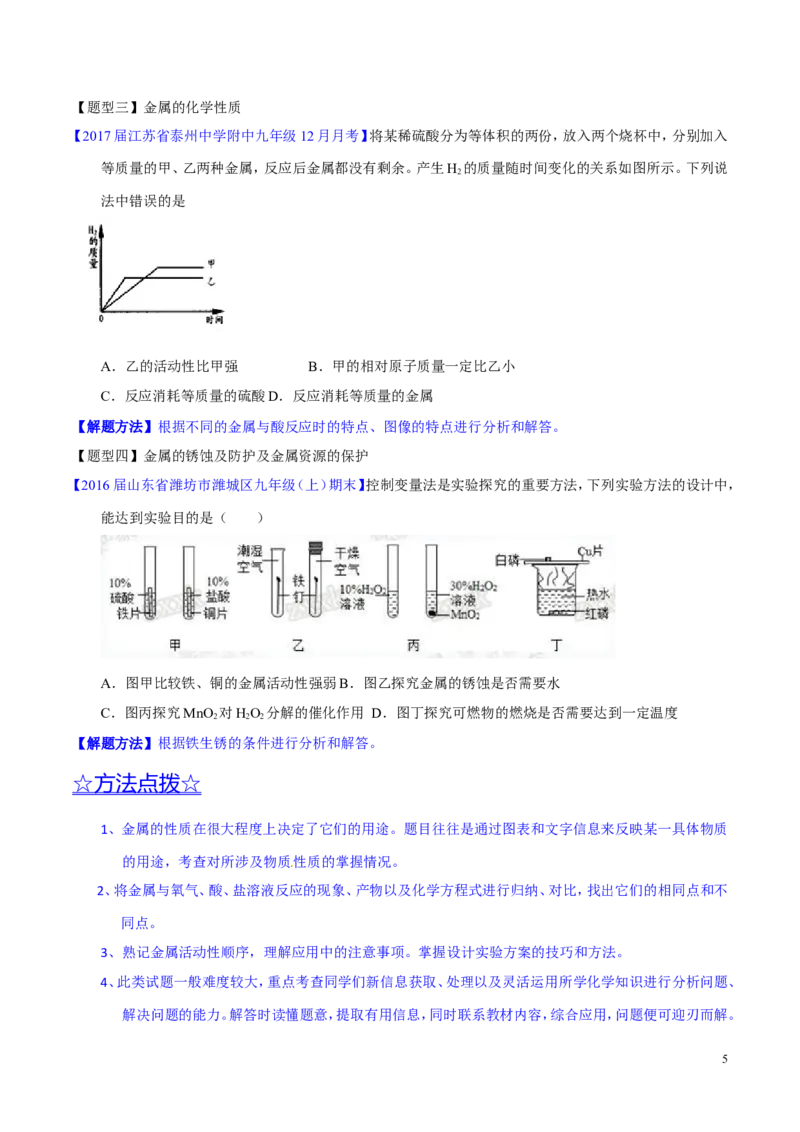
【2016届山东省潍坊市潍城区九年级(上)期末】控制变量法是实验探究的重要方法,下列实验方法的设计中,
能达到实验目的是( )
A.图甲比较铁、铜的金属活动性强弱B.图乙探究金属的锈蚀是否需要水
C.图丙探究MnO 对HO 分解的催化作用 D.图丁探究可燃物的燃烧是否需要达到一定温度
2 2 2
【解题方法】根据铁生锈的条件进行分析和解答。
☆ 方法点拨 ☆
1、金属的性质在很大程度上决定了它们的用途。题目往往是通过图表和文字信息来反映某一具体物质
的用途,考查对所涉及物质性质的掌握情况。
2、将金属与氧气、酸、盐溶液反应的现象、产物以及化学方程式进行归纳、对比,找出它们的相同点和不
同点。
3、熟记金属活动性顺序,理解应用中的注意事项。掌握设计实验方案的技巧和方法。
[来源:学科网]
4、此类试题一般难度较大,重点考查同学们新信息获取、处理以及灵活运用所学化学知识进行分析问题、
解决问题的能力。解答时读懂题意,提取有用信息,同时联系教材内容,综合应用,问题便可迎刃而解。
5☆ 随堂 小练 ☆
[来源:学科网 ZXXK]
1.【2017届河北省秦皇岛市海港区九年级12月月考】下列关于金属的说法正确的是
A.人类使用金属铝的年代早于铜、铁
B.“真金不怕火炼”表明金(Au)在常温条件下也很难与氧气反应
C.不锈钢用于制作医疗器械 D.武德合金的熔点高,可用于制造保险丝
2.【2017届黑龙江省哈尔滨第六十九中学九年级上11月月考】下列有关说法错误的是( )
A.铜是人类最早利用的金属材料B.工业炼铁时加入石灰石是为了除去矿石中的二氧化硅
C.降低温度可以使不饱和溶液变为饱和溶液 D.18K黄金中金的含量已经达到75%
3.【2017届黑龙江省哈尔滨第六十九中学九年级上11月月考】下列关于资源、能源的叙述正确的是( )
A.回收利用废旧金属,虽不能减少对环境的污染,却可以节约金属资源
B.目前人类制得的纯金属只有80余种,合金却高达几千种
[来源:学科网]
C.我国矿物储量比较丰富,其中钨、钛、锡等储量居世界前列
D.金属资源只有金、银以单质的形式存在,其余都以化合物形式存在
4.【2017届辽宁省丹东十中九年级上学期第二次月考】下列物质的用途,所利用的性质与另外三种有根本区
别的是
A.铜丝用作导线 B.用冰块冷却饮料
C.用镁粉制作烟花或照明弹 D.干冰用于人工降雨
5.【2017届黑龙江省鸡西十九中九年级上学期期中考试】某金属放入稀硫酸中,不产生气泡,该金属可能是
( )
A.Mg B.Al C.Zn D.Ag
6.【2017届江苏省兴化市顾庄学区三校九年级上月考二】X、Y、Z为三种金属,已知①Y与稀硫酸不反应
②Y+2ZNO=Y(NO )+2Z ③X+HSO =XSO +H ↑,则三种金属的活动性顺序是
3 3 2 2 4 4 2
A.Y Z X B.Y X Z C.X Y Z D.X Z Y
7.【2017届黑龙江省鸡西十九中九年级上学期期中考试】现有X、Y、Z三种金属,将X、Y分别放入稀硫酸溶
液中,结果Y表面产生氢气,X无变化,另取X放入Z的盐溶液中,结果X表面有Z析出,则X、Y、Z三
种金属的活动顺序是 ( )
A.X>Y>Z B.Y>Z>X C.X>Z>Y D.Y>X>Z
6