文档内容
一轮复习:中考化学基本理论溶液
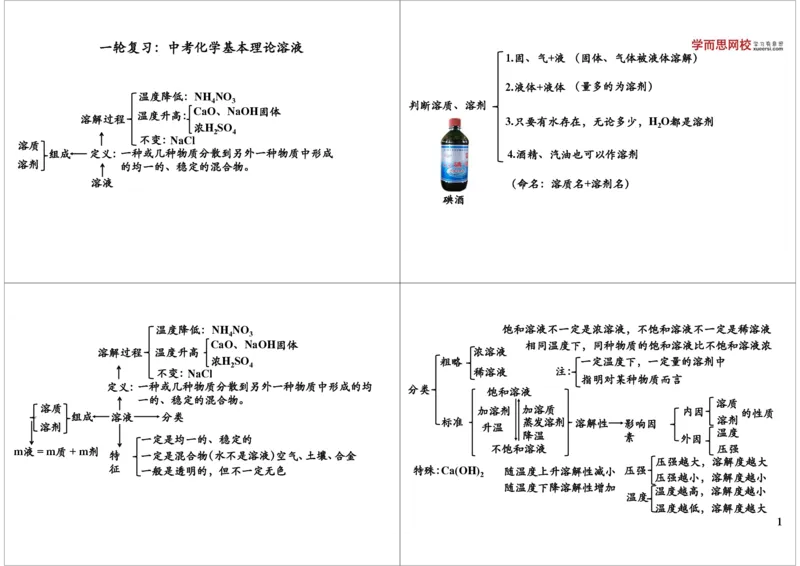
1.固、气+液 (固体、气体被液体溶解)
2.液体+液体 (量多的为溶剂)
温度降低:NH NO
4 3
判断溶质、溶剂
CaO、NaOH固体
温度升高:
溶解过程 3.只要有水存在,无论多少,H O都是溶剂
浓H SO 2
2 4
不变:NaCl
溶质
组成 定义:一种或几种物质分散到另外一种物质中形成 4.酒精、汽油也可以作溶剂
溶剂 的均一的、稳定的混合物。
溶液 (命名:溶质名+溶剂名)
碘酒
温度降低:NH NO 饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液
4 3
CaO、NaOH固体 相同温度下,同种物质的饱和溶液比不饱和溶液浓
溶解过程 温度升高 浓溶液
浓H SO 粗略 一定温度下,一定量的溶剂中
2 4
不变:NaCl 稀溶液 注:
指明对某种物质而言
定义:一种或几种物质分散到另外一种物质中形成的均
分类 饱和溶液
一的、稳定的混合物。
溶质
溶质 加溶剂 加溶质 内因 的性质
组成 溶液 分类
标准 蒸发溶剂 溶解性 影响因 溶剂
溶剂 升温
温度
一定是均一的、稳定的 降温 素 外因
m液= m质+ m剂 不饱和溶液 压强
特 一定是混合物(水不是溶液)空气、土壤、合金
压强越大,溶解度越大
征 一般是透明的,但不一定无色 特殊:Ca(OH) 随温度上升溶解性减小 压强
2 压强越小,溶解度越小
随温度下降溶解性增加
温度越高,溶解度越小
温度
温度越低,溶解度越大
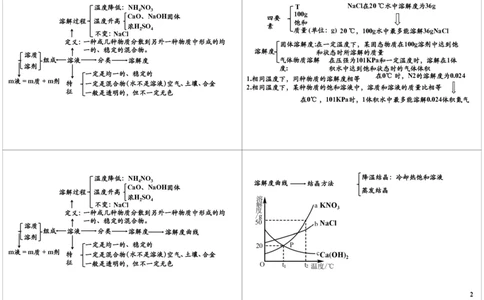
1温度降低:NH NO T NaCl在20℃水中溶解度为36g
4 3
100g
CaO、NaOH固体
四要
溶解过程 温度升高 饱和
浓H SO 素
2 4 质量(单位:g) 20℃,100g水中最多能溶解36gNaCl
不变:NaCl
定义:一种或几种物质分散到另外一种物质中形成的均
固体溶解度:在一定温度下,某固态物质在100g溶剂中达到饱
一的、稳定的混合物。 溶解度 和状态时所溶解的质量
溶质
组成 溶液 分类 溶解度 气体物质溶解 在压强为101KPa和一定温度时,溶解在1体
溶剂 度: 积水中达到饱和状态时的气体体积
一定是均一的、稳定的 在0℃时,N2的溶解度为0.024
m液= m质+ m剂
1.相同温度下,同种物质的溶解度相等
特 一定是混合物(水不是溶液)空气、土壤、合金
2.相同温度下,某种物质的饱和溶液中,溶质和溶液的质量比相等
征 一般是透明的,但不一定无色
在0℃,101KPa时,1体积水中最多能溶解0.024体积氮气
温度降低:NH NO 降温结晶:冷却热饱和溶液
4 3 溶解度曲线 结晶方法
CaO、NaOH固体
溶解过程 温度升高 蒸发结晶
浓H SO
2 4
不变:NaCl
定义:一种或几种物质分散到另外一种物质中形成的均
一的、稳定的混合物。
溶质
组成 溶液 分类 溶解度 溶解度曲线
溶剂
一定是均一的、稳定的
m液= m质+ m剂
特 一定是混合物(水不是溶液)空气、土壤、合金
征 一般是透明的,但不一定无色
2m溶质
温度降低:NH NO 溶质的质量分数= ×100%
4 3 m溶液
溶质的质量分数 CaO、NaOH固体
溶解过程 温度升高 =
m溶质
×100%
浓H 2 SO 4 m溶质+ m溶剂
溶液组成的表示方法 不变:NaCl
定义:一种或几种物质分散到另外一种物质中形成的均
一的、稳定的混合物。 饱和溶液变成不饱和溶液质量分数不一定减小
溶质
组成 溶液 分类 溶解度 溶解度曲线 不饱和溶液变成饱和溶液质量分数不一定增大
溶剂
相同温度下,同种物质的饱和溶液质量分数相等
一定是均一的、稳定的
m液= m质+ m剂
特 一定是混合物(水不是溶液)空气、土壤、合金
征 一般是透明的,但不一定无色
配制 温度降低:NH NO 步骤:计算、称量/量取、溶解 玻璃棒
4 3
用固体物质配制
溶质的质量分数 CaO、NaOH固体 仪器:托盘天平、药匙、量筒、胶头滴管、烧杯、
溶解过程 温度升高 配制
浓H SO 步骤:计算、量取、溶解
2 4
浓溶液稀释
溶液组成的表示方法 不变:NaCl
仪器:量筒、胶头滴管、烧杯、玻璃棒
定义:一种或几种物质分散到另外一种物质中形成的均
一的、稳定的混合物。 稀释前后溶质质量不变
溶质
组成 溶液 分类 溶解度 溶解度曲线 m浓 × ω浓 = m稀 ×ω稀
溶剂
一定是均一的、稳定的
m液= m质+ m剂
特 一定是混合物(水不是溶液)空气、土壤、合金
征 一般是透明的,但不一定无色
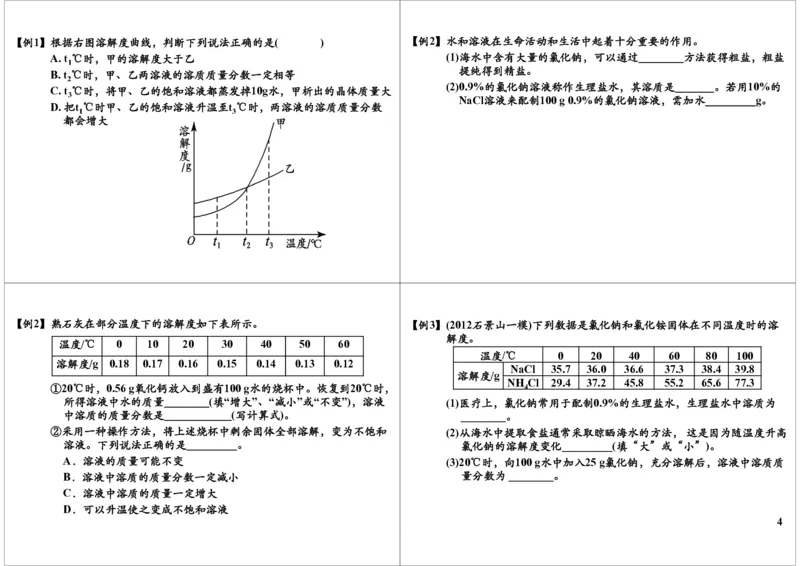
3【例1】根据右图溶解度曲线,判断下列说法正确的是( ) 【例2】水和溶液在生命活动和生活中起着十分重要的作用。
A. t ℃时,甲的溶解度大于乙 (1)海水中含有大量的氯化钠,可以通过________方法获得粗盐,粗盐
1
B. t ℃时,甲、乙两溶液的溶质质量分数一定相等 提纯得到精盐。
2
C. t ℃时,将甲、乙的饱和溶液都蒸发掉10g水,甲析出的晶体质量大
(2)0.9%的氯化钠溶液称作生理盐水,其溶质是_______。若用10%的
3
NaCl溶液来配制100 g 0.9%的氯化钠溶液,需加水_________g。
D. 把t ℃时甲、乙的饱和溶液升温至t ℃时,两溶液的溶质质量分数
1 3
都会增大
【例2】熟石灰在部分温度下的溶解度如下表所示。 【例3】(2012石景山一模)下列数据是氯化钠和氯化铵固体在不同温度时的溶
解度。
温度/℃ 0 10 20 30 40 50 60
温度/℃ 0 20 40 60 80 100
溶解度/g 0.18 0.17 0.16 0.15 0.14 0.13 0.12
NaCl 35.7 36.0 36.6 37.3 38.4 39.8
溶解度/g
NH Cl 29.4 37.2 45.8 55.2 65.6 77.3
①20℃时,0.56 g氧化钙放入到盛有100 g水的烧杯中。恢复到20℃时, 4
所得溶液中水的质量________(填“增大”、“减小”或“不变”),溶液 (1)医疗上,氯化钠常用于配制0.9%的生理盐水,生理盐水中溶质为
中溶质的质量分数是____________(写计算式)。 ________。
②采用一种操作方法,将上述烧杯中剩余固体全部溶解,变为不饱和 (2)从海水中提取食盐通常采取晾晒海水的方法,这是因为随温度升高
溶液。下列说法正确的是_________。 氯化钠的溶解度变化_________(填“大”或“小”)。
A.溶液的质量可能不变 (3)20℃时,向100 g水中加入25 g氯化钠,充分溶解后,溶液中溶质质
B.溶液中溶质的质量分数一定减小 量分数为________。
C.溶液中溶质的质量一定增大
D.可以升温使之变成不饱和溶液
4【例3】(4)现有200 g溶质质量分数为10%的氯化钠溶液,若使溶液的溶质质量 【例4】(2012西城一模)溶液的应用非常广泛。
分数增加一倍,应该蒸发掉______g水。 (1)K CO 和KNO 在不同温度时的溶解度及其溶解度曲线如下。
2 3 3
(5)30℃时,向两个分别盛有相同质量的氯化钠和氯化铵的烧杯中,各
温度/℃ 20 30 50 60 80
加入100 g水,充分溶解后,恢复至30℃,其结果如右图所示。有关
K CO 110 114 121 126 139
下列说法中,正确的是____(填字母序号)。 溶解度/g 2 3
KNO 31.6 45.8 85.5 110 169
3
A.烧杯②中溶液是不饱和溶液
①图中能表示KNO 溶解度曲线的是_____(填“甲”或“乙”)。
B.升高温度或增加溶剂都有可能将烧杯①中固体全部溶解 3
C.若将烧杯①中的溶液变为不饱和溶液,溶液中溶质质量分数一 ②曲线上M点的含义是________________________________。
定减小
D.将得到的烧杯②中溶液降温至0℃时,溶液中溶质质量分数一定
减小
【例4】③20℃时,K CO 饱和溶液中溶质与溶剂的质量比为______)结果用最 【例4】(2)某KNO 样品中含有少量K CO ,其提纯过程如下:
2 3 3 2 3
简整数比表示)。
④30 ℃时,向114 g K CO 固体中加入100 g水,充分溶解后升温至
2 3
40℃,该溶液中溶质的质量分数______(填“变大”、“变小”或
“不变”)。
小资料:K CO + Ca(NO ) = CaCO ↓+ 2KNO
2 3 3 2 3 3
①操作2的名称是________。
②溶液B和溶液C中属于饱和溶液的是_________(填序号)。
③样品中钾元素的质量为_______g(结果保留整数)。
5