文档内容
一轮复习:中考化学物质碳和碳的化合物
性质:无色透明、正八面体“、最硬”
单质
金刚石 用途:玻璃刀、钻头、钻石(装饰)
化
5-6万 结构:三维空间成骨架状
学
纯净物
2000℃ 变 性质:灰黑色、软、滑、导电性
化
碳单质
石墨 结构:原子呈层状排列
用途:铅笔、润滑剂、电极、石墨炸弹等
碳
足球烯 由分子构成
C
60
用途:催化剂、超导体等
混合物 区别:原子排列不同
物理性质
单质
木炭:结构疏松多孔,具有吸附性,可用作冰箱除味剂
纯净物
黑火药:S、C、KNO3
点燃
S + 2KNO3+ 3C== K2S + N2 + 3CO2
无定形碳
活性炭:结构疏松多孔,具有很强吸附性,用作防毒面具
(混合物)
碳 焦炭:“冶金”
炭黑:制作墨汁、油漆、鞋油,增强轮胎的耐磨力
混合物 无定形碳
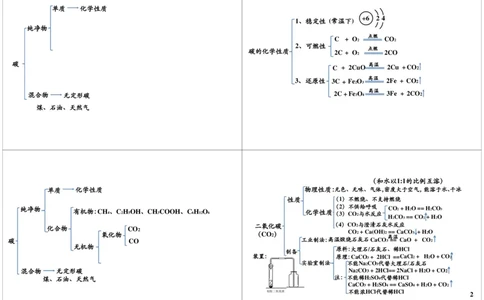
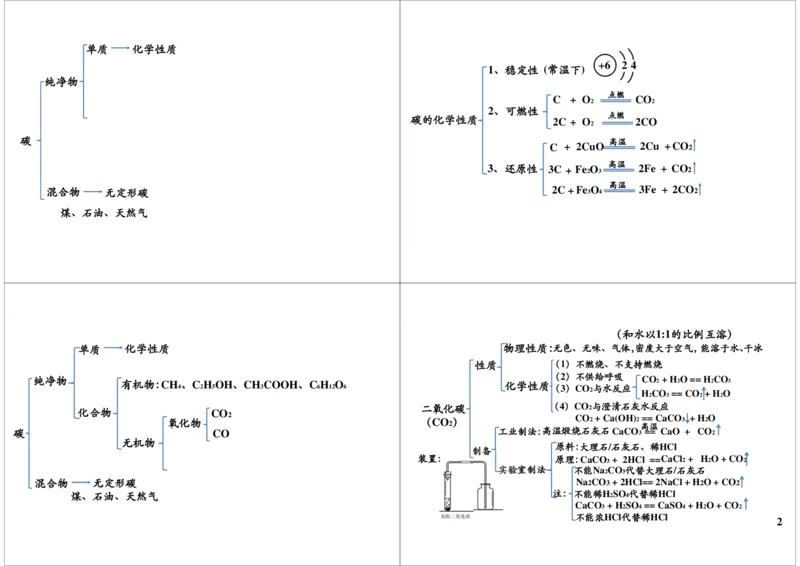
1单质 化学性质
+6 2 4
1、稳定性 (常温下)
纯净物
点燃
C + O CO
2 2
2、可燃性
点燃
碳的化学性质 2C + O 2CO
2
碳 C + 2CuO 高温 2Cu +CO 2
3、还原性 3C + Fe 2 O 3 高温 2Fe + CO 2
混合物 无定形碳 2C+Fe 3 O 4 高温 3Fe + 2CO 2
煤、石油、天然气
(和水以1:1的比例互溶)
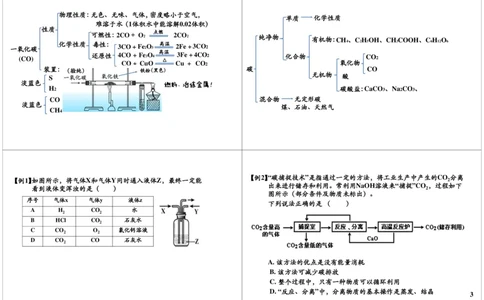
单质 化学性质 物理性质:无色、无味、气体,密度大于空气,能溶于水、干冰
性质 (1)不燃烧、不支持燃烧
纯净物 有机物:CH 4 、C 2 H 5 OH、CH 3 COOH、C 6 H 12 O 6 化学性质 ( ( 2 3 ) ) 不 CO 供 2与 给 水 呼 反 吸 应
H
CO
C
2
O
+ H
==
2 O
C
=
O
= H
+
2
H
CO
O
3
2 3 2 2
二氧化碳 (4)CO 2与澄清石灰水反应
化合物 CO
2 CO + Ca(OH) == CaCO + H O
氧化物 (CO 2) 2 2 3 2
高温
碳 CO 工业制法:高温煅烧石灰石CaCO 3 == CaO + CO 2
无机物
原料:大理石/石灰石、稀HCl
制备
装置: 原理:CaCO 3 + 2HCl ==CaCl 2 + H 2 O + CO 2
实验室制法 不能Na 2 CO 3代替大理石/石灰石
混合物 无定形碳 Na2CO3+ 2HCl== 2NaCl+ H2O + CO2
煤、石油、天然气 注:不能稀H 2 SO 4代替稀HCl
CaCO + H SO == CaSO + H O + CO
3 2 4 4 2 2
不能浓HCl代替稀HCl
2物理性质:无色、无味、气体,密度略小于空气,
单质 化学性质
难溶于水(1体积水中能溶解0.02体积)
性质
点燃
可燃性:2CO+ O 2CO
2 2 纯净物
有机物:CH 、C H OH、CH COOH、C H O
4 2 5 3 6 12 6
一氧化碳 化学性质 毒性: 3CO+Fe 2 O 3 高温 2Fe +3CO 2
(CO) 还原性 4CO + Fe 3 O 4 高温 3Fe +4CO 2 化合物 CO 2
CO + CuO Cu + CO 氧化物
2
装置:(验纯) 铁粉(黑色) 碳 CO
S 无机物 酸
淡蓝色 燃料、冶炼金属!
H 2 碳酸盐:CaCO 3、Na 2 CO 3、
CO 混合物 无定形碳
淡蓝色
煤、石油、天然气
CH
4
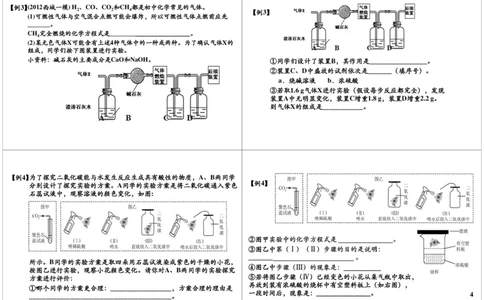
【例2】“碳捕捉技术”是指通过一定的方法,将工业生产中产生的CO 分离
【例1】如图所示,将气体X和气体Y同时通入液体Z,最终一定能 2
出来进行储存和利用。常利用NaOH溶液来“捕捉”CO ,过程如下
看到液体变浑浊的是( ) 2
图所示(部分条件及物质未标出)。
序号 气体x 气体y 液体z
下列说法正确的是( )
A H CO 水
2 2
B HCl CO 石灰水
2
C CO O 氯化钙溶液
2 2
D CO CO 石灰水
2
A. 该方法的优点是没有能量消耗
B. 该方法可减少碳排放
C. 整个过程中,只有一种物质可以循环利用
D. “反应、分离”中,分离物质的基本操作是蒸发、结晶
3【例3】(2012西城一模) H 、CO、CO 和CH 都是初中化学常见的气体。
2 2 4 【例3】 气体 后续
(1)可燃性气体与空气混合点燃可能会爆炸,所以可燃性气体点燃前应先 气体X 燃烧 装置
装置
_______。
碱石灰
CH 完全燃烧的化学方程式是_________________________。
4
澄清石灰水
(2)某无色气体X可能含有上述4种气体中的一种或两种。为了确认气体X的
组成,同学们按下图装置进行实验。 A B C D
小资料:碱石灰的主要成分是CaO和NaOH。 ①同学们设计了装置B,其作用是_________________。
气体X 气 燃 体 烧 后 装 续 置 ②装置C、D中盛放的试剂依次是_______(填序号)。
装置
a.烧碱溶液 b.浓硫酸
碱石灰
③若取1.6 g气体X进行实验(假设每步反应都完全),发现
澄清石灰水
装置A中无明显变化,装置C增重1.8 g,装置D增重2.2 g。
A B C D 则气体X的组成是____________。
【例4】为了探究二氧化碳能与水发生反应生成具有酸性的物质,A、B两同学
分别设计了探究实验的方案。A同学的实验方案是将二氧化碳通入紫色
【例4】
石蕊试液中,观察溶液的颜色变化,如图:
②图甲实验中的化学方程式是________________。
③图乙中第(Ⅰ)(Ⅱ)步骤的目的是说明:
_______________________________。
所示。B同学的实验方案是取四朵用石蕊试液染成紫色的干燥的小花,
④图乙中步骤(Ⅲ)的现象是:___________
按图乙进行实验,观察小花颜色变化。请你对A、B两同学的实验探究
方案进行评价:
⑤若将图乙步骤(Ⅳ)已经变色的小花从集气瓶中取出,
再放到装有浓硫酸的烧杯中有空塑料板上(如右图),
①哪个同学的方案更合理:__________________,方案合理的理由是
一段时间后,现象是:________________。 4
__________________________________________。【例5】三位同学用下图所示装置做一氧化碳还原氧化铁的实验.当观察到玻
【例5】小光通过查询有关资料得知:
璃管A中的粉末由红棕色逐渐变为黑色时,停止加热,继续通一氧化
(1)一氧化碳与氧化铁在加热条件下,可发生如下反应:
碳,冷却到室温,停止通气,同时观察到 3Fe O +CO 高温2Fe O +CO
2 3 3 4 2
澄清的石灰水变浑浊. (2)四氧化三铁(Fe O )为黑色固体,有强磁性,能够被磁
3 4
铁吸引.
因此,小光认为小明和小红的结论都不能成立,你是否同意
他的说法?______________请具体说明你的理由:
_______________________________________________________
_______________________________________________________
用一氧化碳还原氧化铁的实验装置 _____________________________________________
小明认为:依据上述实验现象
可以判断出生成的黑色固体为金属铁.
小红认为:仅从上述实验现象,不足以证明生成的黑色固体为金
属铁,她增加了一个实验:用磁铁靠近生成的黑色固体,看到有黑色
固体被磁铁吸引.于是得出生成的黑色固体为金属铁的结论。
【例5】(3)小光欲通过实验检验生成的黑色固体是否含有金属铁.请你帮 【例6】CO 2 是初中化学重点研究的气体之一。某化学兴趣小组设计了如下
实验来探究CO 的制取和性质:
他设计实验并填写下表. 2
(1)该兴趣小组用干燥管、烧杯、铜网等设计装配了一个在实验
实验步骤 实验现象 实验结论
室中制取二氧化碳气体的装置,如右图所示。在干燥管内的铜网上
__________________ _____________________ _______________________
应盛放________________;
__________________ _____________________ _______________________
__________________ 若将铜网换成铁网,可能产生的后果是
_________________________________________________,其原因
(4)除上述方案,还可以采取另一种实验方案,所用的试剂是 是_________________________________________(用化学方程式
____________________ ,将该试剂与黑色固体混合,通过观察 表示)
______________________________,判断黑色固体中是否含金属铁.
5【例6】(2)实验表明,不能用块状大理石与稀硫酸制取CO 气体,而能
2
用大理石粉末与稀硫酸制取CO 气体。由此得出的合理结论是
2
( )
A.能发生反应的物质之间是否发生反应,与反应的条件有关
B.反应物之间接触面积越大,越有利于反应的进行
C.块状大理石与大理石粉末的化学性质不同
D.块状大理石与大理石粉末中各元素原子间电子的结合状况不同
6