文档内容
一轮复习:中考化学物质金属和金属材料(二)
【例1】下列有关图像正确的是( ) 【例2】向一定质量AgNO 和Cu(NO ) 的混合溶液中加入Zn,溶液
3 3 2
质量与加入Zn的质量关系如右图所示,下列说法正确的是( )
A.a点溶液中的溶质有2种
B.c点溶液中溶质为Zn(NO )
3 2
Zn C.若取b~c段溶液,滴加稀盐酸,有白色沉淀
D.取d点的固体,加入稀盐酸,无气泡产生
A .向一定质量的稀盐酸中加入镁粉至过量
B. 向两份完全相同的稀盐酸中分别加入锌粉、镁粉
C. 等质量的镁和铁分别与过量且完全相同的稀硫酸反应
D. 过量的镁、锌、铁与质量分数相同的盐酸反应
【例3】将一定量铝粉和氧化铜混合加热,反应的化学方程式为: 【例4】向一定量硫酸和硫酸铜的混合溶液中,逐滴加入一定质量
高温
3CuO+2Al == 3Cu+ Al O 。反应结束后,为了检验氧化铜是否完全 分数的氢氧化钠溶液,直至过量。某同学依据实验事实绘制了如图
2 3
反应,取少量反应后的固体,加入足量稀硫酸,充分反应后,将铁 所示的曲线。
片插入溶液中。下列叙述的现象中,能说明氧化铜没有完全反应的 下列说法正确的是( )
是( )
A.a至b段对应溶液的pH逐渐减小
A.加入稀硫酸后,有气泡生成
B.b点对应溶液中的溶质为硫酸钠
B.加入稀硫酸后,没有气泡生成
C.c点对应溶液中的溶质种类最少
C.加入稀硫酸后,溶液中有红色不溶物质
D.a至d段硫酸钠的质量逐渐增大
D.插入溶液中的铁片表面有红色物质出现
1【例5】现有两种金属单质组成的混合物。向100 g稀盐酸中加入该混合物, 【例6】将盛有等质量等质量分数的盐酸的烧杯放在托盘天平的两端,天平
加入混合物的质量与生成氢气的质量关系如右图所示。下列说法正确的是 平衡,将铝片放入左盘的的烧杯中将镁片放入右盘的烧杯中,充分反应后
( ) 盐酸有剩余,天平仍然平衡,则所加入的铝和镁的质量之比为( )
A.若混合物为Zn和Cu,则m大于0.2 g A. 33:32 B. 2:3 C. 3:4 D. 27:24
B.若混合物为Zn和Fe,则m可能是0.2 g
C.若混合物为Fe和Cu,稀盐酸中溶质质量分数为7.3%
D.若混合物为Fe和Cu,m为0.1 g,则混合物中Fe和Cu的质量比为1:1
【例7】金属在生产生活中起着重要的作用。 【例7】(4)向一定量的氧化铜中加入稀硫酸使其完全溶解,得到一种蓝
(1)铜可以做电线,利用了金属铜的延展性和______性。 色溶液。再加入铁粉充分反应,过滤,得到滤渣和滤液。向滤渣中加入足
量稀硫酸,有气泡冒出,充分反应后,剩余固体的质量为12.8 g。
(2)铝在空气中表现出良好的抗腐蚀性能,用化学方程式表示其原因
_________________________________。 ①氧化铜与稀硫酸反应的化学方程式是_________________________
(3)工业常用赤铁矿(主要成分是氧化铁)和一氧化碳冶炼铁,该反应 ②滤渣的成分是___________。
的化学方程式是_____________________________。 ③氧化铜的质量为_____g。
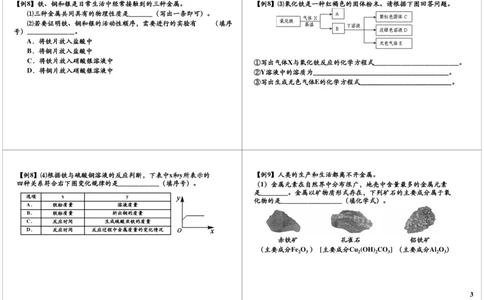
2【例8】铁、铜和银是日常生活中经常接触到的三种金属。 【例8】⑶氧化铁是一种红褐色的固体粉末。请根据下图回答问题。
⑴三种金属共同具有的物理性质是_______(写出一条即可)。
⑵若要证明铁、铜和银的活动性顺序,需要进行的实验有 (填序
号)______________。
A.将铁片放入盐酸中
B.将铜片放入盐酸中
C.将铁片放入硝酸银溶液中 ①写出气体X与氧化铁反应的化学方程式_________________________。
D.将铜片放入硝酸银溶液中 ②Y溶液中的溶质为________________________________________。
③写出生成无色气体E的化学方程式___________________________。
【例8】⑷根据铁与硫酸铜溶液的反应判断,下表中x和y所表示的 【例9】人类的生产和生活都离不开金属。
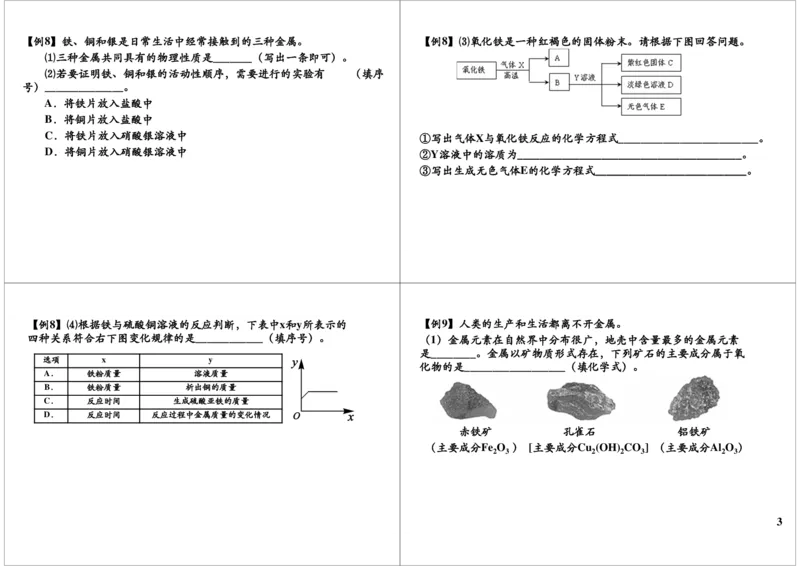
四种关系符合右下图变化规律的是____________(填序号)。 (1)金属元素在自然界中分布很广,地壳中含量最多的金属元素
是________。金属以矿物质形式存在,下列矿石的主要成分属于氧
选项 x y
化物的是__________________(填化学式)。
A. 铁粉质量 溶液质量
B. 铁粉质量 析出铜的质量
C. 反应时间 生成硫酸亚铁的质量
D. 反应时间 反应过程中金属质量的变化情况
赤铁矿 孔雀石 铝铁矿
(主要成分Fe O ) [主要成分Cu (OH) CO ] (主要成分Al O )
2 3 2 2 3 2 3
3【例9】 【例10】金属的应用非常广泛。
(2)铁是应用最广泛的金属。 (1)生活中常用铁锅炒菜,主要利用了铁的性质是(填序号)_____。
①工业常用赤铁矿和一氧化碳在高温条件下炼铁,该反应的化学方 A. 导热性 B. 导电性 C. 延展性 D. 有金属光泽
程式为____________________________。 (2)下列能与铁发生反应的是(填序号)_________。
②使用过的菜刀、铁锅等铁制品,清洗后需要及时擦干放置,可以 A. 氧气 B. 稀盐酸 C. 硫酸铜溶液 D. 氯化锌溶液
减少________对铁锈蚀的影响。
(3)工业上,常在高温下用一氧化碳把铁从铁矿石中还原出来。若用
磁铁矿(主要成分为四氧化三铁)冶炼铁,写出发生反应的化学方程
式_______________________________。一些铁制品容易生锈。铁制品
(3)将一定量的锌加入稀硫酸、硫酸亚铁和硫酸铜的混合溶液中,
充分反应后过滤,向滤渣中加入盐酸,有气泡产生。滤渣和滤液中 生锈的条件是___________________。
一定有的物质是_____________________。
【例10】(4)某同学在探究金属活动性时做了下列实验:将一条铝片伸入 【例11】金属材料在国防建设中起着重要的作用。
盛有硫酸铜溶液的试管中,开始时没有明显现象,一段时间后,铝片的表
面有气泡出现,且有红色固体生成。为了解释此“反常”现象,他查阅资
料得知:配制硫酸铜溶液时常加入少量稀硫酸。上述实验中共发生了_____
个反应,其中产生红色固体物质的化学反应方程式是
________________________________。
(5)若向铜和稀硫酸的混合物中滴加过氧化氢溶液,只观察到溶 (1)改装前的“辽宁舰”锈迹 图1 斑斑,钢铁锈蚀主要是铁与______作用的结
液颜色变蓝,发生反应的化学方程式为_______________________。 果。工业生产中常用稀盐酸除去铁制品表面的铁锈,该反应的化学方程式
为_________________________________。
4【例11】 【例11】某电镀厂排放的污水中含有CuSO 、ZnSO 、FeSO ,为
4 4 4
(2)为避免轮船的钢质外壳被腐蚀,通常 减少水污染及节约成本,回收重要物质硫酸锌及有关金属,设计如
下所示流程。
在轮船外壳上镶嵌比铁活动性强的金属。 加过量 Cu
小明为探究锌、铁、铜三种金属的活动性 固体A 乙溶液 固体D
操作② 加适量甲
顺序,设计了如图2所示的两个实验: 加过量甲
滤液C
操作③
某污水
操作① 滤液B
①实验1中,小明以“金属表面产生气泡的
滤液B ZnSO
快慢”为标准来判断锌、铁的活动性强弱, 蒸发 4 蒸发
有同学认为不合理,理由是__________。
该回收流程中:固体A的成分是_______________;含铁元素的物
②通过实验2,可证明铁的活动性比铜强,反应的化学方程式是
质(污水除外)有___________(填字母序号)。
____________________________________________。
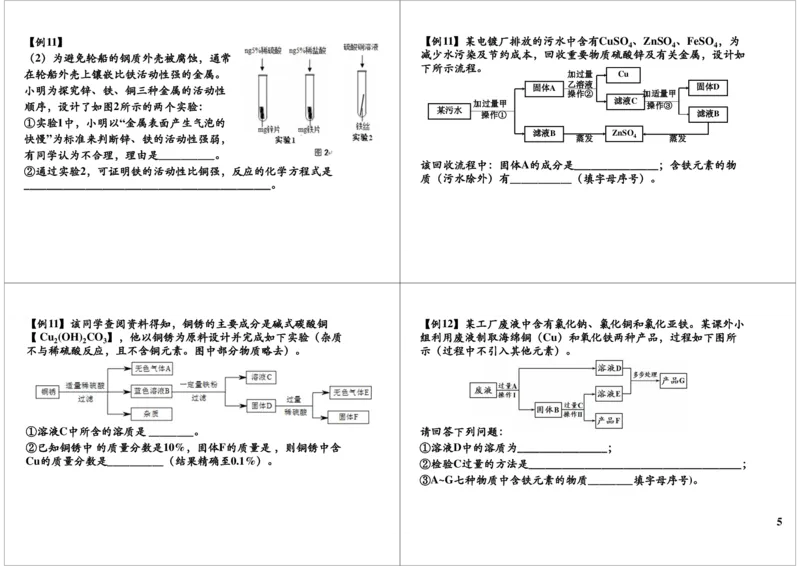
【例11】该同学查阅资料得知,铜锈的主要成分是碱式碳酸铜 【例12】某工厂废液中含有氯化钠、氯化铜和氯化亚铁。某课外小
【Cu (OH) CO 】,他以铜锈为原料设计并完成如下实验(杂质 组利用废液制取海绵铜(Cu)和氧化铁两种产品,过程如下图所
2 2 3
不与稀硫酸反应,且不含铜元素。图中部分物质略去)。 示(过程中不引入其他元素)。
①溶液C中所含的溶质是________。 请回答下列问题:
②已知铜锈中的质量分数是10%,固体F的质量是,则铜锈中含 ①溶液D中的溶质为________________;
Cu的质量分数是__________(结果精确至0.1%)。 ②检验C过量的方法是______________________________________;
③A~G七种物质中含铁元素的物质________填字母序号)。
5