文档内容
夯实双基
1.夏飞同学在化学课上提出,可用澄清石灰水来检验人呼出的气体是否含有二氧化碳气体,就这一过程而言,
属于科学探究环节中的( )
A.提出假设 B.收集证据 C.设计实验 D.做出结论
【答案】C
【解析】 “用澄清石灰水来检验人呼出的气体是否是二氧化碳气体”这是在设计用澄清的石灰水来验证是
否是二氧化碳,因此不属于建立假设、做出结论、收集证据环节,而属于设计实验.故选C.学科*网
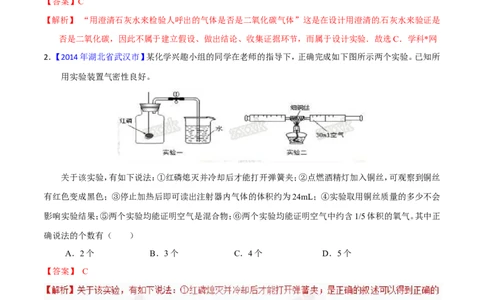
2.【2014年湖北省武汉市】某化学兴趣小组的同学在老师的指导下,正确完成如下图所示两个实验。已知所
用实验装置气密性良好。
关于该实验,有如下说法:①红磷熄灭并冷却后才能打开弹簧夹;②点燃酒精灯加入铜丝,可观察到铜丝
有红色变成黑色;③停止加热后即可读出注射器内气体的体积约为24mL;④实验取用铜丝质量的多少不会
影响实验结果;⑤两个实验均能证明空气是混合物;⑥两个实验均能证明空气中约含1/5体积的氧气。其中正
确说法的个数有( )
A.2个 B.3个 C.4个 D.5个
【答案】 C
3.【2016年河北省】用图10所示装置探究可燃物的燃烧条件a实验过程如下:①将白磷放在燃烧匙内,塞好
1胶塞 寒;②从长颈漏斗向瓶内迅速注入60~C的水至刚刚浸没白磷;③连接好注射器,向瓶内推入空气,
瓶内水面下降,当白磷露出水面时立即燃烧,停止推入空气:④白磷熄火后,瓶内水面上升,最后淹没白磷。
请同答下列问题:
(1)白磷燃烧的化学方程式为 。
(2)对比③中白磷露出水面前、后的现象,说明燃烧需要的条件是 。
(3)④中瓶内水面上升的原因 。
点燃
【答案】(1)4P+5O====== 2PO(2)氧气 (3)瓶内气体压强减小
2 2 5
【解析】(1)白磷燃烧生成五氧化二磷:4P+5O ====== 2P O ;(2)白磷露出水面后接触到了氧气,故说明燃烧
2 2 5
需要氧气;(3)白磷燃烧消耗氧气,导致集气瓶内的压强变小,故瓶内水面会上升。学科*网
4.【2016年山东省淄博市】 (1)我们的祖先很早就掌握了炼铜的工艺,通过学习,同学们知道木炭可以作还
原剂把氧化铜中的铜还原出来,小明查阅了大量的资料后,建议用超细炭粉与氧化铜粉末混合进行实验,他
的理由是 。
[来源:学,科,网Z,X,X,K]
(2)同学们按如图装置进行实验,当看到澄清的石灰水刚刚出现浑浊时, (填写“可以”或者“不
能”)确定氧化铜和炭粉已经开始反应。
[来源:学§科§网]
(3)为了使氧化铜中的铜完全被还原,对于下列三组氧化铜和炭粉的质量比例,你建议选择 (填写
字母),简要说明你的理由 。
A.36:3 B.40:3 C.48:3
【答案】(1)增大反应物的接触面积,使反应更充分 (2)不能 (3)C;反应中炭粉会与试管内的氧气反应而部
分消耗,故稍过量的炭粉有利于反应的进行
2故答案为:不能;(3)在选择氧化铜和碳的质量比例时要考虑到氧气消耗的炭,不能按反应的比例选择,碳粉
要稍多一些,有利于反应充分进行,2CuO+C 2Cu+CO ↑;
2 [来源:学科网]
160 12
即40:3,而碳粉稍微多一点,即在给定选项中选:C,所以选择的理由是:反应中炭粉会与试管内的氧气
反应而部分消耗,故稍过量的炭粉有利于反应的进行;故答案为:C;反应中炭粉会与试管内的氧气反应
而部分消耗,故稍过量的炭粉有利于反应的进行 学科*网
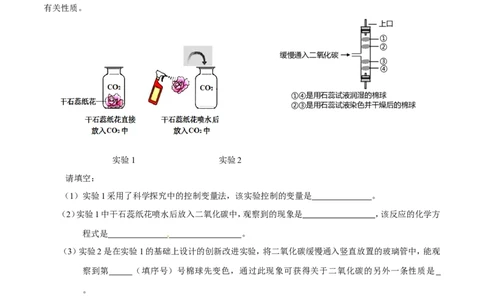
5.【2016年山东省青岛市】 实验是进行科学探究的重要方式。某同学设计如下图所示实验,探究二氧化碳的
有关性质。
上口
①
②
缓慢通入二氧化碳
③
④
①④是用石蕊试液润湿的棉球
②③是用石蕊试液染色并干燥后的棉球
实验1 实验2
请填空:
(1)实验1采用了科学探究中的控制变量法,该实验控制的变量是 。
(2)实验1中干石蕊纸花喷水后放入二氧化碳中,观察到的现象是 ,该反应的化学方
程式是 。
(3)实验2是在实验1的基础上设计的创新改进实验,将二氧化碳缓慢通入竖直放置的玻璃管中,能观
察到第 (填序号)号棉球先变色,通过此现象可获得关于二氧化碳的另外一条性质是
。
【答案】(1)水 (2)纸花由紫变红 CO+H O=HCO (3)④ 密度比空气大
2 2 2 3
6.【2016年江苏省徐州市】 化学兴趣小组探究金属的性质时,将一段去除氧化膜的镁条,放入一定量的稀盐
酸中,有气泡产生,充分反应后静置,发现试管中有灰白色沉淀。
【提出问题】 灰白色沉淀是什么物质?
【猜想假设】
3小华认为灰白色沉淀为碳酸镁(MgCO ),其他同学认为不需要实验就能否定小华的猜想,理由是
3
。
小宇认为由于反应后氯化镁的生成量偏多,灰白色沉淀为不能再溶解的氯化镁固体。
小彤认为灰白色沉淀为脱落的镁粉细颗粒。
【实验探究1】
实验操作 现象 结论
①取试管中的上层清液,加入适量的氯化镁固体 (选填“溶
小宇猜想错误
氯化镁固体 解”或“不溶解”)
(选填“有”或“没
②取适量白色沉淀加入足量稀盐酸中 小彤猜想错误
有”)气泡冒出
基于以上探究与分析,原有猜想均遭到了否定。
【查阅资料】
HCl+AgNO ═HNO +AgCl↓,AgCl是一种白色沉淀。
3 3
【实验探究2】
他们又另取灰白色沉淀放入试管中加热,将蘸有硝酸银溶液的玻璃棒伸入试管内,玻璃棒上的溶
液出现白色浑浊,证明产生了 气体。再将湿润的蓝色石蕊试纸悬于试管口,试纸
变 色。
同学们请教老师后得知,足量的镁与稀盐酸反应时,溶液会经历从酸性到碱性且碱性逐步增强的
过程,从而生成了碱式氯化镁沉淀.据文献介绍,碱式氯化镁存在多种组成结构,化学通式可表示
为Mg(OH)Cl•mH O(其中2x﹣y﹣z=0,0≤m≤6)。
x y z 2
【反思拓展】
(1)做镁与稀盐酸反应的实验时,镁条的用量宜少不宜多。
(2)铁片和铜片放入稀硫酸中产生的现象也不相同,据此推测出铁的活性比铜 。还可
根据铁和硫酸铜溶液的反应来确定这两种金属的活动性强弱,该反应的化学方程式 为
。
【答案】【猜想假设】反应物中没有碳元素,不会生成碳酸镁【实验探究1】溶解;没有【实验探究2】氯化氢
红【反思拓展】强 Fe+CuSO =FeSO +Cu
4 4
【解析】【猜想假设】小华认为灰白色沉淀为碳酸镁(MgCO ),其他同学认为不需要实验就能否定小华的猜想,
3
理由是:反应物中没有碳元素,不会生成碳酸镁;【实验探究1】饱和溶液中不能溶解某种溶质,镁会与盐
酸反应生成氯化镁和氢气,
实验操作 现象 结论
①取试管中的上层清液,加入适量的氯化镁固体 氯化镁固体溶解 小宇猜想错误
②取适量白色沉淀加入足量稀盐酸中 没有气泡冒出 小彤猜想错误
4【实验探究2】氯离子和银离子会生成氯化银沉淀,氯化氢是酸性气体,能使蓝色石蕊试纸变蓝色,所以
将蘸有硝酸银溶液的玻璃棒伸入试管内,玻璃棒上的溶液出现白色浑浊,证明产生了氯化氢气体。
再将湿润的蓝色石蕊试纸悬于试管口,试纸变红色;
【反思拓展】铁会与稀硫酸反应,铜不会与硫酸反应,所以推测出铁的活性比铜强,铁和硫酸铜反应生成
硫酸亚铁和铜,化学方程式为:Fe+CuSO =FeSO +Cu。学科网
4 4
能力提升
1.【2016年黑龙江省绥化市】 有一包白色固体,可能含有碳酸钾、硫酸钠、氯化钠、硝酸钡、氢氧化钾中的一
种或几种.某化学兴趣小组为探究其成分,进行如下实验:
(1)取少量固体于烧杯中,逐渐加水并不断搅拌,待烧杯中的物质充分反应后过滤,得到白色沉淀和滤液.
(2)取少量滤液于试管中,滴加酚酞溶液,酚酞溶液不变色.
(3)向白色沉淀中滴加过量稀硝酸并不断搅拌,沉淀部分溶解.
请根据上述实验过程和发生的现象,回答问题:
原白色固体中一定含有________,一定不含有________,可能含有________.
【答案】 硫酸钠、碳酸钾、硝酸钡;氢氧化钾;氯化钠。
2.【2016年湖北省荆州市】小明同学将一定量的氢化钙(CaH)加入到足量的NaCO 溶液中,充分反应后过
2 2 3
滤,分离出滤渣和滤液.
【提出问题】滤液中溶质的成份是什么?
【查阅资料】CaH 遇水迅速反应生成Ca(OH) 和H .反应的化学方程式为__________.
2 2 2
【结论推理】滤液中溶质一定有NaOH,可能有Na CO 或__________.
2 3
【实验验证】请结合题意,在下列表格的空白中填写恰当的内容.
实验方法 实验现象 实验结论
取滤液少许,向其中滴加[来源:学科网] 无明显显现 (1)__________
Na CO 溶液.
2 3 [来源:学_科_网Z_X_X_K]
(2)__________ 有气体放出 滤液中有Na CO 存在
2 3
【反思与拓展】
(1)如果要从上述滤液中以最小生产成本获得大量NaOH,你建议向滤液中加入适量的__________溶液.
(2)小明同学认为CaH 与水的反应是复分解反应.请谈谈你的看法并说明理由__________。
2
5【答案】【查阅资料】CaH +2H O═Ca(OH) +2H ↑;【结论推理】Ca(OH) ;【实验验证】
2 2 2 2 2
实验方法 实验现象 实验结论
取滤液少许,向其中滴加Na CO 溶液 无明显显现 (1)说明滤液中没有氢氧化钙
2 3
(2)另取滤液,向其中加入足量稀盐酸 有气体放出 [来源:Z.xx.k.Com] 滤液中有Na 2 CO 3 存在
【反思与拓展】(1)氢氧化钙;(2)不属于复分解反应;氢化钙和水反应生成氢氧化钙和氢气,生成物中氢
气属于单质。
3.【2016年内蒙古呼和浩特市】 某同学将一定质量的碳酸氢钠和稀硫酸混合,反应完全后(假设反应产生的
气体全部逸出),对反应后溶液中溶质的成分进行如下探究:
【实验用品】pH试纸、Zn片、氧化铜粉末、稀硫酸、氢氧化钠溶液、氯化钡溶液。
【假设猜想】猜想一:硫酸钠 猜想二:硫酸钠、碳酸氢钠 猜想三:硫酸钠、硫酸
【实验探究】同学们取反应后的溶液用不同方案进行如下实验,请根据现象或结论填空。
6【得出结论】猜想三正确。
【评价反思】老师对同学们能用多种方案进行探究,并且得出正确的实验结论给予了肯定,同时指出探究中存
在两处明显错误。分别是:
① ; ② 。
【总结提高】依据所给实验用品,你还有什么不同类方案确认猜想三是正确的。请你写出你的实验方案
。
【答案】实验现象:有气泡产生,锌片不断溶解;实验结论:猜想二不正确【评价反思】①方案B中pH试纸浸入
溶液中②方案D中硫酸钠与氯化钡反应也会产生白色沉淀,不能证明一定有硫酸存在【总结提高】取少
量氧化铜粉末于试管中,加入足量反应后的溶液,若氧化铜溶解,溶液变蓝,则猜想三正确
4. 【2016年陕西省】某学习小组同学用右图实验装置来探究鸡蛋壳里含有CO2-(以CaCO 的形式存在)的可
3 3
能性,请你一起参与学习探究。
7【讨论交流】同学们讨论后一致认为若鸡蛋壳里含有CO2-,实验时广口瓶中一定会产生气泡,玻璃片上石灰
3
水会变浑浊,据此写出有气泡生成的化学方程式: 。
【进行实验】小明和小红在各自的实验中均看到广口瓶中产生气泡,小明还看到玻璃片上石灰水变浑浊,而小
红却未看到。他们很好奇,于是进一步探究。
【提出问题】小红的实验中,玻璃片上的石灰水为什么不变浑浊呢?
【做出猜想】小红猜想:可能鸡蛋壳中含有铁等较活泼金属,而不含CO2-;
3
小明猜想:可能是小红实验所用的盐酸中溶质质量分数过大,挥发出HCl气体。
依据所学化学知识和生活常识,你认为 的猜想是不合理的。
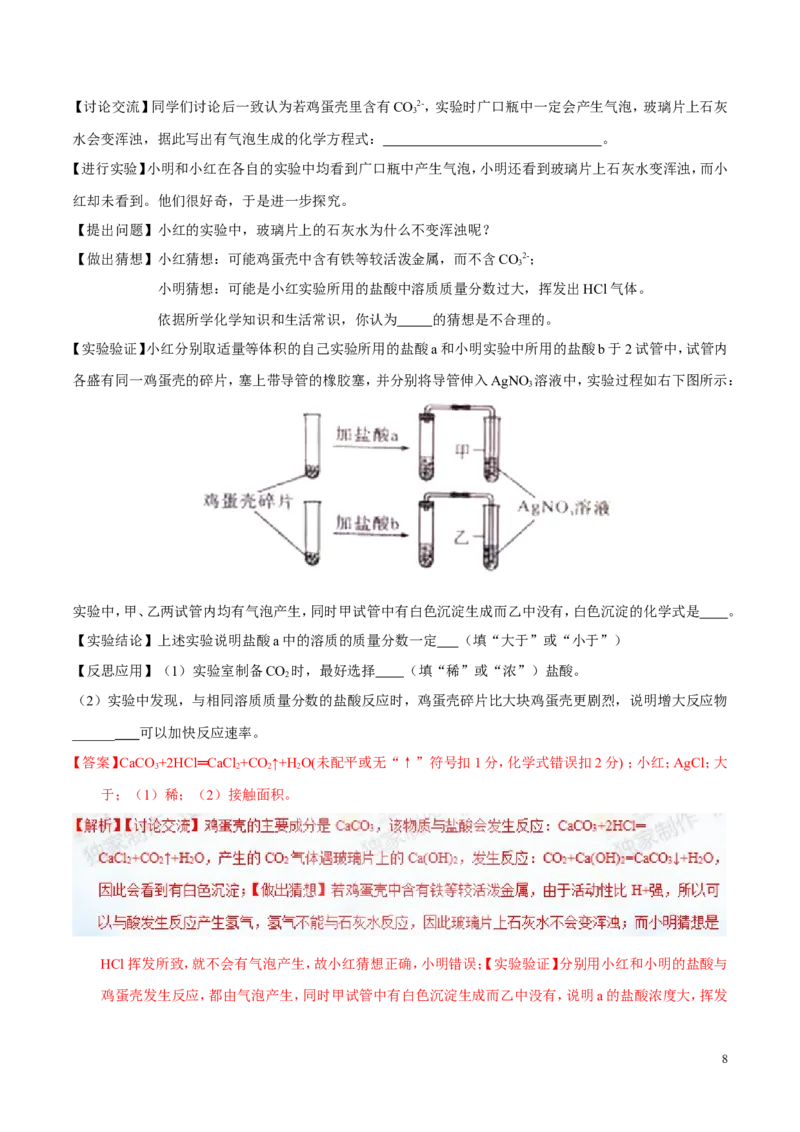
【实验验证】小红分别取适量等体积的自己实验所用的盐酸a和小明实验中所用的盐酸b于2试管中,试管内
各盛有同一鸡蛋壳的碎片,塞上带导管的橡胶塞,并分别将导管伸入AgNO 溶液中,实验过程如右下图所示:
3
实验中,甲、乙两试管内均有气泡产生,同时甲试管中有白色沉淀生成而乙中没有,白色沉淀的化学式是 。
【实验结论】上述实验说明盐酸a中的溶质的质量分数一定 (填“大于”或“小于”)
【反思应用】(1)实验室制备CO 时,最好选择 (填“稀”或“浓”)盐酸。
2
(2)实验中发现,与相同溶质质量分数的盐酸反应时,鸡蛋壳碎片比大块鸡蛋壳更剧烈,说明增大反应物
______ 可以加快反应速率。
【答案】CaCO +2HCl═CaCl +CO ↑+H O(未配平或无“↑”符号扣1分,化学式错误扣2分) ;小红;AgCl;大
3 2 2 2
于;(1)稀;(2)接触面积。
HCl挥发所致,就不会有气泡产生,故小红猜想正确,小明错误;【实验验证】分别用小红和小明的盐酸与
鸡蛋壳发生反应,都由气泡产生,同时甲试管中有白色沉淀生成而乙中没有,说明a的盐酸浓度大,挥发
8产生HCl与AgNO 溶液发生复分解反应:HCl+ AgNO =AgCl↓+HNO ,故白色沉淀的化学式是AgCl;
3 3 3
【实验结论】上述实验说明盐酸a中的溶质的质量分数一定大于b;【反思应用】(1)实验室制备CO 时,
2
为减少HCl对气体制取的影响,最好选择稀盐酸;(2)实验中发现,与相同溶质质量分数的盐酸反应时,
鸡蛋壳碎片比大块鸡蛋壳更剧烈,说明增大反应物接触面积可以加快反应速率。
5. 【2016年湖南省郴州市】 某化学兴趣小组完成了下列两个实验:
实验1:用试管取一定量NaOH溶液,并滴加2滴酚酞溶液,再加入稀盐酸,红色恰好消失。
实验2:用试管取一定量澄清的石灰水,然后加入饱和的Na CO 溶液。
2 3
实验结束后,把两支试管里的物质倒入同一烧杯,静置,烧杯中有白色沉淀,上层澄清液显红色。
点燃
同学们欲对该澄清液成份进行探究,请你参与,完成下列问题:
【问题分析】
(1)实验1的目的是验证 (填化学原理);
(2)实验2中产生白色沉淀的化学方程式 ;
(3)澄清液显红色,说明该澄清液显碱性,其中溶质除一定有NaOH外,还可能含有
或 。
【实验验证】
①取澄清液,加入适量的CaCl 溶液,无明显现象,则澄清液中不含 ;
2
②取澄清液,通入CO 气体,产生浑浊,写出产生浑浊的化学方程式 。
2
【交流反思】化学反应后形成的溶液中溶质的确定,既要考虑反应产物,也要考虑反应物是否过量。
【答案】【问题分析】(1)NaOH+HCl=NaCl+H O(2)Ca(OH)+Na CO =CaCO ↓+2NaOH(3)碳酸钠 氢氧化
2 2 2 3 3
钙【实验验证】①碳酸钠 ②CO +Ca(OH)=CaCO ↓+H O
2 2 3 2
9