文档内容
第二课时 烷烃的性质
[明确学习目标] 1.了解烷烃的物理性质及用途。2.了解烷烃的化学性质、
认识取代反应的特点。
学生自主学习
1.烷烃的物理性质
烷烃均为 □ 难 溶于水的 □ 无 色物质,其熔点、沸点和密度一般随着分子中碳
原子数增加(同时相对分子质量也在增大)而 □ 升高 ,在常温下的状态由气态变为
□ 液态 ,再到 □ 固态 。
2.烷烃的化学性质
在通常情况下,烷烃比较稳定,与 □ 强酸 、 □ 强碱 、 □ 强氧化剂 都不反应。
如甲烷 □ 不能 使高锰酸钾溶液褪色。但是在特定条件下,烷烃也会发生某些反应。
(1)氧化反应
纯净的甲烷在空气中安静的燃烧,火焰呈 □ 淡蓝色 ,放出890 kJ的热量,反
应的化学方程式为 □ CH + 2O ――→ CO + 2H O。
4 2 2 2
丙烷燃烧的化学方程式为:
□ C H + 5O ――→ 3CO + 4H O。
3 8 2 2 2
(2)烷烃在较高温度下会发生分解
如:CH ――→C+2H
4 2
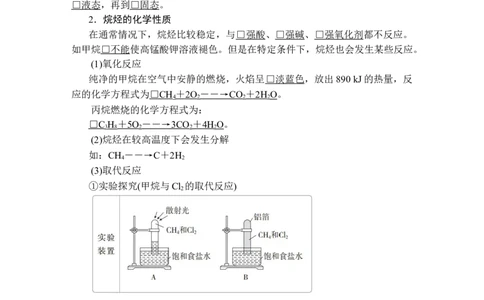
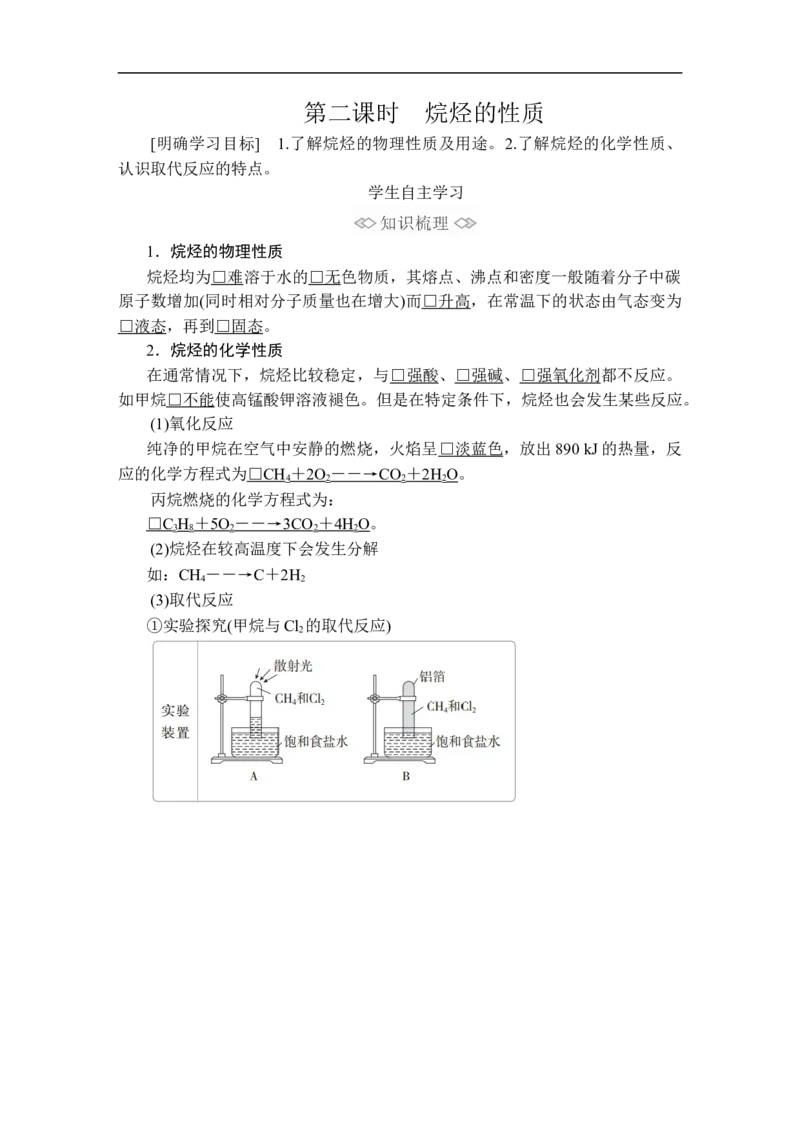
(3)取代反应
①实验探究(甲烷与Cl 的取代反应)
2②甲烷四种氯代产物的性质
a.水溶性:CH Cl、CH Cl 、CHCl 、CCl 均 □ 不 溶于水。
3 2 2 3 4
b.状态:常温下除 □ CH Cl 是气体,其余三种均为液体。
3
③取代反应概念:有机物分子里的某些 □ 原子或原子团 被其他 □ 原子或原子
团所替代的反应。
④烷烃在一定条件下,可以与 □ 卤素单质 发生取代反应。
能否用CH 和Cl 按1∶1的体积比混合来制取纯净的CH Cl?
4 2 3
提示:CH 和Cl 的反应是连锁反应,不可能只发生第一步取代反应,生成
4 2
物为混合物,即CH Cl、CH Cl 、CHCl 和CCl 四种有机物与氯化氢形成的混合
3 2 2 3 4
物,CH Cl的产率低,因此不能用CH 和Cl 按1∶1的体积比混合来制取纯净的
3 4 2
CH Cl。
3
课堂互动探究
1.烷烃的物理性质
(1)烷烃难溶于水。
(2)常温下,碳原子数小于或等于4的烷烃为气态(新戊烷常温下也为气态)。
(3)碳原子数相同的烷烃,支链越多,沸点越低。如沸点:正戊烷>异戊烷>
新戊烷。
2.烷烃的化学性质
(1)通常较稳定,不能被酸性高锰酸钾溶液等强氧化剂氧化,也不能与强酸、强碱发生反应。
(2)烷烃完全燃烧的通式为
C H +O ――→nCO +(n+1)H O。
n 2n+2 2 2 2
(3)在光照条件下,烷烃与Cl 、Br 等卤素单质的气体发生取代反应,生成多
2 2
种卤代产物和相应的卤化氢气体。烷烃与卤素单质发生一卤代反应的通式为:
C H +X ――→C H X+HX,C H X可与X 继续发生取代反应生成二卤
n 2n+2 2 n 2n+1 n 2n+1 2
代物,甚至多卤代产物。
甲烷发生取代反应的有关规律
(1)反应条件和反应物
反应条件为光照,但不能用太阳光直射,以防爆炸,应用散射光,反应物为
甲烷与卤素单质,与氯水、溴水等不反应。
(2)反应产物
甲烷与氯气反应生成的产物是 CH Cl、CH Cl 、CHCl 和CCl 四种有机物与
3 2 2 3 4
HCl形成的混合物,虽然反应物的比例、反应的时间长短等因素会造成各种产物
的比例不同,但很难出现全部是某一种产物的情况。
(3)反应特点
①连锁反应
甲烷的取代反应是一种连锁反应,即第一步反应一旦开始,后续反应立即进
行。生成物中各物质均含有,其中HCl的物质的量最多。
②数量关系
CH 与Cl 发生取代反应时,每1 mol H被取代,消耗1 mol Cl ,同时生成1
4 2 2
mol HCl。即 1 mol C H 与 Cl 发生完全取代,消耗 Cl 最多为 y mol。n(Cl )=
x y 2 2 2
n(H)=n(HCl)。
在标准状况下,22.4 L CH 与氯气在光照下发生取代反应,待反应完全
4
后,测得四种有机取代物的物质的量相等,则消耗的氯气为( )
A.1.25 mol B.2 mol C.2.5 mol D.4 mol
[批注点拨]
[解析] 1 mol CH 与氯气发生取代反应,生成CH Cl、CH Cl 、CHCl 、CCl
4 3 2 2 3 4
各0.25 mol,该四种取代物中n(Cl)=0.25 mol×(1+2+3+4)=2.5 mol,即1 molCH 中被取代的氢原子为2.5 mol,每取代1 mol氢原子,消耗1 mol Cl ,故消耗
4 2
的氯气为2.5 mol。
[答案] C
[练1] 甲烷和氯气以物质的量之比 1∶3混合,在光照条件下,得到的有机
产物是( )
①CH Cl ②CH Cl ③CHCl ④CCl
3 2 2 3 4
A.只有① B.①和②的混合物
C.只有② D.①②③④的混合物
答案 D
解析 无论反应物的物质的量之比是多少,都会得到各种氯代物的混合物。
[练2] 将等物质的量的甲烷和氯气混合后,在漫射光的照射下充分反应,
生成物中物质的量最大的是( )
A.HCl B.CH Cl
3
C.CH Cl D.CCl
2 2 4
答案 A
解析 若CH 和Cl 均为1 mol,二者反应后生成 CH Cl、CH Cl 、CHCl 、
4 2 3 2 2 3
CCl 和HCl,根据反应原理和碳、氯原子守恒可知,前四种物质与剩余CH 的物
4 4
质的量之和为1 mol,HCl为1 mol。
规律方法
(1)有机反应比较复杂,常伴随很多副反应发生,因此有机反应的化学方程式
常用“―→”。
(2)CH 与Cl 的反应逐步进行,应分步书写。
4 2
(3)当 n(CH )∶n(Cl )=1∶1 时,反应并不只发生 CH +Cl ――→CH Cl+
4 2 4 2 3
HCl,其他反应仍发生。
(4)甲烷与氯气发生取代反应时,取代 H原子的个数是难以控制的,因此制
备CH Cl一般不采用取代反应。
3
本课归纳总结
1.甲烷结构与性质的记忆口诀
性质稳定是甲烷,光照氯代四连环;
立体构型四面体,易燃防爆分解难。
2.甲烷与氯气的取代反应是分步进行的,每有 1 mol氢原子被取代,需消
耗1 mol氯气。
3.取代反应:有机物分子里的某些原子或原子团被其他原子或原子团所替
代的反应。
4.随着碳原子数的增加,烷烃的熔、沸点逐渐升高,密度逐渐增大,其中
碳原子数不超过4的烷烃标准状况下为气体。5.烷烃的化学性质与甲烷类似,能发生取代反应和氧化反应,烷烃燃烧的
通式为C H +O ――→nCO +(n+1)H O。
n 2n+2 2 2 2
学习效果检测
1.有关烷烃的叙述:①都是易燃物;②特征反应是取代反应;③相邻两个
烷烃在分子组成上相差一个甲基,其中正确的是( )
A.①和③ B.②和③ C.只有① D.①和②
答案 D
解析 相邻烷烃在分子组成上相差一个CH 原子团,而不是—CH 。
2 3
2.下列物质在一定条件下可与乙烷发生化学反应的是( )
A.氯气 B.溴水
C.氯水 D.酸性高锰酸钾溶液
答案 A
解析 类比甲烷的化学性质,乙烷与氯气在光照条件下发生取代反应,和溴
水、氯水、酸性高锰酸钾溶液不反应。
3.在下列5种物质沸点的排列顺序中,正确的是( )
①正丁烷 ②2甲基丙烷[CH CH(CH )CH ]
3 3 3
③正戊烷 ④2甲基丁烷[CH CH(CH )CH CH ]
3 3 2 3
⑤2,2二甲基丙烷[C(CH ) ]
3 4
A.①>②>③>④>⑤ B.⑤>④>③>②>①
C.③>④>⑤>①>② D.②>①>⑤>④>③
答案 C
解析 根据烃类的熔沸点大小判断规律:在有机物同系物中,随着碳原子数
的增加,相对分子质量的增大,分子间作用力增大,熔沸点逐渐升高;分子式相
同的烃,支链越多,熔沸点越低。①②均只有4个C原子,③④⑤均有5个碳原
子,故①②的沸点小于③④⑤的沸点;②有 1 个支链,而①无支链,故沸点
①>②;③无支链,④只有1个支链,⑤有2个支链,故沸点③>④>⑤;综上所
述:沸点③>④>⑤>①>②。
4.某气态烷烃20 mL,完全燃烧时,恰好消耗同温同压下的氧气 100 mL,
该烃的化学式是( )
A.CH B.C H C.C H D.C H
4 3 8 4 10 5 12
答案 B
解析 设烷烃为C H
n 2n+2
C H +O ――→nCO +(n+1)H O
n 2n+2 2 2 2
1
20 mL 100 mL
即=则n=3,所以分子式为C H 。
3 8
5.下列反应属于取代反应的是( )
A.C H +3O ――→2CO +2H O
2 4 2 2 2
B.Zn+CuSO ===ZnSO +Cu
4 4
C.NaCl+AgNO ===AgCl↓+NaNO
3 3
D.CH Cl +Cl ――→CHCl +HCl
2 2 2 3
答案 D
解析 取代反应是有机物分子中的某些原子或原子团被其他原子或原子团所
替代的反应。A项C H 的燃烧不是取代反应;B项为置换反应;C项为复分解反
2 4
应;D项中Cl原子取代了CH Cl 中的一个H原子,故属于取代反应。
2 2
6.下列物质中,不能和氯气发生取代反应的是( )
A.CH Cl B.CCl C.CH Cl D.CH
3 4 2 2 4
答案 B
解析 由甲烷与Cl 发生取代反应的过程可知,CCl 分子中不再含有氢原子,
2 4
不能再与Cl 发生取代反应。
2