文档内容
生活中常见的盐
一、基本考点
考点1.生活中常见的盐
[来
(1)氯化钠(NaCl):①俗名:食盐。②存在:在自然界中分布很广,存在于海水、盐湖、盐井、
盐矿中。③用途: a.调味品,b. 配制生理盐水,c. 工业原料,d. 工业上用来做原料制取
碳酸钠、氢氧化钠、氯气、盐酸等,e. 农业上用氯化钠溶液来选种等。
(2)碳酸钠(NaCO):俗名:纯碱、苏打;用途:用于生产玻璃、造纸、纺织、洗涤剂。
2 2
(3)碳酸氢钠(NaHCO):俗名:小苏打;用途:在食品工业上用作食品添加剂,在医疗上是
3
治疗胃酸过多的一种药剂。
(4)碳酸钙(CaCO):它是大理石或石灰石的主要成分;用途:用作建筑材料及补钙剂。
3
考点2.盐的化学性质和复分解反应
(1)盐的化学性质:①盐与金属反应生成另一种金属和另一种盐;如
Zn+CuSO==ZnSO+Cu 。 ② 盐 和 酸 反 应 生 成 另 一 种 盐 和 另 一 种 酸 ; 如 :
4 4
BaCl+HSO==BaSO↓+2HCl。③盐和碱反应生成另一种盐和另一种碱;如:
2 2 4 4
CuSO+2NaOH==Cu(OH)↓ +NaSO 。 ④ 盐 和 盐 反 应 生 成 两 种 新 盐 ; 如 :
4 2 2 4
NaCl+AgNO==AgCl↓+NaNO。
3 3
(3)复分解反应:①定义:两种化合物相互交换成分生成另外两种化合物的反应叫复分解
反应。如NaOH+HCl==NaCl+HO。②发生的条件:酸、碱、盐之间并不是都能发生反应,只有
2
当两种化合物相互交换成分,有沉淀、水或气体生成时,复分解反应才能发生。
考点3.粗盐提纯
粗盐中含有较多的可溶性杂质(氯化镁、氯化钙等)和不溶性杂质(泥沙等),可以通过过
滤的方法把不溶于液体的固体物质跟液体分离。过滤时,液体穿过滤纸上的小孔,而固态
物质留在滤纸上,从而使固体和液体分离。粗盐提纯时,把粗盐溶解在水里,经过过滤,把
泥沙等杂质从食盐水中除去,然后再通过蒸发结晶,得到食盐晶体。
1粗盐提纯中需要的主要仪器有:托盘天平、量筒、铁架台、烧杯、玻璃棒、漏斗、滤纸、酒精
灯、蒸发皿。
考点4. CO2、
SO2
、 Cl的检验方法
3 4
(1) 的检验方法:首先将待测样品装入试管中,再加稀盐酸,若观察到产生大量气
CO2
3
泡,将产生的气体通入澄清石灰水中,如果澄清石灰水变浑浊,则样品中含有 。(2)
CO2
3
的检验方法:首先将待测样品装入试管中,再加入Ba(NO) 溶液和稀硝酸,若观察
SO2 3 2
4
到产生白色沉淀则样品中含有
SO2
。(3) Cl的检验方法:首先将待测样品装入试管中,
4
再加入AgNO
3
溶液和稀硝酸,若观察到有白色沉淀产生,则样品中含有 Cl。
二、能力与综合考点
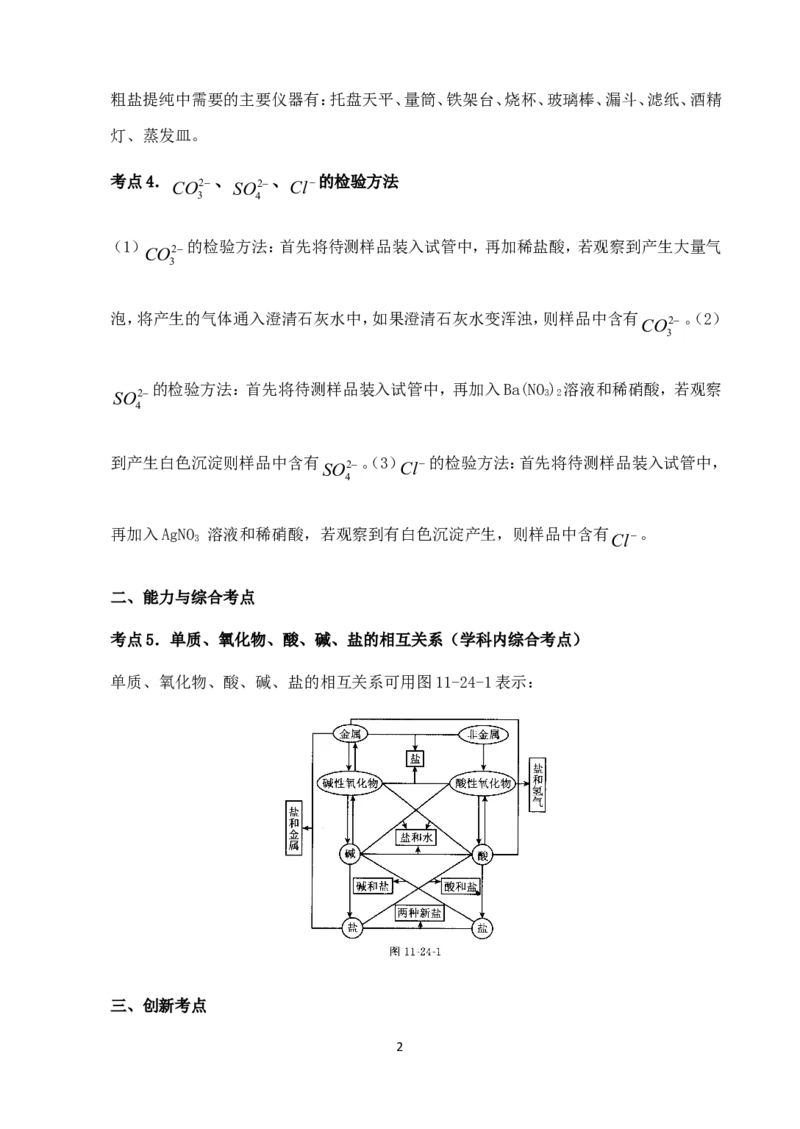
考点5.单质、氧化物、酸、碱、盐的相互关系(学科内综合考点)
单质、氧化物、酸、碱、盐的相互关系可用图11-24-1表示:
三、创新考点
2考点6.离子的共存(探究性考点)
同一溶液中若离子之间符合下列三个条件之一就会发生离子反应,离子间便不能在溶液
中大量共存。①生成沉淀物:如Cl—与Ag+,Ba2+与 ,OH—与Cu2+、Fe3+, 与Ca2+、
SO2 CO2
4 3
Ba2+等不能大量共存;②生成气体:如OH—与 ,H+与 、 等不能共存;③生
NH CO2 HCO
4 3 3
成HO:如H+与OH—不能共存。另外还应注意题中的附加条件,如溶液无色透明,则溶液中
2
肯定没有有色离子(常见的有色离子如Fe3+、Cu2+、Fe2+、 等);pH=1为强酸性溶液;
MnO
4
pH=14为强碱性溶液。
3