文档内容
2014.01
注意事项:
1.本试卷分选择题和非选择题,共36题,满分100分;考试用时100分钟。
2.答题前,考生务必将自己的姓名、考点名称、考场号、座位号、考试号填写清楚,并用
2B铅笔认真正确填涂考试号下方的数字;
[来源:学科网]
3.答选择题必须用2B铅笔把答题卡上对应题目的答案标号涂黑,如需改动,请用橡皮
擦干净后,再选涂其他答案;答非选择题必须用0.5毫米黑色墨水签字笔写在答题卡指定的
位置上,不在答题区域内的答案一律无效,不得用其他笔答题:
4.考生答题必须答在答题卡上,答在试卷和草稿纸上一律无效。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Mg-24 Zn-65 Fe-56
S-32 Ca-40 Cu-64
选择题(共60分)
一、单项选择题(包括30题,每题2分,共60分。每题只有一个选项符合题意。)
1.今年苏州进入秋冬以来,频频出现雾霾天气,下列措施对改善雾霾天气不利的是
A.多植树,美化环境
B.积极建造高楼大厦,以满足人们生活的需要
C.研究新能源汽车
D.禁止焚烧秸秆
2.下列物质的用途,是利用其化学性质的是
A.活性炭除去冰箱内异味 B.用氢气填充探空气球
C.氧气用于急救病人 D.干冰进行人工降雨
3.下列化学用语与其含义相符的是
A.MgCl——氯化镁 B.Fe2+——铁离子
2
C. 2H——2个氢元素 D.O——2个氧原子
2
4.缺乏下列哪种元素易导致智力低下患侏儒症的是
A.钙 B.碘 C.锌 D.铁
5.不同元素的本质区别是
A.中子数不同 B.电子数不同
C.核电荷数不同 D.相对原子质量不同
6.在下列概念中,一定属于描述物质化学变化规律的是
A.汽化 B.液化 C.爆炸 D.缓慢氧化
7.下列物质中不能由金属与酸发生置换反应直接得到的是A.ZnlCl B.Al(SO) C.MgCl D.Fe(SO)
2 2 4 3 2 2 4 3
8.下列关于燃烧现象的描述,正确的是
A.氢气在空气中燃烧产生明亮的蓝紫色火焰
B.木炭在氧气中燃烧生成黑色固体
C.镁条在空气中燃烧发出耀眼的白光
D.铁丝在空气中剧烈燃烧,火星四射
9.下列洗涤方法中利用了乳化原理的是
A.用汽油洗去手上的油污 B.用洗洁精洗去餐具上的油污
C.用酒精洗去试管中的碘 D.用稀盐酸洗去石灰水瓶壁上的白膜
10.我国南海海底蕴藏着丰富的锰结核——含有锰、铁、铜等金属的矿物。已知锰原子的核内
质子数为25,相对原子质量为55,则锰原子的核外电子数为
A.25 B.30 C.55 D.80
11.下列各组物质,按单质、化合物、混合物顺序排列的是
A.固态氮、干冰、冰水共存物 B.稀有气体、氯化氢气体、河水
C.液态氧、蒸馏水、铁矿石 D.氧气、食盐水、过氧化氢溶液
12.下列做法正确的是
A.用铝锅盛放酸性食物 B.菜刀使用后放在潮湿的砧板上
C.用水浇灭锅中着火的油 D.天然气泄漏应该及时的开窗通风,并报燃气公司维修
13.下列实验操作正确的是
A.未说明药品用量,液体一般取5mL左右,固体只需盖满试管底部
B.将试管夹从试管底部往上套,夹在试管的中上部
C.为了避免酒精洒出,酒精灯内的酒精越少越好
[来源:学科网]
D.用托盘天平称量15.5g食盐固体时,左盘放15g砝码,游码调至0.5g处
14.用化学的观点解释下列成语,错误的是
A.火上浇油:增加可燃物,使燃烧更剧烈 B.釜底抽薪:将可燃物撤出燃烧区
C.十年树木:树木生长,无化学变化 D.百炼成钢:逐渐降低生铁中碳、硅等含量
15.在实验室里,利用下列物质和装置制取气体的方法正确的是
A.二氧化锰和氯酸钾制取氧气
B.大理石和浓盐酸制取二氧化碳
C.二氧化锰和6%的过氧化氢溶液制取氧气
D.铜和稀硫酸制取氢气
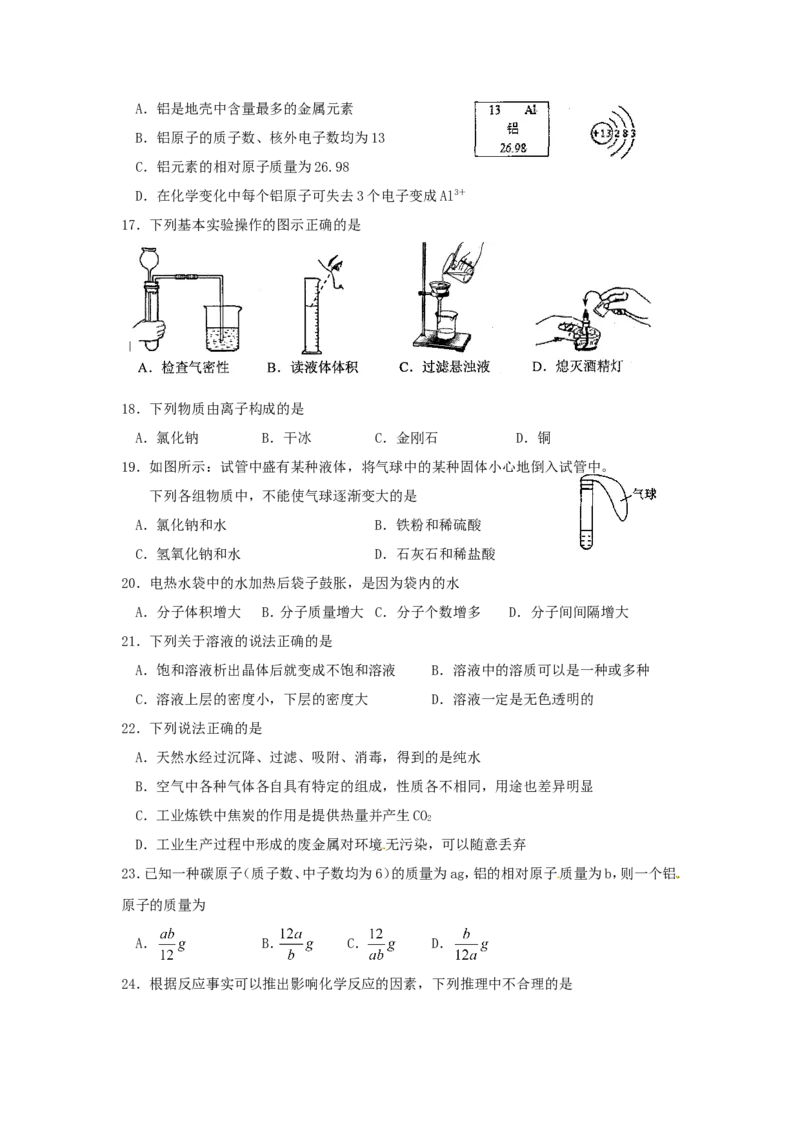
16.下图为铝在元素周期表中的信息和原子结构示意图,由此不能得到的信息是A.铝是地壳中含量最多的金属元素
B.铝原子的质子数、核外电子数均为13
C.铝元素的相对原子质量为26.98
D.在化学变化中每个铝原子可失去3个电子变成Al3+
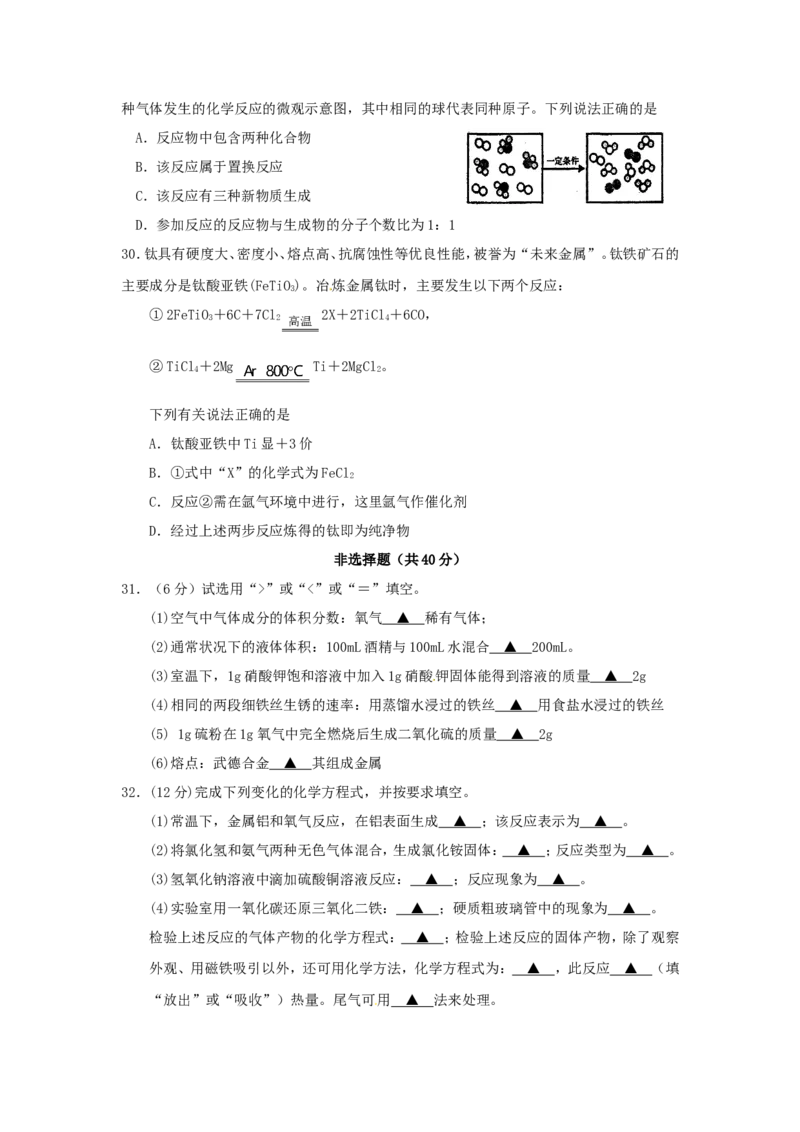
17.下列基本实验操作的图示正确的是
18.下列物质由离子构成的是
A.氯化钠 B.干冰 C.金刚石 D.铜
19.如图所示:试管中盛有某种液体,将气球中的某种固体小心地倒入试管中。
下列各组物质中,不能使气球逐渐变大的是
A.氯化钠和水 B.铁粉和稀硫酸
C.氢氧化钠和水 D.石灰石和稀盐酸
20.电热水袋中的水加热后袋子鼓胀,是因为袋内的水
A.分子体积增大 B.分子质量增大 C.分子个数增多 D.分子间间隔增大
21.下列关于溶液的说法正确的是
A.饱和溶液析出晶体后就变成不饱和溶液 B.溶液中的溶质可以是一种或多种
C.溶液上层的密度小,下层的密度大 D.溶液一定是无色透明的
22.下列说法正确的是
A.天然水经过沉降、过滤、吸附、消毒,得到的是纯水
B.空气中各种气体各自具有特定的组成,性质各不相同,用途也差异明显
C.工业炼铁中焦炭的作用是提供热量并产生CO
2
D.工业生产过程中形成的废金属对环境无污染,可以随意丢弃
23.已知一种碳原子(质子数、中子数均为6)的质量为ag,铝的相对原子质量为b,则一个铝
原子的质量为
A. B. C. D.
24.根据反应事实可以推出影响化学反应的因素,下列推理中不合理的是25.下列图像与实验相符合的是
A.图①表示镁带在空气中燃烧
B.图②表示将饱和Ca(OH) 溶液升温
2
C.图③表示等质量的稀硫酸中加入足量的镁粉和锌粉
D.图④表示向含少量Cu粉的铁粉中滴加稀盐酸至过量
26.下表列举了四组待鉴别的物质和对应的鉴别方法,其中不可行的是
27.一种新型的抗流感病毒药物“帕拉米韦氯化钠注射液“已获得加速审批通过。帕拉米韦
的化学式为C H NO,下列有关说法正确的是
15 28 4 4
A.帕拉米韦属于化合物 B.帕拉米韦中氢元素质量分数最高
C.帕拉米韦由四种原子构成 D.帕拉米韦中氮元素和氧元素的质量比为1:1
28.下列实验操作正确的是
A.“物质燃烧的条件”实验中,用玻璃杯罩住燃着的蜡烛以降低蜡烛的着火点
B.“粗盐的初步提纯”实验中,进行蒸发操作时,当出现大量固体时,用玻璃棒搅拌
C.“配制一定溶质质量分数的NaCl溶液”实验中,量取一定的水时俯视读数,则所配制
溶液溶质质量分数偏小
D.“高锰酸钾制取氧气”实验中,收集好气体后应先将导管移出水槽再停止加热
29.在“宏观——微观——符号”之间建立联系,是化学学科特有的思维方式。下图表示两种气体发生的化学反应的微观示意图,其中相同的球代表同种原子。下列说法正确的是
A.反应物中包含两种化合物
B.该反应属于置换反应
C.该反应有三种新物质生成
D.参加反应的反应物与生成物的分子个数比为1:1
30.钛具有硬度大、密度小、熔点高、抗腐蚀性等优良性能,被誉为“未来金属”。钛铁矿石的
主要成分是钛酸亚铁(FeTiO)。冶炼金属钛时,主要发生以下两个反应:
3
①2FeTiO+6C+7Cl 2X+2TiCl+6CO,
3 2 高温 4
②TiCl+2Mg Ti+2MgCl。
4 2
下列有关说法正确的是
A.钛酸亚铁中Ti显+3价
B.①式中“X”的化学式为FeCl
2
C.反应②需在氩气环境中进行,这里氩气作催化剂
D.经过上述两步反应炼得的钛即为纯净物
非选择题(共40分)
31.(6分)试选用“>”或“<”或“=”填空。
(1)空气中气体成分的体积分数:氧气 ▲ 稀有气体;
(2)通常状况下的液体体积:100mL酒精与100mL水混合 ▲ 200mL。
(3)室温下,1g硝酸钾饱和溶液中加入1g硝酸钾固体能得到溶液的质量 ▲ 2g
(4)相同的两段细铁丝生锈的速率:用蒸馏水浸过的铁丝 ▲ 用食盐水浸过的铁丝
(5) 1g硫粉在1g氧气中完全燃烧后生成二氧化硫的质量 ▲ 2g
(6)熔点:武德合金 ▲ 其组成金属
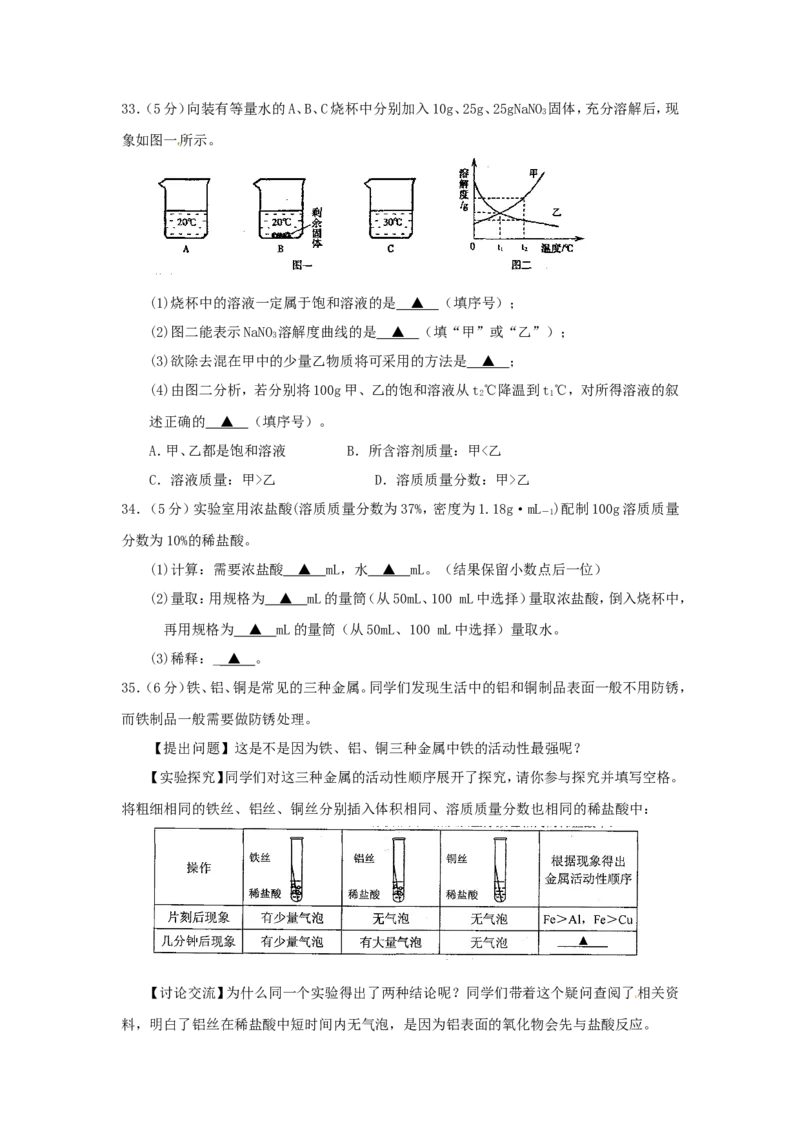
32.(12分)完成下列变化的化学方程式,并按要求填空。
(1)常温下,金属铝和氧气反应,在铝表面生成 ▲ ;该反应表示为 ▲ 。
(2)将氯化氢和氨气两种无色气体混合,生成氯化铵固体: ▲ ;反应类型为 ▲ 。
(3)氢氧化钠溶液中滴加硫酸铜溶液反应: ▲ ;反应现象为 ▲ 。
(4)实验室用一氧化碳还原三氧化二铁: ▲ ;硬质粗玻璃管中的现象为 ▲ 。
检验上述反应的气体产物的化学方程式: ▲ ;检验上述反应的固体产物,除了观察
外观、用磁铁吸引以外,还可用化学方法,化学方程式为: ▲ ,此反应 ▲ (填
“放出”或“吸收”)热量。尾气可用 ▲ 法来处理。33.(5分)向装有等量水的A、B、C烧杯中分别加入10g、25g、25gNaNO 固体,充分溶解后,现
3
象如图一所示。
(1)烧杯中的溶液一定属于饱和溶液的是 ▲ (填序号);
(2)图二能表示NaNO 溶解度曲线的是 ▲ (填“甲”或“乙”);
3 [来源:学科网ZXXK]
(3)欲除去混在甲中的少量乙物质将可采用的方法是 ▲ ;
[来源:学科网]
(4)由图二分析,若分别将100g甲、乙的饱和溶液从t℃降温到t℃,对所得溶液的叙
2 1
述正确的 ▲ (填序号)。
A.甲、乙都是饱和溶液 B.所含溶剂质量:甲<乙
C.溶液质量:甲>乙 D.溶质质量分数:甲>乙
34.(5分)实验室用浓盐酸(溶质质量分数为37%,密度为1.18g·mL )配制100g溶质质量
-1
分数为10%的稀盐酸。
(1)计算:需要浓盐酸 ▲ mL,水 ▲ mL。(结果保留小数点后一位)
(2)量取:用规格为 ▲ mL的量筒(从50mL、100 mL中选择)量取浓盐酸,倒入烧杯中,
再用规格为 ▲ mL的量筒(从50mL、100 mL中选择)量取水。
(3)稀释:_ ▲ 。
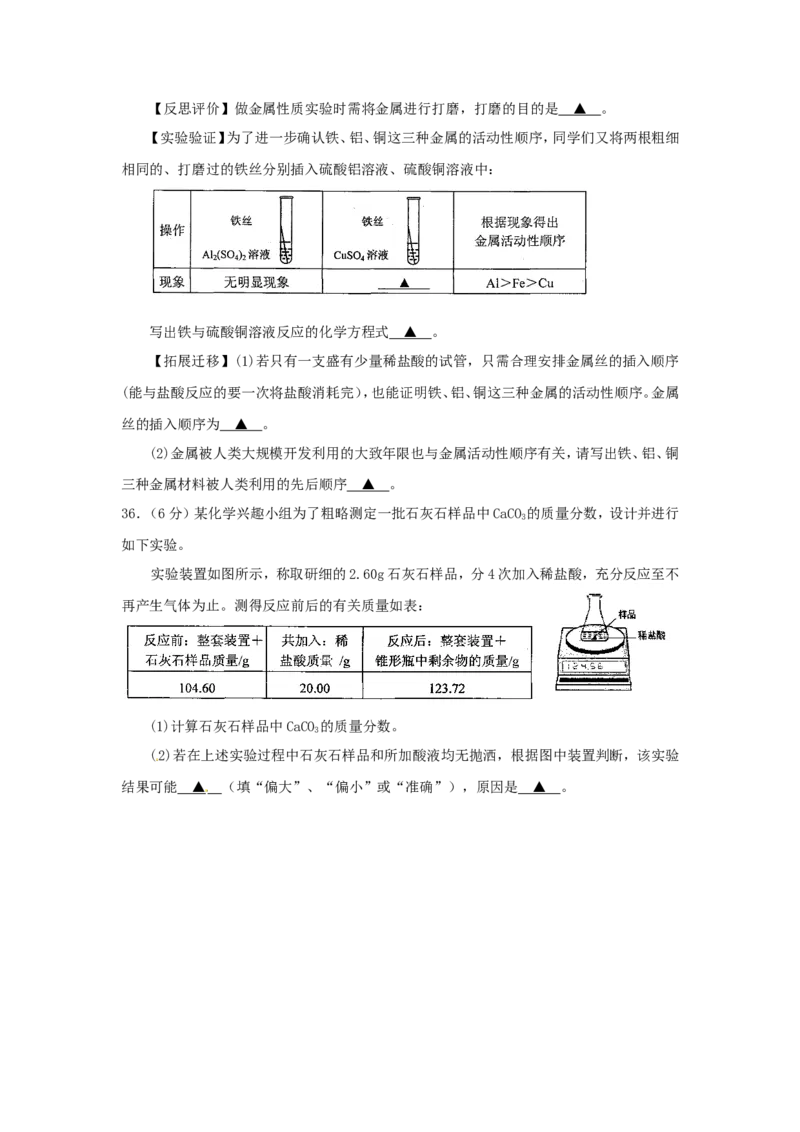
35.(6分)铁、铝、铜是常见的三种金属。同学们发现生活中的铝和铜制品表面一般不用防锈,
而铁制品一般需要做防锈处理。
【提出问题】这是不是因为铁、铝、铜三种金属中铁的活动性最强呢?
【实验探究】同学们对这三种金属的活动性顺序展开了探究,请你参与探究并填写空格。
将粗细相同的铁丝、铝丝、铜丝分别插入体积相同、溶质质量分数也相同的稀盐酸中:
【讨论交流】为什么同一个实验得出了两种结论呢?同学们带着这个疑问查阅了相关资
料,明白了铝丝在稀盐酸中短时间内无气泡,是因为铝表面的氧化物会先与盐酸反应。【反思评价】做金属性质实验时需将金属进行打磨,打磨的目的是 ▲ 。
【实验验证】为了进一步确认铁、铝、铜这三种金属的活动性顺序,同学们又将两根粗细
相同的、打磨过的铁丝分别插入硫酸铝溶液、硫酸铜溶液中:
写出铁与硫酸铜溶液反应的化学方程式 ▲ 。
【拓展迁移】(1)若只有一支盛有少量稀盐酸的试管,只需合理安排金属丝的插入顺序
(能与盐酸反应的要一次将盐酸消耗完),也能证明铁、铝、铜这三种金属的活动性顺序。金属
丝的插入顺序为 ▲ 。
[来源:学§科§网]
(2)金属被人类大规模开发利用的大致年限也与金属活动性顺序有关,请写出铁、铝、铜
三种金属材料被人类利用的先后顺序 ▲ 。
36.(6分)某化学兴趣小组为了粗略测定一批石灰石样品中CaCO 的质量分数,设计并进行
3
如下实验。
实验装置如图所示,称取研细的2.60g石灰石样品,分4次加入稀盐酸,充分反应至不
再产生气体为止。测得反应前后的有关质量如表:
(1)计算石灰石样品中CaCO 的质量分数。
3
(2)若在上述实验过程中石灰石样品和所加酸液均无抛洒,根据图中装置判断,该实验
结果可能 ▲ (填“偏大”、“偏小”或“准确”),原因是 ▲ 。参考答案