文档内容
九年级化学上册期末测试题
姓名_________ 分数_________
(考试时间:100分钟 分数:100分)
可供参考使用相对原子质量:C:12 H:1 O:16 Na:23 Ba:137 Cl:35.5
Fe:56 Zn:65
一.选择题
1.下列变化过程中只发生物理变化的是
A.用燃烧法区别羊毛和合成纤维 B.气球充气过多爆炸
C.以大米、高粱、小麦等粮食为原料酿酒 D.铜制品在潮湿的空气中变成铜
绿
2.下列各组物质中,带点的同种元素的化合价相同的是
A.Cl、NaCl B.NHCl、HNO C. MnO 、KMnO D. P O、Ca (PO)
2 4 3 2 2 4 2 5 3 4 2
3、下列化学方程式书写正确的是 ( )
A. 4P + 5O 2PO B.2Fe + 6HCl = 2FeCl + 3H↑
2 2 5 3 2
点燃
C.Zn + 2HCl = ZnCl + H D.2KMnO = KMnO + MnO + O↑
2 2 4 2 4 2 2
4. 下列有关分子、原子和离子的说法正确的是
A.分子是保持物质性质的一种粒子
B.物体有热胀冷缩现象,主要是因为物体中的粒子大小随温度的改变而改变
C. 分子、原子、离子都可以直接构成物质
D. 在化学反应中,任何离子都不能再分
5.下列实验操作正确的是( )
镊子
100m
进 L
气
pH 试
浓 硫 纸 9.0mL
酸
A.干燥氧气 B.测定溶液pH C.量取9.0mL液体 D.向试管中滴加液体
6.物质的性质决定了物质的用途,下列物质的用途由其化学性质决定的是( )
A.氢气充探空气球 B.酒精作燃料 C.干冰用作人工降雨 D.木材可以制
作桌椅
17.右下图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意
图,
其中不同的圆球代表不同原子。下列说法错误的是( )
A.此反应有单质生成
B.原子在化学变化中是不可分的
催化剂→
C.图中生成物全部是化合物
D.参加反应的两种分子的个数比为1∶1 (反应前) (反应后)
8、某合作学习小组讨论辨析以下说法:①纯净水和矿泉水都是纯净物;②用活性炭
可将硬水进行软化;③太阳能、风能和天然气都是可再生能源;④霉变的大米
(含有黄曲霉毒素)只要洗干净就可放心食用;⑤合金比组成合金的纯金属强度
和硬度更高、抗腐蚀性能更好;⑥回收利用废旧金属不仅可以节约资源,而且可
以减少对环境的污染。其中正确的是( )
A. ⑤⑥ B. ③⑤⑥ C. ② ④⑤ D. ①②③④
9、下列粒子结构示意图中,表示阴离子的是( )
10、过氧化钠(化学式为NaO,其中Na元素显+1价)是潜水艇中的制氧剂,它是一
2 2
种淡黄色粉末,能与物质 R 反应生成氧气,反应的化学方程式为:2NaO +
2 2
2R=2Na CO + O ,则下列有关判断中,错误的是( )
2 3 2
A.NaO 中氧元素化合价为-1价 B.R的化学式为CO
2 2 2
C.NaCO 的相对分子质量为106 D.NaO 中含有氧分子
2 3 2 2
11、苹果中富含苹果酸,苹果酸的化学式为C HO。下列说法正确的是
4 4 4
A.苹果酸中含有12个原子
B.苹果酸的相对分子质量为112
C.苹果酸中碳元素的质量分数约为41.4%
D.苹果酸中C、H、O三元素的质量比为4:4:4
12、下列实验现象中,描述正确的是
A.木炭在氧气中燃烧,有无色刺激性气味气体生成
B.镁条在盐酸中剧烈反应,产生大量气泡,试管壁发热
C.红磷在氧气中剧烈燃烧,放出热量,有大量白色气体生成
D.铁丝在空气中剧烈燃烧,放出大量的热,火星四射,有黑色熔融物溅落瓶底
213. 在一定条件下,在一个密闭容器内发生某反应,测得反应过程中各物质的质量如
下表所示,下列说法错误的是
物质 a b c d
反应前质量(g) 10 10 10 2
反应后质量(g) 待测 2 21 2
A.该反应是化合反应,d可能是催化剂
B.a、b两种物质中元素种类一定与c物质中元素种类相同
C.b物质可能是单质
D.反应后a物质的质量为3g
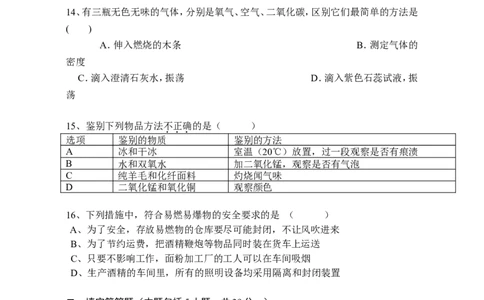
14、有三瓶无色无味的气体,分别是氧气、空气、二氧化碳,区别它们最简单的方法是
( )
A.伸入燃烧的木条 B.测定气体的
密度
C.滴入澄清石灰水,振荡 D.滴入紫色石蕊试液,振
荡
15、鉴别下列物品方法不正确的是( )
选项 鉴别的物质 鉴别的方法
A 冰和干冰 室温(20℃)放置,过一段观察是否有痕渍
B 水和双氧水 加二氧化锰,观察是否有气泡
C 纯羊毛和化纤面料 灼烧闻气味
D 二氧化锰和氧化铜 观察颜色
16、下列措施中,符合易燃易爆物的安全要求的是 ( )
A、为了安全,存放易燃物的仓库要尽可能封闭,不让风吹进来
B、为了节约运费,把酒精鞭炮等物品同时装在货车上运送
C、只要不影响工作,面粉加工厂的工人可以在车间吸烟
D、生产酒精的车间里,所有的照明设备均采用隔离和封闭装置
二、填空简答题(本题包括5小题,共29分。)
16、(5分)用化学用语回答:
(1)天然气的主要成分____________ ;(2)三个带三个单位正电荷的铝离子
_____________;
(3)氧化铁中+3价的铁元素____________________________。
(4)在某原子的结构示意图中 ,x=_________ ,其中y = ___________。
317、(8分) 写出下列反应的化学方程式:
(1)铁丝在氧气中燃烧:_____________________________________;
(2)碳 酸 钠 溶 液 与 稀 盐 酸 溶 液 反 应 , 可 用 于 灭 火 :
__________________________________________;
(3)实 验 室 制 氢 气 用 锌 和 稀 硫 酸 反 应 :
___________________________________________
(4)煅烧石灰石:_____________________________________。
18、(2分)学习了燃烧和灭火后,小槟设计了如右图所示的实验,甲烧杯中有高低两
支燃烧的蜡烛,向甲中加入适量碳酸钠和盐酸,在乙烧杯上倒扣在高低两支蜡烛上方,
请你帮她分析两实验的现象有何区别:
_________________ _
____________________________________________。
19、(6分)2009年9月7日潍坊市政府与中国海洋石油总公司举行石油化工、盐化工
一体化工程启动仪式。石油化工生产中,可通过反应制得甲烷、乙烯、丙烯、苯等重要
有机物。请回答:
(1)有机物中都含有碳元素,碳元素的原子结构示意图是 。
(2)天然气(主要成分是甲烷)可做环保汽车的燃料,它完全燃烧的化学方程式是
。可燃物要燃烧必须具备的条件是
。
(3自然界中消耗二氧化碳的主要途径是光合作用和海水吸收等,海水中的水与二
氧化碳反应的化学方程式是 。
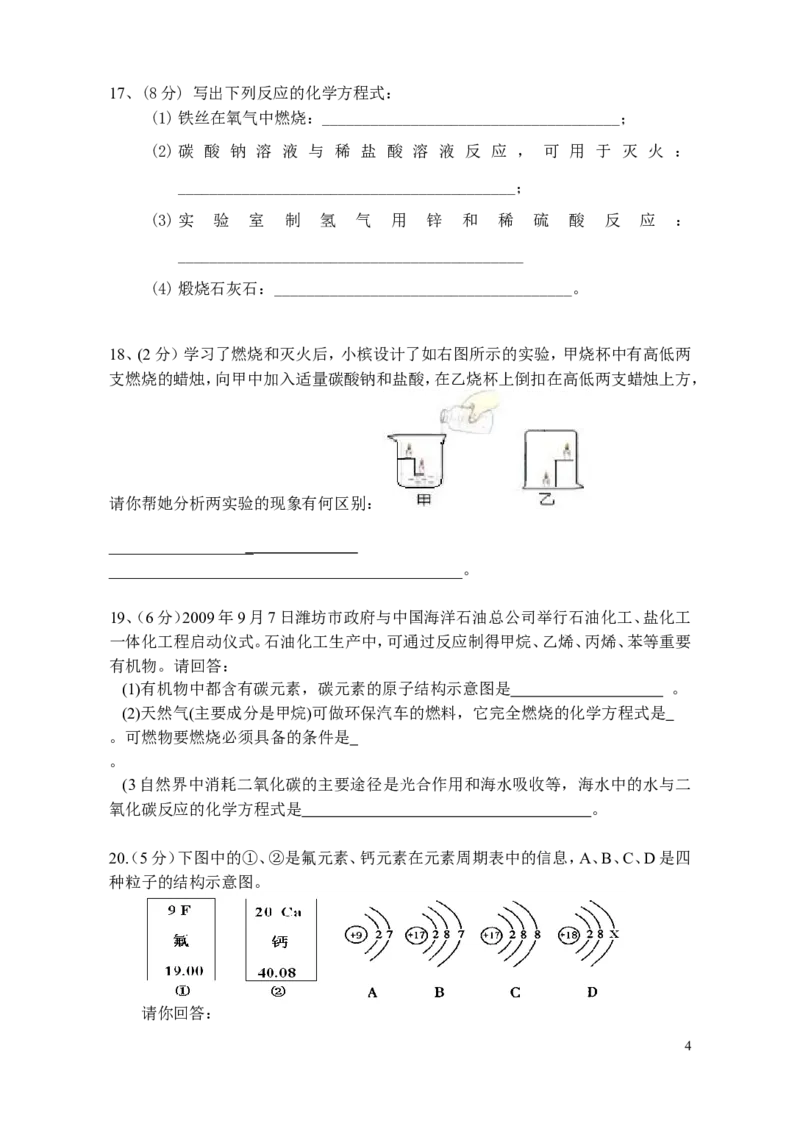
20(. 5分)下图中的①、②是氟元素、钙元素在元素周期表中的信息,A、B、C、D是四
种粒子的结构示意图。
请你回答:
4(1)氟元素的相对原子质量为 ,钙元素的原子序数为 ;
(2)X= ;
(3)A、B、C、D属于同种元素的粒子是 (填序号);
(4)A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似 (填序号)。
21(5分)2008年北京奥运会火炬的燃料是丙烷,丙烷的分子模型如下图所示:
(1)丙烷的化学式是 ;
(2)一个丙烷分子中有 个原子;
(3)丙烷完全燃烧后生成水和二氧化碳,
试写出丙烷完全燃烧的化学方程
式
;
(4)甲烷、乙烷(C H)、丙烷、丁烷(C H )、戊烷(C H )……、n烷(C H)等分子
2 6 4 10 5 12 n y
结构相似的一类有机物,统称为“烷烃”。在C H 中y= (用含n
n y
的代数式表达)。
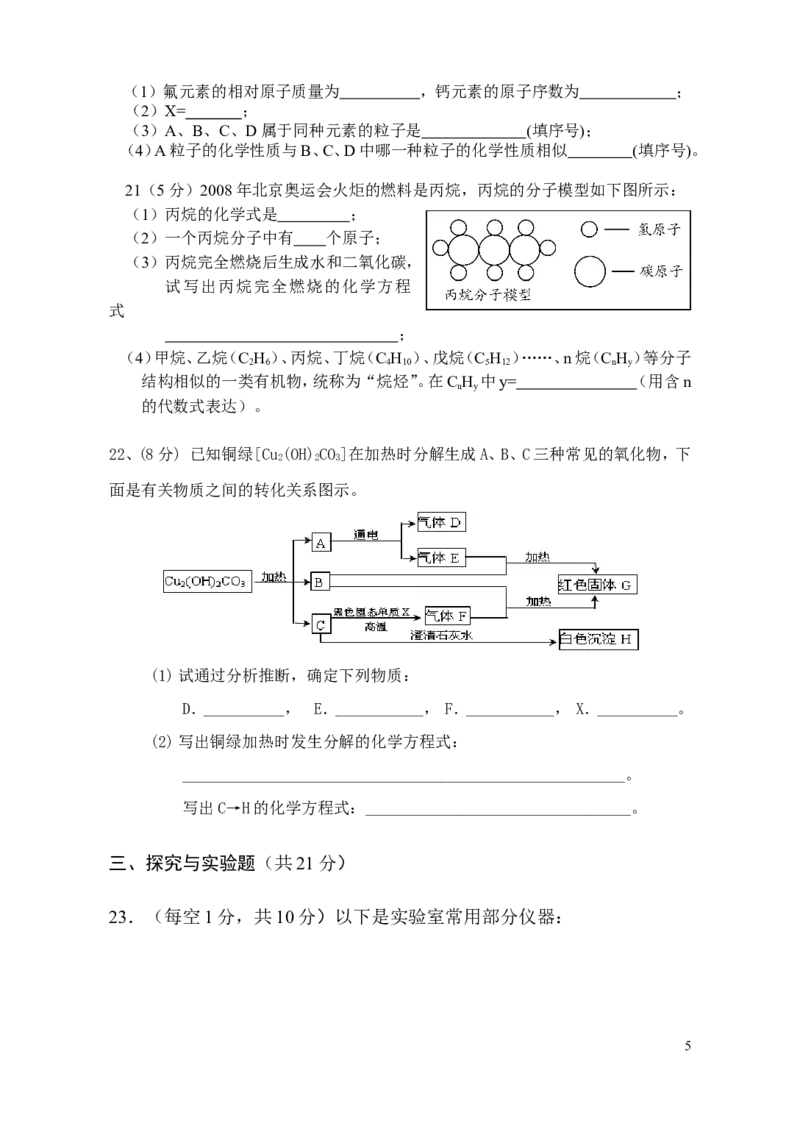
22、(8分) 已知铜绿[Cu(OH)CO]在加热时分解生成A、B、C三种常见的氧化物,下
2 2 3
面是有关物质之间的转化关系图示。
(1)试通过分析推断,确定下列物质:
D.__________, E.___________, F.___________, X.__________。
(2)写出铜绿加热时发生分解的化学方程式:
_______________________________________________________。
写出C→H的化学方程式:_________________________________。
三、探究与实验题(共21分)
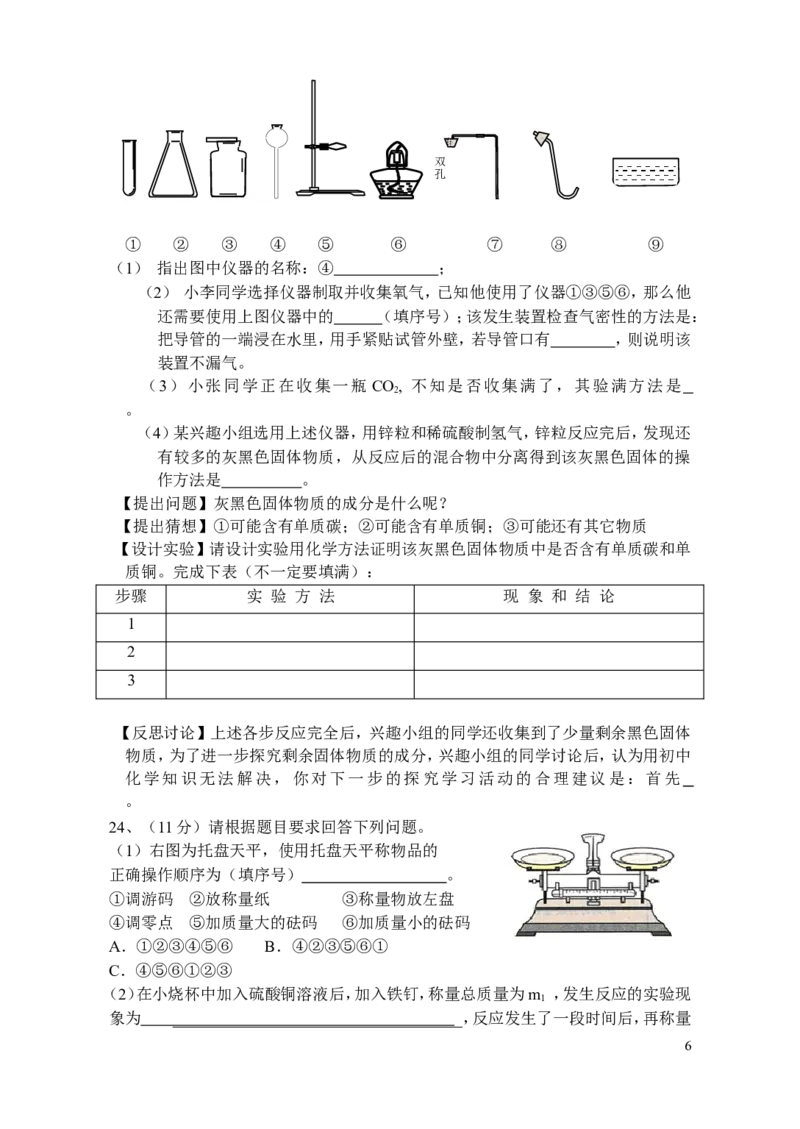
23.(每空1分,共10分)以下是实验室常用部分仪器:
5双
孔
① ② ③ ④ ⑤ ⑥ ⑦ ⑧ ⑨
(1) 指出图中仪器的名称:④ ;
(2) 小李同学选择仪器制取并收集氧气,已知他使用了仪器①③⑤⑥,那么他
还需要使用上图仪器中的 (填序号);该发生装置检查气密性的方法是:
把导管的一端浸在水里,用手紧贴试管外壁,若导管口有 ,则说明该
装置不漏气。
(3)小张同学正在收集一瓶 CO, 不知是否收集满了,其验满方法是
2
。
(4)某兴趣小组选用上述仪器,用锌粒和稀硫酸制氢气,锌粒反应完后,发现还
有较多的灰黑色固体物质,从反应后的混合物中分离得到该灰黑色固体的操
作方法是 。
【提出问题】灰黑色固体物质的成分是什么呢?
【提出猜想】①可能含有单质碳;②可能含有单质铜;③可能还有其它物质
【设计实验】请设计实验用化学方法证明该灰黑色固体物质中是否含有单质碳和单
质铜。完成下表(不一定要填满):
步骤 实 验 方 法 现 象 和 结 论
1
2
3
【反思讨论】上述各步反应完全后,兴趣小组的同学还收集到了少量剩余黑色固体
物质,为了进一步探究剩余固体物质的成分,兴趣小组的同学讨论后,认为用初中
化学知识无法解决,你对下一步的探究学习活动的合理建议是:首先
。
24、(11分)请根据题目要求回答下列问题。
(1)右图为托盘天平,使用托盘天平称物品的
正确操作顺序为(填序号) 。
①调游码 ②放称量纸 ③称量物放左盘
④调零点 ⑤加质量大的砝码 ⑥加质量小的砝码
A.①②③④⑤⑥ B.④②③⑤⑥①
C.④⑤⑥①②③
(2)在小烧杯中加入硫酸铜溶液后,加入铁钉,称量总质量为m ,发生反应的实验现
1
象为 __________________________________ __,反应发生了一段时间后,再称量
6小烧杯及
烧杯内物质的总质量为 m ,则(填“=”“>”
2
“<”)m m 。
1 2
(3)如右图装置中,称量小烧杯中所有物质的质
量m ,
1
然后将小烧杯中的碳酸钠与盐酸完全混合,发生
反应的
化学方程式为 ,
反应发生了一段时间后,再称量小烧杯及烧瓶内物质的总
质量为 m ,则(填“=”“>”“<”)m m ,
2 1 2
其原因为
。
(4)在4A + 5B = 4C + 6D的反应中,C、D相对分子质量之比为15:9,若有1.7g
A与B完全反应生成3gC,则B和C的质量比为 。
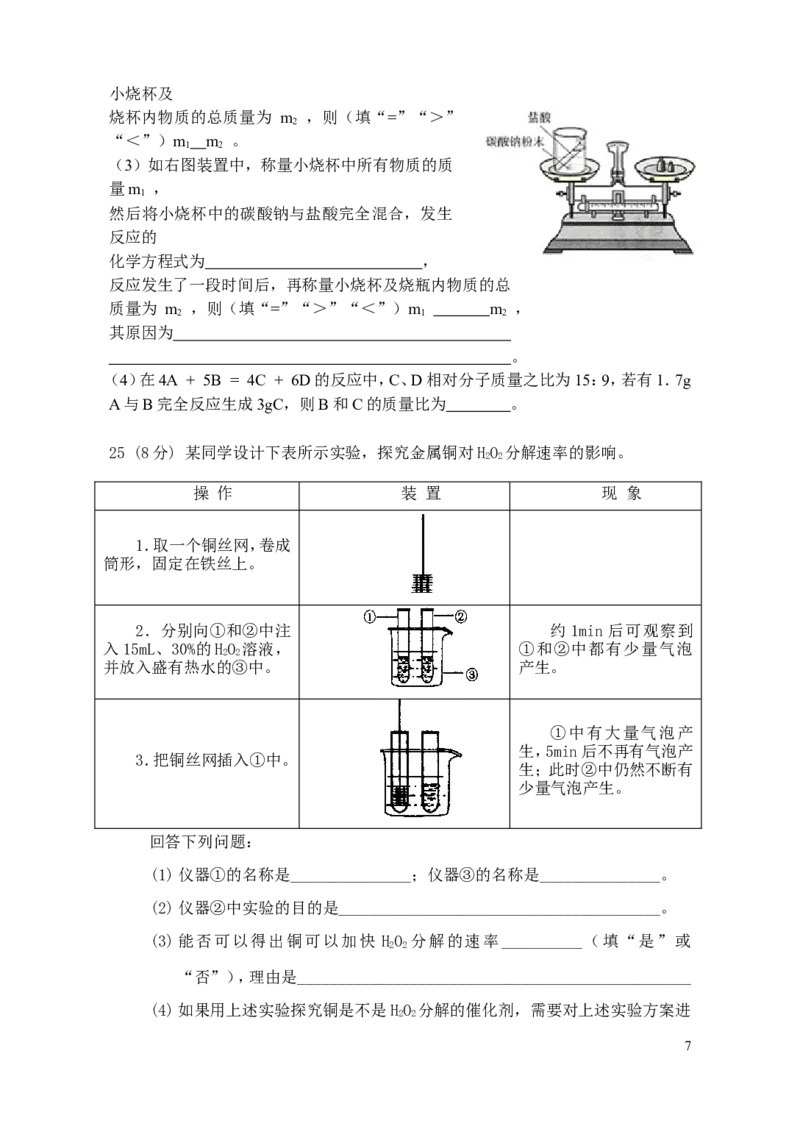
25 (8分) 某同学设计下表所示实验,探究金属铜对HO 分解速率的影响。
2 2
操 作 装 置 现 象
1.取一个铜丝网,卷成
筒形,固定在铁丝上。
2.分别向①和②中注 约1min后可观察到
入15mL、30%的HO 溶液, ①和②中都有少量气泡
2 2
并放入盛有热水的③中。 产生。
①中有大量气泡产
生,5min后不再有气泡产
3.把铜丝网插入①中。
生;此时②中仍然不断有
少量气泡产生。
回答下列问题:
(1)仪器①的名称是_______________;仪器③的名称是_______________。
(2)仪器②中实验的目的是________________________________________。
(3)能否可以得出铜可以加快 HO 分解的速率__________(填“是”或
2 2
“否”),理由是_________________________________________________
(4)如果用上述实验探究铜是不是HO 分解的催化剂,需要对上述实验方案进
2 2
7行补充,其中必要的是_______________。
A.称量实验前铜丝网的质量和实验后干燥铜丝网的质量
B.向仪器②中加入二氧化锰
C.将实验后的铜丝网插入AgNO 溶液中
3
D.将铁丝换成铜丝
E.将过氧化氢溶液加水稀释
四、计算题(本题共10分。)
26、向一定质量的碳酸钙中加入100g稀盐酸,反应一段时间后,称得剩余
溶液的质量为105.6g。求参加反应的碳酸钙质量。
27、氧化铜和铜的混合物2g,用氢气完全还原后铜粉的质量为1.8g,求原
混合物中铜的质量分数是多少?
8