文档内容
人教版九年级下《盐 化肥》精品同步测试
一、我会选择(每小题2分,共30分,每小题只有一个选项符合题意)
1.下列几组物质按酸、碱、盐顺序排列的是( )
A.KNO、NaOH、HCl B.Ca(OH)、HCl、NaCl
3 2
C.HSO 、NaCO、Ba(OH) D.HNO、KOH、CuSO
2 4 2 3 2 3 4
考点:常见的氧化物、酸、碱和盐的判别..
专题:分析比较法.
分析:A、根据酸、碱、盐的定义判断.
B、根据酸、碱、盐的定义判断.
C、根据酸、碱、盐的定义判断.
D、根据酸、碱、盐的定义判断.
解答:解:酸是指电离时生成的阳离子全部是氢离子的化合物,碱是指电离时产生的阴离子全
部是氢氧根离子的化合物,盐是指由金属离子(或铵根离子)与酸根离子构成的化合物.
A、根据酸、碱、盐的定义知,KNO、NaOH、HCl分别是盐、碱、酸,所以错误.
3
B、根据酸、碱、盐的定义知,Ca(OH)、HCl、NaCl分别是碱、酸、盐,所以错误.
2
C、根据酸、碱、盐的定义知,HSO 、NaCO、Ba(OH)分别是酸、盐、碱,所以错误.
2 4 2 3 2
D、根据酸、碱、盐的定义知,HNO、KOH、CuSO 别是酸、碱、盐,所以正确.
3 4
故选D.
点评:物质的分类知识是初中化学的教学难点,也是考查的热点之一,透彻理解有关概念,明
确概念间的相互关系是解题的关键.
2.为了防止病虫害,农民常会对生长过程中的蔬菜喷洒农药.据有关专家介绍,用清水,特别是
碱性溶液浸泡冲洗蔬菜,可使残留在蔬菜上的农药毒性降低.因此买来的蔬菜在食用前可用清
水浸泡一段时间,浸泡蔬菜时最好加入适量下列物质中的( )
A.食醋 B.纯碱 C.白酒 D.白糖
考点:溶液的酸碱性与pH值的关系..
分析:本题考查溶液的酸碱性和习题信息处理.
由信息知用清水,特别是碱性溶液浸泡冲洗蔬菜,可使残留在蔬菜上的农药毒性降低.
因此浸泡蔬菜时最好加入适量的碱性溶液.
解答:解:从四个选项中找出显碱性的物质就是本题答案.
A、食醋显酸性,故A错误.
B、纯碱显碱性,故B正确.
C、白酒显中性,故C错误.
D、白糖显中性,故D错误.
故选B.
点评:要熟悉生活中常见物质的溶液的酸碱性.
3.(2分)下列化肥属于复合肥的是( )
A.NH HPO B.NaNO C.KSO D.NH HCO
4 2 4 3 2 4 4 3
考点:常见化肥的种类和作用..
专题:常见的盐 化学肥料.
分析:含有氮元素的肥料称为氮肥,含有磷元素的肥料称为磷肥,含有钾元素的肥料称为钾
肥,同时含有氮、磷、钾三种元素中的两种或两种以上的肥料称为复合肥.
解答:解:A、NH HPO 中含有磷元素和氮元素,属于复合肥.
4 2 4
B、NaNO 中含有氮元素,属于氮肥.
3
C、KSO 中含有钾元素,属于钾肥.
2 4
D、NH HCO 中含有氮元素,属于氮肥.
4 3
故选:A.点评:本题主要考查化肥的分类方面的知识,确定化肥中营养元素的种类、化肥的分类方法是
正确解答此类题的关键.
4.(2分)(2013•湘潭)植物因缺氮元素会引起叶片发黄,这时应该施加下列哪种肥料( )
A.NH NO B.KSO C.KCl D.Ca(HPO )
4 3 2 4 2 4 2
考点:常见化肥的种类和作用..
专题:常见的盐 化学肥料.
分析:含有氮元素的肥料称为氮肥.氮肥能使农作物枝叶繁茂、叶色浓绿、还能提高产量.
解答:解:植物叶片发黄,说明土壤中缺乏营养元素氮元素.
A、NH NO 中含有氮元素,故正确;
4 3
B、KSO 中不含有氮元素,故错误;
2 4
C、KCl不含有氮元素,故错误;
D、Ca(HPO ) 中不含有氮元素,故错误;
2 4 2
故选A.
点评:解答本题要掌握各种化肥对植物生长的作用,只有这样才能对问题做出正确的判断.
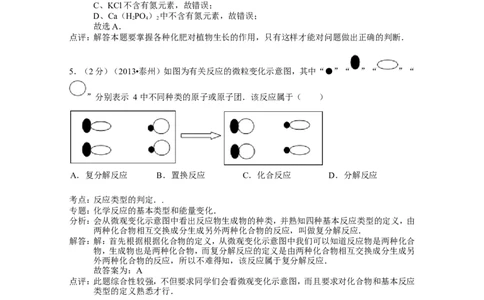
5.(2分)(2013•泰州)如图为有关反应的微粒变化示意图,其中“●”“ ”“ ”“
”分别表示 4 中不同种类的原子或原子团.该反应属于( )
A.复分解反应 B.置换反应 C.化合反应 D.分解反应
考点:反应类型的判定..
专题:化学反应的基本类型和能量变化.
分析:会从微观变化示意图中看出反应物生成物的种类,并熟知四种基本反应类型的定义,由
两种化合物相互交换成分生成另外两种化合物的反应,叫做复分解反应.
解答:解:首先根据根据化合物的定义,从微观变化示意图中我们可以知道反应物是两种化合
物,生成物也是两种化合物,而复分解反应的定义是由两种化合物相互交换成分生成另
外两种化合物的反应,所以不难得知,该反应属于复分解反应.
故答案为:A
点评:此题综合性较强,不但要求同学们会看微观变化示意图,而且要求对化合物和基本反应
类型的定义熟悉才行.
6.(2分)(2011•鄂州)化学影响着社会的发展和人们的生活质量,以下说法正确的是( )
A.焚烧废旧塑料可以解决“白色污染”问题
B.为了加强食品的色、香、味,可以大量使用添加剂
C.糖类和油脂在人体内经氧化放出能量,为机体活动和维持恒定体温提供能量
D.将草木灰和碳铵混合施用有利于提高肥效
考点:白色污染与防治;常见化肥的种类和作用;生命活动与六大营养素..
专题:生产、生活、环保类简答题.
分析:A、根据焚烧秸秆后对空气的影响进行分析.
B、根据添加剂的作用和危害进行分析.
C、根据糖类和油脂的生理机理来分析.D、根据物质的化学性质及肥效进行分析.
解答:解:A、焚烧秸秆后会产生大量烟雾,严重污染环境,造成了二次污染.错误.
B、添加剂有的是激素,有的是致癌物质,过量使用将对人体健康产生影响,如熟肉中加
的着色素是亚硝酸钠,是严重的致癌物,所以添加剂必须严格按照国家食品标准执行.
错误.
C、糖类和油脂在人体内经氧化放出能量,为机体活动和维持恒定体温提供能量,正确.
D、草木灰呈碱性,可以和碳铵反应,生成氨气,降低了氮肥的肥效,错误.
故选C
点评:环境、食品安全、营养健康是人们关注的话题,与此相关的知识一直是中考的考点.
7.(2分)下列有关物质用途的描述,不正确的是( )
A.碳酸氢钠用作治疗胃酸过多症 B.食盐用作调味品
C.含亚硝酸钠的工业盐用来制酱油 D.碳酸钙用作补钙剂
考点:常用盐的用途..
专题:常见的盐 化学肥料.
分析:物质的性质决定物质的用途,根据已有的物质的性质进行分析解答即可.
解答:解:A、碳酸氢钠能与胃酸反应,对人体没有危害,可以用于治疗胃酸过多,正确;
B、食盐是常用的是调味品,正确;
C、亚硝酸钠是有毒的物质,对人体有害,不能用含亚硝酸钠的工业盐用来制酱油,错误;
D、碳酸钙含有钙元素,能用于补钙剂的成分,正确;
故选C.
点评:本题考查的是常见的物质的用途,完成此题,可以依据已有的物质的性质进行.
8.(2分)(2012秋•息县月考)下列各组溶液,相互能发生反应的是( )
①碳酸钠和氯化钙 ②氢氧化钾和盐酸 ③硫酸和氯化钠 ④碳酸钠和氯化
钠 ⑤氯化钠和氢氧化钙.
A.①② B.④⑤ C.③⑤ D.①③
考点:复分解反应及其发生的条件..
专题:化学反应的基本类型和能量变化.
分析:根据复分解反应的含义以及条件进行解答.两种化合物相互交换成分,生成另外两种新
的化合物的反应叫复分解反应;复分解反应发生的条件:生成物中有气体、水或沉淀生
成.
解答:解:①碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,有沉淀生成;②氢氧化钾和盐酸
生成水和氯化钾,有水生成,所以①②能发生反应.而③硫酸和氯化钠、④碳酸钠和氯化
钠、⑤氯化钠和氢氧化钙交换成分后没有水、气体、沉淀生成,故不能反应;
故选:A.
点评:本题考查物质之间的复分解反应,熟悉复分解反应发生的条件及常见物质的状态、溶解
性即可解答,在判断两种物质是否发生反应时,可先假设反应,相互交换成分,观察有无
气体、沉淀或水生成,如有,则能反应.
9.(2分)(2012秋•息县月考)下列叙述中,正确的是( )
A.酸和碱中都一定含有氢、氧两种元素
B.能跟碱反应生成盐和水的化合物不一定是酸
C.有盐参加的反应都是复分解反应
D.生成盐和水的反应都是中和反应
考点:氧化物、酸、碱和盐的概念;中和反应及其应用;复分解反应及其应用..
专题:物质的分类;常见的酸 酸的通性.
分析:根据已有的概念进行分析,酸是指电离时生成的阳离子全部是氢离子的化合物,碱是指电离时生成的阴离子全部是氢氧根离子的化合物,中和反应是指酸和碱的反应.
解答:解:A、酸中一定含有氢元素,不一定含有氧元素,例如HCl,故A错误;
B、能跟碱反应生成盐和水的化合物不一定是酸,例如二氧化碳能与氢氧化钠反应生成
碳酸钠和水,故B正确;
C、有盐参加的反应不一定是复分解反应,例如铁和硫酸铜溶液的反应时置换反应,故C
错误;
D、生成盐和水的反应不一定都是中和反应,例如金属氧化物和酸的反应,故D错误;
故选B.
点评:本题考查了有关的概念,完成此题,可以依据概念进行.要求同学们熟练掌握有关的概
念并理解,以便灵活应用.
10.(2分)(2010•佛山模拟)在“粗盐提纯”实验中,将提纯后的氯化钠与粗盐作比较,以计算
精盐的产率.下列可能引起产率偏高的原因是( )
A.粗盐未完全溶解 B.溶解粗盐的烧杯壁上还蘸有溶液
C.过滤时液面高于滤纸边缘 D.蒸发时有液滴飞溅出去
考点:氯化钠与粗盐提纯;实验数据处理或者误差分析的探究..
专题:化学计算;结合课本知识的信息.
分析:
精盐的产率= ×100%,产率偏高只能是精盐的质量多了或粗盐的质量少了.
解答:解:A、粗盐未完全溶解,导致精盐的量少了,产率偏低,故A错误,
B、溶解粗盐的烧杯壁上蘸有溶液,会导致精盐质量减少,产率偏低,故B错误,
C、滤液高于滤纸边缘,会使没有过滤的液体进入滤液,导致精盐中含有一定的杂质,而
使精盐质量增加,产率偏高,故C正确,
D、液滴飞溅出去,会使精盐质量减少,产率偏低,故D错误.
故选:C.
点评:本题主要考查了对粗盐产率偏高或偏低的分析探究,综合性较强.
11.(2分)下列各组中的物质能发生反应,并且反应后溶液的质量增加的是( )
A.碳酸钠溶液和稀盐酸 B.硫酸钠溶液和氯化钡溶液
C.大理石和稀盐酸 D.碳酸钠溶液和氢氧化钠溶液
考点:复分解反应及其发生的条件;质量守恒定律及其应用..
专题:化学反应的基本类型和能量变化.
分析:根据复分解反应发生的条件,若两种物质相互交换成分有沉淀、气体或水生成,则能发
生化学反应,据此结合质量守恒定律进行分析判断即可.
解答:解:A、碳酸钠溶液和稀盐酸相互交换成分生成氯化钠、水和二氧化碳,有二氧化碳气体
产生,故反应后溶液的质量减小,故选项错误.
B、硫酸钠溶液和氯化钡溶液相互交换成分硫酸钡沉淀和氯化钠,有硫酸钡白色沉淀生
成,故反应后溶液的质量减小,故选项错误.
C、大理石和稀盐酸反应相互交换成分氯化钙、水和二氧化碳,虽然有二氧化碳气体生
成,反应前溶液只是稀盐酸的质量,反应后由于溶解的大理石的质量大于生成的二氧化
碳的质量,所以溶液的质量增加,故选项正确.
D、碳酸钠溶液和氢氧化钠溶液,相互交换成分没有沉淀、气体或水生成,不能发生反应,
故选项错误.
故选:C.
点评:本题难度不大,掌握复分解反应发生的条件(相互交换成分有沉淀、气体或水生成)、质
量守恒定律并能灵活运用是正确解答本题的关键.
12.(2分)(2011•江津区)化学实验室有四个药品橱分类存放药品情况如下:现新购进了一瓶碳酸钾,应存放的药品橱是( )
A.甲橱 B.乙橱 C.丙橱 D.丁橱
考点:物质的简单分类;氧化物、酸、碱和盐的概念..
专题:物质的分类.
分析:首先分析各柜中存放药品的类别,然后观察需要存放的属于哪个类别进行选择.
解答:解:碳酸钾是由金属离子和酸根离子形成的化合物,属于盐,
A、石蕊、甲基橙属于酸碱指示剂,不属于盐,故A错误;
B、硝酸和硫酸属于酸,不能与盐一起存放,故B错误;
C、氢氧化钙和氢氧化钾属于碱,而碳酸钾属于盐,故C错误;
D、硝酸钾和氯化钾属于盐,碳酸钾也属于盐,可以一起存放;
故选D.
点评:在解此类题时,首先分析各柜中存放药品的类别,然后结合需要存放的药品的类别进行
分析.
13.(2分)(2009•番禺区一模)要将待提纯的物质中杂质(括号内为杂质)除去,所用试剂和方
法均正确的是( )
选项 待提纯物质 选用试剂 操作方法
A CuCl (FeCl ) 铜片 过滤
2 2
B CaO(CaCO ) 盐酸 蒸发
3
C Cu(Fe) 硫酸铜溶液 过滤,洗涤
D FeCl 溶液(盐酸) 氢氧化钠溶液 过滤,洗涤
3
A.A B.B C.C D.D
考点:物质除杂或净化的探究..
专题:物质的分离、除杂、提纯与共存问题.
分析:A、根据铜和铁的活泼性进行解答;
B、根据所选用试剂能否与杂质反应,能否与待提纯物质反应;
C、根据所选用试剂能否与杂质反应,能否与待提纯物质反应;
D、根据所选用试剂能否与杂质反应,能否与待提纯物质反应;
解答:解:A、铜的活泼性没有铁强,铜不可以将氯化亚铁中的铜铁置换出来,所以杂质氯化亚
铁就除不去,故A错误;
B、盐酸既可以和碳酸钙反应,也会和氧化钙反应,既除去了杂质,也除去了原物质,故B
错误;
C、铁会和硫酸铜反应,而铜不会和硫酸铜反应,加硫酸铜后,铁溶解在硫酸铜中,经过过
滤剩下铜,故C正确;
D、氢氧化钠能和盐酸反应,也能和氯化铁反应,达不到除杂的目的,故D错误.
故选C.
点评:解答除杂质题的原则是在除杂质的同时,不能引入新的杂质,可以根据物质的性质方面
进行分析、判断,从而得出正确的结论
14.(2分)(2010•济南)有三瓶失去标签的无色溶液,已知它们分别是HCl溶液、BaCl 溶液、
2
NaOH溶液中的一种.下列四种试剂中,能将上述三种无色溶液一次鉴别出来的是( )
A.CuSO 溶液 B.HSO 溶液 C.MgCl 溶液 D.酚酞试液
4 2 4 2考点:酸、碱、盐的鉴别..
专题:物质的鉴别题.
分析:把所选试剂加入被鉴别的溶液中出现三种不同的现象即可鉴别出来,一般为有气泡产
生、有沉淀产生、没有明显现象.
解答:解:A、硫酸铜分别与三种溶液混合,产生白色沉淀的是氯化钡,产生蓝色沉淀的是氢氧
化钠,不反应的是盐酸,故可以鉴别.
B、硫酸分别与三种溶液混合,产生白色沉淀的是氯化钡,无现象的是盐酸和氢氧化钠,
不能区分盐酸和氢氧化钠,故B错误;
C、氯化镁分别与三种溶液混合,产生白色沉淀的是氢氧化钠,无现象的是盐酸和氯化
钡,不能区分盐酸和氯化钡,故C错误;
D、将酚酞试液分别滴入三种溶液中,变红色的是氢氧化钠溶液,不变色的是盐酸和氯化
钡溶液,故D错误;
故选A
点评:解答本题要掌握酸碱盐的化学性质及混合时的实验现象方面的内容,只有这样才能对相
关方面的问题做出正确的判断.
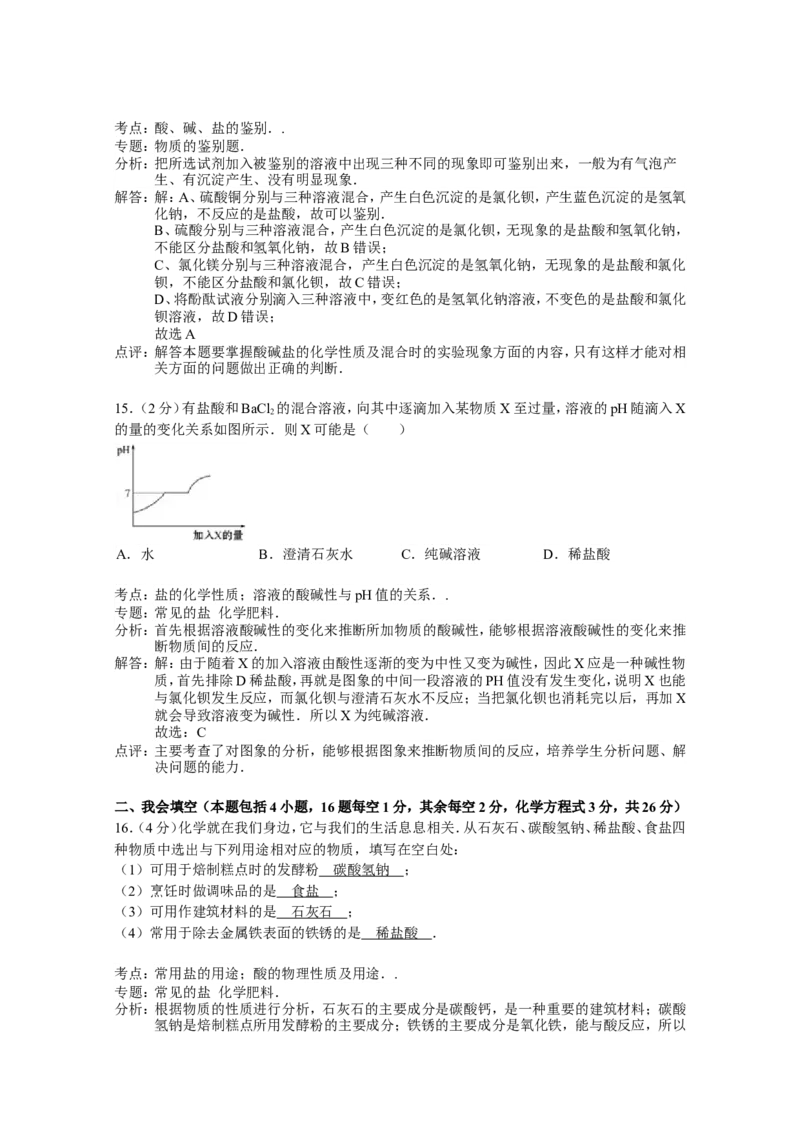
15.(2分)有盐酸和BaCl 的混合溶液,向其中逐滴加入某物质X至过量,溶液的pH随滴入X
2
的量的变化关系如图所示.则X可能是( )
A.水 B.澄清石灰水 C.纯碱溶液 D.稀盐酸
考点:盐的化学性质;溶液的酸碱性与pH值的关系..
专题:常见的盐 化学肥料.
分析:首先根据溶液酸碱性的变化来推断所加物质的酸碱性,能够根据溶液酸碱性的变化来推
断物质间的反应.
解答:解:由于随着X的加入溶液由酸性逐渐的变为中性又变为碱性,因此X应是一种碱性物
质,首先排除D稀盐酸,再就是图象的中间一段溶液的PH值没有发生变化,说明X也能
与氯化钡发生反应,而氯化钡与澄清石灰水不反应;当把氯化钡也消耗完以后,再加X
就会导致溶液变为碱性.所以X为纯碱溶液.
故选:C
点评:主要考查了对图象的分析,能够根据图象来推断物质间的反应,培养学生分析问题、解
决问题的能力.
二、我会填空(本题包括4小题,16题每空1分,其余每空2分,化学方程式3分,共26分)
16.(4分)化学就在我们身边,它与我们的生活息息相关.从石灰石、碳酸氢钠、稀盐酸、食盐四
种物质中选出与下列用途相对应的物质,填写在空白处:
(1)可用于焙制糕点时的发酵粉 碳酸氢钠 ;
(2)烹饪时做调味品的是 食盐 ;
(3)可用作建筑材料的是 石灰石 ;
(4)常用于除去金属铁表面的铁锈的是 稀盐酸 .
考点:常用盐的用途;酸的物理性质及用途..
专题:常见的盐 化学肥料.
分析:根据物质的性质进行分析,石灰石的主要成分是碳酸钙,是一种重要的建筑材料;碳酸
氢钠是焙制糕点所用发酵粉的主要成分;铁锈的主要成分是氧化铁,能与酸反应,所以经常用稀盐酸除去铁表面的铁锈;食盐是重要的调味品,据此解答.
解答:解:(1)碳酸氢钠是焙制糕点所用发酵粉的主要成分故填:碳酸氢钠;
(2)食盐是重要的调味品,故填:食盐;
(3)石灰石的主要成分是碳酸钙,是一种重要的建筑材料故填:石灰石;
(4)铁锈的主要成分是氧化铁,能与酸反应,所以经常用稀盐酸除去铁表面的铁锈,故
填:稀盐酸.
点评:本题考查了常见物质的用途,完成此题,可以依据已有的物质的性质进行.
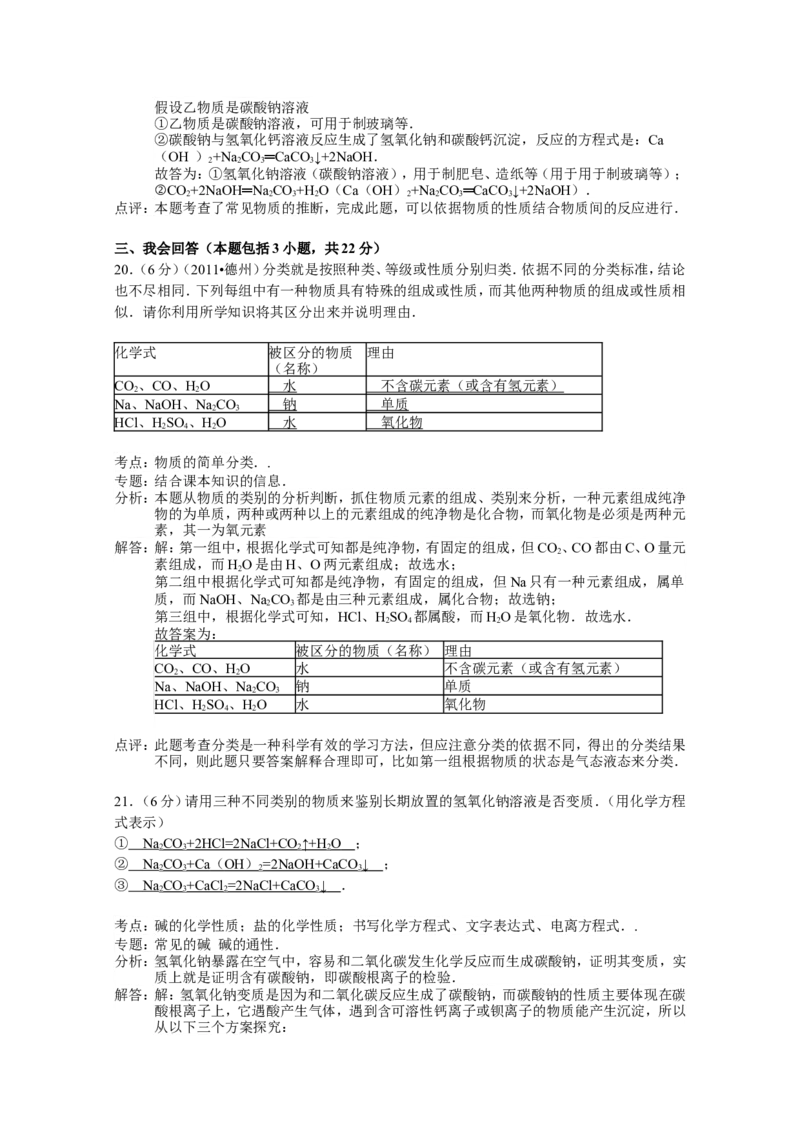
17.(7分)(2012•青岛)归纳总结是学习化学的重要方法,下面是某同学对有关知识的总结,请
你填写空格:
(1)逻辑关系:物质类属间存在着如下关系,其中酸和盐属于 并列 关系.
(2)转化关系:下图表示几种化合物能通过一步反应转化为含镁化合物M.
图中物质M属于 盐 (选填“单质”、“氧化物”、“酸”、“碱”或“盐”);从①﹣③表
示的化学反应中任选一个,写出化学方程式: MgO+H SO ═MgSO+H O .
2 4 4 2
考点:氧化物、酸、碱和盐的概念;物质的相互转化和制备;书写化学方程式、文字表达式、电离
方程式..
专题:概念关系型;压轴实验题;物质的制备.
分析:根据图示进行分析,酸和盐属于化合物,为并列关系;根据图示可以看出硫酸锌、氧化镁
和硫酸都能转化生成M,故M是硫酸镁,属于盐类物质,氧化镁能与硫酸反应生成硫酸
镁.
解答:解:(1)酸和盐属于化合物,为并列关系,故填:并列;
(2)硫酸锌、氧化镁和硫酸都能转化生成M,M是含镁化合物,故M是硫酸镁,属于盐类
物质,氧化镁能与硫酸反应生成硫酸镁和水,故填:盐,MgO+H SO ═MgSO+H O.
2 4 4 2
点评:本题考查了物质类别的关系以及物质间的转化,完成此题,可以依据物质的性质进行.
18.(8分)小敏到舅父家做客,看到一个化肥“蛇皮袋”上印有如图所示的标签,还嗅到一股
臭味.她向舅父解释说:
(1)这包化肥是 氮 肥,能促使作物茎叶生长茂盛,叶色浓绿;每袋化肥中含该元素至少为
8.69 kg.
(2)该化肥 受热 时容易分解,在施用时不能与 碱 性物质混用.考点:常见化肥的种类和作用;铵态氮肥的检验;混合物中某元素的质量计算..
专题:常见的盐 化学肥料.
分析:(1)根据化肥的主要成分就可判断;根据硝酸铵的化学式可计算出碳酸氢铵中N的质量
分数,进而求出每袋化肥中含该元素的质量.
(2)欲正确解答本题,须知碳酸氢铵的性质.
解答:解:(1)由标签信息可知,碳酸氢铵中含有氮元素,是氮肥;每袋中氮元素的质量至少为:
50 kg×17.38%=8.69 kg;
(2)碳酸氢铵不稳定,受热易分解;铵态氮肥与碱性物质反应会放出氨气而失去肥效,所
以在施用时不能与碱性物质混用.
故答案为:(1)氮;8.69;(2)受热;碱.
点评:本题主要考查学生对硝酸铵这种化肥的成分的认识,以及根据化学式计算的能力.
19.(7分)(2013•云霄县校级模拟)不同类别的物质间存在着一定的关系,如图所示.(“﹣”
表示相连的两种物质能发生反应,“→”表示某种物质可转化为另一种物质.)
(1)碳酸钠溶液、氢氧化钠溶液和稀盐酸之间的变化关系如图所示,回答下列问题:
①乙物质是 氢氧化钠溶液(或碳酸钠溶液) ,它的一种用途是 用于制肥皂、造纸等(用于
用于制玻璃等) .
②写出“乙→丙”的化学方程式 CO +2NaOH═Na CO+H O ( Ca ( OH )
2 2 3 2
+Na CO═CaCO ↓+2NaOH ) .
2 2 3 3
考点:物质的鉴别、推断;酸的化学性质;盐的化学性质;书写化学方程式、文字表达式、电离方
程式..
专题:常见物质的推断题.
分析:根据提供的物质结合物质的性质进行分析,甲能与乙和丙反应,而给出的物质中,盐酸
能与氢氧化钠和碳酸钠反应,故甲是盐酸,乙能转化生成丙,而二氧化碳能与氢氧化钠
反应生成碳酸钠,碳酸钠能与氢氧化钙反应生成氢氧化钠,故乙和丙不确定,据此解答
即可.
解答:解:由题中物质之间的关系可以可出,甲能与乙和丙反应,而给出的物质中,盐酸能与氢
氧化钠和碳酸钠反应,故甲是盐酸,乙能转化生成丙,而二氧化碳能与氢氧化钠反应生
成碳酸钠,碳酸钠能与氢氧化钙反应生成氢氧化钠,故乙和丙不确定,
假设乙是氢氧化钠溶液
①乙物质是氢氧化钠溶液,可用于制肥皂、造纸等.
②氢氧化钠与二氧化碳的反应,生成碳酸钠和水,反应的方程式是:
CO+2NaOH═Na CO+H O.
2 2 3 2假设乙物质是碳酸钠溶液
①乙物质是碳酸钠溶液,可用于制玻璃等.
②碳酸钠与氢氧化钙溶液反应生成了氢氧化钠和碳酸钙沉淀,反应的方程式是:Ca
(OH )+Na CO═CaCO↓+2NaOH.
2 2 3 3
故答为:①氢氧化钠溶液(碳酸钠溶液),用于制肥皂、造纸等(用于用于制玻璃等);
②CO +2NaOH═Na CO+H O(Ca(OH)+Na CO═CaCO↓+2NaOH).
2 2 3 2 2 2 3 3
点评:本题考查了常见物质的推断,完成此题,可以依据物质的性质结合物质间的反应进行.
三、我会回答(本题包括3小题,共22分)
20.(6分)(2011•德州)分类就是按照种类、等级或性质分别归类.依据不同的分类标准,结论
也不尽相同.下列每组中有一种物质具有特殊的组成或性质,而其他两种物质的组成或性质相
似.请你利用所学知识将其区分出来并说明理由.
化学式 被区分的物质 理由
(名称)
CO、CO、HO 水 不含碳元素(或含有氢元素)
2 2
Na、NaOH、NaCO 钠 单质
2 3
HCl、HSO 、HO 水 氧化物
2 4 2
考点:物质的简单分类..
专题:结合课本知识的信息.
分析:本题从物质的类别的分析判断,抓住物质元素的组成、类别来分析,一种元素组成纯净
物的为单质,两种或两种以上的元素组成的纯净物是化合物,而氧化物是必须是两种元
素,其一为氧元素
解答:解:第一组中,根据化学式可知都是纯净物,有固定的组成,但CO、CO都由C、O量元
2
素组成,而HO是由H、O两元素组成;故选水;
2
第二组中根据化学式可知都是纯净物,有固定的组成,但Na只有一种元素组成,属单
质,而NaOH、NaCO 都是由三种元素组成,属化合物;故选钠;
2 3
第三组中,根据化学式可知,HCl、HSO 都属酸,而HO是氧化物.故选水.
2 4 2
故答案为:
化学式 被区分的物质(名称) 理由
CO、CO、HO 水 不含碳元素(或含有氢元素)
2 2
Na、NaOH、NaCO 钠 单质
2 3
HCl、HSO 、HO 水 氧化物
2 4 2
点评:此题考查分类是一种科学有效的学习方法,但应注意分类的依据不同,得出的分类结果
不同,则此题只要答案解释合理即可,比如第一组根据物质的状态是气态液态来分类.
21.(6分)请用三种不同类别的物质来鉴别长期放置的氢氧化钠溶液是否变质.(用化学方程
式表示)
① N aCO+2HCl=2NaCl+CO ↑+H O ;
2 3 2 2
② N aCO +Ca ( OH ) =2NaOH+CaCO ↓ ;
2 3 2 3
③ N aCO+CaCl =2NaCl+CaCO ↓ .
2 3 2 3
考点:碱的化学性质;盐的化学性质;书写化学方程式、文字表达式、电离方程式..
专题:常见的碱 碱的通性.
分析:氢氧化钠暴露在空气中,容易和二氧化碳发生化学反应而生成碳酸钠,证明其变质,实
质上就是证明含有碳酸钠,即碳酸根离子的检验.
解答:解:氢氧化钠变质是因为和二氧化碳反应生成了碳酸钠,而碳酸钠的性质主要体现在碳
酸根离子上,它遇酸产生气体,遇到含可溶性钙离子或钡离子的物质能产生沉淀,所以
从以下三个方案探究:(1)方案一:滴加几滴稀盐酸,有气泡逸出,说明变质,化学方程式为:
NaCO+2HCl=2NaCl+CO ↑+H O;
2 3 2 2
(2)方案二:滴加几滴Ca(OH) 溶液,有沉淀出现,说明变质,化学方程式为:
2
NaCO+Ca(OH)=2NaOH+CaCO ↓;
2 3 2 3
(3)方案三:滴入几滴CaCl 溶液,有沉淀出现,说明变质,化学方程式为:
2
NaCO+CaCl =2NaCl+CaCO ↓.
2 3 2 3
故答案为:(1)NaCO+2HCl=2NaCl+CO ↑+H O;
2 3 2 2
(2)NaCO+Ca(OH)=2NaOH+CaCO ↓;
2 3 2 3
(3)NaCO+CaCl =2NaCl+CaCO ↓.
2 3 2 3
点评:本题考查了氢氧化钠的性质以及碳酸根的检验方法,注意检验碳酸根离子时,所用的试
剂在发生化学反应时必须有明显的实验现象,且必须考虑到氢氧化钠和碳酸钠都显碱
性.
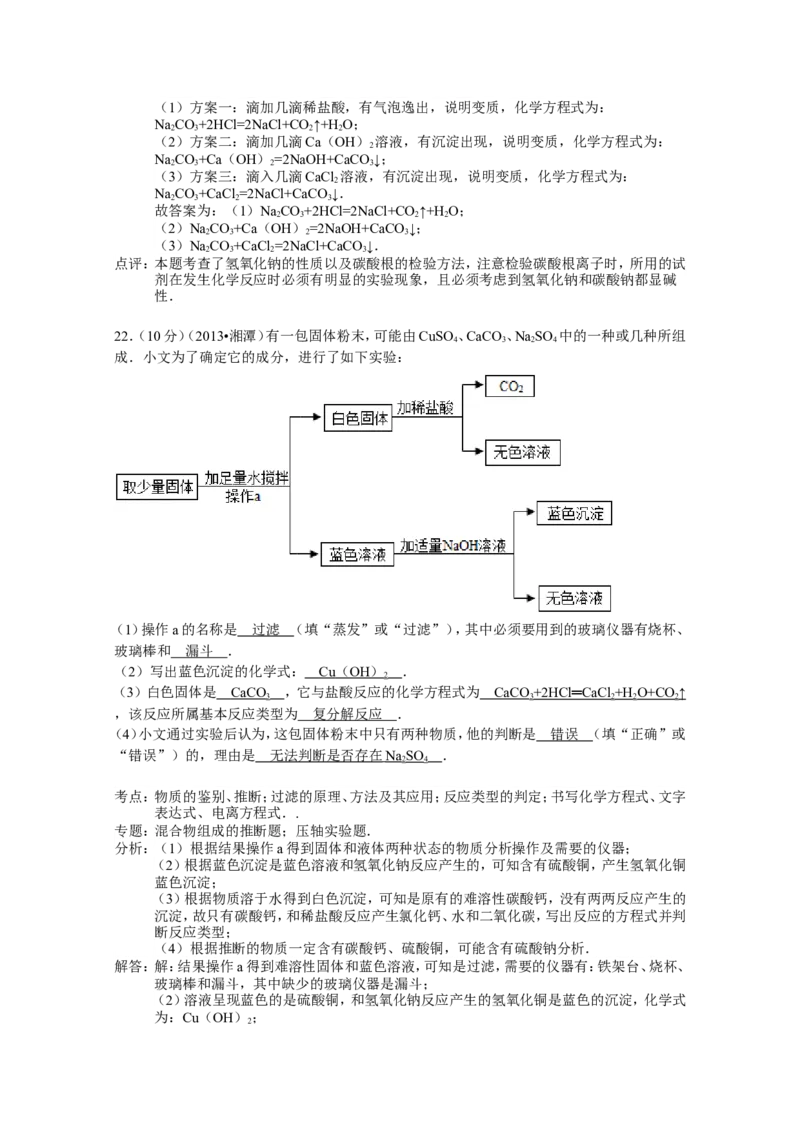
22.(10分)(2013•湘潭)有一包固体粉末,可能由CuSO 、CaCO 、NaSO 中的一种或几种所组
4 3 2 4
成.小文为了确定它的成分,进行了如下实验:
(1)操作a的名称是 过滤 (填“蒸发”或“过滤”),其中必须要用到的玻璃仪器有烧杯、
玻璃棒和 漏斗 .
(2)写出蓝色沉淀的化学式: C u ( OH ) .
2
(3)白色固体是 CaCO ,它与盐酸反应的化学方程式为 CaCO +2HCl═CaCl +H O+CO↑
3 3 2 2 2
,该反应所属基本反应类型为 复分解反应 .
(4)小文通过实验后认为,这包固体粉末中只有两种物质,他的判断是 错误 (填“正确”或
“错误”)的,理由是 无法判断是否存在 N aSO .
2 4
考点:物质的鉴别、推断;过滤的原理、方法及其应用;反应类型的判定;书写化学方程式、文字
表达式、电离方程式..
专题:混合物组成的推断题;压轴实验题.
分析:(1)根据结果操作a得到固体和液体两种状态的物质分析操作及需要的仪器;
(2)根据蓝色沉淀是蓝色溶液和氢氧化钠反应产生的,可知含有硫酸铜,产生氢氧化铜
蓝色沉淀;
(3)根据物质溶于水得到白色沉淀,可知是原有的难溶性碳酸钙,没有两两反应产生的
沉淀,故只有碳酸钙,和稀盐酸反应产生氯化钙、水和二氧化碳,写出反应的方程式并判
断反应类型;
(4)根据推断的物质一定含有碳酸钙、硫酸铜,可能含有硫酸钠分析.
解答:解:结果操作a得到难溶性固体和蓝色溶液,可知是过滤,需要的仪器有:铁架台、烧杯、
玻璃棒和漏斗,其中缺少的玻璃仪器是漏斗;
(2)溶液呈现蓝色的是硫酸铜,和氢氧化钠反应产生的氢氧化铜是蓝色的沉淀,化学式
为:Cu(OH);
2(3)白色固体是难溶性的碳酸钙,化学式为:CaCO ;稀盐酸和碳酸钙反应生成氯化钙、
3
水和二氧化碳,故反应的化学方程式为:CaCO +2HCl═CaCl +H O+CO↑;该反应是酸和
3 2 2 2
盐发生的复分解反应;
(4)经过推断一定含有的物质是碳酸钙、硫酸铜,而硫酸钠不影响实验的现象,所以可能
含有硫酸钠,因此认为这包固体粉末中只有两种物质的判断是错误的,因为无法判断是
否存在NaSO .
2 4
故答案为:(1)过滤;漏斗;
(2)Cu(OH);
2
(3)CaCO ;CaCO +2HCl═CaCl +H O+CO↑;复分解反应;
3 3 2 2 2
(4)错误;无法判断是否存在NaSO .
2 4
点评:在解此类题时,首先从物质的颜色、物质之间的关系,然后根据现象推出可以确定存在
或不存在的物质,对于现象不能确定的只能再设计实验进行验证.
四、我会实验(本题包括1小题,每空2分,化学方程式3分,共16分)
23.(16分)(2011•咸宁)碳酸氢钠是一种重要的盐类物质,在生活中用途广泛.小红同学设计
实验对碳酸氢钠的性质进行了探究.请你参与她的探究活动.
【探究实验1】碳酸氢钠溶液的酸碱性.
【实验方案】取少量该固体加入试管中,加适量水溶解,再滴入几滴酚酞试液,振荡.现象:溶液
变成浅红色.结论:① 碳酸氢钠溶液呈碱性 .
【探究实验2】能与酸反应.
【实验方案】取少量该固体加入试管中,滴加稀盐酸.现象:② 产生气泡 .反应的化学方程
式为:③ NaHCO +HCl=NaCl+H O+CO ↑ .
3 2 2
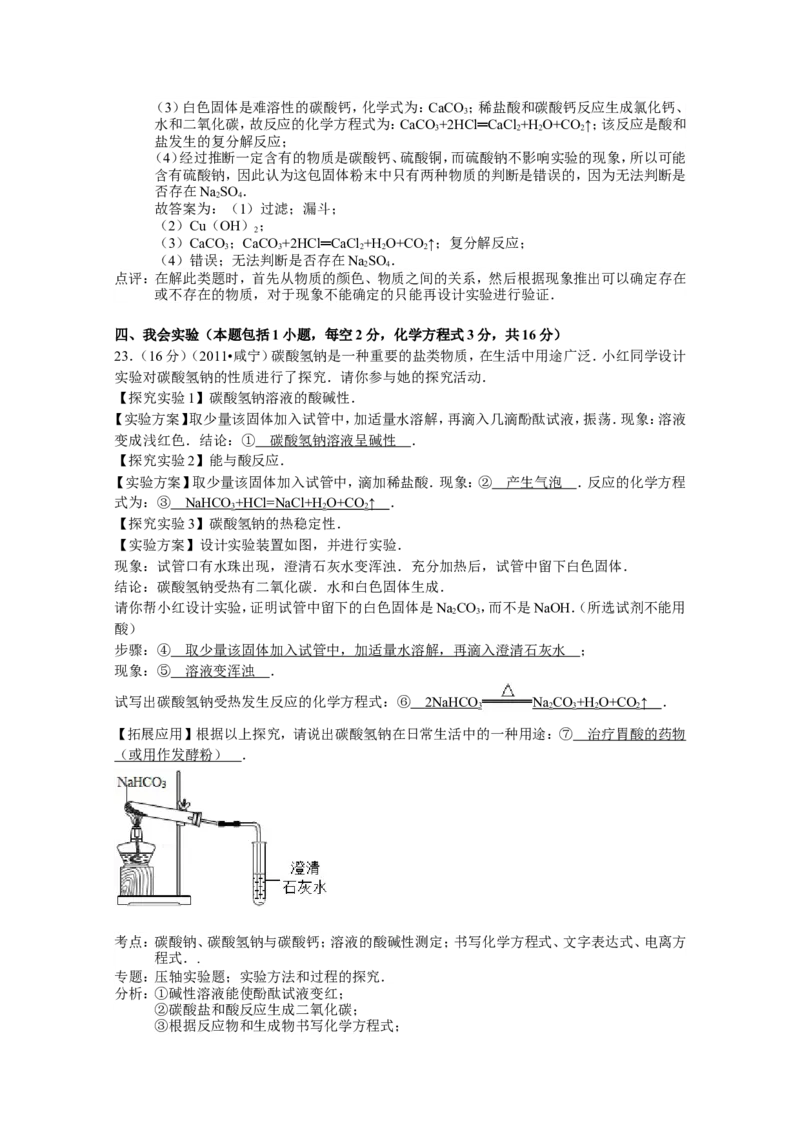
【探究实验3】碳酸氢钠的热稳定性.
【实验方案】设计实验装置如图,并进行实验.
现象:试管口有水珠出现,澄清石灰水变浑浊.充分加热后,试管中留下白色固体.
结论:碳酸氢钠受热有二氧化碳.水和白色固体生成.
请你帮小红设计实验,证明试管中留下的白色固体是NaCO,而不是NaOH.(所选试剂不能用
2 3
酸)
步骤:④ 取少量该固体加入试管中,加适量水溶解,再滴入澄清石灰水 ;
现象:⑤ 溶液变浑浊 .
试写出碳酸氢钠受热发生反应的化学方程式:⑥ 2NaHCO NaCO+H O+CO ↑ .
3 2 3 2 2
【拓展应用】根据以上探究,请说出碳酸氢钠在日常生活中的一种用途:⑦ 治疗胃酸的药物
(或用作发酵粉) .
考点:碳酸钠、碳酸氢钠与碳酸钙;溶液的酸碱性测定;书写化学方程式、文字表达式、电离方
程式..
专题:压轴实验题;实验方法和过程的探究.
分析:①碱性溶液能使酚酞试液变红;
②碳酸盐和酸反应生成二氧化碳;
③根据反应物和生成物书写化学方程式;④区分碳酸钠和氢氧化钠可用钙盐的溶液,根据生成沉淀区别.
⑤碳酸钙不溶于水;
⑥根据碳酸氢钠能和酸反应的性质填空.
解答:解:①因为碱性溶液能使酚酞变红,所以此现象说明碳酸氢钠溶液呈碱性.
②碳酸氢钠和盐酸反应二氧化碳气体,会看到溶液中能产生气泡.③反应的化学方程式
为:NaHCO +HCl=NaCl+H O+CO↑.
3 2 2
④碳酸钠能和氢氧化钙反应生成沉淀,而氢氧化钠和氢氧化钙不反应,故取少量该固体
加入试管中,加适量水溶解,再滴入澄清石灰水;
⑤二氧化碳能使澄清石灰水溶液变浑浊.
⑥碳酸氢钠受热发生反应的化学方程式 2NaHCO NaCO+H O+CO↑.
3 2 3 2 2
⑦碳酸氢钠能和酸反应生成二氧化碳,故可以用作治疗胃酸的药物(或用作发酵粉).
故答案为:①碳酸氢钠溶液呈碱性(说明:回答“碳酸氢钠呈碱性”或“碱性”不给分)
②产生气泡
③NaHCO +HCl=NaCl+H O+CO↑
3 2 2
④取少量该固体加入试管中,加适量水溶解,再滴入澄清石灰水
⑤溶液变浑浊(说明:根据④设计方案的不同⑤的现象也不同,只要合理均可给分)
⑥2NaHCO NaCO+H O+CO↑
3 2 3 2 2
⑦治疗胃酸的药物(或用作发酵粉)
点评:碳酸盐和酸反应放出二氧化碳气体,二氧化碳能使石灰水变浑浊,碳酸盐溶液能和钙盐
溶液反应生成沉淀.
五、我会计算(本题包括1小题,共6分)
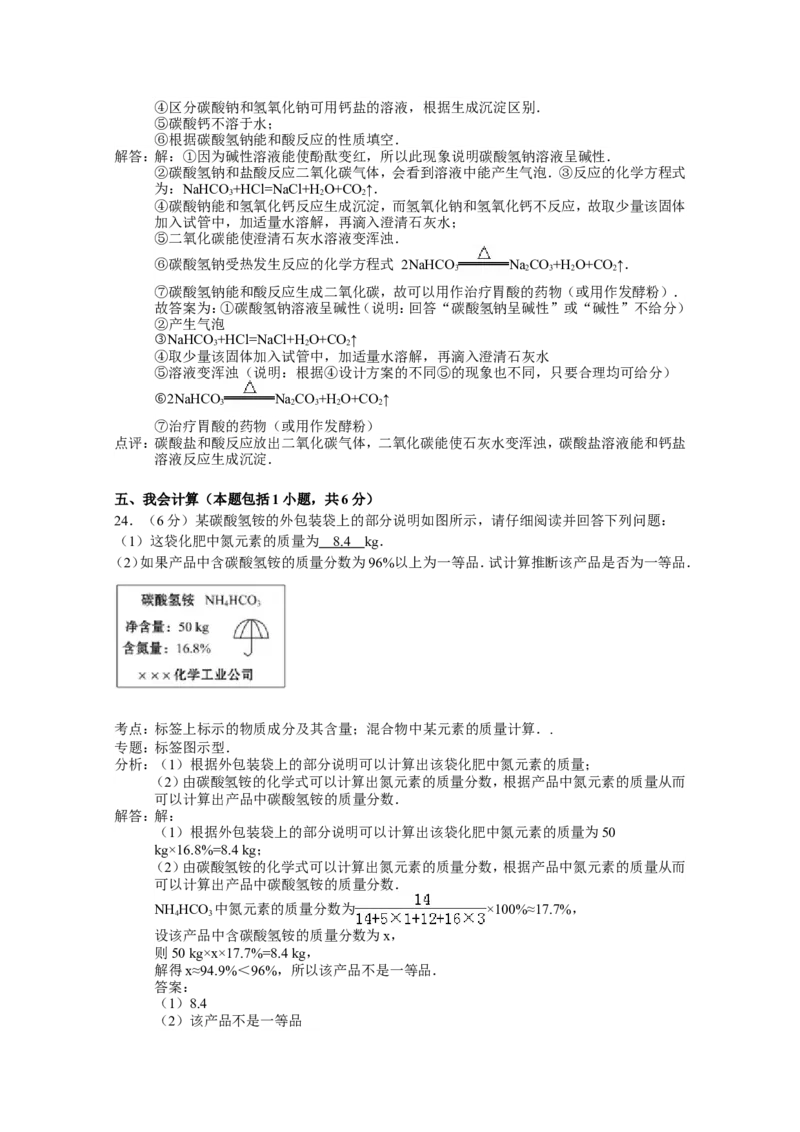
24.(6分)某碳酸氢铵的外包装袋上的部分说明如图所示,请仔细阅读并回答下列问题:
(1)这袋化肥中氮元素的质量为 8. 4 kg.
(2)如果产品中含碳酸氢铵的质量分数为96%以上为一等品.试计算推断该产品是否为一等品.
考点:标签上标示的物质成分及其含量;混合物中某元素的质量计算..
专题:标签图示型.
分析:(1)根据外包装袋上的部分说明可以计算出该袋化肥中氮元素的质量;
(2)由碳酸氢铵的化学式可以计算出氮元素的质量分数,根据产品中氮元素的质量从而
可以计算出产品中碳酸氢铵的质量分数.
解答:解:
(1)根据外包装袋上的部分说明可以计算出该袋化肥中氮元素的质量为50
kg×16.8%=8.4 kg;
(2)由碳酸氢铵的化学式可以计算出氮元素的质量分数,根据产品中氮元素的质量从而
可以计算出产品中碳酸氢铵的质量分数.
NH HCO 中氮元素的质量分数为 ×100%≈17.7%,
4 3
设该产品中含碳酸氢铵的质量分数为x,
则50 kg×x×17.7%=8.4 kg,
解得x≈94.9%<96%,所以该产品不是一等品.
答案:
(1)8.4
(2)该产品不是一等品点评:会根据化学式进行有关相对分子质量、某元素质量分数的计算是解此类题的关健.