文档内容
人教版九年级下《盐 化肥》单元检测试卷
可能用到的相对原子质量:H—1 C—12 O—16 Cl—35.5 Na—23 Ba—137
班别 学号 姓名 评分
一、 单项选择题(每小题3分,共30分,每小题只有一个选项符合题意)
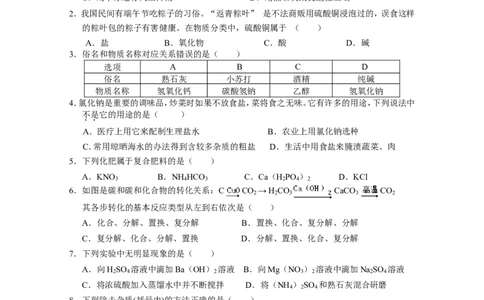
1.下列物质在使用过程中与化学性质无关的是( )
A.用小苏打治疗胃酸过多 B.用食醋除去暖水瓶中的水垢
C.用干冰进行人工降雨 D.用熟石灰改良酸性土壤
2.我国民间有端午节吃粽子的习俗。“返青粽叶” 是不法商贩用硫酸铜浸泡过的,误食这样
的粽叶包的粽子有害健康。在物质分类中,硫酸铜属于 ( )
A.盐 B.氧化物 C.酸 D.碱
3.俗名和物质名称对应关系错误的是( )
选项 A B C D
俗名 熟石灰 小苏打 酒精 纯碱
物质名称 氢氧化钙 碳酸氢钠 乙醇 氢氧化钠
4.氯化钠是重要的调味品,炒菜时如果不放食盐,菜将食之无味。它有许多的用途,下列说法中
不是它的用途的是( )
A.医疗上用它来配制生理盐水 B.农业上用氯化钠选种
C.常用晾晒海水的办法得到含较多杂质的粗盐 D.生活中用食盐来腌渍蔬菜、肉
5.下列化肥属于复合肥料的是( )
A.KNO
3
B.NH
4
HCO
3
C.Ca(H
2
PO
4
)
2
D.KCl
6.如图是碳和碳和化合物的转化关系:C CO
2
→ H
2
CO
3
CaCO
3
CO
2
其各步转化的基本反应类型从左到右依次是( )
A.化合、分解、置换、复分解 B.置换、化合、复分解、分解
C.复分解、化合、分解、置换 D.分解、置换、化合、复分解
7.下列实验中无明显现象的是( )
A.向H SO 溶液中滴加Ba(OH) 溶液 B.向Mg(NO ) 溶液中滴加Na SO 溶液
2 4 2 3 2 2 4
C.将浓硫酸加入蒸馏水中并不断搅拌 D.将(NH ) SO 和熟石灰混合研磨
4 2 4
8.下列除去杂质(括号内)的方法正确的是( )
A.CO(CO ):通过灼热的氧化铜 B. NaOH溶液(Na CO):加适量稀盐酸
2 2 3
C.NaCl溶液(盐酸):加热蒸发 D.铁粉(氧化铜粉末):加入足量稀硫酸
9.完成对四组无色溶液成分探究后,小江记录了以下四组数据,其中没有错误的一组是( )
A.HSO Na SO KNO B.CuSO HSO NaCl
2 4 2 4 3 4 2 4
C.NaOH NaCl HCl D.HSO Na CO NaNO
2 4 2 3 3
10.向含有稀盐酸和氯化铜的混合溶液中滴加NaOH溶液,下图曲线中描述正确的是 ( )
溶液 溶液 沉淀 沉淀
pH 质量/g 质量/g 质量/g
·
7
0 V(NaOH)/ 0 V(NaOH)/ 0 V(NaOH)/ 0 V(NaOH)/
mL mL mL mLA B C D
二、填空与简答题(本大题共4小题,共23分)
11.(4分)用给定化合价的五种元素写出符合要求的物质化学式:
(1)可溶性碱 (2)水溶液呈蓝色的盐
(3)单质 (4)氮的氧化物
12.(5分)小明经常利用所学知识帮父母解决实际问题们。
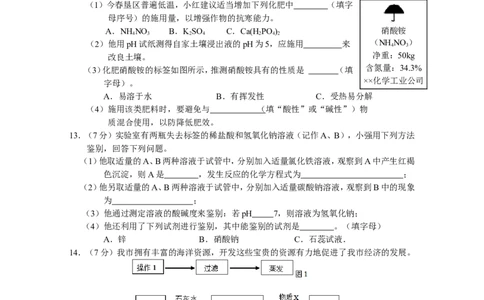
(1)今春垦区普遍低温,小红建议适当增加下列化肥中 (填字
母序号)的施用量,以增强作物的抗寒能力。
A.NH NO B.KSO C.Ca(HPO ) 硝酸铵
4 3 2 4 2 4 2
(2)他用pH试纸测得自家土壤浸出液的pH为5,应施用 来 (NH
4
NO
3
)
改良土壤。 净重:50kg
(3)化肥硝酸铵的标签如图所示,推测硝酸铵具有的性质是 (填 含氮量:34.3%
字母)。
××化学工业公司
A.易溶于水 B.有挥发性 C.受热易分解
(4)施用该类肥料时,要避免与 (填“酸性”或“碱性”)物
质混合使用,以防降低肥效。
13.(7分)实验室有两瓶失去标签的稀盐酸和氢氧化钠溶液(记作A、B),小强用下列方法
鉴别,回答下列问题。
(1)他取适量的A、B两种溶液于试管中,分别加入适量氯化铁溶液,观察到A中产生红褐
色沉淀,则A是 ,发生反应的化学方程式为 ;
(2)他另取适量的A、B两种溶液于试管中,分别加入适量碳酸钠溶液,观察到B中的现象
为 ;
(3)他通过测定溶液的酸碱度来鉴别:若pH 7,则溶液为氢氧化钠;
(4)他还利用了下列试剂进行鉴别,其中能鉴别的试剂是 。(填字母)
A.锌 B.硝酸钠 C.石蕊试液.
14.(7分)我市拥有丰富的海洋资源,开发这些宝贵的资源有力地促进了我市经济的发展。
(1)从海 水中提取出的
粗盐中除了NaCl外,还含有泥沙等杂质。请完善下列实验室中除去泥沙等杂质的实
验步骤,并回答相关问题:(如图1)其中操作1的名称是 ;在过滤操作中要用
到的玻璃仪器有烧杯、玻璃棒、 (填仪器名称);在加热蒸发过程中,当蒸发
皿中 时,停止加热。
(2)上述除去泥沙后的澄清滤液中,还含有Ca2+、Mg2+等阳离子。要想知道该滤液是硬水还
是软水,可加入 进行检验。(3)海水提取出粗盐后的母液中,还含有较多的氯化镁,用氯化镁可制得金属镁。工业上从
母液中提取氯化镁的过程如图2:物质X是 (填名称),反应2的反应方
程式是 。
三、综合应用题(本题包括2小题,共15分)
15.(7分)如图中所涉及到的物质均为初中化学常见物质,它
们之间的转化关系如图所示(图中反应条件均已略去)。
其中A、D都是碱,A俗称熟石灰;A溶液与C溶液能发生
复分解反应;E是天然气的主要成分。请回答下列问题:
(1)请写出图中A、E的化学式: A E
(2)写出下列反应的化学方程式:①D与F反应
②B与G反应 ,属于 反应。
16 .(8
分)
轻
质
碳酸钙广泛应用于橡胶、塑料、油漆、水性涂料以及造纸等行业,日常生活中的牙膏也常用
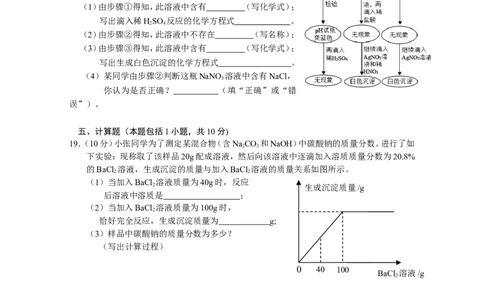
它作摩擦剂。目前轻质碳酸钙的生产主要是碳化法,工艺流程见下图:
请分析轻质碳酸钙的生产流程,回答下列问题:
(1)物质B的化学式为 ;
(2)在A→B之间,过滤操作的目前是 ;
(3)在B+C→CaCO 的过程中,应控制物质C的流量,原因是 (用化学方
3
程式表示,下同);
(4)生产轻质碳酸钙的方法很多请再设计一种制备方法 。
四、实验与探究题(本题包括2小题,共22分)
17.(12分)丽丽的爸爸旅游归来,带回一些钟乳硒石块送给了她。丽丽和同学们想验证钟乳石
的主要成分是碳酸盐,于是她们将其中一块钟乳石带进实验室进行探究。
(1)请你帮助丽丽完成以下探究方案。
实验操作 预期的实验现象 实验结论
①取一小块钟乳石于试管中,向试管中 有气泡生成 钟乳石的主要成分是碳
加入 ,观察现象。 酸盐
② ,观察现象。
(2)查阅资料得知钟乳石的主要成分是碳酸钙(假设杂质不溶于水且不与酸发生反应)。上述
预期的实验现象中有气泡生成的反应的化学方程式为 。
(3)实验后,为了防止废液腐蚀下水管道或对水质产生不良影响,丽丽将所有的废液倒入了
一个洁净的烧杯中。她取样测定了废液的酸碱性,你认为她选择的试剂可以是
。测试后得知该废液显酸性,则烧杯中废液的溶质是 。(4)丽丽向烧杯中的废液里加入过量的 (填序号)能使废液呈中性,过滤后才可安
全排放。
①碳酸钙 ②熟石灰 ③生石灰 ④氢氧化钠
18.(10分)实验时,有同学不小心放错了胶头滴管,使得
NaNO 溶液的试剂瓶中可能混入NaCl、NaOH、NaCO
3 2 3
和 NaSO 中的一种或几种。为了验证,他进行了如图
2 4
所
示的实验。请回答:
(1)由步骤①得知,此溶液中含有 (写化学式);
写出滴入稀HSO 反应的化学方程式 。
2 4
(2)由步骤②得知,此溶液中不存在 (写名称);
(3)由步骤③得知,此溶液中含有 (写化学式);
写出生成白色沉淀的化学方程式 。
(4)某同学由步骤②判断这瓶NaNO 溶液中含有NaCl,
3
你认为是否正确? (填“正确”或“错
误”)。
五、计算题(本题包括1小题,共10分)
19.(10分)小张同学为了测定某混合物(含NaCO 和NaOH)中碳酸钠的质量分数。进行了如
2 3
下实验:现称取了该样品20g配成溶液,然后向该溶液中逐滴加入溶质质量分数为20.8%
的BaCl 溶液,生成沉淀的质量与加入BaCl 溶液的质量关系如图所示。
2 2
(1)当加入BaCl 溶液质量为40g时,反应
2 生成沉淀质量/g
后溶液中溶质是 ;
(2)当加入BaCl 溶液质量为100g时,
2
恰好完全反应,生成沉淀质量为 g;
(3)样品中碳酸钠的质量分数为多少?
(写出计算过程)
0 40 100
BaCl 溶液/g
2
参考答案
一.单项选择题(每小题3分,共30分,每小题只有一个选项符合题意)
1、C 2、A 3、D 4、C 5、A 6、B 7、B 8、C 9、A 10、D
二、填空与简答题(本大题共4小题,共23分)
11.(每空1分共4分)(1)Ba(OH) (2)Cu(NO ) (3)N (4)NO
2 3 2 2 2 5
12.(每空1分共4分)(1)C (2)熟石灰 (3)AC (4)碱13.(共7分)(1)NaOH;FeCl + 3NaOH==Fe(OH) ↓+ 3NaCl;
3 3
(2)有气泡产生 (3)> (4)AC
14.(共7分)(1)溶解、漏斗、有大量固体析出。(2)肥皂水(3)盐酸、
Mg(OH) +2HCl===MgCl +2H O
2 2 2
三、综合应用题(本题包括2小题,共15分)
15.(共7分)(1)A:Ca(OH) E:CH(2)①NaOH+CO==NaCO+HO
2 4 2 2 3 2
② CaCO +2HCl==CaCl +H O+CO ↑;复分解反应
3 2 2 2
16.(共8分)(1)Ca(OH) (2)除去不反应(不溶于水)的CaCO
2 3
(3)CaCO +H O+CO==Ca(HCO )
3 2 2 3 2
(4)NaCO + Ca(OH) ===CaCO ↓ + 2NaOH
2 3 2 3
四、实验与探究题(本题包括2小题,共22分)
17.(共12分)(1)实验操作:①稀盐酸②将①产生的气体通入澄清石灰水。实验现象:石灰
水变浑浊(2)CaCO +2HCl==CaCl +H O+CO ↑
3 2 2 2
(3)紫色石蕊;CaCl 和HCl (4)①
2
18.(共10分)(1)NaOH、2NaOH+H SO ===Na SO +2H O ( 2)硫酸钠和碳酸钠 (3)NaCl
2 4 2 4 2
NaCl+AgNO ===AgCl↓+NaNO (4)错误
3 3
五、计算题(本题包括1小题,共10分)
19.(共10分)(1)NaCl、NaOH、NaCO (2)19.7
2 3
(3)设样品中含碳酸钠的质量为X,反应生成的碳酸钡的质量为y
NaCO + BaCl ===BaCO ↓ + 2NaCl
2 3 2 3
106 208 197
x 100g×20.8% y
解:x=10.6g y=19.7g
10.6g/20g×100%=53%