文档内容
第十一单元 《盐 化肥》检测题
班级 姓名 成绩
相对原子质量:H-1 C-12 O-16 Cl-35.5 Ca-40
一、选择题(本题共10小题,每小题只有一个选项符合题意。每小题2分,共20分)
1 . 下 列 生 活 中 常 见 物 质 的 主 要 成 分 , 属 于 盐 的 是
( )
A.醋 B.生石灰 C.纯碱 D.烧碱
2.植物在缺氮的情况下,生长迟缓、叶色发黄。这时需施用的化肥是
( )
A.KCl B.NH HCO C.KCO D.Ca(HPO )
4 3 2 3 2 4 2
3.下列各组物质名称不代表同一物质的一组是 ( )
A.氢氧化钙、熟石灰 B.氢氧化钠、苛性钠
C.碳酸钠、纯碱 D.碳酸氢钠、苏打
4.下列关于化肥的说法不正确的是 ( )
A.CO(NH)(尿素)、(NH )SO 和NaNO 均可用作氮肥
2 2 4 2 4 3
B.加熟石灰研磨能闻到刺激性气味是磷肥的性质
C.区分各种化肥一般先观察外观、溶解性,再观察化学反应中的现象
D.过度使用化肥可能导致土壤酸化、水域氮和磷含量升高
5.在贝壳上滴稀盐酸,能产生使澄清石灰水浑浊的气体, 这说明贝壳中含有的离子是 (
)
A.CO2- B.SO 2- C.Ca2+ D.OH-
3 4
6.胃酸能帮助消化,但过多的胃酸会危害健康。可用于治疗胃酸过多的物质是 ( )
A.NaHCO B.NaCl C.CaO D.NaOH
3
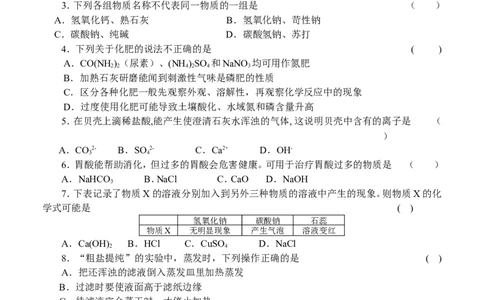
7.下表记录了物质X的溶液分别加入到另外三种物质的溶液中产生的现象。则物质X的化
学式可能是 ( )
氢氧化钠 碳酸钠 石蕊
物质X 无明显现象 产生气泡 溶液变红
A.Ca(OH) B.HCl C.CuSO D.NaCl
2 4
8.“粗盐提纯”的实验中,蒸发时,下列操作正确的是 ( )
A.把还浑浊的滤液倒入蒸发皿里加热蒸发
B.过滤时要使液面高于滤纸边缘
C.待滤液完全蒸干时,才停止加热
D.蒸发皿中出现多固体时,停止加热
9.下表列出了除去物质中所含少量杂质的方法,其中错误的是( )
物质 所含杂质 除去杂质的方法
A CO CO 通过足量氢氧化钠溶液,干燥
2
B NaCl 泥沙 溶解、过滤、蒸发
C NaOH溶液 NaCO 加入足量稀盐酸至不再产生气泡
2 3
D Cu(NO) 溶液 AgNO 加入过量的铜粉,过滤
32 3
10.“NaCl+CO +NH+H O==NaHCO ↓+NHCl”是著名的“侯氏制碱法”的重要反应。
2 3 2 3 4
1下面是4位同学对该反应涉及的有关知识发表的部分见解。其中不正确的是 ( )
析出固体后的溶
该条件下NaHCO
3 液为NaHCO 的
的溶解度较小 3
不饱和溶液
NaHCO 不
3 从该反应可
是纯碱
以获得氮肥
A B C D
二、选择题(本题共5小题,每小题有一个或两个选项符合题意。错选、多选不给分。有两个答案
的,只选一个且正确,给1分。每小题2分,共10分)
11.进行蒸发操作时不需要使用的仪器是 ( )
A.蒸发皿 B.漏斗 C.酒精灯 D.玻璃棒
12.下列说法正确的是 ( )
A.碳酸钠广泛用于玻璃、造纸、纺织和洗涤剂的生产
B.pH小于5.6的雨水是酸雨
C.胃酸过多的病人在空腹时最好多喝一些柠檬汁
D.用pH试纸伸入某溶液中测定其pH
13.在一定条件下,下列转化不能由一步反应实现的是 ( )
A.Fe O→FeCl B.HCO→CO C.CuCl→Cu D.NaCO→NaOH
2 3 2 2 3 2 2 2 3
14.下列离子能在pH=2的无色溶液中大量共存的是 ( )
A.SO 2-、Fe3+、Na+、OH- B.K+、SO 2-、Cu2+、NO -
4 4 3
C .Cl-、K+、SO 2-、Na+ D.Ca2+、Cl-、CO2-、Na+
4 3
15.现有铁、氧化铁、稀盐酸、氢氧化钙溶液、碳酸钠溶液五种物质.存在如图所示的相互反
应和转化关系。图中“——”表示两端的物质间可以发生化学反应.“→”表示物质间存在相
应的转化关系。下列判断合理的是( )
X Y 铁
A.X一定是碳酸钠溶液
B.Y一定是稀盐酸
C.N转化为铁的反应都属于置换反应
M N
D.X、Y、M两两之间都可以发生复分解反应
三、填空题(本题共4小题,第16、17题化学式每空1分,其余每空2分,共36分)
16.写出具有下列用途的物质(或其主要成分)的化学式。请从以下物质中选择:
甲烷、食盐、熟石灰、小苏打、石灰石、盐酸、硝酸钾、
①用于除去铁锈的是 ; ②可作为化肥的是 ;
③可作为调味品的是 ; ④用于改良酸性土壤的是 ;
⑤用于焙制糕点所用的发酵粉的是 ; ⑥天然气的主要成分是 。
17.只用Ca、C、O、Cl、H五种元素的一种或几种,按要求填空:
⑴ 各写出一个化学式:①氧化物________,②酸________,③碱________,④盐_________。
⑵ 各写出一个化学方程式:
①分解反应__________________________;②复分解反应__________________________。
18.某化学兴趣小组设计出下列粗盐提纯的实验方案,请你一起来完成以下问题。
2泥沙
操作①
含有泥沙的 含有泥沙的 操作②
粗盐3.0g 混合液
操作③
溶液 精盐2.0g
(1) 操作①②③的名称依次是 、 、 ;若在操作②结束后发现
溶液仍浑浊,应采取的措施是 。
(2) 实施操作③时玻璃棒要不断搅拌,直到 时停止加热;
(3)计算精盐的产率是 (计算结果取小数点后一位);
(4)若精盐的产率偏低,则可能的原因是 (填字母序号)
A.过滤时滤纸有破损
B.蒸发时有固体溅出
C.溶解含有泥沙的粗盐时,加入的水量过多
D.转移精盐时,蒸发皿中有残留的固体
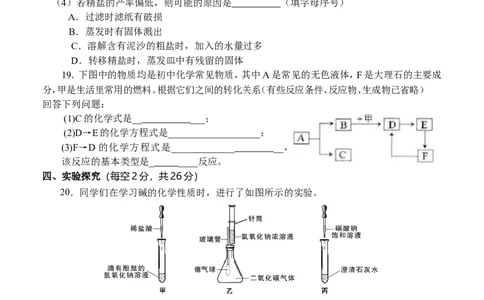
19.下图中的物质均是初中化学常见物质,其中A是常见的无色液体,F是大理石的主要成
分,甲是生活里常用的燃料。根据它们之间的转化关系(有些反应条件、反应物、生成物已省略)
回答下列问题:
(1)C的化学式是__ ___;
(2)D→E的化学方程式是___________________;
(3)F→D的化学方程式是_____________ __,
该反应的基本类型是_ ____反应。
四、实验探究(每空2分,共26分)
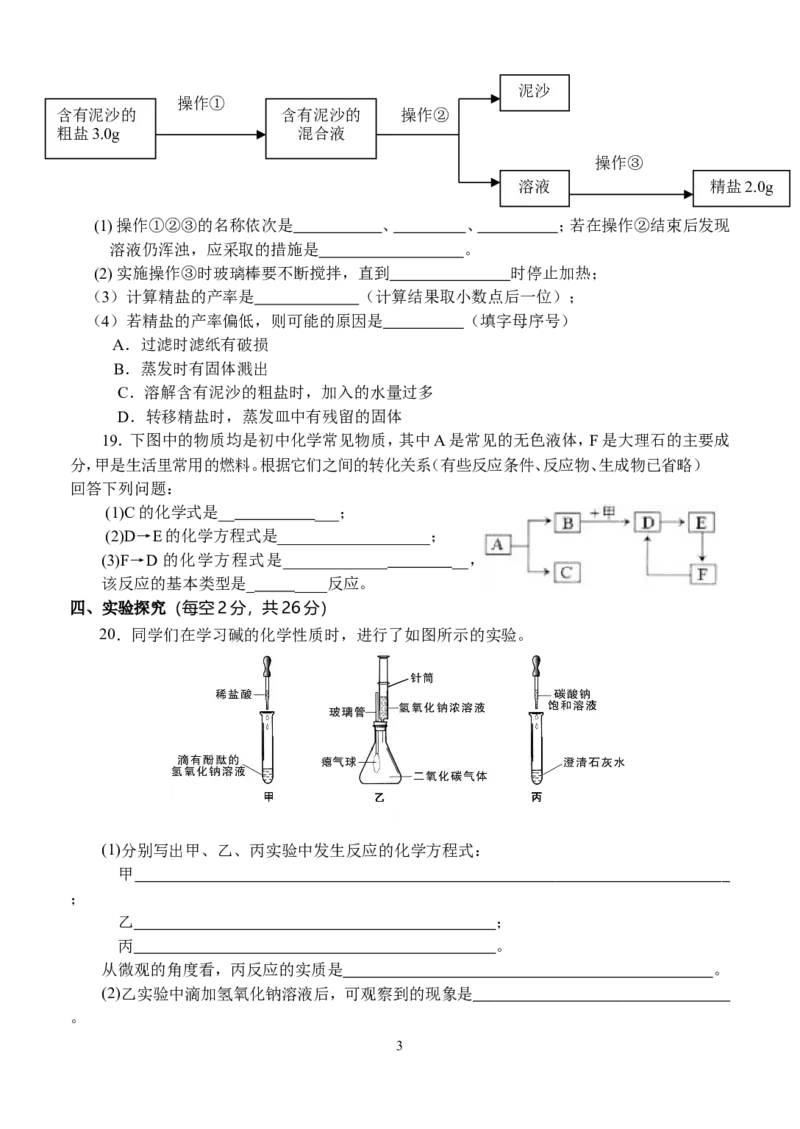
20.同学们在学习碱的化学性质时,进行了如图所示的实验。
(1)分别写出甲、乙、丙实验中发生反应的化学方程式:
甲
;
乙 ;
丙 。
从微观的角度看,丙反应的实质是 。
(2)乙实验中滴加氢氧化钠溶液后,可观察到的现象是
。
3(3)丙实验中观察到试管内有白色沉淀产生。
(4)实验结束后,同学们将甲、乙、丙三个实验的废液倒入同一个干净的废液缸中,最终看到
废液浑浊并呈红色,产生疑问。
[提出问题] 废液中含有哪些物质?
[交流讨论]①一定含有的物质:碳酸钙、指示剂、水和 (写物质名称)。
②还含有能使废液呈碱性的物质。
能使废液呈碱性的物质是什么?同学们有如下猜想。
小云认为:只有碳酸钠
小红认为:只有氢氧化钙
小林认为:是氢氧化钠和碳酸钠
你认为还可能是 (写一种猜想)。
[实验设计]小方想用氯化钙溶液来验证小云、小红、小林的猜想。查阅资料获悉氯化钙溶液
呈中性,并设计如下实验。请你将小方的实验设计补充完整。
实验内容 预计现象 预计结论
取少量废液缸中上层清液 ①有白色沉淀,溶液呈红色。 的猜想正确。
于试管中,加入过量 ② 。 的猜想正确。
氯化钙溶液,静置。 ③ 。 的猜想正确。
[反思拓展]在分析化学反应后所得物质的成分时,除了考虑生成物外还需考虑
。
五、计算题(第(1)、(2)每空1分,第(3)小题6分,共8分)
21.以下是某地生产的加钙食盐包装标签上的部分文字。请仔细阅读后回答下列问题。
配料表:氯化钠、食用碳酸钙、碘酸钾
净含量:500g
成分表:氯化钠≥88℅
钙(以Ca计)0.5℅~1.3℅
碘(以I计)20~50mg/kg
(1)包装标签上的钙含量是指 (填“单质钙”、“碳酸钙”、“钙元素”) 。
(2)为了检验此盐中是否含有碳酸钙,在家庭厨房里可选用的物质是 。
(3)为了测定此盐中钙元素含量,取10g这种盐溶于水,加入足量盐酸,生成0.132g二氧化碳。
请计算此加钙食盐中钙元素的质量分数。
4第十一单元 《盐 化肥》
一、选择题(每小题2分,共20分)
1.C 2.B 3.D 4. B 5.A 6.A 7.B 8.D 9.C 10.C
二、选择题(每小题2分,共10分)
11.B 12.AB 13.A 14.C 15.BD
三、填空题(第16、17题化学式每空1分,其余每空2分,共36分)
16.略
17.举例答案:
(1)①CaO ②HCl ③Ca(OH) ④CaCl
2 2
(2)①2H O 2H ↑+O ↑ ②CaCO +2HCl==CaCl +H O+CO ↑
2 2 2 3 2 2 2
18.(1) 溶解、过滤、蒸发;重新过滤(重新实验)(2) 出现较多固体(3)66.7%(4)BD
19. (1)H (2)CO+2NaOH==NaCO+H O等
2 2 2 3 2
(3)CaCO+2HCl==CaCl +H O+CO↑ 复分解反应(或CaCO CaO+CO↑ 分解反应)
3 2 2 2 3 2
四、实验探究(每空2分,共26分)
20.(1)NaOH+HCl==NaCl+H O CO+2NaOH==Na CO+H O
2 2 2 3 2
NaCO+Ca(OH) ==CaCO ↓+2NaOH Ca2+和CO2-结合生成CaCO 沉淀
2 3 2 3 3 3
(2)气球胀大
(4)[交流讨论]① NaCl ②氢氧化钠(合理均可)
[实验设计] ①小林 ②有白色沉淀,溶液由红色变为无色 小云
③ 没有白色沉淀,溶液呈红色 小红(合理均可)
[反思拓展] 反应物是否有剩余 (合理均可)
五、计算题(第(1)、(2)每空1分,第(3)小题6分,共8分)
21. (1)钙元素 (2)食醋 (3)1.2%
5