文档内容
《晶体结构与性质》基础过关单元检测
学校:___________姓名:___________班级:___________考号:___________
一、单选题(16小题,每小题3分,共48分)
1.下列关于晶体的说法中正确的是
A.自然形成的水晶柱是晶体,从水晶柱上切削下来的粉末不是晶体
B.晶胞中任何一个粒子都属于该晶胞
C.玻璃制成的弹珠具有规则的几何外形,所以玻璃弹珠是晶体
D.缺角的NaCl晶体在饱和NaCl溶液中慢慢变为完美的立方体块,体现了晶体的自范性
2.金属玻璃是由金属元素或金属元素为主要成分的熔体通过快速冷却得到的具有非晶态结
构的金属固体。以下关于金属玻璃的说法正确的是
A.金属玻璃能自发呈现多面体外形
B.金属玻璃具有固定的熔点
C.鉴别金属玻璃是否为晶体最可靠的科学方法为X射线衍射实验
D.金属玻璃是金属与二氧化硅的混合物
3.下列叙述错误的是
A.超分子是由两个或多个分子相互“组合”在一起形成具有特定结构和功能的聚集体,
能表现出不同于单个分子的性质
B.液晶内部分子沿分子长轴方向有序排列,使液晶具有各向异性
C.液晶是液体和晶体的混合物
D.纳米材料包括纳米颗粒与颗粒间的界面两部分组成
4.下列有关等离子体的叙述,不正确的是
A.等离子体是物质的另一种聚集状态 B.等离子体是很好的导体
C.水可能形成等离子体状态 D.等离子体中的微粒不带电荷
5.下列关于共价晶体、分子晶体的叙述中,正确的是
A.HI的相对分子质量大于HF,所以HI的沸点高于HF
B.晶体中分子间作用力越大,分子越稳定
C.金刚石为网状结构,碳原子与周围4个碳原子形成正四面体结构
D.在SiO 晶体中,1个硅原子和2个氧原子形成2个共价键
2
6.下列说法中,正确的是
A.冰融化时,分子中H-O发生断裂
B.共价晶体中,共价键越强,熔点越高
C.分子晶体中,分子间作用力越大,对应的物质越稳定
D.分子晶体中,共价键键能越大,该分子晶体的熔、沸点一定越高
7.晶胞是晶体结构中可重复出现的最小的结构单元,C 晶胞结构如下图所示,下列说法
60
正确的是A.C 摩尔质量是720
60
B.C 与苯互为同素异形体
60
C.C 晶体中仅存在范德华力
60
D.每个C 分子周围与它距离最近且等距离的C 分子有12个
60 60
8.根据量子力学计算,氮化碳有五种结构,其中一种 氮化碳硬度超过金刚石晶体,成
为首屈一指的超硬新材料,已知该氮化碳的二维晶体结构如图所示。下列有关该氮化碳的
说法不正确的是
A.该晶体中的碳、氮原子核外最外层都满足8电子稳定结构
B.氮化碳中碳元素显 价,氮元素显 价
C.每个碳原子与四个氮原子相连,每个氮原子和三个碳原子相连
D.氮化碳的分子式为
9.金刚石、石墨、C 和石墨烯的结构示意图分别如图所示,下列说法不正确的是
60A.金刚石和石墨烯中碳原子的杂化方式不同
B.金刚石、石墨、C 和石墨烯的关系:互为同素异形体
60
C.这四种物质完全燃烧后的产物都是CO
2
D.石墨与C 的晶体类型相同
60
10.下列各组物质中,化学键类型相同,形成的晶体类型也相同的是
A. 和 B. 和 C. 和 D.KCl和HCl
11.下列关于金属键或金属的性质说法正确的是
①金属的导电性是由金属阳离子和自由电子的定向移动实现的
②金属键是金属阳离子和自由电子之间存在的强烈的静电吸引作用
③ 、 、 的沸点依次升高
④金属键没有方向性和饱和性,金属中的电子在整个三维空间运动,属于整个金属
A.①② B.②③ C.③④ D.①④
12.下列叙述正确的是
A.分子晶体中的每个分子内一定含有共价键
B.共价晶体中的相邻原子间只存在非极性共价键
C.离子晶体中可能含有共价键
D.金属晶体的熔点和沸点都很高
13.下列各组物质熔化或升华时,所克服的粒子间作用属于同种类型的是
A.MgO和SiC B.Fe和S C.CO 和SiO D.碘和干冰升华
2 2
14.共价键、离子键和范德华力都是微观粒子之间的不同作用力,下列物质:①NaO;
2 2
②SiO; ③CO; ④C ; ⑤NaCl; ⑥石墨;其中含有至少两种作用力的组合
2 2 60
是
A.①③④⑤⑥ B.①③④⑥ C.①②③ D.①②③⑤⑥
15.在碱性溶液中,Cu2+可与缩二脲形成紫色配离子,其结构如图。下列说法错误的是A.该配离子中非金属元素的电负性大小顺序为O>N>C>H
B.该配离子中铜离子的配位数是4
C.基态Cu原子的价电子排布式是3d104s1
D.该配离子中能与水分子形成氢键的原子只有N和O
16.某化合物的化学式为CoCl ·4NH ,1mol此化合物中加入足量的AgNO 溶液,能生成
3 3 3
1mol的白色沉淀,以强碱处理并加热没有NH 放出,则此化合物的说法正确的是
3
A.该化合物的配体数为4 B.Co3+只与NH 分子形成配位键
3
C.该化合物可以写成[Co(NH )Cl]Cl D.该化合物可能显平面正方形结构
3 4 2
二、填空题(4小题,共52分)
17.(13分)平行六面体晶胞中粒子个数的计算。
(1)晶胞的顶角原子是_______个晶胞共用的,晶胞棱上的原子是_______个晶胞共用的,晶
胞面上的原子是_______个晶胞共用的。
(2)晶胞中微粒数目的确定。
“均摊法”是计算每个晶胞平均拥有的粒子数目的常用方法。其基本理念是每个粒子被n
个晶胞所共用,则该粒子有1/n属于这个晶胞。
晶胞中微粒数目的确定
①金属铜晶胞中原子个数的计算。
金属铜的一个晶胞中,位于晶胞_______的铜原子有_______个,位于_______的铜原有
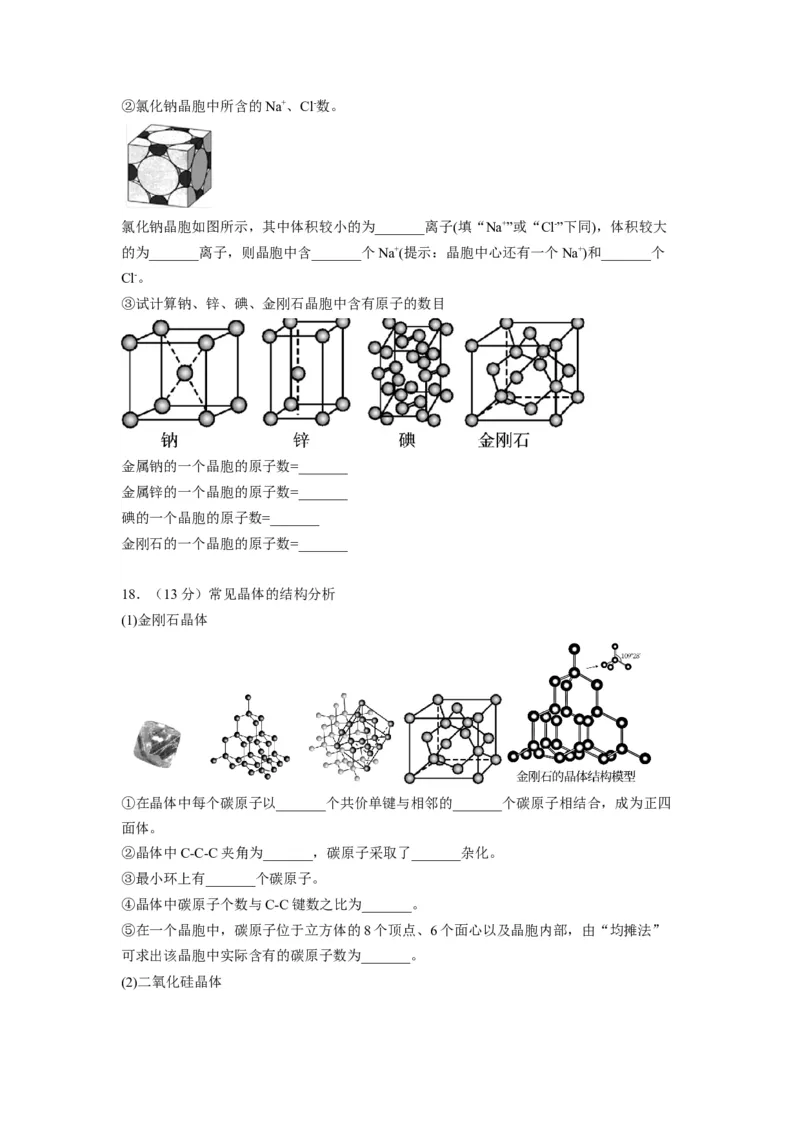
_______个,金属铜晶胞中所含的铜原子数为_______。②氯化钠晶胞中所含的Na+、Cl-数。
氯化钠晶胞如图所示,其中体积较小的为_______离子(填“Na+”或“Cl-”下同),体积较大
的为_______离子,则晶胞中含_______个Na+(提示:晶胞中心还有一个Na+)和_______个
Cl-。
③试计算钠、锌、碘、金刚石晶胞中含有原子的数目
金属钠的一个晶胞的原子数=_______
金属锌的一个晶胞的原子数=_______
碘的一个晶胞的原子数=_______
金刚石的一个晶胞的原子数=_______
18.(13分)常见晶体的结构分析
(1)金刚石晶体
①在晶体中每个碳原子以_______个共价单键与相邻的_______个碳原子相结合,成为正四
面体。
②晶体中C-C-C夹角为_______,碳原子采取了_______杂化。
③最小环上有_______个碳原子。
④晶体中碳原子个数与C-C键数之比为_______。
⑤在一个晶胞中,碳原子位于立方体的8个顶点、6个面心以及晶胞内部,由“均摊法”
可求出该晶胞中实际含有的碳原子数为_______。
(2)二氧化硅晶体①每个硅原子与相邻的_______个氧原子以共价键相结合构成_______结构,硅原子在正四
面体的中心,4个氧原子在正四面体的4个顶点。晶体中Si原子与O原子个数比为_______。
②每个Si原子与4个O原子成键,每个O原子与_______个Si原子成键,最小的环是
_______元环。
③每个最小的环实际拥有的硅原子为_______,氧原子数为_______。
④1molSiO 晶体中含Si-O键数目为_______,在SiO 晶体中Si、O原子均采取_______杂化。
2 2
⑤SiO 具有许多重要用途,是制造水泥、玻璃、人造红宝石、单晶硅、硅光电池、芯片和
2
光导纤维的原料。
19.(13分)各图为几种分子、晶体或晶胞的结构示意图。
请回答下列问题:
(1)这些物质对应的晶体中,构成晶体的粒子之间主要以范德华力结合形成的晶体是
_______、 晶体;构成晶体的粒子之间主要以氢键结合形成的晶体是_______。
(2)冰、金刚石、 、 、干冰5种晶体的熔点由高到低的顺序为_______。
(3)每个 晶胞中实际占有_______个 原子,每个MgO晶胞中实际占有_______个镁离
子, 晶体中每个 周围距离最近且相等的 有_______个。(4)金刚石和 晶体都是碳元素形成的单质, 晶体中含 键数目为_______。
20.(13分)铜及其化合物在工农业生产中有广泛的应用。
Ⅰ.金属铜的原子堆积模型如图-1所示,
(1)该晶胞中每个Cu原子周围最近距离的Cu原子数目为_______。
Ⅱ. 能与 、 、 、 等形成配位数为4的配合物。
(2)向 溶液中加入过量NaOH溶液可生成 。 中除了配
位键外,还存在的化学键类型有_______(填字母)。
A.离子键 B.金属键 C.极性共价键 D.非极性共价键
(3)将CuO投入 、 的混合溶液中进行“氨浸”,控制温度为50~55℃,pH约
为9.5,CuO转化为 溶液。
①CuO被浸取的离子方程式为_______。
② 结构中,若用两个 分子代替两个 分子,可以得到两种不同结构
的化合物,由此推测 的空间构型为_______。
(4) 可以与乙二胺( )形成配离子,如题图-2所示:
③H、O、N三种元素的电负性从大到小的顺序为_______。
④乙二胺分子中N原子成键时采取的杂化类型是_______。乙二胺和三甲胺 均
属于胺,但乙二胺比三甲胺的沸点高很多,原因是_______。
Ⅲ.将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质,
(5)下列物质中,属于顺磁性物质的是_______(填标号)。A. B. C.倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育