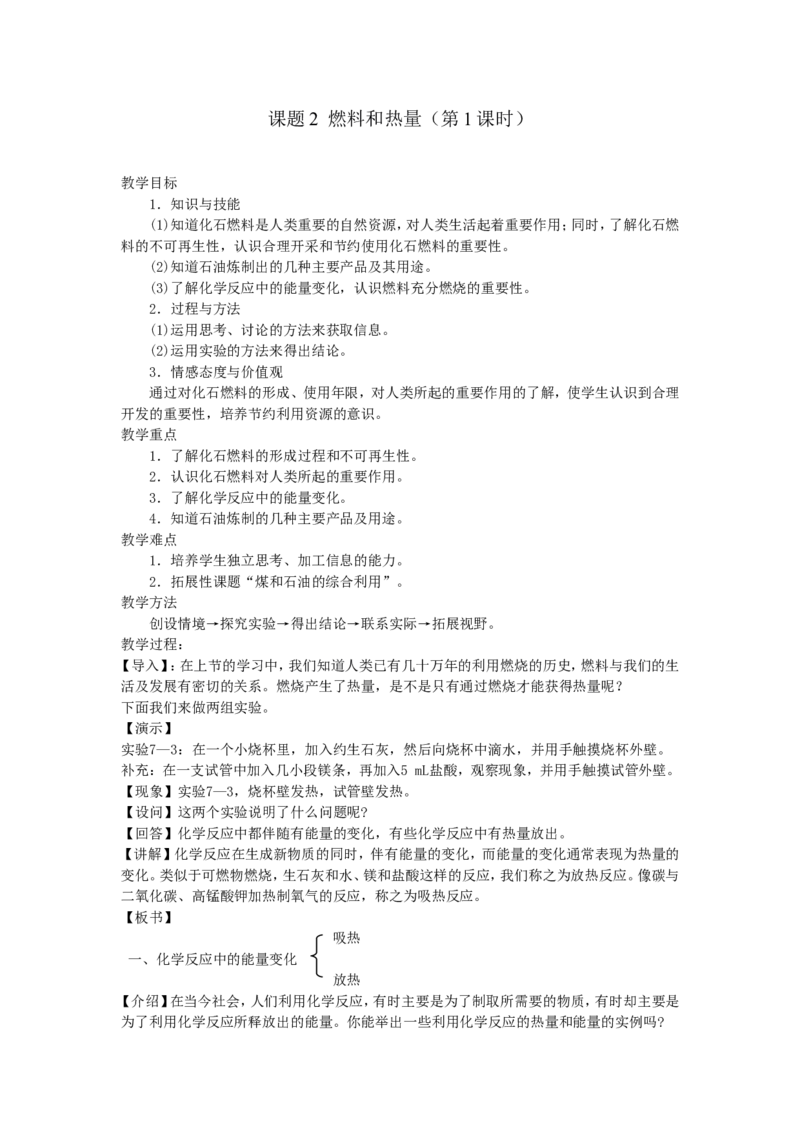文档内容
第七单元 燃料及其利用
课题1 燃烧和灭火(第一课时)
[教学目标]
一、知识与技能
1、认识燃烧的条件和灭火原理。
2、通过活动与探究,培养学生的实验操作能力、观察能力、合作与交流能力,在学生体验科
学探究过程中,培养学生思维能力,分析问题、解决问题的能力,提高学生的科学素养。
二、过程与方法
1、通过实验、探究燃烧的条件和灭火的原理。
2、能用化学科学知识解释日常生活中的某些燃烧现象。
三、情感态度与价值观
1、学习对获得的事实进行分析得出结论的科学方法。
2、培养学生收集和处理信息的能力。
教学过程
[引入新课]:
[演示]:点燃酒精灯
[设问]:这是什么现象?
[设问]:燃烧是我们熟悉的现象,它有什么特征?
学生归纳燃烧的特征:发光、放热。
引出燃烧的定义:
一、燃烧
燃烧是一种发光、放热的剧烈的化学反应。(投影)
[设问]:是不是只要发光发热的变化就是燃烧呢?比如电灯发光、发热是不是燃烧?
[展示]:一片木板
[设问]:木板能燃烧吗?
[演示]:在酒精灯上点燃木板
[设疑]:木板为什么点不燃呢?燃烧需要哪些条件呢?
二、燃烧的条件:(投影)
[过渡]:下面我们一起通过实验来探究
[实验1]:在两个蒸发皿中分别倒入酒精和水,用火柴点燃。
[交流讨论]:分析实验现象及原因,教师引导学生得出正确的实验结论。
[结论]:酒精能燃烧,水不能燃烧。燃烧需要可燃物。
[实验2]:白磷、红磷的燃烧对比实验
[设问1]:小烧杯中白磷燃烧而红磷不燃烧,说明燃烧需要什么条件?
引出着火点的概念:[解说]:原来物质要燃烧,它的温度必须达到着火点, 着火点就是可燃物达到燃烧所需要的
最低温度。
着火点:可燃物达到燃烧所需要的最低温度。(投影)
[投影]:几种常见物质的着火点。
[设问]:小烧杯中的白磷燃烧而热水中的白磷不燃烧,说明燃烧还需要什么条件?
[交流讨论]:分析实验现象及原因,教师引导学生得出正确的实验结论。
[结论]:因为水隔绝了空气,说明燃烧还需要有氧气。
[设疑]:如果水中的白磷接触到氧气那又会怎样?
[实验3]:让水中白磷接触氧气。
[设问]:这个实验再一次说明燃烧需要什么条件?
[结论]:燃烧确实需要氧气。
[解说]:这个实验说明只要具备了燃烧的所有条件,即使在水中燃烧也可以发生。
[设问]:哪个同学来总结一下燃烧的条件?
燃烧的条件:1、可燃物
2、可燃物与氧气(或空气)接触 (三者缺一不可)(投 影)
3、温度要达到可燃物的着火点
[投影]:“火三角”图片。
[设问]:这个图说明什么意思?
[过渡]:其实燃烧在生活中经常用到,比如炒菜、煮饭等等,但燃烧失控会引起火灾,就会给
人类带来灾难。
[投影]:火灾图片。
[设问]:那么一旦发生火灾,如何灭火?灭火的原理是什么?
三、灭火原理和方法(投影)
[解说]:根据燃烧的条件可知,要灭火只要破坏燃烧的一个条件就可以了。下面我们继续通
过实验来进行探究。
[实验4]:分别让学生上讲台演示一种方法来熄灭蜡烛,并说出是运用了什么原理来灭火的?
[归纳总结]:灭火的原理:
1、清除可燃物或与可燃物隔离
2、隔绝氧气(或空气) (具备一个即可)(投 影)
3、使温度降低到着火点以下
[课堂练习]:见投影
[课堂总结]:通过本节课的学习,你知道了什么?
课题1 燃烧和灭火(第二课时)教学目标
1、知识与技能
(1) 几种常用灭火器的灭火原理和适用范围。
(2)了解易燃物和易爆物的安全知识。
2、过程与方法
(1)学习运用比较、观察、实验等方法获取信息。
(2)学习运用主动探究的方法,设计实验。
3、情感态度与价值观
(1)利用化学知识解释生活问题,使学生对化学保持强烈的好奇心和探究欲。
(2)增强日常生活中的防范灾害的意识,并注意采取安全措施。
教学重点
了解易燃物和易爆物的安全知识。
教学难点
1、培养学生提出问题,分析问题和解决问题的能力。
2、培养学生进行知识迁移的能力。
教学过程:
[复习提问]1、什么是燃烧?燃烧的条件有哪些?
[回答] 燃烧是一种发光、放热的剧烈的化学反应。燃烧的条件:需要可燃物、
可燃物与氧气(或空气)接触、温度要达到可燃物的着火点 。
[复习提问]2、灭火的原理有哪些?
[回答] 原理:清除可燃物、隔绝氧气、降温至着火点以下。
[过渡]大家注意看老师给大家带来的一个魔术——烧不坏的手帕。
[演示]用一块棉手帕(不要用合成纤维的),在盛有乙醇的体积分数为70%酒精的烧杯中浸
泡,用镊子夹住两角,在火焰上点燃,当火焰熄灭后,观察现象。
[设问]同学们看到了什么现象?
[回答]火焰熄灭后,手帕完好无损。
[追问]那么,大家想想为什么会出现这样的现象呢?
[回答]因为手帕上沾有酒精,我们所看到的是酒精的燃烧。在整个燃烧的过程中,对于手帕
来说,并没有达到它的着火点,所以手帕并没有燃烧。
[过渡]在我们日常生活中,“灭火器”可能也是比较常见的。那么灭火器都一样吗?它们
的原理都相同吗?我们一起来学习生活中常见的几种灭火器。
[投影]教材p131表7-2的内容
[比一比,赛一赛]你能很快记住它们吗?以小组为单位,利用三分钟时间,我们通过游戏来
选出冠军得主。
[游戏]教师选出六名同学分别拿着不同类型的灭火器的道具,然后给他们列出几种物质燃
烧,要求他们用适当的灭火器灭火,看最后谁的正确率高,谁得冠军。(形式不限)
[讲解]看来不同的物质燃烧需要不同的方法来进行灭火,这就是我们要学习的第2个问
题——灭火的方法。
[板书]2.方法:
[过渡]可燃物在具备了燃烧的条件后,就能急剧地燃烧,如果在有限的空间内就会给生命和
财产造成严重的损害,为了使警钟长鸣,所以,大家在一些易燃、易爆场合会经常看到下面的
—些图标,同学们讨论讨论,这些图标向人们传递了什么样的信息?
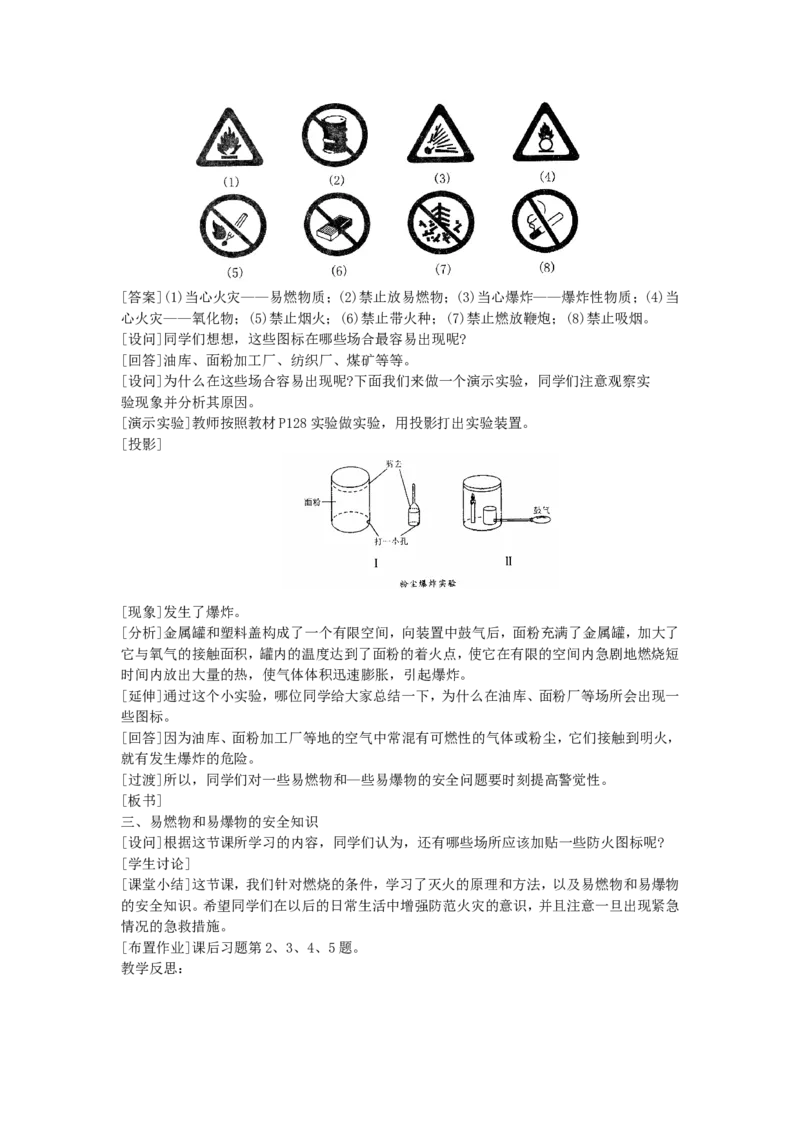
[投影][答案](1)当心火灾——易燃物质;(2)禁止放易燃物;(3)当心爆炸——爆炸性物质;(4)当
心火灾——氧化物;(5)禁止烟火;(6)禁止带火种;(7)禁止燃放鞭炮;(8)禁止吸烟。
[设问]同学们想想,这些图标在哪些场合最容易出现呢?
[回答]油库、面粉加工厂、纺织厂、煤矿等等。
[设问]为什么在这些场合容易出现呢?下面我们来做一个演示实验,同学们注意观察实
验现象并分析其原因。
[演示实验]教师按照教材P128实验做实验,用投影打出实验装置。
[投影]
[现象]发生了爆炸。
[分析]金属罐和塑料盖构成了一个有限空间,向装置中鼓气后,面粉充满了金属罐,加大了
它与氧气的接触面积,罐内的温度达到了面粉的着火点,使它在有限的空间内急剧地燃烧短
时间内放出大量的热,使气体体积迅速膨胀,引起爆炸。
[延伸]通过这个小实验,哪位同学给大家总结一下,为什么在油库、面粉厂等场所会出现一
些图标。
[回答]因为油库、面粉加工厂等地的空气中常混有可燃性的气体或粉尘,它们接触到明火,
就有发生爆炸的危险。
[过渡]所以,同学们对一些易燃物和—些易爆物的安全问题要时刻提高警觉性。
[板书]
三、易燃物和易爆物的安全知识
[设问]根据这节课所学习的内容,同学们认为,还有哪些场所应该加贴一些防火图标呢?
[学生讨论]
[课堂小结]这节课,我们针对燃烧的条件,学习了灭火的原理和方法,以及易燃物和易爆物
的安全知识。希望同学们在以后的日常生活中增强防范火灾的意识,并且注意一旦出现紧急
情况的急救措施。
[布置作业]课后习题第2、3、4、5题。
教学反思:课题2 燃料和热量(第1课时)
教学目标
1.知识与技能
(1)知道化石燃料是人类重要的自然资源,对人类生活起着重要作用;同时,了解化石燃
料的不可再生性,认识合理开采和节约使用化石燃料的重要性。
(2)知道石油炼制出的几种主要产品及其用途。
(3)了解化学反应中的能量变化,认识燃料充分燃烧的重要性。
2.过程与方法
(1)运用思考、讨论的方法来获取信息。
(2)运用实验的方法来得出结论。
3.情感态度与价值观
通过对化石燃料的形成、使用年限,对人类所起的重要作用的了解,使学生认识到合理
开发的重要性,培养节约利用资源的意识。
教学重点
1.了解化石燃料的形成过程和不可再生性。
2.认识化石燃料对人类所起的重要作用。
3.了解化学反应中的能量变化。
4.知道石油炼制的几种主要产品及用途。
教学难点
1.培养学生独立思考、加工信息的能力。
2.拓展性课题“煤和石油的综合利用”。
教学方法
创设情境→探究实验→得出结论→联系实际→拓展视野。
教学过程:
【导入】:在上节的学习中,我们知道人类已有几十万年的利用燃烧的历史,燃料与我们的生
活及发展有密切的关系。燃烧产生了热量,是不是只有通过燃烧才能获得热量呢?
下面我们来做两组实验。
【演示】
实验7—3:在一个小烧杯里,加入约生石灰,然后向烧杯中滴水,并用手触摸烧杯外 壁。
补充:在一支试管中加入几小段镁条,再加入5 mL盐酸,观察现象,并用手触摸试管外壁。
【现象】实验7—3,烧杯壁发热,试管壁发热。
【设问】这两个实验说明了什么问题呢?
【回答】化学反应中都伴随有能量的变化,有些化学反应中有热量放出。
【讲解】化学反应在生成新物质的同时,伴有能量的变化,而能量的变化通常表现为热量的
变化。类似于可燃物燃烧,生石灰和水、镁和盐酸这样的反应,我们称之为放热反应。像碳与
二氧化碳、高锰酸钾加热制氧气的反应,称之为吸热反应。
【板书】
吸热
一、化学反应中的能量变化
放热
【介绍】在当今社会,人们利用化学反应,有时主要是为了制取所需要的物质,有时却主要是
为了利用化学反应所释放出的能量。你能举出一些利用化学反应的热量和能量的实例吗?【讨论】举例。
【过渡】目前,人类通过化学反应获得的能量,大多来自于化石燃料,化石燃料有哪些呢?
【介绍】煤和石油都是由古代生物遗体埋在地层下,在地壳中经过一系列非常复杂的变化而
形成的。由于煤和石油的用途非常广泛,和人类的关系极为密切,所以,人们常把煤称为“工
业的粮食”,把石油称为“工业的血液”。
【阅读】课本P138内容,你能从中学到什么知识?
【板书】(归纳)二、化石燃料:(石油、煤、天然气)
1、煤和石油煤与石油的比较
煤 石油
主要成分 碳元素 碳和氢元素
隔绝空气加热 利用沸点不同,将它们加热炼制
炼制方法
(化学变化) (物理变化)
焦碳、煤焦油、煤气等 汽油、煤油、柴油、石蜡等
产品与用途
2、天然气
有人说天然气就是甲烷,甲烷就是天然气,对不对?
【演示】实验7-4:教师演示后,学生描述现象,归纳填写在书上。
【讨论】:这个实验说明甲烷中含有哪些元素?
【讲述】:甲烷特性:无色、无味气体、度比空气小、难溶于水,具有可燃性
CH+2O CO+2HO(点燃之前要验纯)
4 2 2 2
3、可燃冰:甲烷水合物。
【精讲】:
(1)、化石燃料的特点是不可再生,总有一天会用完,这一天还很早,不用着急,对吗?
根据书P141的数据计算多少年后石油和天然气将被耗尽?你有怎样的对策?
(2)、讨论解决能源危机的思路(节约现有能源,开发新能源)
(3)、讨论提高燃料燃烧利用率的方法。
【练习】(1)煤是一种常用的化石燃料,家庭用煤经过了从“煤球”到“蜂窝煤”的变化:以
前人们把煤粉加工成略大于乒乓球的球体,后来人们把煤粉加工成圆柱体,并在圆柱体内打
上一些孔。请你分析这种变化的优点是:_________。
(2)煤在燃烧时会产生许多污染物,为了减少煤燃烧时对环境的污染,可设法把煤转化成清
洁的燃料。将水蒸气通过炽热的煤层,可得到较洁净的水煤气(主要成分是CO和H),请你写
2
出该反应的化学方程式___________。
答案:(1)使煤与空气的接触面积增大,燃烧更充分 (2)C+HO CO+H
2 2
[课堂总结]:通过本节课的学习,你知道了什么?
[课后作业]:基础训练
教学反思:课题2 燃料的合理利用与开发(第2课时)
一、教学目标
1.知识与技能:
(1)了解化石燃料燃烧对环境的影响;
(2)了解氢气的实验室制法;
(3)认识使用和开发新能源的重要性。
2.过程与方法:
(1)利用各种资源,认识化石燃料燃烧对环境造成的污染;
(2)通过观看视频,充分认识酸雨的危害;
(3)利用两则资料,让学生深刻感受大气污染对人类造成的危害,并深刻感受到开发利用新
能源的重要性与迫切性。
3.情感态度与价值观:
(1)通过燃料对环境影响的学习来树立保护环境的意识,体会化学与社会发展的关系;
(2)通过实验和讨论来培养善于合作、勤于思考、严谨求实、勇于创新实践的科学精神。
二、教学重点与难点
1. 重点:了解燃料对环境的影响,懂得选择对环境污染较小的燃料。认识新能源开发重要性。
2. 难点:燃料燃烧对空气污染的原因,树立爱护资源、保护地球、爱护地球的意识。
四、教学过程
【情境导入】环境问题已经成为世界关注的问题
燃料的使用对人们的生活带来了很多方便,但是,有些燃料在燃烧提供能量的同时,却
对环境造成了不良的影响。
一、燃料燃烧对空气的影响
下面我们一起来看一幅漫画:酸雨的危害
请同学们思考:
1.从这幅漫画中,反映
出的环境问题是什么?
2.造成这种环境问题的原
因是什么?
【学生交流】漫画所反映出的环境问题是“酸雨”,由于有些燃料燃烧会排放出二氧化硫、二
氧化氮等污染物,这些气体或气体在空气中反应后的生成物溶于雨水,会形成酸雨。
【观看视频】酸雨的危害
【讨论交流】通过我们刚刚观看的有关“酸雨的危害”视频,请你思考:酸雨对哪些物质有腐
蚀破坏作用?
【交流展示】学生回答,教师归纳:
酸雨的危害:酸雨对植物、金属制品、大理石制品、土壤、水体、人体健康等都有危害。
【联系实际】请同学们听听如下两则报道:
1、2006年,中国对559个主要城市进行的监测显示,有37.6%的城市大气质量未达到国
家标准,悬浮颗粒物、二氧化物、氮氧化物是主要污染物。据世界银行估计,中国有6亿人生
活在二氧化硫超过世界卫生组织标准的环境中,而生活在总悬浮颗粒物超过世界卫生组织
标准的环境中人数达到了10亿。
2、近年来,许多研究表明,大气污染与人群的许多疾病,特别是呼吸系统疾病、心血管疾病、免疫系统疾病、肿瘤的患病率和死亡率密切相关。全球每年由于城市空气污染造成大约
80万人死亡。亚洲地区每年因大气污染造成48.7万多人死亡。中国每年因城市大气污染而
造成的呼吸系统门诊病例35万人,急诊病例680万人,大气污染造成的环境与健康损失占中
国GDP的7%。
【思考交流】1、从上述两则报道中,你有何感受呢?
2、为了减少大气的污染,你认为可采取的措施有哪些呢?
【归纳总结】
(1)减少使用化石燃料;(2)含硫燃料脱硫后再使用;(3)尾气处理后再排放;
(4)使用清洁燃料;(5)改进发动机结构,使燃料燃烧充分;(6)开发利用新能源等
二、使用和开发新的燃料
1.乙醇
【交流讨论】请你根据课本知识,完成下面的表格:
燃料 乙醇
制取的方法 由高粱、玉米、薯类等经过发酵、蒸馏制得的,属于可再生
能源
化学式及俗名 CHOH 俗名:酒精
2 5
燃烧的化学反应方程式 CHOH+3O 点燃 2CO+3HO
2 5 2 2 2
2.氢气
最清洁的燃料 氢气
有哪些方法可以制得氢气? 电解水、锌与稀硫酸反应等
实验室制取氢气的原理 Zn+HSO === ZnSO+ H↑
2 4 4 2
实验室收集氢气的方法 排水法;向下排空气法
实验室制取氢气的发生装置 固液不加热型发生装置
氢气燃烧的化学方程式 点燃
2H+O 2HO
2 2 2
【思考问题】氢气作燃料,有哪些优缺点?
学生小结:
优点:氢气本身无毒,极易燃烧,燃烧值高,其产物是水等。
缺点:制取成本高,贮存困难等 。
因此,氢气作为燃料暂时还不能广泛使用。
【拓展信息】除了乙醇和氢气,你还知道哪些新能源吗?
学生列举:新能源有风能、太阳能、地热能、潮汐能、核能等。
【图片展示】新能源
【讲解】这些新能源的开发和利用,不但可以部分解决化石燃料面临耗尽的问题,还可以减少
对环境的污染。希望同学们将来长大了,能将自己所学知识应用到开发和利用更理想更实用
的清洁能源方面,为人类生活质量的进一步提高作出自己的贡献。
【小结内容】对本节课的知识进行小结
布置作业:基础训练
教学反思: