文档内容
2013—2014学年第一学期期中考试
初三化学
注意事项:1.答案全部填在答题卷上,填写在试题纸上一律无效。
2.选用的相对原子质量在答题卷首。
3.考试时间:90分钟;试卷满分:100分。
第I卷(选择题 共25分)
一、单项选择题(本题包括25小题,每题只有1个选项符合题意,共25分)
1.下列变化属于化学变化的是
A.分离液态空气制氧气 B.蜡烛燃烧 C.水结冰 D.酒精挥发
2.“加碘食盐”、“高钙牛奶”、“加铁酱油”中的“碘”“钙”“铁”指的是
A.原子 B.分子 C.元素 D.离子
3.地壳中含量最多的金属元素和非金属元素组成的物质的化学式是
A.SiO B.AlO C.AlO D.FeO
2 2 3
4.下列图示实验操作中,正确的是
D.熄灭酒精灯
A.给液体加热 B.闻气体气味 C.读取液体体积
5. 有一位同学暑假去西藏发生了严重的高原反应,医生让他吸氧后症状缓解。吸氧可以帮助人克服高原反
应的原因是
A.氧气是无色无味的无毒气体 B.氧气可以燃烧
C.吸氧为人体呼吸提供了适量的氧气 D.氧气可以支持燃烧
6.下列变化中,不属于缓慢氧化的是
A.火药爆炸 B.钢铁生锈 C.酿酒酿醋 D.动物呼吸
7.钛和钛合金被认为是21世纪的重要金属材料。钛原子的质子数为22,中子数为26,则钛原子的核外电子
数为
A. 48 B. 26 C. 22 D. 4
8.亚硒酸钠(NaSeO)能消除加速人体衰老的活性氧,其中硒(Se)的化合价为
2 3
A.+2 B.+3 C.+4 D.+6
9. 从分子角度解释下列现象,其中错误的是
A.氨水挥发—分子运动后分子间间隔增大 B.花香四溢—分子在不断地运动
C.热胀冷缩—分子大小随温度改变而改变 D.氢气燃烧—分子本身发生改变
10. 实验室利用氯酸钾和二氧化锰制取氧气的主要步骤有:①固定装置;②装入药品;
③加热;④检查装置的气密性;⑤用排水法收集;⑥熄灭酒精灯;⑦从水槽中移出导气管。其操作顺序正确
的是
A.④②①③⑤⑦⑥ B.②③①⑥④⑤⑦
C.①②③④⑤⑥⑦ D.⑥④①②⑦⑤③
11.空气是一种宝贵的自然资源,下列有关说法错误的是
A.法国化学家拉瓦锡研究得出氧气约占空气总体积的4/5
B.饼干在空气中变软是因为空气中含有水蒸气
C.氮气是制造硝酸和氮肥的重要原料
D.稀有气体都没有颜色、没有气味,在通电时能发出不同颜色的光
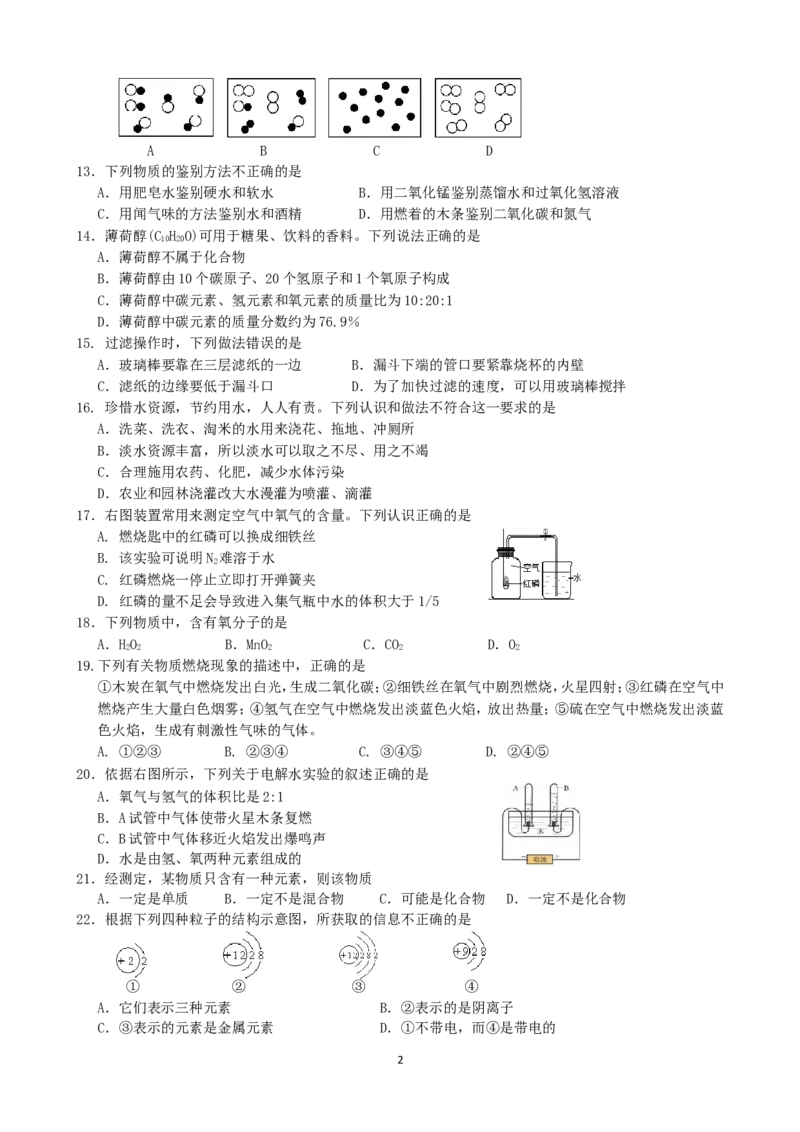
12.下列各图中“○”“●”分别表示两种不同元素的原子,其中表示混合物的是
1A B C D
13.下列物质的鉴别方法不正确的是
A.用肥皂水鉴别硬水和软水 B.用二氧化锰鉴别蒸馏水和过氧化氢溶液
C.用闻气味的方法鉴别水和酒精 D.用燃着的木条鉴别二氧化碳和氮气
14.薄荷醇(C H O)可用于糖果、饮料的香料。下列说法正确的是
10 20
A.薄荷醇不属于化合物
B.薄荷醇由10个碳原子、20个氢原子和1个氧原子构成
C.薄荷醇中碳元素、氢元素和氧元素的质量比为10:20:1
D.薄荷醇中碳元素的质量分数约为76.9%
15. 过滤操作时,下列做法错误的是
A.玻璃棒要靠在三层滤纸的一边 B.漏斗下端的管口要紧靠烧杯的内壁
C.滤纸的边缘要低于漏斗口 D.为了加快过滤的速度,可以用玻璃棒搅拌
16. 珍惜水资源,节约用水,人人有责。下列认识和做法不符合这一要求的是
A.洗菜、洗衣、淘米的水用来浇花、拖地、冲厕所
B.淡水资源丰富,所以淡水可以取之不尽、用之不竭
C.合理施用农药、化肥,减少水体污染
D.农业和园林浇灌改大水漫灌为喷灌、滴灌
17.右图装置常用来测定空气中氧气的含量。下列认识正确的是
A. 燃烧匙中的红磷可以换成细铁丝
B. 该实验可说明N 难溶于水
2
C. 红磷燃烧一停止立即打开弹簧夹
D. 红磷的量不足会导致进入集气瓶中水的体积大于1/5
18.下列物质中,含有氧分子的是
A.HO B.MnO C.CO D.O
2 2 2 2 2
19.下列有关物质燃烧现象的描述中,正确的是
①木炭在氧气中燃烧发出白光,生成二氧化碳;②细铁丝在氧气中剧烈燃烧,火星四射;③红磷在空气中
燃烧产生大量白色烟雾;④氢气在空气中燃烧发出淡蓝色火焰,放出热量;⑤硫在空气中燃烧发出淡蓝
色火焰,生成有刺激性气味的气体。
A. ①②③ B. ②③④ C. ③④⑤ D. ②④⑤
20.依据右图所示,下列关于电解水实验的叙述正确的是
A.氧气与氢气的体积比是2:1
B.A试管中气体使带火星木条复燃
C.B试管中气体移近火焰发出爆鸣声
D.水是由氢、氧两种元素组成的
21.经测定,某物质只含有一种元素,则该物质
A.一定是单质 B.一定不是混合物 C.可能是化合物 D.一定不是化合物
22.根据下列四种粒子的结构示意图,所获取的信息不正确的是
① ② ③ ④
A.它们表示三种元素 B.②表示的是阴离子
C.③表示的元素是金属元素 D.①不带电,而④是带电的
223.某同学用量筒量液体,开始时仰视,读数为20mL,倒出部分液体后俯视,读数为15mL,试判断,该同学倒
出的液体体积实际为
A.等于5mL B.小于5mL C.大于5mL D.A、B、C都有可能
24. 蜡烛(足量)在如下左图密闭的集气瓶内燃烧至熄灭,
用仪器测出瓶内氧气含量的变化如下右图所示。下列判 断正确的是
A.蜡烛燃烧前瓶内只有氧气
B.氧气浓度小于一定值时,蜡烛无法燃烧
C.过程中瓶内物质发生了化合反应
D.蜡烛熄灭后瓶内只剩二氧化碳气体
25.某同学梳理并归纳了以下知识点:①质子数相同的 两种粒子一定
属于同种元素;②过氧化氢是由氢分子和氧分子构成;③化学反应前后,元素种类一定不变;④最外层电子
数为8的粒子不一定是稀有气体的原子;⑤无论是吸入的空气还是呼出的气体中含量最多的气体都是氮气;
⑥纯净物一定是由同种分子构成的。其中正确的是
A.①②④ B.③④⑤ C.①③⑥ D.②⑤⑥
第Ⅱ卷(非选择题 共75分)
二、(本题共8小题,每空1分,共42分)
26.(1)(6分)现有H、O、N、C四种元素,请选用其中的元素写出符合下列要求的物质各一个(用化学式表
示):
①食品包装中用以防腐的气体 ;②能使带火星的木条复燃的气体 ;
③点燃前需检验纯度的气体 ;④生物体中含量最多的物质 ;
⑤能使澄清石灰水浑浊的气体 ;⑥会污染空气的有害气体 。
(2)(6分)用化学符号填写下列空格:
①2个氮原子 ;②3个硫酸根离子 ;③+2价的铜元素 ;④碳酸钙 ;⑤保持二氧化碳
化学性质的最小粒子 ;⑥氧化汞分解中的最小粒子 。
27.(6分)写出下列化学反应的符号表达式,并在括号内注明基本反应类型:
(1)电解水 ;( )反应
(2)铁丝在氧气中燃烧 ;( )反应
(3)红磷在空气中燃烧 ;
(4)硝酸铵受热分解生成NO气体和水 。
2
28.(3分)正确规范的操作是实验成功的关键。请回答下列实验操作的理由。
(1)倾倒液体时,试剂瓶贴标签的一面要朝向手心处 ;
(2)给试管中的固体加热时,试管口应略向下倾斜 ;
(3)铁丝在氧气中燃烧时,集气瓶底部先放一些水 。
29.(3分)有下列物质:①洁净的空气;②液氮;③二氧化碳;④高锰酸钾加热后剩余的固体;⑤氯酸钾;⑥
水银;⑦蒸馏水。其中属于混合物的是 (填序号),属于单质的是 (填化学式),属
于氧化物的是 (填化学式)。
30.(4分)有A、B、C、D四种元素,已知A是地壳中含量最多的元素,B元素的原子失去一个电子后只剩下一
个质子,C元素是海水中含量最高的金属元素,D2-的电子层结构与氩原子相同。请回答:A元素的名称或
符号 ;B元素的离子符号 ;C元素组成单质的化学式 ;A、C、D元素组成化
合物的化学式 。
31.(3分)加强对空气质量的监测是保护环境的一项重要措施,下表是某市一年四季空气质量监测的平均
数据。请据表回答问题:
可吸入颗粒物(TSP) 氮氧化合物 二氧化硫 空气质量级别
春季 88 40 44 Ⅱ
夏季 67 33 36 Ⅱ
秋季 90 46 54 Ⅱ
3冬季 98 69 60 Ⅱ
(1)对该市空气质量影响最大的指标是 。
(2)该市空气质量最差的季节是 。
(3)为了减少空气污染可采取的有效措施是 。(答一点即可)
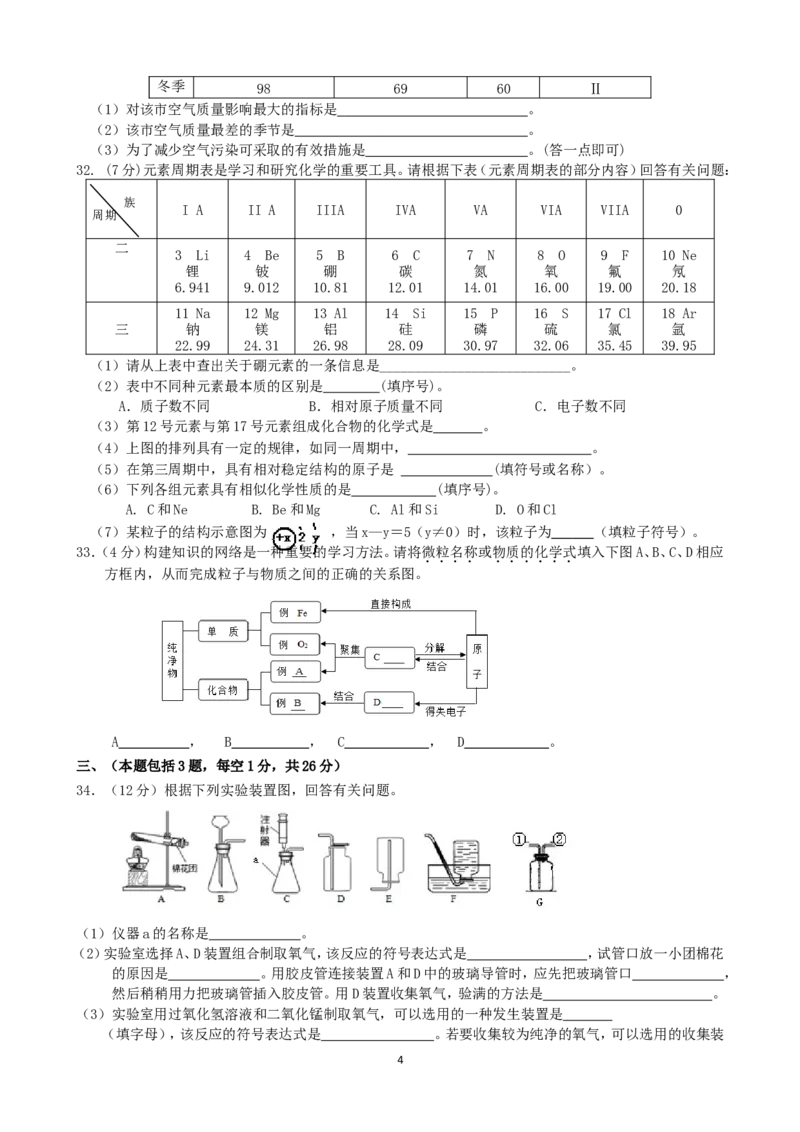
32. (7分)元素周期表是学习和研究化学的重要工具。请根据下表(元素周期表的部分内容)回答有关问题:
族
I A II A IIIA IVA VA VIA VIIA 0
周期
二
3 Li 4 Be 5 B 6 C 7 N 8 O 9 F 10 Ne
锂 铍 硼 碳 氮 氧 氟 氖
6.941 9.012 10.81 12.01 14.01 16.00 19.00 20.18
11 Na 12 Mg 13 Al 14 Si 15 P 16 S 17 Cl 18 Ar
三 钠 镁 铝 硅 磷 硫 氯 氩
22.99 24.31 26.98 28.09 30.97 32.06 35.45 39.95
(1)请从上表中查出关于硼元素的一条信息是___________________________。
(2)表中不同种元素最本质的区别是 (填序号)。
A.质子数不同 B.相对原子质量不同 C.电子数不同
(3)第12号元素与第17号元素组成化合物的化学式是 。
(4)上图的排列具有一定的规律,如同一周期中, 。
(5)在第三周期中,具有相对稳定结构的原子是 (填符号或名称)。
(6)下列各组元素具有相似化学性质的是 (填序号)。
A. C和Ne B. Be和Mg C. Al和Si D. O和Cl
(7)某粒子的结构示意图为 ,当x—y=5(y≠0)时,该粒子为 (填粒子符号)。
33.(4分)构建知识的网络是一种重要的学习方法。请将微粒名称或物质的化学式填入下图A、B、C、D相应
方框内,从而完成粒子与物质之间的正确的关系图。
A , B , C , D 。
三、(本题包括3题,每空1分,共26分)
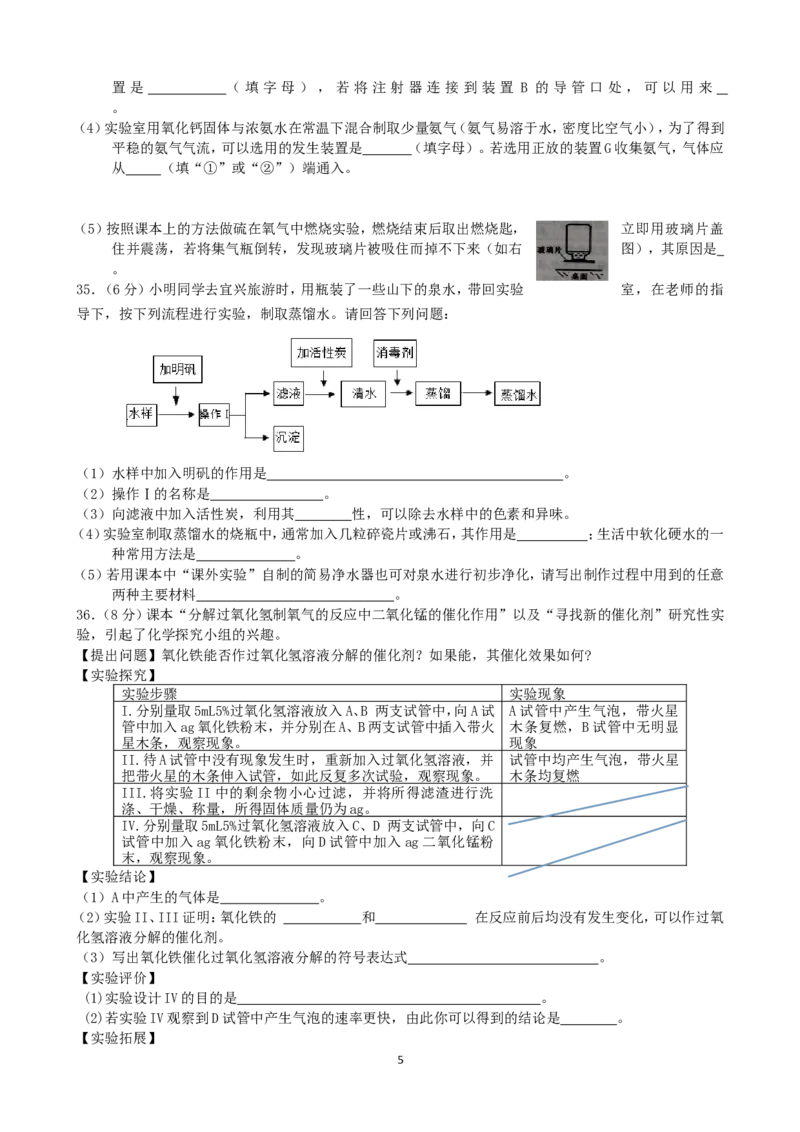
34.(12分)根据下列实验装置图,回答有关问题。
(1)仪器a的名称是 。
(2)实验室选择A、D装置组合制取氧气,该反应的符号表达式是 ,试管口放一小团棉花
的原因是 。用胶皮管连接装置A和D中的玻璃导管时,应先把玻璃管口 ,
然后稍稍用力把玻璃管插入胶皮管。用D装置收集氧气,验满的方法是 。
(3)实验室用过氧化氢溶液和二氧化锰制取氧气,可以选用的一种发生装置是
(填字母),该反应的符号表达式是 。若要收集较为纯净的氧气,可以选用的收集装
4置 是 ( 填 字 母 ) , 若 将 注 射 器 连 接 到 装 置 B 的 导 管 口 处 , 可 以 用 来
。
(4)实验室用氧化钙固体与浓氨水在常温下混合制取少量氨气(氨气易溶于水,密度比空气小),为了得到
平稳的氨气气流,可以选用的发生装置是 (填字母)。若选用正放的装置G收集氨气,气体应
从 (填“①”或“②”)端通入。
(5)按照课本上的方法做硫在氧气中燃烧实验,燃烧结束后取出燃烧匙, 立即用玻璃片盖
住并震荡,若将集气瓶倒转,发现玻璃片被吸住而掉不下来(如右 图),其原因是
。
35.(6分)小明同学去宜兴旅游时,用瓶装了一些山下的泉水,带回实验 室,在老师的指
导下,按下列流程进行实验,制取蒸馏水。请回答下列问题:
(1)水样中加入明矾的作用是 。
(2)操作Ⅰ的名称是 。
(3)向滤液中加入活性炭,利用其 性,可以除去水样中的色素和异味。
(4)实验室制取蒸馏水的烧瓶中,通常加入几粒碎瓷片或沸石,其作用是 ;生活中软化硬水的一
种常用方法是 。
(5)若用课本中“课外实验”自制的简易净水器也可对泉水进行初步净化,请写出制作过程中用到的任意
两种主要材料 。
36.(8分)课本“分解过氧化氢制氧气的反应中二氧化锰的催化作用”以及“寻找新的催化剂”研究性实
验,引起了化学探究小组的兴趣。
【提出问题】氧化铁能否作过氧化氢溶液分解的催化剂?如果能,其催化效果如何?
【实验探究】
实验步骤 实验现象
I.分别量取5mL5%过氧化氢溶液放入A、B 两支试管中,向A试 A试管中产生气泡,带火星
管中加入ag氧化铁粉末,并分别在A、B两支试管中插入带火 木条复燃,B试管中无明显
星木条,观察现象。 现象
II.待A试管中没有现象发生时,重新加入过氧化氢溶液,并 试管中均产生气泡,带火星
把带火星的木条伸入试管,如此反复多次试验,观察现象。 木条均复燃
III.将实验II中的剩余物小心过滤,并将所得滤渣进行洗
涤、干燥、称量,所得固体质量仍为ag。
IV.分别量取5mL5%过氧化氢溶液放入C、D 两支试管中,向C
试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉
末,观察现象。
【实验结论】
(1)A中产生的气体是 。
(2)实验II、III证明:氧化铁的 和 在反应前后均没有发生变化,可以作过氧
化氢溶液分解的催化剂。
(3)写出氧化铁催化过氧化氢溶液分解的符号表达式 。
【实验评价】
(1)实验设计IV的目的是 。
(2)若实验IV观察到D试管中产生气泡的速率更快,由此你可以得到的结论是 。
【实验拓展】
5(1)查阅资料得知:CuO、CuSO、马铃薯等也可以做过氧化氢溶液分解的催化剂。下列有关催化剂的说法中正
4
确的是 (填序号)。
A.MnO 只能作过氧化氢溶液分解的催化剂
2
B.同一个化学反应可以有多种催化剂
C.催化剂只能加快化学反应的速率
D.用作催化剂的物质不可能是其他反应的反应物或生成物
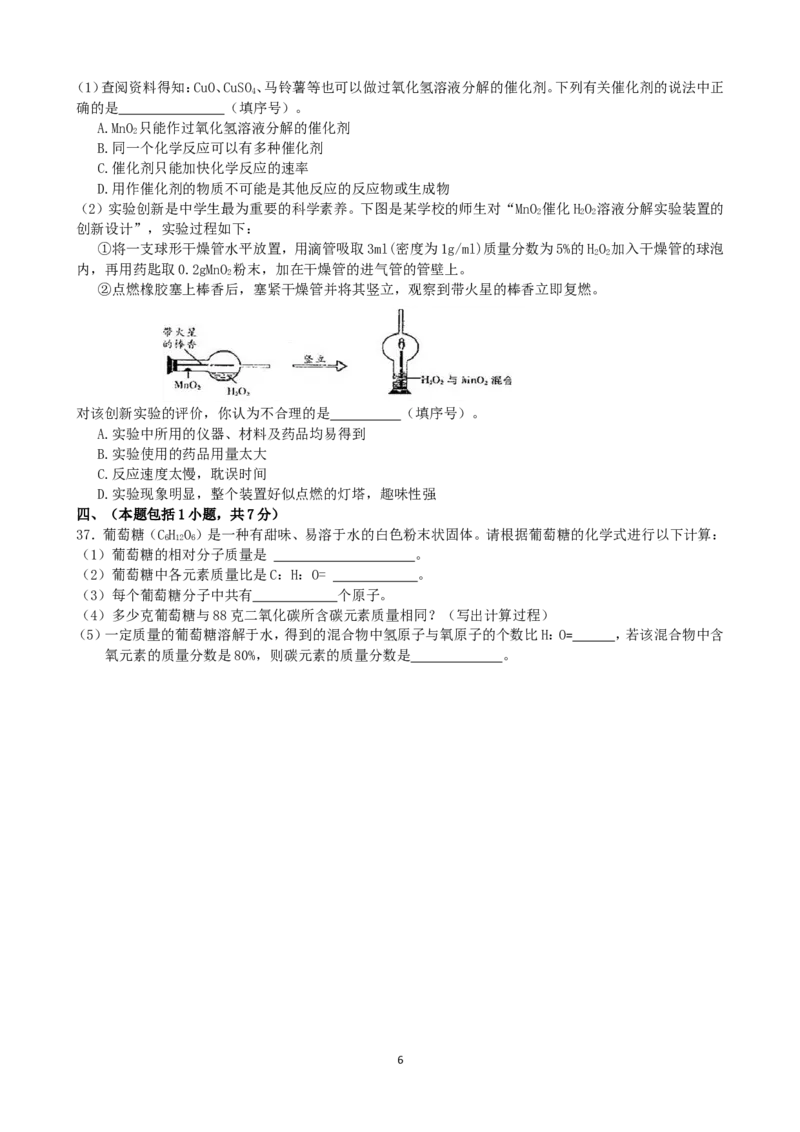
(2)实验创新是中学生最为重要的科学素养。下图是某学校的师生对“MnO 催化HO 溶液分解实验装置的
2 2 2
创新设计”,实验过程如下:
①将一支球形干燥管水平放置,用滴管吸取3ml(密度为1g/ml)质量分数为5%的HO 加入干燥管的球泡
2 2
内,再用药匙取0.2gMnO 粉末,加在干燥管的进气管的管壁上。
2
②点燃橡胶塞上棒香后,塞紧干燥管并将其竖立,观察到带火星的棒香立即复燃。
对该创新实验的评价,你认为不合理的是 (填序号)。
A.实验中所用的仪器、材料及药品均易得到
B.实验使用的药品用量太大
C.反应速度太慢,耽误时间
D.实验现象明显,整个装置好似点燃的灯塔,趣味性强
四、(本题包括1小题,共7分)
37.葡萄糖(CH O)是一种有甜味、易溶于水的白色粉末状固体。请根据葡萄糖的化学式进行以下计算:
6 12 6
(1)葡萄糖的相对分子质量是 。
(2)葡萄糖中各元素质量比是C:H:O= 。
(3)每个葡萄糖分子中共有 个原子。
(4)多少克葡萄糖与88克二氧化碳所含碳元素质量相同?(写出计算过程)
(5)一定质量的葡萄糖溶解于水,得到的混合物中氢原子与氧原子的个数比H:O= ,若该混合物中含
氧元素的质量分数是80%,则碳元素的质量分数是 。
62013—2014 学年第一学期期中考试
初三化学答卷(参考答案)
说明: 1.凡专用名词写错别字均不给分。
2.答主观题时,若使用与参考答案不同的其他合理答案同样给分。
第I卷(选择题 共25分)
一、单项选择题(本题包括25小题,每小题只有1个选项符合题意,共25分)
题号
1 2 3 4 5 6 7 8 9 10
答案
B C C D C A C C C A
题号
11 12 13 14 15 16 17 18 19 20
答案
A B D D D B B D D D
题号
21 22 23 24 25
答案
D B C B B
第Ⅱ卷(非选择题 共75分)
二、(本题共8小题,每空1分,共42分)
26.(1)① N , ② O , ③ H , ④ H O ,
2 2 2 2
⑤ C O , ⑥ N O 或 C O 或 N O 。+2
2 2
(2)① 2 N , ② 3S O 2 - , ③ C u , ④ CaC O ,
4 3
⑤ C O ,⑥ H g 、 O 。
2
27.(1) 略 ;( 分解 )
(2) ;( 化合 )
(3) ;
(4) 。
28.(1) 防止残留液流下来腐蚀标签 ;
(2) 防止冷凝水回流到热的试管底部,使试管破裂 ;
(3) 防止铁丝燃烧时生成的高温的四氧化三铁烫裂集气瓶 。
29. ①④ , N 、 H g , C O 、 H O 。
2 2 2
30. O (氧) ; H + ; N a ; N aSO (或 N aSO) 。
2 4 2 3
31.(1) 可吸入颗粒物或 TS P 。 (2) 冬季 。
(3) 使用清洁燃料,大量植树造林等 。
32.(1) 合理即可 。
(2) A 。(3) MgCl 。
2
(4) 电子层数相同 或 从左到右最外层电子数从 1 到 8 依次增加 。
(5) 氩( A r ) 。(6) B 。(7) A l 3 + 。
7
______________
号试考
___________
名姓
___________
级班
____________
校学
-
-------
----------------------------------------题--------答--------要--------不--------请--------内--------线--------封--------密----------------------------------------33. H O 或 C O 等 , NaC l 或 CuS O 等 , 分子 , 离子 。
2 2 4
三、(本题包括3题,每空1分,共26分)
34.(1) 锥形瓶 。
(2) 略 ,
防止加热时高锰酸钾粉末进入导管 , 用水润湿 ,
将带火星的木条放在集气瓶口,木条复燃,则已集满 。
(3) B 或 C , 略 ,
F 或 G , 检查装置的气密性 。
(4) C , ② 。
(5) 二氧化硫溶于水,瓶内压强小于外界大气压 。
35. (1) 明矾溶于水形成胶状物吸附杂质,使杂质沉降,达到净水的目的 。
(2) 过滤 。(3) 吸附 。(4) 防止暴沸 ; 煮沸 。
(5) 活性炭、小卵石(或石英沙)等 。
36.【实验结论】
(1) O 。(2) 质量 和 化学性质 。
2
(3) 略 。
【实验评价】
(1) 比较 氧化铁 与 二氧化锰的催化效果 。
(2) 二氧化锰的催化效果比氧化铁好 。
【实验拓展】
(1) B 。(2) B 、 C 。
四、(本题包括1小题,共7分)
37.(1) 18 0 。(2) 6 : 1 : 8 。(3) 2 4 。
(4)解:88g×12/44 ×100%= 24g …………………………1分
24g÷(12×6/180×100%) = 60g …………………………1分
(若全对,关注格式1分)
(5) 2 : 1 , 10 % 。
8