文档内容
第3课时 溶液的形成 溶解度
考点1 溶液
1.把少量的下列物质分别放入水中,充分搅拌,不能得到溶液的是( )
A.食盐 B.植物油
C.蔗糖 D.高锰酸钾
2.下列有关溶液的说法正确的是( )
A.形成溶液的溶质都是固态物质
B.饱和溶液的质量分数一定比不饱和溶液的质量分数大
C.溶液具有均一性和稳定性
D.所有物质溶于水形成溶液都要吸收热量
考点2 溶解的现象
3.在装有水的烧杯中分别加入以下物质,其中形成的溶液温度降低的是( )
A.生石灰 B.氢氧化钠
C.氯化钠 D.硝酸铵
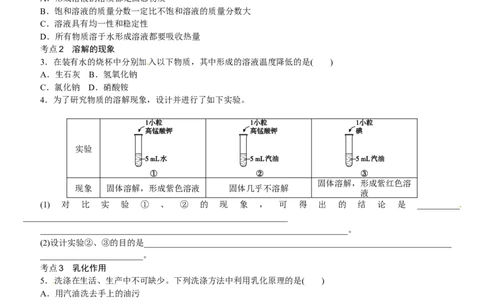
4.为了研究物质的溶解现象,设计并进行了如下实验。
实验
固体溶解,形成紫红色溶
现象 固体溶解,形成紫色溶液 固体几乎不溶解
液
(1) 对 比 实 验 ① 、 ② 的 现 象 , 可 得 出 的 结 论 是 __________
______________________________________________________________
________________________________________________________________________。
(2)设计实验②、③的目的是________________________________________________________________________
________________________。
考点3 乳化作用
5.洗涤在生活、生产中不可缺少。下列洗涤方法中利用乳化原理的是( )
A.用汽油洗去手上的油污
B.用洗洁精洗去餐具上的油污
C.用酒精洗去试管中的碘
D.用稀盐酸洗去盛石灰水的试剂瓶内壁的白膜
考点4 饱和溶液与不饱和溶液[来源:Zxxk.Com]
6.把不饱和溶液变成饱和溶液的最可靠、最简单的方法是( )
A.降低温度 B.蒸发溶剂
C.加入溶质 D.增大压强
考点5 固体物质的溶解度
7.20 ℃时,氯化钠的溶解度为36 g。对这句话理解错误的是( )
A.20 ℃时,100 g水中最多能溶解氯化钠36 g
B.20 ℃时,100 g氯化钠饱和溶液中含氯化钠36 gC.20 ℃时,氯化钠饱和溶液中水与氯化钠的质量比为100∶36
D.20 ℃时,将36 g氯化钠溶解于100 g水中,所得溶液为该温度下氯化钠的饱和溶液
8.20 ℃时,食盐的溶解度是36 g。在20 ℃时,将20 g食盐放在50 g水中,所得溶液的质量是( )
A.70 g B.69 g C.68 g D.67 g
考点6 气体的溶解度
9.生活中的下列现象,能说明气体的溶解度随压强变化而变化的是( )
A.夏季,鱼塘中的鱼常常会浮在水面呼吸
B.喝了汽水以后,常常会打嗝[来源:学科网]
C.打开汽水瓶盖,有大量气泡冒出
D.烧开水时,沸腾前水中有气泡产生
考点7 溶解度曲线
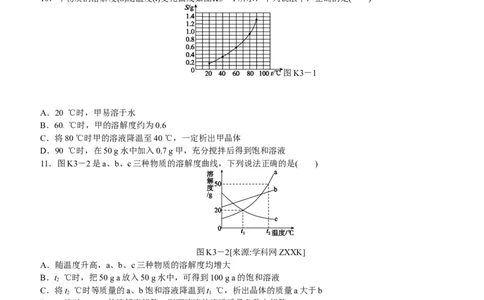
10.甲物质的溶解度(S)随温度(t)变化曲线如图K3-1所示,下列说法中,正确的是( )
图K3-1
A.20 ℃时,甲易溶于水
B.60 ℃时,甲的溶解度约为0.6
C.将80 ℃时甲的溶液降温至40 ℃,一定析出甲晶体
D.90 ℃时,在50 g水中加入0.7 g甲,充分搅拌后得到饱和溶液
11.图K3-2是a、b、c三种物质的溶解度曲线,下列说法正确的是( )
图K3-2[来源:学科网ZXXK]
A.随温度升高,a、b、c三种物质的溶解度均增大
B.t ℃时,把50 g a放入50 g水中,可得到100 g a的饱和溶液
2
C.将t ℃时等质量的a、b饱和溶液降温到t ℃,析出晶体的质量a大于b
2 1
D.t ℃时,a、c的溶解度相等,则两溶液的溶质质量分数也相等
1
1.下列关于溶液的说法错误的是( )
A.固体、液体、气体都可以作溶质
B.NH NO 溶解过程中吸热,溶液温度降低[来源:学+科+网Z+X+X+K]
4 3
C.欲使100克KNO 溶液的质量分数由5%变成10%,可向其中加入5克KNO 固体
3 3
D.25 ℃时,将某KNO 溶液蒸发10克水析出a克晶体,再蒸发10克水析出b克晶体,a与b的质量不一定相等
3
2.高氯酸钾(KClO)可用作火箭推进剂,其溶解度如下表。下列说法正确的是( )
4
20[来
温度/℃ 40 60 80
源:学科网]
溶解度/g 1.68 3.73 7.3 13.4
A.高氯酸钾的溶解度随温度升高而减小
B.20 ℃时,将2 g高氯酸钾溶于98 g水可配制2%的溶液
C.60 ℃时,高氯酸钾饱和溶液中溶质的质量分数是7.3%
D.80 ℃的高氯酸钾饱和溶液冷却至40 ℃有结晶现象
图K3-3
3.三种固体物质a、b、c的溶解度曲线如图K3-3所示,则下列说法不正确的是( )
A.t ℃时三种物质的饱和溶液中溶质的质量分数大小为b>a=c
1
B.a、b、c三种物质的饱和溶液从t ℃降温到t ℃时都有晶体析出
2 1
C.t ℃时,将50 g a物质加入到100 g水中完全溶解形成饱和溶液
2
D.a中混有少量b时可采取降温结晶的方法提纯得到a
4.如图K3-4是氯化钠、氯化铵和碳酸氢钠三种物质的溶解度曲线,分析曲线得到的以下说法中,正确的是( )
图K3-4
①氯化钠和氯化铵是易溶物质,碳酸氢钠是可溶物质
②在20 ℃时,三种物质饱和溶液的溶质质量分数为NH Cl>NaCl>NaHCO
4 3
③在30 ℃时,氯化钠和氯化铵固体各20 g分别溶于50 g水,所得溶液都是饱和溶液
④利用结晶法从氯化钠、氯化铵混合物中分离出氯化铵的最佳温度在10 ℃以下
A.①②③ B.①②④ [来源:Zxxk.Com]
C.②③④ D.①③④
5.图K3-5是对20 ℃一定质量的甲的溶液进行恒温蒸发结晶的实验过程,请回答:
图K3-5
(1)蒸发前原溶液是________(填“饱和”或“不饱和”)溶液。n的数值是________。
(2)依据上述实验,你认为甲的溶解度随温度变化的趋势是________(填序号)。
A.随温度升高而增大
B.随温度升高而减小
C.无法判断参考答案
夯实基础
1.B 2.C 3.D
4.(1)同种溶质在不同溶剂中的溶解性不同
(2)不同溶质在同一种溶剂中的溶解性不同[来源:Zxxk.Com]
[解析] (1)实验①、②是高锰酸钾加入等体积的水、汽油中,现象分别是①固体溶解,形成紫色溶液;②固体几乎不溶解,说明同种溶质在不同的溶剂中溶解性不同。(2)实验②、③分别是高锰酸钾、碘加入等体积的汽油里,现象分别是②固
体几乎不溶解;③固体溶解,形成紫红色溶液,说明不同溶质在同一种溶剂中溶解性不同。
5.B 6.C 7.B 8.C 9.C
10.D [解析] 20 ℃时,甲物质的溶解度是0.2 g,甲微溶于水;60 ℃时,甲的溶解度约为0.6 g;将80 ℃时甲的饱和
溶液降温至40 ℃,一定析出甲晶体;90 ℃时,甲物质的溶解度是1.3 g,所以在50 g水中加入0.7 g甲,充分搅拌后得到
饱和溶液。
11.C
能力提升
1.C 2.D 3.B
4.B [解析] ①在20 ℃时,氯化钠和氯化铵的溶解度大于10 g,是易溶物质,碳酸氢钠的溶解度大于1小于10,是
可溶物质;②在20 ℃时,三种物质的溶解度大小为NH Cl>NaCl>NaHCO ,由饱和溶液的溶质质量分数=×100%,可
4 3
知三种物质饱和溶液的溶质质量分数为NH Cl>NaCl>NaHCO ;③30 ℃时,氯化铵的溶解度大于40 g,20 g氯化铵能
4 3
完全溶于50 g水,所得溶液不是饱和溶液,氯化钠的溶解度小于40 g,20 g氯化钠不能全部溶解,所得溶液是饱和溶液;
④由三种物质的溶解度变化规律可知,利用结晶法从氯化钠、氯化铵混合物中分离出氯化铵的最佳温度在10 ℃以下。
5.(1)不饱和 11 (2)C
[解析] (1)根据图示,第一次与第二次蒸发水的质量相同,而析出溶质的质量不同,说明蒸发前原溶液不是饱和溶液。
析出晶体后的溶液是饱和的,因此,第三次蒸发10 g水,析出的晶体质量与第二次相同,为6 g-1 g=5 g,共析出5 g+6
g=11 g甲物质。由于三次均是在恒温下蒸发结晶,因此并不知道该物质的溶解度随温度的变化情况。