文档内容
第六章 化学反应与能量
单元测试卷
(考试时间:90分钟 试卷满分:100分)
第Ⅰ卷(选择题 44 分)
一、选择题:本题包括22小题,每小题只有以个选项符合题意,每小题2分,共44分。
1.下列关于能量的说法不合理的是( )
A.原电池将化学能转化为电能 B.太阳能电池将化学能转化为电能
C.火力发电涉及多种能量之间的转化 D.物质发生化学变化,一定伴随着能量变化
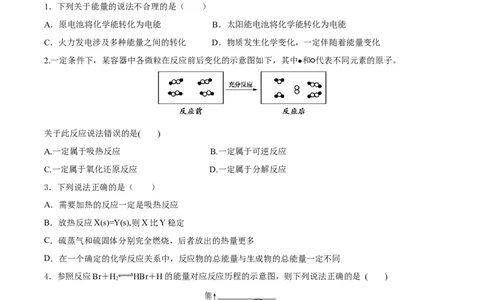
2.一定条件下,某容器中各微粒在反应前后变化的示意图如下,其中 和 代表不同元素的原子。
关于此反应说法错误的是( )
A.一定属于吸热反应 B.一定属于可逆反应
C.一定属于氧化还原反应 D.一定属于分解反应
3.下列说法正确的是( )
A.需要加热的反应一定是吸热反应
B.放热反应X(s)=Y(s),则X比Y稳定
C.硫蒸气和硫固体分别完全燃烧,后者放出的热量更多
D.在一个确定的化学反应关系中,反应物的总能量与生成物的总能量一定不同
4.参照反应Br+H HBr+H的能量对应反应历程的示意图,则下列说法正确的是 ( )
2
A.正反应为吸热反应 B.吸热反应一定要加热后才能发生
C.反应物总能量高于生成物总能量 D.逆反应为放热反应且放热与正反应吸热数值不等
5.化学反应条件的控制具有重要的现实意义。如下反应条件的控制中,不恰当的是( )
A.为防止铁生锈,在其表面涂一层防锈油漆B.为防止火灾,在面粉厂、加油站等场所要严禁烟火
C.为加快KClO 的分解速率而加入MnO
3 2
D.降温加快HO 的分解速率
2 2
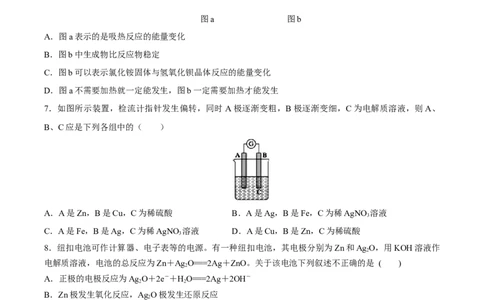
6.如图所示,有关化学反应和能量变化的说法正确的是( )
图a 图b
A.图a表示的是吸热反应的能量变化
B.图b中生成物比反应物稳定
C.图b可以表示氯化铵固体与氢氧化钡晶体反应的能量变化
D.图a不需要加热就一定能发生,图b一定需要加热才能发生
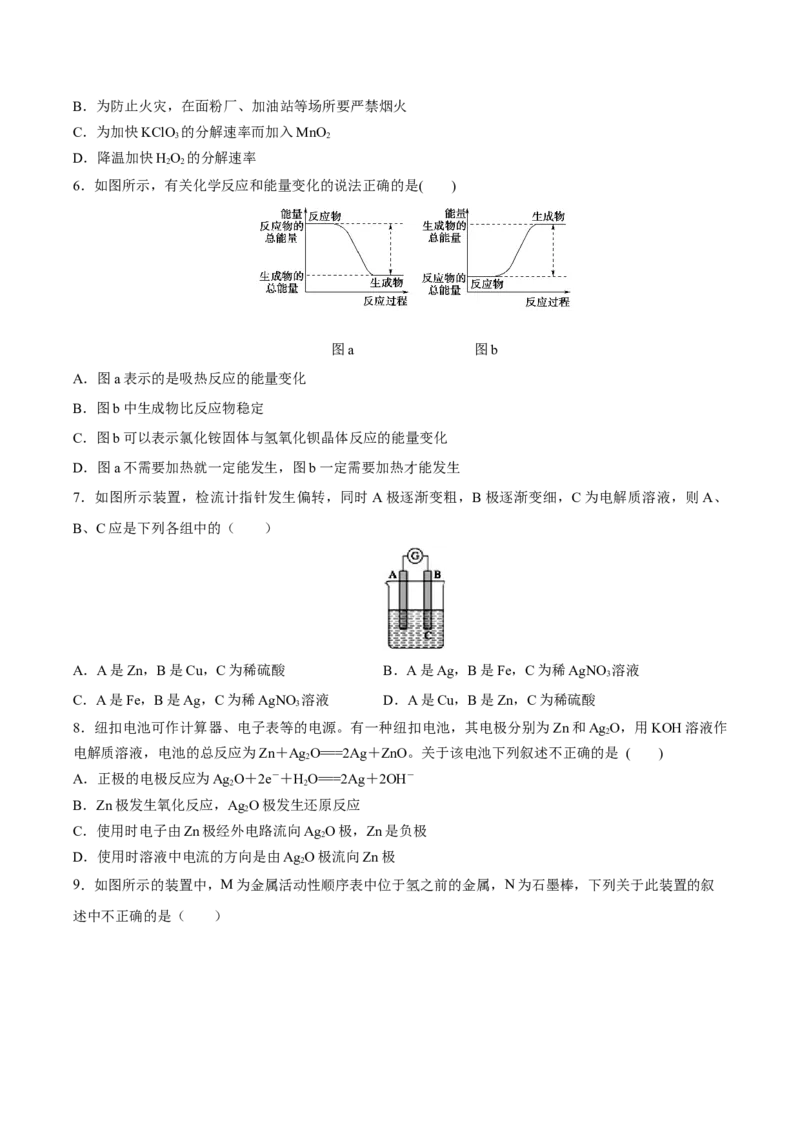
7.如图所示装置,检流计指针发生偏转,同时A极逐渐变粗,B极逐渐变细,C为电解质溶液,则A、
B、C应是下列各组中的( )
A.A是Zn,B是Cu,C为稀硫酸 B.A是Ag,B是Fe,C为稀AgNO 溶液
3
C.A是Fe,B是Ag,C为稀AgNO 溶液 D.A是Cu,B是Zn,C为稀硫酸
3
8.纽扣电池可作计算器、电子表等的电源。有一种纽扣电池,其电极分别为Zn和Ag O,用KOH溶液作
2
电解质溶液,电池的总反应为Zn+Ag O===2Ag+ZnO。关于该电池下列叙述不正确的是 ( )
2
A.正极的电极反应为Ag O+2e-+HO===2Ag+2OH-
2 2
B.Zn极发生氧化反应,Ag O极发生还原反应
2
C.使用时电子由Zn极经外电路流向Ag O极,Zn是负极
2
D.使用时溶液中电流的方向是由Ag O极流向Zn极
2
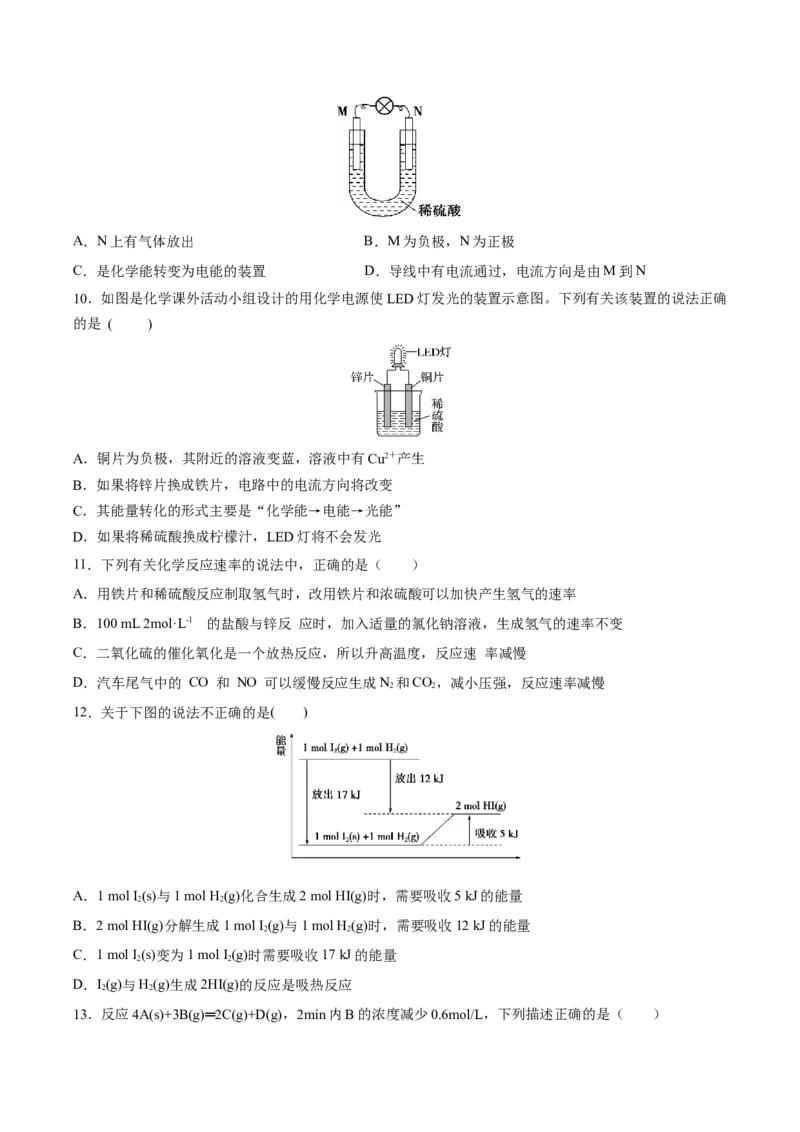
9.如图所示的装置中,M为金属活动性顺序表中位于氢之前的金属,N为石墨棒,下列关于此装置的叙
述中不正确的是( )A.N上有气体放出 B.M为负极,N为正极
C.是化学能转变为电能的装置 D.导线中有电流通过,电流方向是由M到N
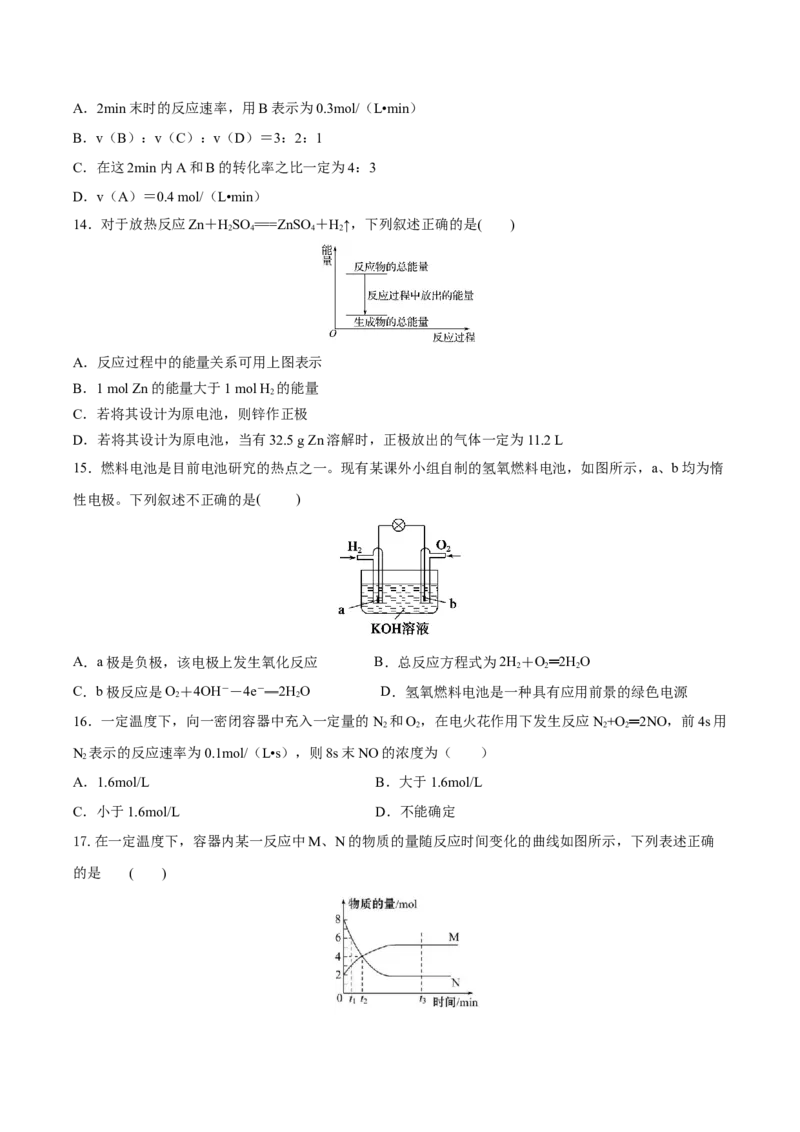
10.如图是化学课外活动小组设计的用化学电源使LED灯发光的装置示意图。下列有关该装置的说法正确
的是 ( )
A.铜片为负极,其附近的溶液变蓝,溶液中有Cu2+产生
B.如果将锌片换成铁片,电路中的电流方向将改变
C.其能量转化的形式主要是“化学能→电能→光能”
D.如果将稀硫酸换成柠檬汁,LED灯将不会发光
11.下列有关化学反应速率的说法中,正确的是( )
A.用铁片和稀硫酸反应制取氢气时,改用铁片和浓硫酸可以加快产生氢气的速率
B.100 mL 2mol·L-1 的盐酸与锌反 应时,加入适量的氯化钠溶液,生成氢气的速率不变
C.二氧化硫的催化氧化是一个放热反应,所以升高温度,反应速 率减慢
D.汽车尾气中的 CO 和 NO 可以缓慢反应生成N 和CO,减小压强,反应速率减慢
2 2
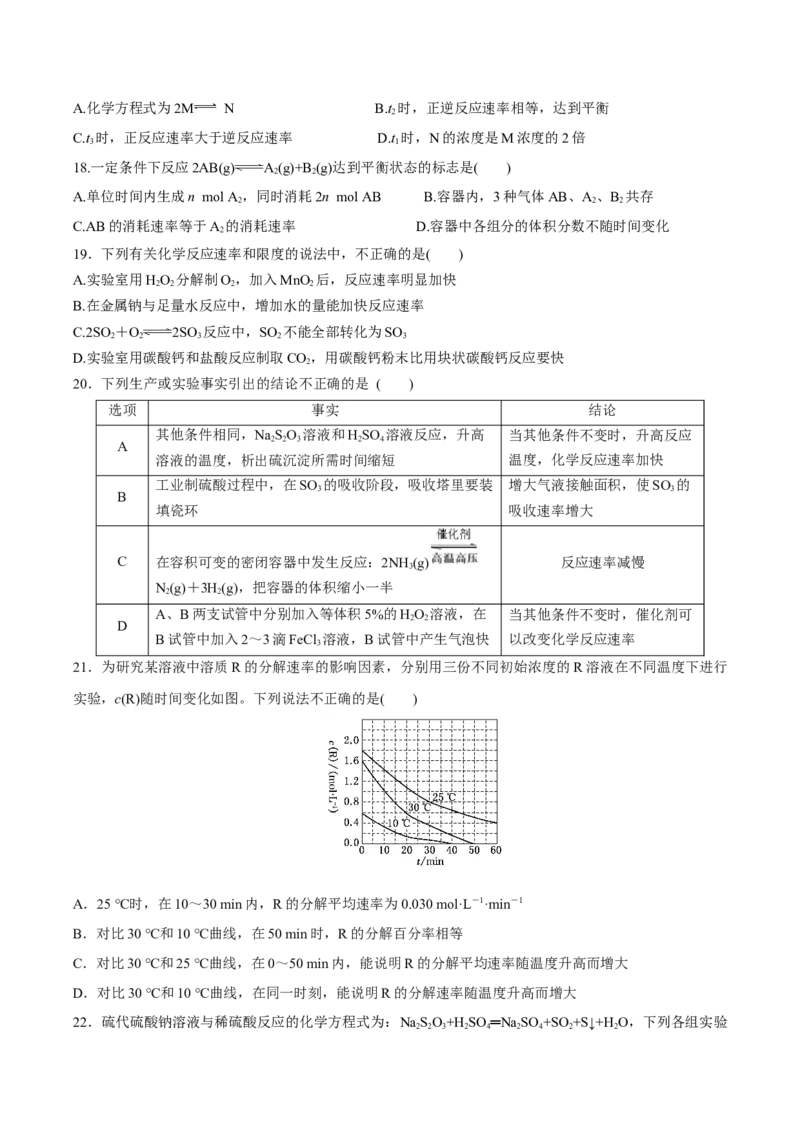
12.关于下图的说法不正确的是( )
A.1 mol I (s)与1 mol H (g)化合生成2 mol HI(g)时,需要吸收5 kJ的能量
2 2
B.2 mol HI(g)分解生成1 mol I (g)与1 mol H (g)时,需要吸收12 kJ的能量
2 2
C.1 mol I (s)变为1 mol I (g)时需要吸收17 kJ的能量
2 2
D.I(g)与H(g)生成2HI(g)的反应是吸热反应
2 2
13.反应4A(s)+3B(g)═2C(g)+D(g),2min内B的浓度减少0.6mol/L,下列描述正确的是( )A.2min末时的反应速率,用B表示为0.3mol/(L•min)
B.v(B):v(C):v(D)=3:2:1
C.在这2min内A和B的转化率之比一定为4:3
D.v(A)=0.4 mol/(L•min)
14.对于放热反应Zn+HSO ===ZnSO +H↑,下列叙述正确的是( )
2 4 4 2
A.反应过程中的能量关系可用上图表示
B.1 mol Zn的能量大于1 mol H 的能量
2
C.若将其设计为原电池,则锌作正极
D.若将其设计为原电池,当有32.5 g Zn溶解时,正极放出的气体一定为11.2 L
15.燃料电池是目前电池研究的热点之一。现有某课外小组自制的氢氧燃料电池,如图所示,a、b均为惰
性电极。下列叙述不正确的是( )
A.a极是负极,该电极上发生氧化反应 B.总反应方程式为2H+O═2H O
2 2 2
C.b极反应是O+4OH--4e-═2HO D.氢氧燃料电池是一种具有应用前景的绿色电源
2 2
16.一定温度下,向一密闭容器中充入一定量的N 和O,在电火花作用下发生反应N+O ═2NO,前4s用
2 2 2 2
N 表示的反应速率为0.1mol/(L•s),则8s末NO的浓度为( )
2
A.1.6mol/L B.大于1.6mol/L
C.小于1.6mol/L D.不能确定
17.在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图所示,下列表述正确
的是 ( )A.化学方程式为2M N B.t 时,正逆反应速率相等,达到平衡
2
C.t 时,正反应速率大于逆反应速率 D.t 时,N的浓度是M浓度的2倍
3 1
18.一定条件下反应2AB(g) A(g)+B (g)达到平衡状态的标志是( )
2 2
A.单位时间内生成n mol A,同时消耗2n mol AB B.容器内,3种气体AB、A、B 共存
2 2 2
C.AB的消耗速率等于A 的消耗速率 D.容器中各组分的体积分数不随时间变化
2
19.下列有关化学反应速率和限度的说法中,不正确的是( )
A.实验室用HO 分解制O,加入MnO 后,反应速率明显加快
2 2 2 2
B.在金属钠与足量水反应中,增加水的量能加快反应速率
C.2SO +O 2SO 反应中,SO 不能全部转化为SO
2 2 3 2 3
D.实验室用碳酸钙和盐酸反应制取CO,用碳酸钙粉末比用块状碳酸钙反应要快
2
20.下列生产或实验事实引出的结论不正确的是 ( )
选项 事实 结论
其他条件相同,NaSO 溶液和HSO 溶液反应,升高 当其他条件不变时,升高反应
2 2 3 2 4
A
溶液的温度,析出硫沉淀所需时间缩短 温度,化学反应速率加快
工业制硫酸过程中,在SO 的吸收阶段,吸收塔里要装 增大气液接触面积,使SO 的
3 3
B
填瓷环 吸收速率增大
C 在容积可变的密闭容器中发生反应:2NH (g) 反应速率减慢
3
N(g)+3H(g),把容器的体积缩小一半
2 2
A、B两支试管中分别加入等体积5%的HO 溶液,在 当其他条件不变时,催化剂可
2 2
D
B试管中加入2~3滴FeCl 溶液,B试管中产生气泡快 以改变化学反应速率
3
21.为研究某溶液中溶质R的分解速率的影响因素,分别用三份不同初始浓度的R溶液在不同温度下进行
实验,c(R)随时间变化如图。下列说法不正确的是( )
A.25 ℃时,在10~30 min内,R的分解平均速率为0.030 mol·L-1·min-1
B.对比30 ℃和10 ℃曲线,在50 min时,R的分解百分率相等
C.对比30 ℃和25 ℃曲线,在0~50 min内,能说明R的分解平均速率随温度升高而增大
D.对比30 ℃和10 ℃曲线,在同一时刻,能说明R的分解速率随温度升高而增大
22.硫代硫酸钠溶液与稀硫酸反应的化学方程式为:NaSO+H SO ═Na SO +SO+S↓+H O,下列各组实验
2 2 3 2 4 2 4 2 2中最先出现浑浊的是( )
实验 反应温度/℃ NaSO 溶液 稀HSO HO
2 2 3 2 4 2
V/mL c/(mol•L﹣1) V/mL c/(mol•L﹣1) V/mL
A 25 5 0.1 10 0.1 5
B 25 5 0.2 5 0.2 10
C 35 5 0.15 5 0.15 5
D 35 5 0.2 5 0.2 20
第 II 卷(非选择题 共 56 分)
二、非选择题:本题共5个小题,共56分。
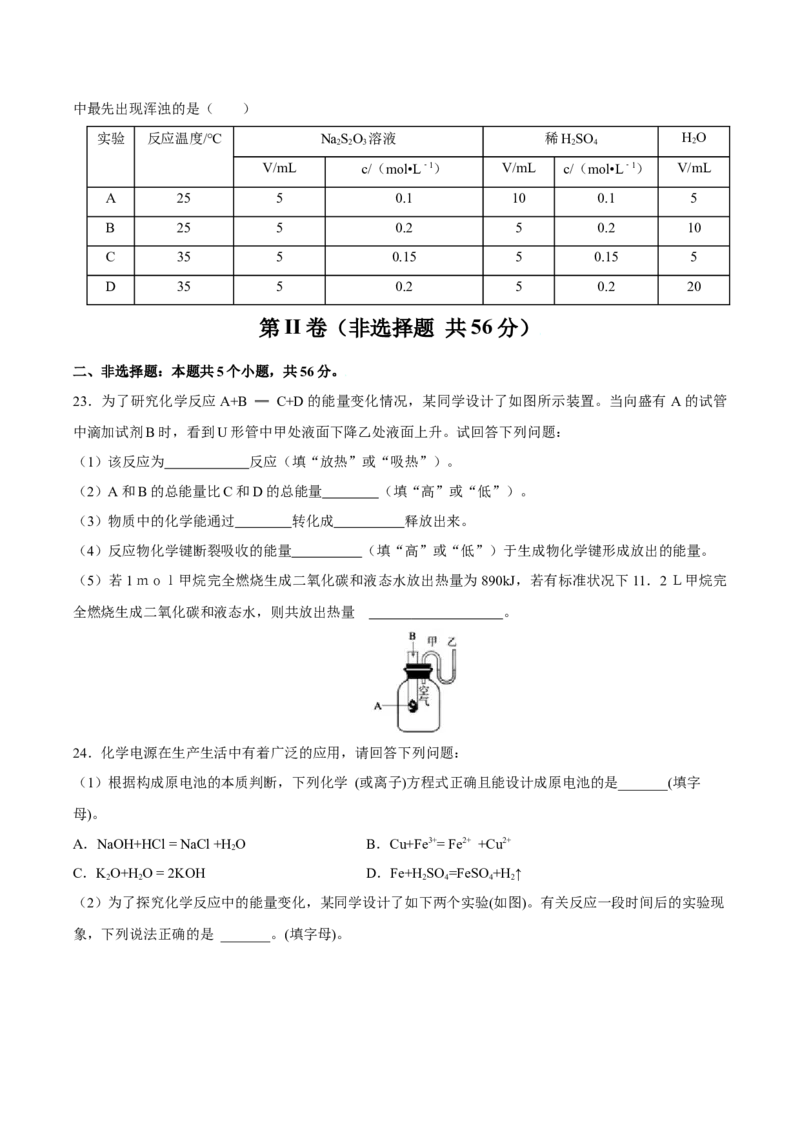
23.为了研究化学反应A+B ═ C+D的能量变化情况,某同学设计了如图所示装置。当向盛有 A的试管
中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。试回答下列问题:
(1)该反应为 反应(填“放热”或“吸热”)。
(2)A和B的总能量比C和D的总能量 (填“高”或“低”)。
(3)物质中的化学能通过 转化成 释放出来。
(4)反应物化学键断裂吸收的能量 (填“高”或“低”)于生成物化学键形成放出的能量。
(5)若1mol甲烷完全燃烧生成二氧化碳和液态水放出热量为 890kJ,若有标准状况下11.2L甲烷完
全燃烧生成二氧化碳和液态水,则共放出热量 。
24.化学电源在生产生活中有着广泛的应用,请回答下列问题:
(1)根据构成原电池的本质判断,下列化学 (或离子)方程式正确且能设计成原电池的是_______(填字
母)。
A.NaOH+HCl = NaCl +H O B.Cu+Fe3+= Fe2+ +Cu2+
2
C.KO+HO = 2KOH D.Fe+H SO =FeSO+H ↑
2 2 2 4 4 2
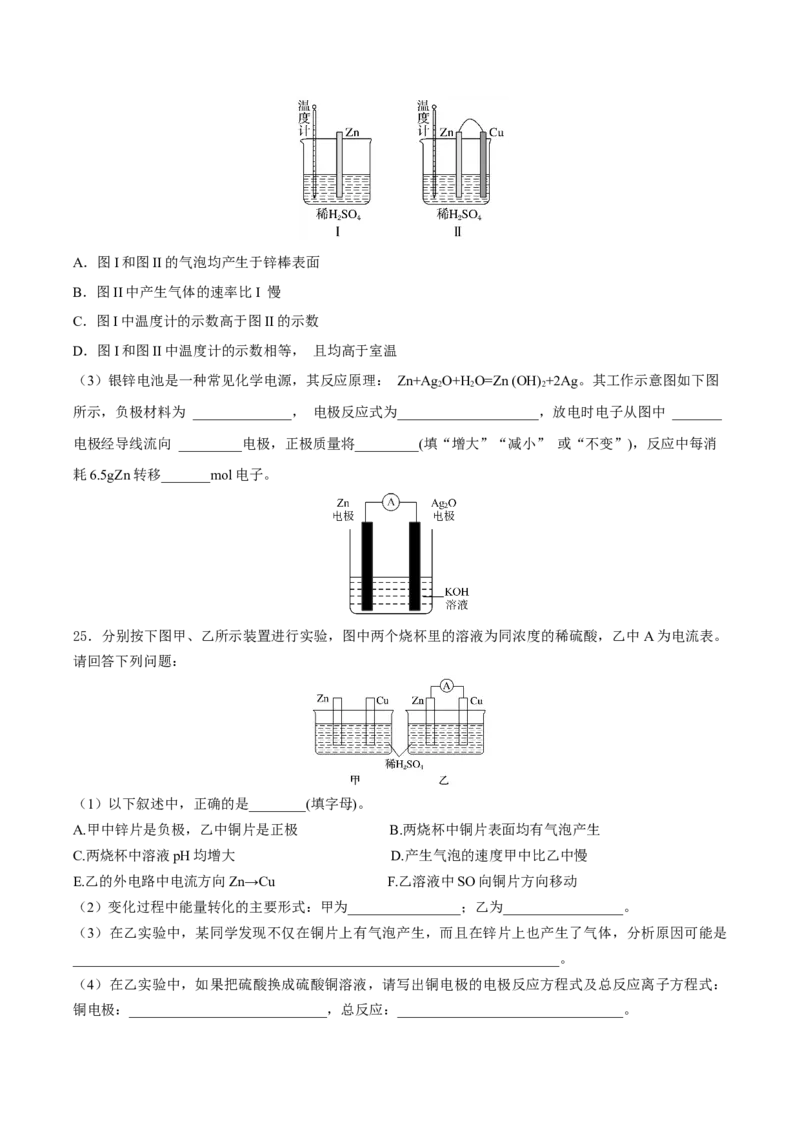
(2)为了探究化学反应中的能量变化,某同学设计了如下两个实验(如图)。有关反应一段时间后的实验现
象,下列说法正确的是 _______。(填字母)。A.图I和图II的气泡均产生于锌棒表面
B.图II中产生气体的速率比I 慢
C.图I中温度计的示数高于图II的示数
D.图I和图II中温度计的示数相等, 且均高于室温
(3)银锌电池是一种常见化学电源,其反应原理: Zn+Ag O+HO=Zn (OH) +2Ag。其工作示意图如下图
2 2 2
所示,负极材料为 ______________, 电极反应式为____________________,放电时电子从图中 _______
电极经导线流向 _________电极,正极质量将_________(填“增大”“减小” 或“不变”),反应中每消
耗6.5gZn转移_______mol电子。
25.分别按下图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中A为电流表。
请回答下列问题:
(1)以下叙述中,正确的是________(填字母)。
A.甲中锌片是负极,乙中铜片是正极 B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液pH均增大 D.产生气泡的速度甲中比乙中慢
E.乙的外电路中电流方向Zn→Cu F.乙溶液中SO向铜片方向移动
(2)变化过程中能量转化的主要形式:甲为________________;乙为_________________。
(3)在乙实验中,某同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是
_____________________________________________________________________。
(4)在乙实验中,如果把硫酸换成硫酸铜溶液,请写出铜电极的电极反应方程式及总反应离子方程式:
铜电极:____________________________,总反应:________________________________。当电路中转移0.25 mol电子时,消耗负极材料的质量为___________ g(Zn的相对原子质量65)。
26.在容积为2L的密闭容器中进行如下反应:A(g)+2B(g) 3C(g)+2D(g),开始时A为4mol,B为
6mol,5min末达到平衡,此时测得C的物质的量为3mol。计算:
(1)平衡时A的物质的量浓度为________________mol/L;前5min内用B表示的化学反应速率v(B)为
_______________mol·L-1·min-1.
(2)判断该反应达到平衡状态的依据是___________(填序号)。
①B减少的反应速率和D减少的反应速率相等
②A、B、C、D的浓度都相等
③A、B、C、D的浓度都不再发生变化
(3)能使该反应的反应速率增大的是___________(填序号)。
a、适当升高温度 b、及时分离出D气体
c、增大B的浓度 d、选择高效的催化剂
(4)微型纽扣电池在现代生活中有广泛应用。有一种银锌电池,其电极分别是Ag O和Zn,电解质溶液
2
为KOH溶液,电极反应式为Zn+2OH--2e-=Zn(OH) ,Ag O+HO+2e-=2Ag+2OH-。根据上述反应式,完
2 2 2
成下列题目。
①判断下列叙述中正确的是___________。
A.在使用过程中,电解质KOH不断被消耗
B.使用过程中,电子由Ag O极经外电路流向Zn极
2
C.Zn是负极,Ag O是正极
2
D.Zn电极发生还原反应,Ag O电极发生氧化反应
2
②写出电池的总反应式:_______________________________。
③使用时,负极区的c(OH-)__________(填“增大”“减小”或“不变”,下同),电解质溶液中的
c(OH-)___________。
27.化学反应速率和限度与生产、生活密切相关。
(1)某学生为了探究锌与盐酸反应过程中的速率变化,在 400 mL稀盐酸中加入足量的锌粉,用排水集气
法收集反应放出的氢气,实验记录如下(累计值):
时间/min 1 2 3 4 5
氢气体积/mL (标准状况) 100 240 464 576 620①哪一时间段反应速率最大__________________________min(填“0~1”“1~2”“2~3”“3~4”或“4~5”),
原因是_________________________________________________________________。
②求3~4 min时间段以盐酸的浓度变化来表示的该反应速率________________(设溶液体积不变)。
(2)另一学生为控制反应速率防止反应过快难以测量氢气体积,他事先在盐酸中加入等体积的下列溶液
以减慢反应速率,你认为不可行的是________(填字母)。
A.蒸馏水 B.KCl溶液
C.KNO 溶液 D.CuSO 溶液
3 4
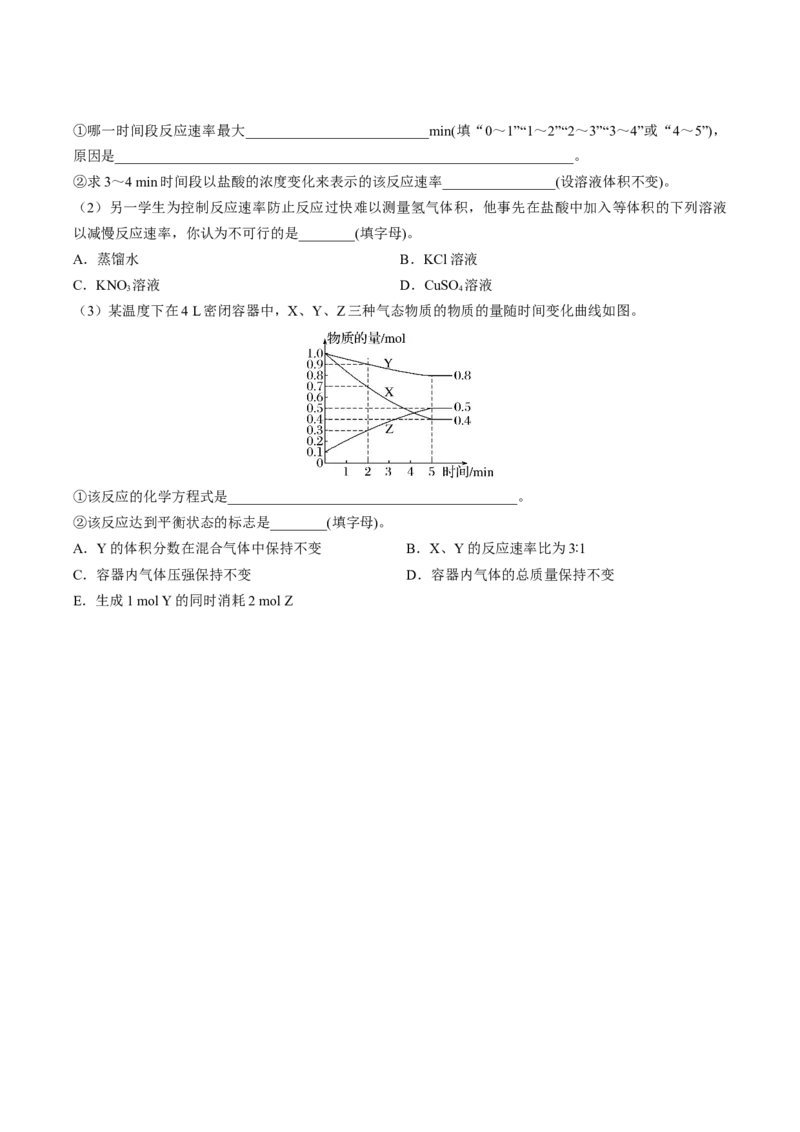
(3)某温度下在4 L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。
①该反应的化学方程式是_________________________________________。
②该反应达到平衡状态的标志是________(填字母)。
A.Y的体积分数在混合气体中保持不变 B.X、Y的反应速率比为3∶1
C.容器内气体压强保持不变 D.容器内气体的总质量保持不变
E.生成1 mol Y的同时消耗2 mol Z