文档内容
第12讲 化学方程式
第1课时 化学方程式和质量守恒定律
一、选择题
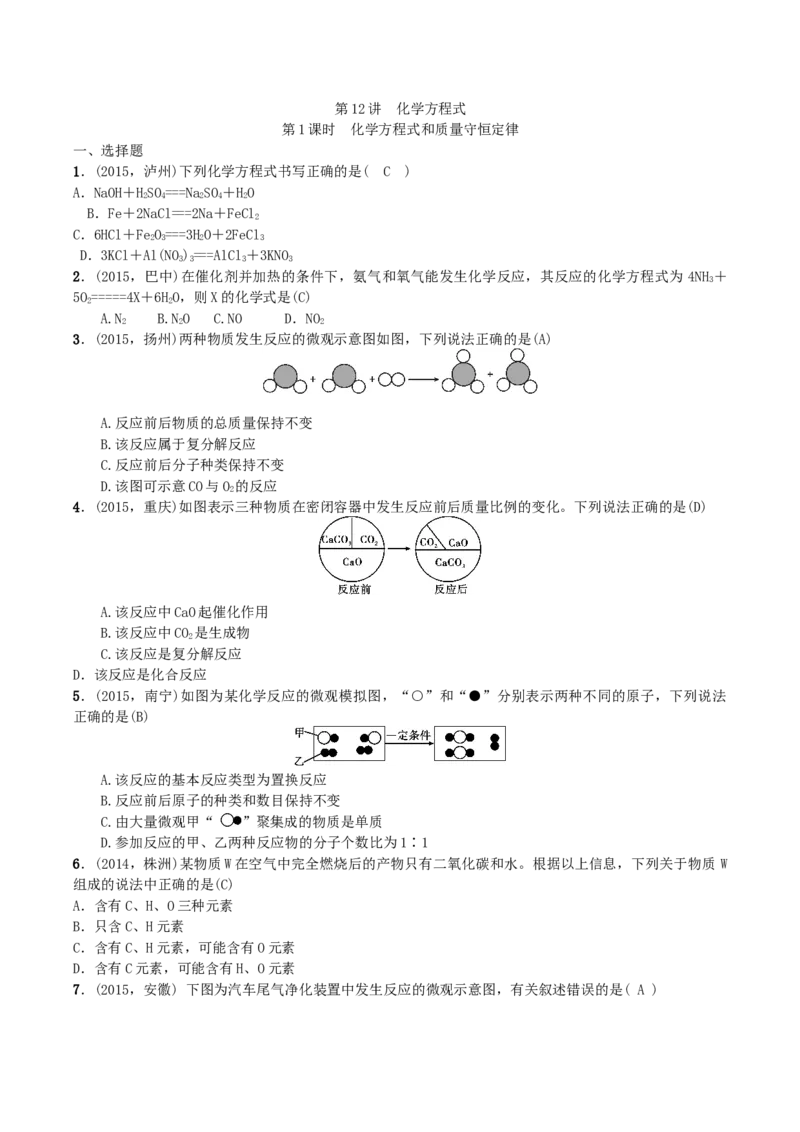
1.(2015,泸州)下列化学方程式书写正确的是( C )
A.NaOH+HSO===NaSO+HO
2 4 2 4 2
B.Fe+2NaCl===2Na+FeCl
2
C.6HCl+FeO===3HO+2FeCl
2 3 2 3
D.3KCl+Al(NO)===AlCl+3KNO
3 3 3 3
2.(2015,巴中)在催化剂并加热的条件下,氨气和氧气能发生化学反应,其反应的化学方程式为 4NH +
3
5O=====4X+6HO,则X的化学式是(C)
2 2
A.N B.NO C.NO D.NO
2 2 2
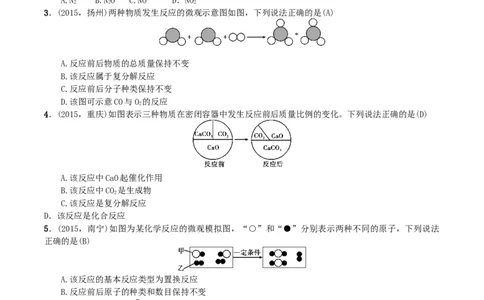
3.(2015,扬州)两种物质发生反应的微观示意图如图,下列说法正确的是(A)
A.反应前后物质的总质量保持不变
B.该反应属于复分解反应
C.反应前后分子种类保持不变
D.该图可示意CO与O 的反应
2
4.(2015,重庆)如图表示三种物质在密闭容器中发生反应前后质量比例的变化。下列说法正确的是(D)
A.该反应中CaO起催化作用
B.该反应中CO 是生成物
2
C.该反应是复分解反应
D.该反应是化合反应
5.(2015,南宁)如图为某化学反应的微观模拟图,“○”和“●”分别表示两种不同的原子,下列说法
正确的是(B)
A.该反应的基本反应类型为置换反应
B.反应前后原子的种类和数目保持不变
C.由大量微观甲“ ”聚集成的物质是单质
D.参加反应的甲、乙两种反应物的分子个数比为1∶1
6.(2014,株洲)某物质W在空气中完全燃烧后的产物只有二氧化碳和水。根据以上信息,下列关于物质 W
组成的说法中正确的是(C)
A.含有C、H、O三种元素
B.只含C、H元素
C.含有C、H元素,可能含有O元素
D.含有C元素,可能含有H、O元素
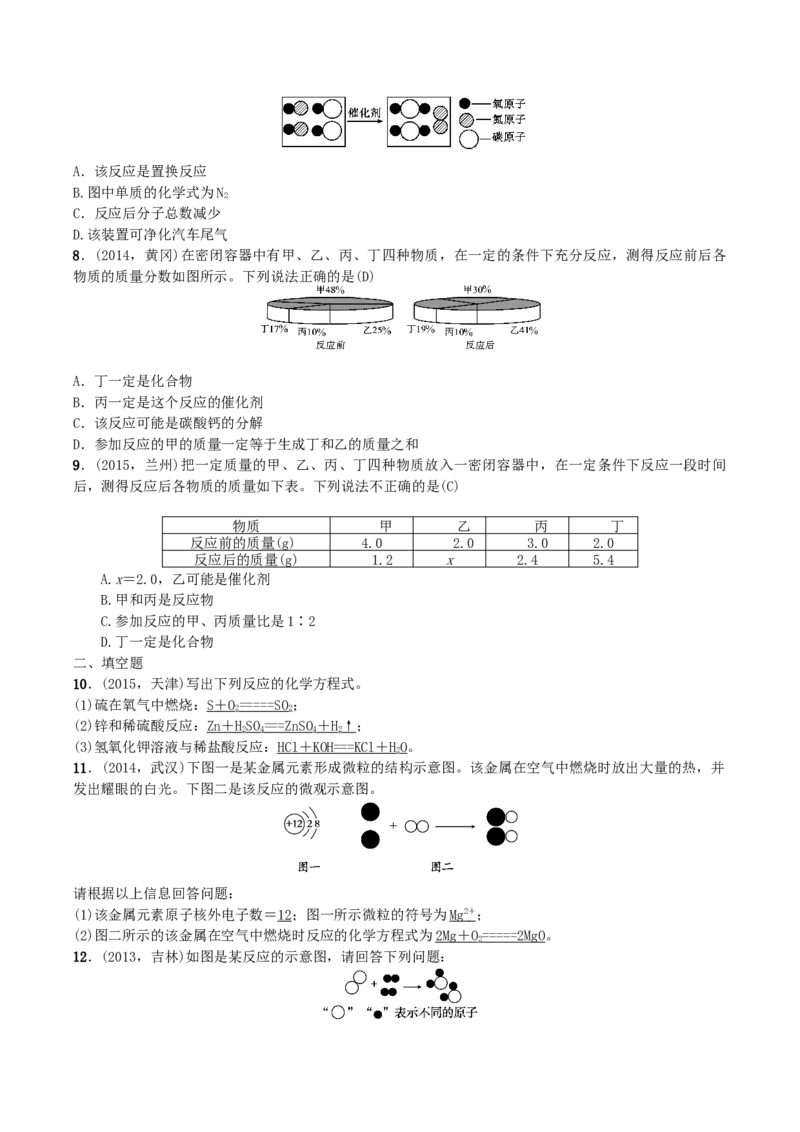
7.(2015,安徽) 下图为汽车尾气净化装置中发生反应的微观示意图,有关叙述错误的是( A )A.该反应是置换反应
B.图中单质的化学式为N
2
C.反应后分子总数减少
D.该装置可净化汽车尾气
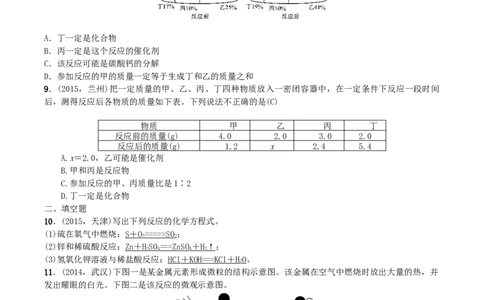
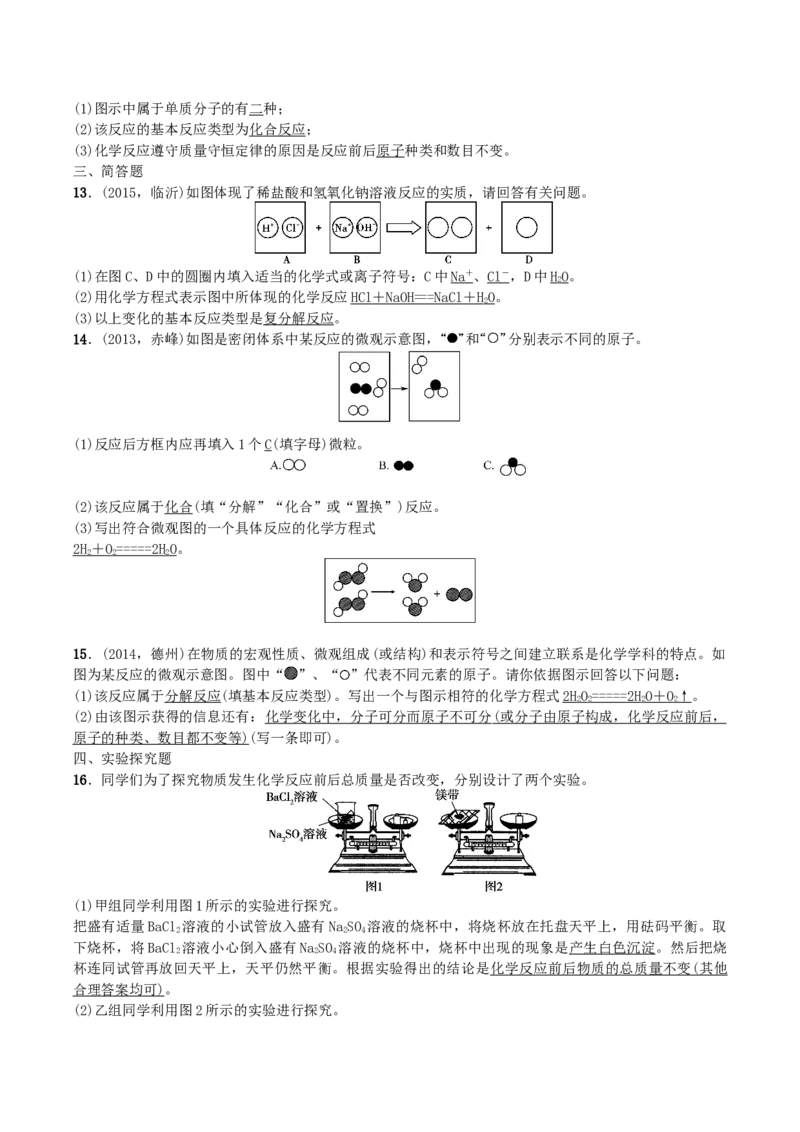
8.(2014,黄冈)在密闭容器中有甲、乙、丙、丁四种物质,在一定的条件下充分反应,测得反应前后各
物质的质量分数如图所示。下列说法正确的是(D)
A.丁一定是化合物
B.丙一定是这个反应的催化剂
C.该反应可能是碳酸钙的分解
D.参加反应的甲的质量一定等于生成丁和乙的质量之和
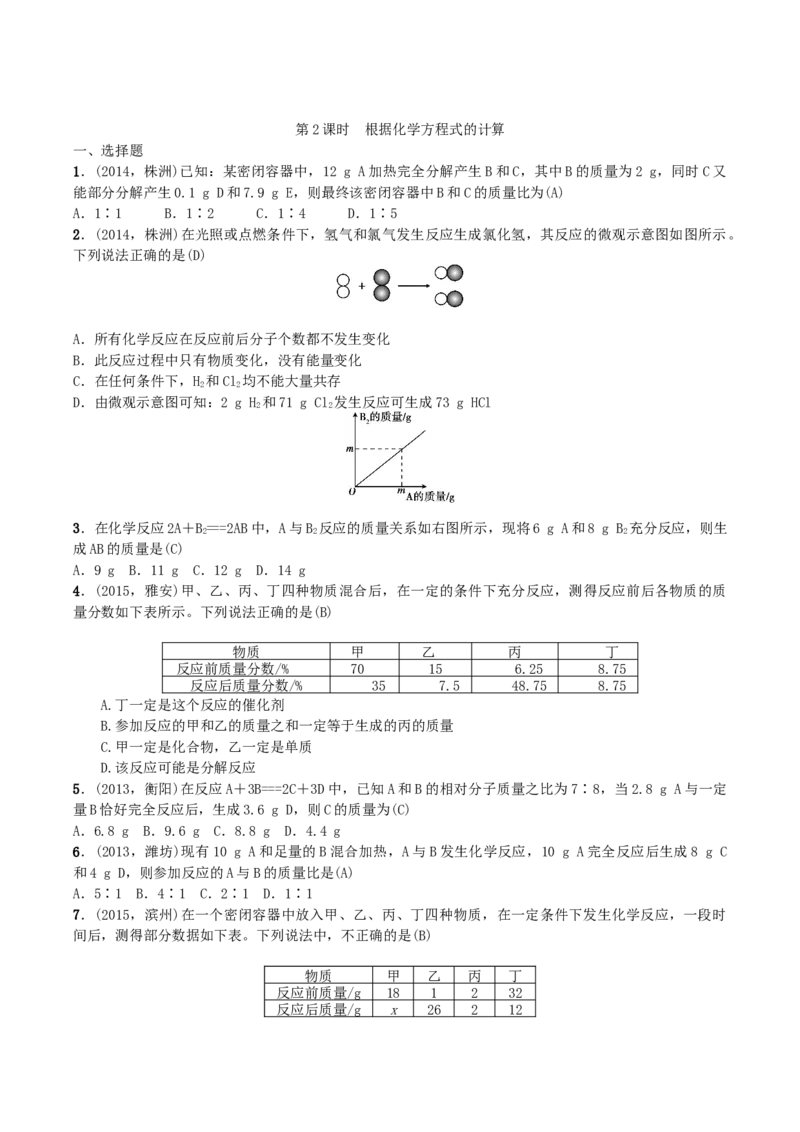
9.(2015,兰州)把一定质量的甲、乙、丙、丁四种物质放入一密闭容器中,在一定条件下反应一段时间
后,测得反应后各物质的质量如下表。下列说法不正确的是(C)
物质 甲 乙 丙 丁
反应前的质量(g) 4.0 2.0 3.0 2.0
反应后的质量(g) 1.2 x 2.4 5.4
A.x=2.0,乙可能是催化剂
B.甲和丙是反应物
C.参加反应的甲、丙质量比是1∶2
D.丁一定是化合物
二、填空题
10.(2015,天津)写出下列反应的化学方程式。
(1)硫在氧气中燃烧: S + O ==== = S O;
2 2
(2)锌和稀硫酸反应: Z n + HSO = = =ZnS O + H↑;
2 4 4 2
(3)氢氧化钾溶液与稀盐酸反应: HC l + KO H = = =KC l + HO。
2
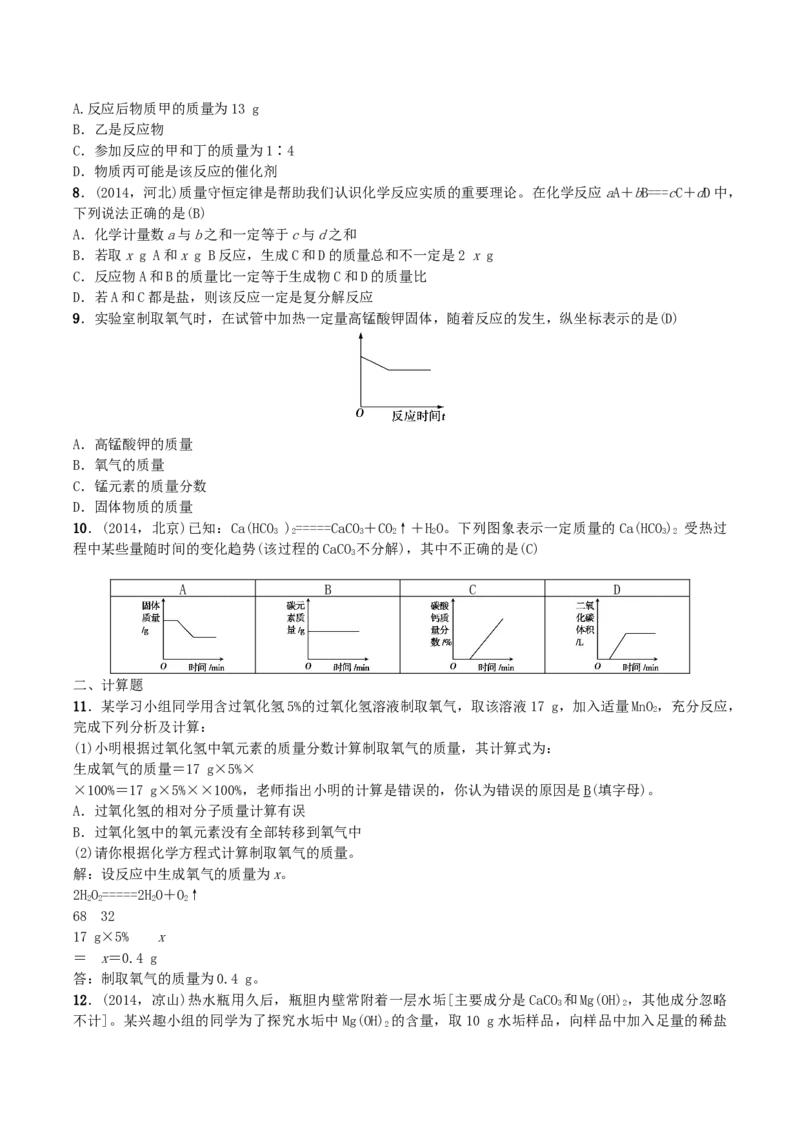
11.(2014,武汉)下图一是某金属元素形成微粒的结构示意图。该金属在空气中燃烧时放出大量的热,并
发出耀眼的白光。下图二是该反应的微观示意图。
请根据以上信息回答问题:
(1)该金属元素原子核外电子数=12;图一所示微粒的符号为 M g 2 + ;
(2)图二所示的该金属在空气中燃烧时反应的化学方程式为 2M g + O ==== = 2Mg O。
2
12.(2013,吉林)如图是某反应的示意图,请回答下列问题:(1)图示中属于单质分子的有二种;
(2)该反应的基本反应类型为化合反应;
(3)化学反应遵守质量守恒定律的原因是反应前后原子种类和数目不变。
三、简答题
13.(2015,临沂)如图体现了稀盐酸和氢氧化钠溶液反应的实质,请回答有关问题。
(1)在图C、D中的圆圈内填入适当的化学式或离子符号:C中 N a + 、 C l - ,D中HO。
2
(2)用化学方程式表示图中所体现的化学反应 HC l + NaO H = = =NaC l + HO。
2
(3)以上变化的基本反应类型是复分解反应。
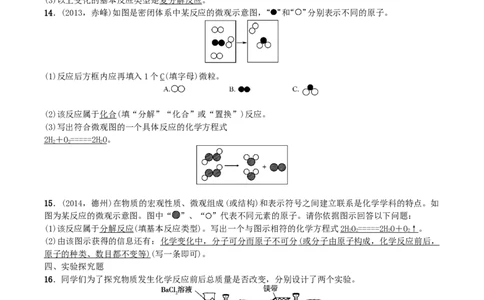
14.(2013,赤峰)如图是密闭体系中某反应的微观示意图, 和 分别表示不同的原子。
(1)反应后方框内应再填入1个C(填字母)微粒。
(2)该反应属于化合(填“分解”“化合”或“置换”)反应。
(3)写出符合微观图的一个具体反应的化学方程式
2H + O ==== = 2 HO。
2 2 2
15.(2014,德州)在物质的宏观性质、微观组成(或结构)和表示符号之间建立联系是化学学科的特点。如
图为某反应的微观示意图。图中“ ”、“ ”代表不同元素的原子。请你依据图示回答以下问题:
(1)该反应属于分解反应(填基本反应类型)。写出一个与图示相符的化学方程式2HO ==== = 2 H O + O↑。
2 2 2 2
(2)由该图示获得的信息还有: 化学变化中,分子可分而原子不可分 ( 或分子由原子构成,化学反应前后,
原子的种类、数目都不变等 )(写一条即可)。
四、实验探究题
16.同学们为了探究物质发生化学反应前后总质量是否改变,分别设计了两个实验。
(1)甲组同学利用图1所示的实验进行探究。
把盛有适量BaCl 溶液的小试管放入盛有NaSO 溶液的烧杯中,将烧杯放在托盘天平上,用砝码平衡。取
2 2 4
下烧杯,将BaCl 溶液小心倒入盛有NaSO 溶液的烧杯中,烧杯中出现的现象是产生白色沉淀。然后把烧
2 2 4
杯连同试管再放回天平上,天平仍然平衡。根据实验得出的结论是 化学反应前后物质的总质量不变 ( 其他
合理答案均可 )。
(2)乙组同学利用图2所示的实验进行探究。取一根用砂纸打磨干净的长镁带和一个石棉网,将它们一起放在托盘天平上,用砝码平衡。取下石棉网,
在石棉网上方点燃镁带,发生反应的化学方程式为 2M g + O ===== 2Mg O。燃烧结束后将所得的物质与石棉网
2
一起再放回托盘天平上称量,意外发现质量减轻了。请你分析产生这一现象的原因可能是部分生成物以白
烟形式逸散到空气中 ( 其他合理答案均可 )。第2课时 根据化学方程式的计算
一、选择题
1.(2014,株洲)已知:某密闭容器中,12 g A加热完全分解产生B和C,其中B的质量为2 g,同时C又
能部分分解产生0.1 g D和7.9 g E,则最终该密闭容器中B和C的质量比为(A)
A.1∶1 B.1∶2 C.1∶4 D.1∶5
2.(2014,株洲)在光照或点燃条件下,氢气和氯气发生反应生成氯化氢,其反应的微观示意图如图所示。
下列说法正确的是(D)
A.所有化学反应在反应前后分子个数都不发生变化
B.此反应过程中只有物质变化,没有能量变化
C.在任何条件下,H 和Cl 均不能大量共存
2 2
D.由微观示意图可知:2 g H 和71 g Cl 发生反应可生成73 g HCl
2 2
3.在化学反应2A+B===2AB中,A与B 反应的质量关系如右图所示,现将6 g A和8 g B 充分反应,则生
2 2 2
成AB的质量是(C)
A.9 g B.11 g C.12 g D.14 g
4.(2015,雅安)甲、乙、丙、丁四种物质混合后,在一定的条件下充分反应,测得反应前后各物质的质
量分数如下表所示。下列说法正确的是(B)
物质 甲 乙 丙 丁
反应前质量分数/% 70 15 6.25 8.75
反应后质量分数/% 35 7.5 48.75 8.75
A.丁一定是这个反应的催化剂
B.参加反应的甲和乙的质量之和一定等于生成的丙的质量
C.甲一定是化合物,乙一定是单质
D.该反应可能是分解反应
5.(2013,衡阳)在反应A+3B===2C+3D中,已知A和B的相对分子质量之比为7∶8,当2.8 g A与一定
量B恰好完全反应后,生成3.6 g D,则C的质量为(C)
A.6.8 g B.9.6 g C.8.8 g D.4.4 g
6.(2013,潍坊)现有10 g A和足量的B混合加热,A与B发生化学反应,10 g A完全反应后生成8 g C
和4 g D,则参加反应的A与B的质量比是(A)
A.5∶1 B.4∶1 C.2∶1 D.1∶1
7.(2015,滨州)在一个密闭容器中放入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,一段时
间后,测得部分数据如下表。下列说法中,不正确的是(B)
物质 甲 乙 丙 丁
反应前质量/g 18 1 2 32
反应后质量/g x 26 2 12A.反应后物质甲的质量为13 g
B.乙是反应物
C.参加反应的甲和丁的质量为1∶4
D.物质丙可能是该反应的催化剂
8.(2014,河北)质量守恒定律是帮助我们认识化学反应实质的重要理论。在化学反应aA+bB===cC+dD中,
下列说法正确的是(B)
A.化学计量数a与b之和一定等于c与d之和
B.若取x g A和x g B反应,生成C和D的质量总和不一定是2 x g
C.反应物A和B的质量比一定等于生成物C和D的质量比
D.若A和C都是盐,则该反应一定是复分解反应
9.实验室制取氧气时,在试管中加热一定量高锰酸钾固体,随着反应的发生,纵坐标表示的是(D)
A.高锰酸钾的质量
B.氧气的质量
C.锰元素的质量分数
D.固体物质的质量
10.(2014,北京)已知:Ca(HCO )=====CaCO +CO↑+HO。下列图象表示一定质量的Ca(HCO) 受热过
3 2 3 2 2 3 2
程中某些量随时间的变化趋势(该过程的CaCO 不分解),其中不正确的是(C)
3
A B C D
二、计算题
11.某学习小组同学用含过氧化氢5%的过氧化氢溶液制取氧气,取该溶液17 g,加入适量MnO,充分反应,
2
完成下列分析及计算:
(1)小明根据过氧化氢中氧元素的质量分数计算制取氧气的质量,其计算式为:
生成氧气的质量=17 g×5%×
×100%=17 g×5%××100%,老师指出小明的计算是错误的,你认为错误的原因是B(填字母)。
A.过氧化氢的相对分子质量计算有误
B.过氧化氢中的氧元素没有全部转移到氧气中
(2)请你根据化学方程式计算制取氧气的质量。
解:设反应中生成氧气的质量为x。
2HO=====2HO+O↑
2 2 2 2
68 32
17 g×5% x
= x=0.4 g
答:制取氧气的质量为0.4 g。
12.(2014,凉山)热水瓶用久后,瓶胆内壁常附着一层水垢[主要成分是CaCO 和Mg(OH) ,其他成分忽略
3 2
不计]。某兴趣小组的同学为了探究水垢中Mg(OH) 的含量,取10 g水垢样品,向样品中加入足量的稀盐
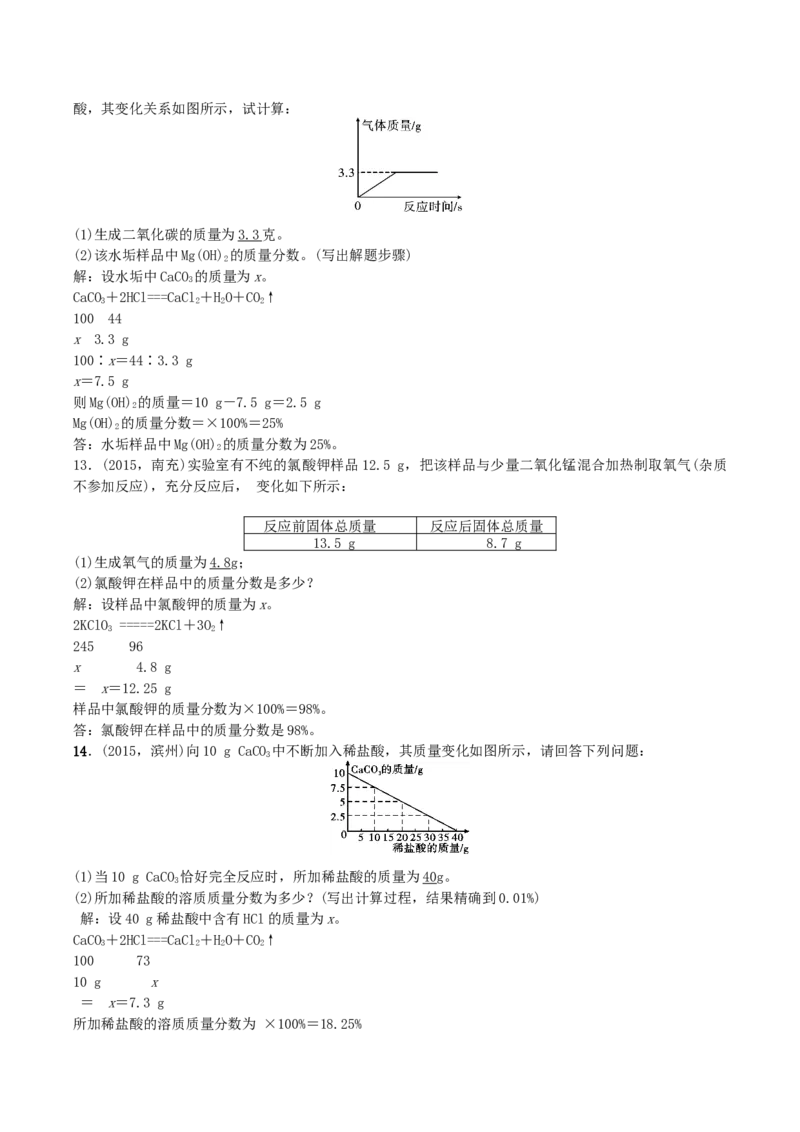
2酸,其变化关系如图所示,试计算:
(1)生成二氧化碳的质量为3.3 克。
(2)该水垢样品中Mg(OH) 的质量分数。(写出解题步骤)
2
解:设水垢中CaCO 的质量为x。
3
CaCO+2HCl===CaCl+HO+CO↑
3 2 2 2
100 44
x 3.3 g
100∶x=44∶3.3 g
x=7.5 g
则Mg(OH) 的质量=10 g-7.5 g=2.5 g
2
Mg(OH) 的质量分数=×100%=25%
2
答:水垢样品中Mg(OH) 的质量分数为25%。
2
13.(2015,南充)实验室有不纯的氯酸钾样品12.5 g,把该样品与少量二氧化锰混合加热制取氧气(杂质
不参加反应),充分反应后, 变化如下所示:
反应前固体总质量 反应后固体总质量
13.5 g 8.7 g
(1)生成氧气的质量为4.8g;
(2)氯酸钾在样品中的质量分数是多少?
解:设样品中氯酸钾的质量为x。
2KClO =====2KCl+3O↑
3 2
245 96
x 4.8 g
= x=12.25 g
样品中氯酸钾的质量分数为×100%=98%。
答:氯酸钾在样品中的质量分数是98%。
14.(2015,滨州)向10 g CaCO 中不断加入稀盐酸,其质量变化如图所示,请回答下列问题:
3
(1)当10 g CaCO 恰好完全反应时,所加稀盐酸的质量为40g。
3
(2)所加稀盐酸的溶质质量分数为多少?(写出计算过程,结果精确到0.01%)
解:设40 g稀盐酸中含有HCl的质量为x。
CaCO+2HCl===CaCl+HO+CO↑
3 2 2 2
100 73
10 g x
= x=7.3 g
所加稀盐酸的溶质质量分数为 ×100%=18.25%答:所加稀盐酸的溶质质量分数为18.25%。