文档内容
《课题3 离子 》 教学案
班级:初三( )姓名: 学科:化学 课型:新授 编者: 审核:备课组
【学习目标】
1、知道原子核外电子是分层排布的。
2、探究分析NaCl的形成过程,了解离子的形成,初步认识离子是构成物质的一种粒子。
3、观察l~20号元素的原子结构示意图,归纳原子最外层电子数与元素性质的关系。
【学习重点】
1.探究分析NaCl的形成过程,了解离子的形成,初步认识离子是构成物质的一种粒子。
2.观察l~20号元素的原子结构示意图,归纳原子最外层电子数与元素性质的关
系
【学习过程】
一. 定向入境
1.预习原子核外电子的分层排布
2.预习离子的形成过程
3.预习并归纳出原子最外层电子数与元素性质的关系
二.自学建架
知识模块
Ⅰ.个人自学
你能说出下列物质是由什么微粒构成的吗? 铁、水、食盐。
(一)核外电子的排布
【自主学习】
1、阅读学生作品──科普小论文《漫游原子世界》,巩固原子结构的知 识。
漫游原子世界
我是一个小、小、小电子,在原子内部很大的空间中围绕着原子核这个小老头不停地转动;我
们在飞,却怎么也飞不高。因为这老头长得很特别:虽然占据原子中央很小的地盘,却是由中
子和质子构成,中子不带电,质子带正电,因此,这小老头也带正电,很有能耐,正好把我们身
上的负电深深吸引,所以我们很难脱离原子核的怀抱。
猜想一下原子核外电子是如何运动的呢?它们能否挣脱原子核的吸引呢?向你的同学说一
说你想象中核外电子如何运动?
2、阅读课本78页图文。
科学家是怎样定义电子层的?利用所学知识进行创意绘画并与同桌交流:(1)氢原子结构图
(2)氧原子结构图(含有8个电子的氧原子中,这8个电子究竟怎样绕核外高速运动呢?)。
3、用原子结构示意图可简明、方便地表示原子的结构。观察课本表4-4中一些原子结构示意
图,你能说出其中每一部分代表的内容吗?
4、从课本上找出什么是相对稳定结构?仔细观察投影:“核电荷数从1—20的各元素的原子
结构示意图”。
思考:不同原子的核外电子排布有无一定规律?
①原子核外第一层最多有几个电子?
1②原子核外第二层最多有几个电子?
③原子核外最外层最多有几个电子?
④决定元素化学性质的是什么?
⑤1—20号元素中哪些是金属元素、非金属元素、稀有气体元素?它们的最外层电子数有何特
点?
【思考交流】
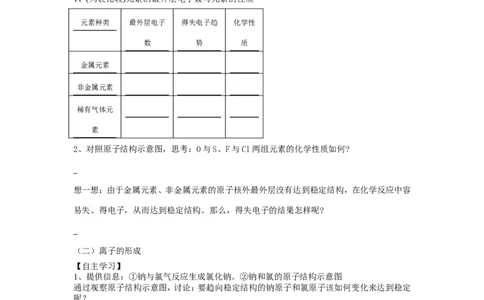
1、(列表比较)元素的最外层电子数与元素的性质
元素种类 最外层电子 得失电子趋 化学性
数 势 质
金属元素
非金属元素
稀有气体元
素
2、对照原子结构示意图,思考:O与S、F与Cl两组元素的化学性质如何?
想一想:由于金属元素、非金属元素的原子核外最外层没有达到稳定结构,在化学反应中容
易失、得电子,从而达到稳定结构。那么,得失电子的结果怎样呢?
(二)离子的形成
【自主学习】
1、提供信息:①钠与氯气反应生成氯化钠。②钠和氯的原子结构示意图
通过观察原子结构示意图,讨论:要趋向稳定结构的钠原子和氯原子该如何变化来达到稳定
呢?
2、阅读课本79页第二段图文。
①找出离子、阴离子、阳离子的概念,并举两例。
离子
阴离子 ;例 。
阳离子 ;例 。
②说说书写离子符号应注意的事项。
2(1) ;(2) ;(3)
三、尝试练习
1、原子与离子的比较
相同点:
不同点:
2、试一试,用图表的形式归纳出:元素、原子、分子、离子、单质、化合物之间的关系。
四、小结
1、原子核外电子是 排布的。最外层最多排 个电了,稳定结构是指:
2、原子结构示意图各部分的意义:
3、金属元素的原子易 形成带 电的 离子;非金属元素的原子易
形成带 电的 离子。
4、离子: 。阳离子带 电;阴离子带 电。
5、原子变成离子的过程中改变的是: ;不变的
是: 。
五、巩固测试
1、原子失去最外层电子或在最外层得到电子后,不发生变化的是 ( )
(1) 元素种类 (2)化学性质 (3)相对原子质量 (4)原子的电性 (5)原子核 (6)电子层数
(7)最外层电子数
A.(1)(3)(5) B.(2)(4)(6)(8) C.(2)(5) D.(1)(5)
2、在下列示意图表示的粒子中,属于原子的有 (填序号,下同),属于阳离子的
有 ,属于阴离子的有________,属于同种元素的为 。
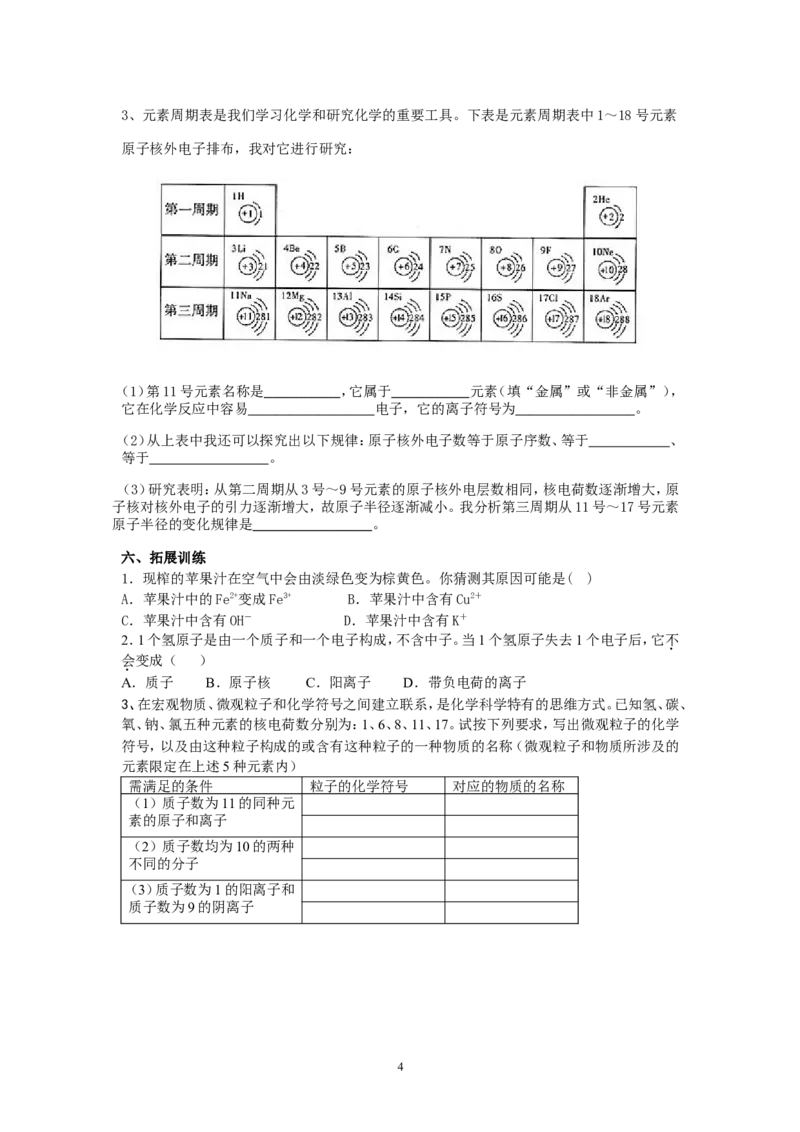
33、元素周期表是我们学习化学和研究化学的重要工具。下表是元素周期表中1~18号元素
原子核外电子排布,我对它进行研究:
(1)第11号元素名称是 ,它属于 元素(填“金属”或“非金属”),
它在化学反应中容易 电子,它的离子符号为 。
(2)从上表中我还可以探究出以下规律:原子核外电子数等于原子序数、等于 、
等于 。
(3)研究表明:从第二周期从3号~9号元素的原子核外电层数相同,核电荷数逐渐增大,原
子核对核外电子的引力逐渐增大,故原子半径逐渐减小。我分析第三周期从11号~17号元素
原子半径的变化规律是 。
六、拓展训练
1.现榨的苹果汁在空气中会由淡绿色变为棕黄色。你猜测其原因可能是( )
A.苹果汁中的Fe2+变成Fe3+ B.苹果汁中含有Cu2+
C.苹果汁中含有OH- D.苹果汁中含有K+
2.1个氢原子是由一个质子和一个电子构成,不含中子。当1个氢原子失去1个电子后,它不
会变成( )
A.质子 B.原子核 C.阳离子 D.带负电荷的离子
3、在宏观物质、微观粒子和化学符号之间建立联系,是化学科学特有的思维方式。已知氢、碳、
氧、钠、氯五种元素的核电荷数分别为:1、6、8、11、17。试按下列要求,写出微观粒子的化学
符号,以及由这种粒子构成的或含有这种粒子的一种物质的名称(微观粒子和物质所涉及的
元素限定在上述5种元素内)
需满足的条件 粒子的化学符号 对应的物质的名称
(1)质子数为11的同种元
素的原子和离子
(2)质子数均为10的两种
不同的分子
(3)质子数为1的阳离子和
质子数为9的阴离子
4