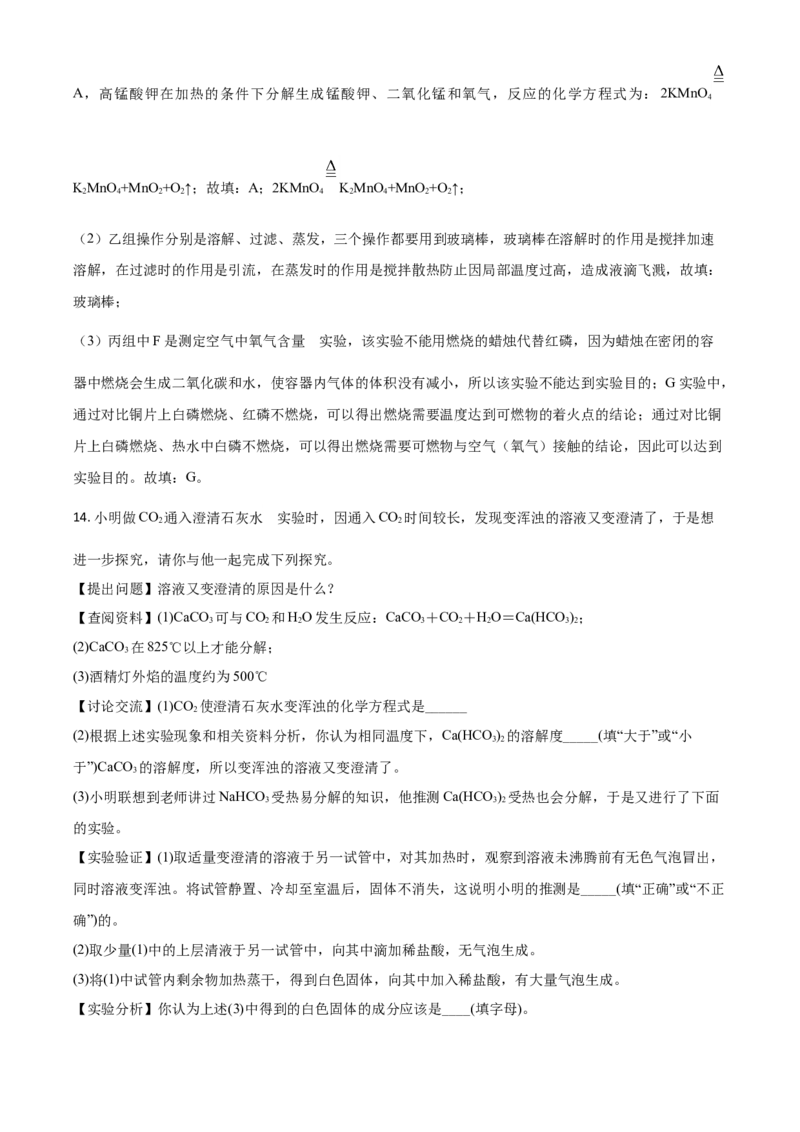文档内容
2015 年陕西省初中毕业学业考试(副题)
一、选择题(共7小题,每小题2分,计14分。每小题只有一个选项是符合题意的)
1. 化学源于生活,也服务于生产、生活。下列说法不正确的是( )
A. 合成纤维制成的衣服结实耐磨,不易褶皱
B. 农作物的丰收,需要化肥、农药的大量使用
C. 合金、水泥、玻璃、塑料等化工产品都是重要的建筑材料
D. 新能源汽车的开发与使用,可减少汽车尾气对空气的污染
【答案】B
【解析】
【详解】A、合成纤维强度高,弹性好,耐磨,耐化学腐蚀,故说法正确,不符合题意;
B、大量使用农药化肥,会导致水污染与土壤板结,并不利于农作物丰收,说法错误,符合题意;
C、合金、水泥、玻璃、塑料等化工产品都是重要的建筑材料,故说法正确,不符合题意;
D、新能源汽车的开发与使用,可减少汽车尾气的排放,减少对空气的污染,说法正确,不符合题意。
故选B。
2. 下列在试管中进行的有关操作正确的是( )
A. 加热液体 B. 收集气体
C. 加固体粉末 D. 滴加液体
【答案】C
【解析】
【详解】A、给试管中的液体加热时,试管中液体体积不应超过试管容积的1/3,选项错误;
B、向下排空气法收集气体时,导管应接近试管底部,图示方法易导致收集气体不纯,选项错误;
C、向试管中加入粉末状固体时,应将试管横放,用药匙或纸槽将固体放在试管底,然后将试管竖起,选
项正确;
D、向试管中滴加液体时,胶头滴管要竖直悬空于试管口的正上方,不能伸入试管,更不能接触试管壁,
选项错误。
故选C。3. “结构 性质 用途”是学习化学 的重要思想方法。下列说法中正确的是( )
①钠原子和钠离子最外层电子数不同,所以它们的化学性质不同;
②金刚石和石墨中碳原子排列方式不同,所以它们的物理性质差异很大;
③水和过氧化氢的分子构成不同,所以它们的化学性质不同;
④氮气常温下化学性质稳定,所以可用于制氮肥;
⑤烧碱能与酸发生中和反应,所以可用于改良酸性土壤;
⑥洗涤剂具有乳化功能,所以可去除油污。
A. ①②③⑥ B. ①②④⑥ C. ②③④⑤ D. ①③④⑤⑥
【答案】A
【解析】
【详解】①最外层电子数决定化学性质,钠原子和钠离子最外层电子数不同,所以它们的化学性质不同,
故正确;
②金刚石和石墨中碳原子排列方式不同,所以它们的物理性质差异很大,故正确;
③水和过氧化氢的分子构成不同,是不同的分子,所以它们的化学性质不同,故正确;
④氮气常温下化学性质稳定,所以可用于食品防腐,故不正确;
⑤烧碱能与酸发生中和反应,但碱性太强,所以不可用于改良酸性土壤,故不正确;
⑥洗涤剂具有乳化功能,所以可去除油污,故正确。
①②③⑥正确,故选A。
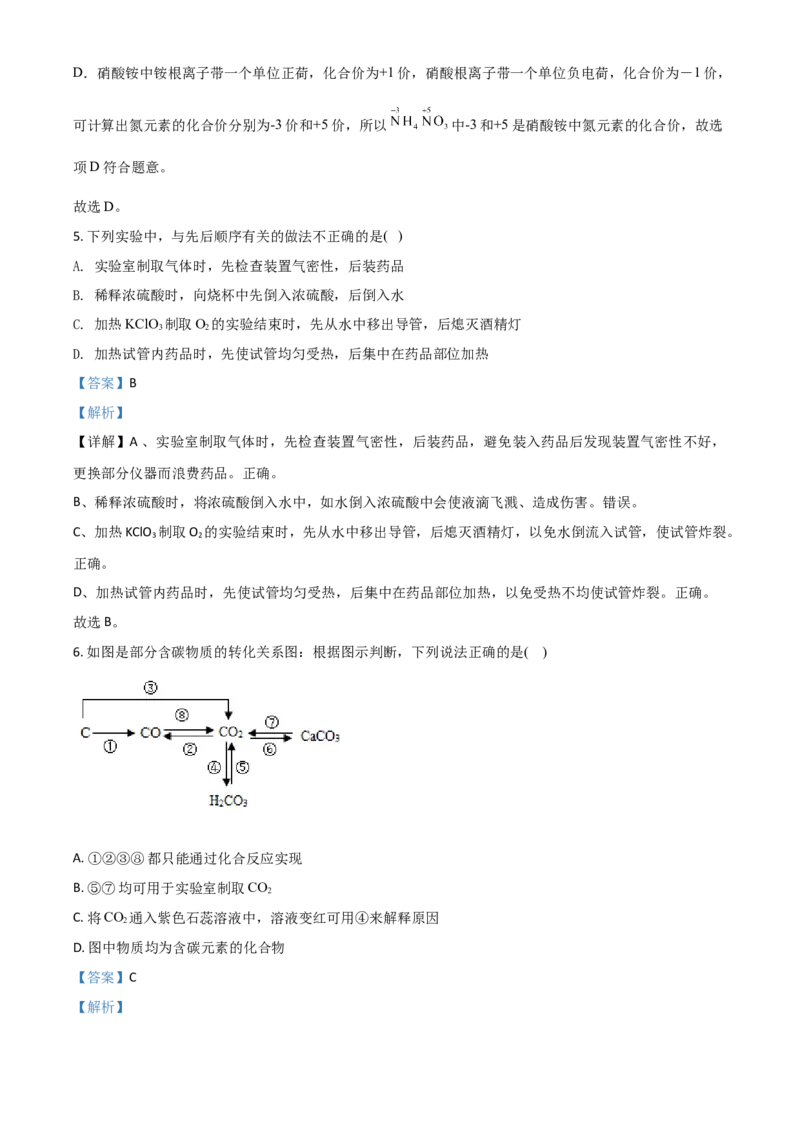
4. 对下而符号、数字、示意图的理解正确的是( )
A. 2H和H 中数字“2”均表示两个氢原子
2
B. Fe2+和Fe3+是铁原子形成的同种离子
C. 和 两种粒子核外电子数相同,属于同种元素的粒子
D. ,中“-3”和“+5”表示硝酸铵中氮元素的化合价
【答案】D
【解析】
【详解】A.H 中数字“2” 表示一个氢分子中含有2个氢原子,故选项A不符合题意;
2
B.Fe2+和Fe3+是铁原子形成的两种不同离子,故选项B不符合题意;
C.元素种类由质子数决定,两种粒子质子数不同,所以属于不同种元素,故选项C不符合题意;D.硝酸铵中铵根离子带一个单位正荷,化合价为+1价,硝酸根离子带一个单位负电荷,化合价为-1价,
可计算出氮元素的化合价分别为-3价和+5价,所以 中-3和+5是硝酸铵中氮元素的化合价,故选
项D符合题意。
故选D。
5. 下列实验中,与先后顺序有关的做法不正确的是( )
A. 实验室制取气体时,先检查装置气密性,后装药品
B. 稀释浓硫酸时,向烧杯中先倒入浓硫酸,后倒入水
C. 加热KClO 制取O 的实验结束时,先从水中移出导管,后熄灭酒精灯
3 2
D. 加热试管内药品时,先使试管均匀受热,后集中在药品部位加热
【答案】B
【解析】
【详解】A 、实验室制取气体时,先检查装置气密性,后装药品,避免装入药品后发现装置气密性不好,
更换部分仪器而浪费药品。正确。
B、稀释浓硫酸时,将浓硫酸倒入水中,如水倒入浓硫酸中会使液滴飞溅、造成伤害。错误。
C、加热KClO 制取O 的实验结束时,先从水中移出导管,后熄灭酒精灯,以免水倒流入试管,使试管炸裂。
3 2
正确。
D、加热试管内药品时,先使试管均匀受热,后集中在药品部位加热,以免受热不均使试管炸裂。正确。
故选B。
6. 如图是部分含碳物质的转化关系图:根据图示判断,下列说法正确的是( )
A. ①②③⑧都只能通过化合反应实现
B. ⑤⑦均可用于实验室制取CO
2
C. 将CO 通入紫色石蕊溶液中,溶液变红可用④来解释原因
2
D. 图中物质均为含碳元素的化合物
【答案】C
【解析】【详解】A、⑧③不一定只能通过化合反应实现,还可分别能通过一氧化碳与氧化铜在加热条件下生成铜
和二氧化碳、碳与氧化铜在高温条件下生成铜和二氧化碳等来实现,错误;
B、实验室常用石灰石与稀盐酸反应制取二氧化碳,同时生成氯化钙、水,碳酸在常温下不稳定,并且碳
酸溶液中碳酸的含量有限,不能通过碳酸分解的方法制取,错误;
C、将CO 通入紫色石蕊溶液中,溶液变红,原因是二氧化碳与水反应生成碳酸,碳酸使紫色石蕊溶液变红
2
色,可用④来解释原因,正确;
D、图中物质中C属于碳的单质,错误。
故选C。
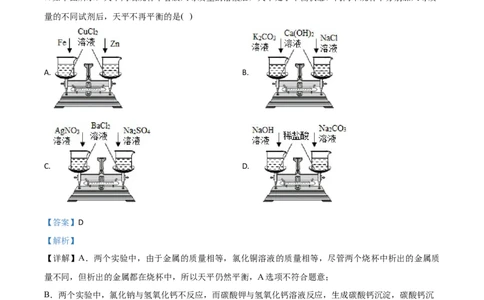
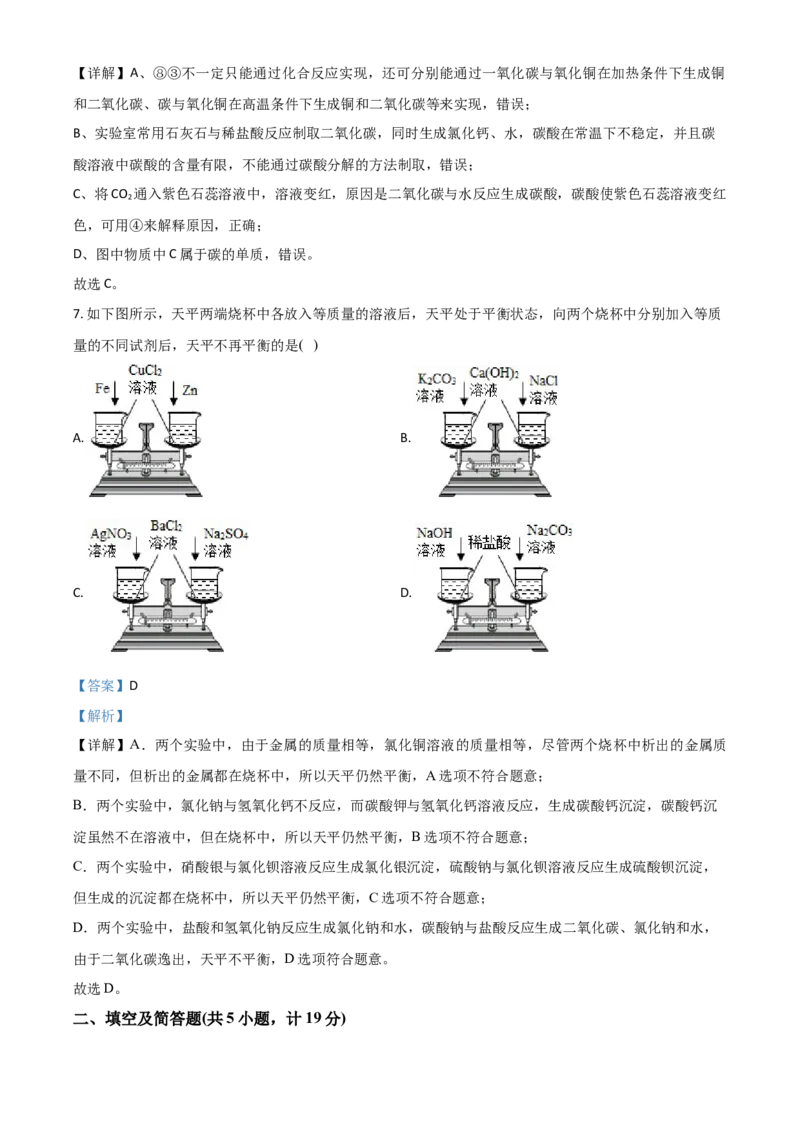
7. 如下图所示,天平两端烧杯中各放入等质量的溶液后,天平处于平衡状态,向两个烧杯中分别加入等质
量的不同试剂后,天平不再平衡的是( )
A. B.
C. D.
【答案】D
【解析】
【详解】A.两个实验中,由于金属的质量相等,氯化铜溶液的质量相等,尽管两个烧杯中析出的金属质
量不同,但析出的金属都在烧杯中,所以天平仍然平衡,A选项不符合题意;
B.两个实验中,氯化钠与氢氧化钙不反应,而碳酸钾与氢氧化钙溶液反应,生成碳酸钙沉淀,碳酸钙沉
淀虽然不在溶液中,但在烧杯中,所以天平仍然平衡,B选项不符合题意;
C.两个实验中,硝酸银与氯化钡溶液反应生成氯化银沉淀,硫酸钠与氯化钡溶液反应生成硫酸钡沉淀,
但生成的沉淀都在烧杯中,所以天平仍然平衡,C选项不符合题意;
D.两个实验中,盐酸和氢氧化钠反应生成氯化钠和水,碳酸钠与盐酸反应生成二氧化碳、氯化钠和水,
由于二氧化碳逸出,天平不平衡,D选项符合题意。
故选D。
二、填空及简答题(共5小题,计19分)8. 2015年3月9日,一架仅依靠太阳能就能做昼夜不间断飞行的不同寻常的飞机——“阳光动力”2号成功
起飞。
(1)该飞机不使用任何化石燃料,所以不会向空气中排放的温室气体是_____。
(2)该飞机机身主体采用新型碳纤维材料,翼展达72米,重量仅为2300千克,可见该材料具有的一种物理
性质是_____。
(3)飞行员每天饮用的功能饮料中含有的“钠、钾、钙”是指_____(填“元素”或“原子”)。
【答案】 (1). CO (或二氧化碳) (2). 密度小 (3). 元素
2
【解析】
【详解】(1)化石燃料燃烧会向空气中排放温室气体二氧化碳,因此该飞机不会排放二氧化碳。
(2)翼展达72米,重量仅为2300千克,根据密度计算公式 可知,说明该材料具有的一种物理性
质是密度小。
(3)功能饮料中含有“钠、钾、钙”,与物质存在形态无关,是指元素。
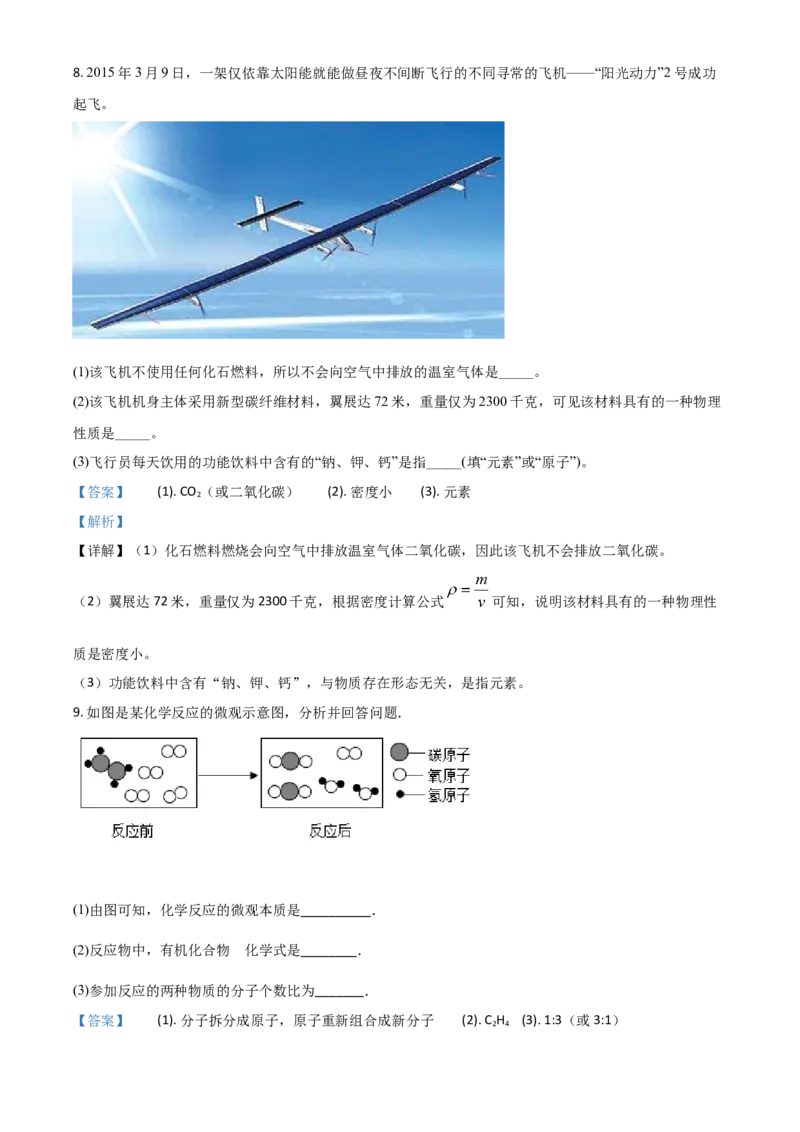
9. 如图是某化学反应的微观示意图,分析并回答问题.
(1)由图可知,化学反应的微观本质是__________.
的
(2)反应物中,有机化合物 化学式是________.
(3)参加反应的两种物质的分子个数比为_______.
【答案】 (1). 分子拆分成原子,原子重新组合成新分子 (2). C H (3). 1:3(或3:1)
2 4【解析】
【详解】(1)化学反应的微观本质是分子拆分成原子,原子重新组合成新分子。
(2)含有碳元素的化合物是有机化合物。根据微观示意图可知,反应物中,1个有机化合物的分子由2个
碳原子和4个氢原子构成。所以化学式是C H 。
2 4
(3)根据微观示意图可知,反应后剩余1个氧气分子。参加反应的两种物质的分子个数比为1:3(或3:
1)。
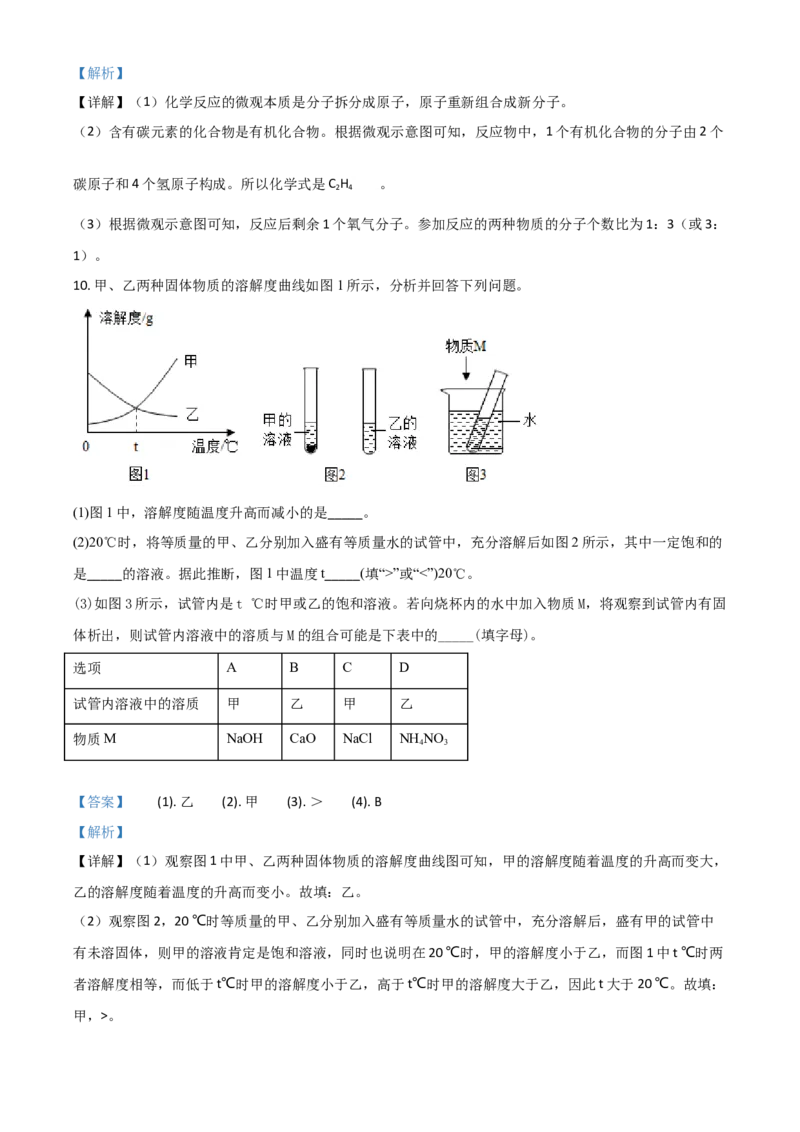
10. 甲、乙两种固体物质的溶解度曲线如图1所示,分析并回答下列问题。
(1)图1中,溶解度随温度升高而减小的是_____。
(2)20℃时,将等质量的甲、乙分别加入盛有等质量水的试管中,充分溶解后如图2所示,其中一定饱和的
是_____的溶液。据此推断,图1中温度t_____(填“>”或“<”)20℃。
(3)如图3所示,试管内是t ℃时甲或乙的饱和溶液。若向烧杯内的水中加入物质M,将观察到试管内有固
体析出,则试管内溶液中的溶质与M的组合可能是下表中的_____(填字母)。
选项 A B C D
试管内溶液中的溶质 甲 乙 甲 乙
物质M NaOH CaO NaCl NH NO
4 3
【答案】 (1). 乙 (2). 甲 (3). > (4). B
【解析】
【详解】(1)观察图1中甲、乙两种固体物质的溶解度曲线图可知,甲的溶解度随着温度的升高而变大,
乙的溶解度随着温度的升高而变小。故填:乙。
(2)观察图2,20 ℃时等质量的甲、乙分别加入盛有等质量水的试管中,充分溶解后,盛有甲的试管中
有未溶固体,则甲的溶液肯定是饱和溶液,同时也说明在20 ℃时,甲的溶解度小于乙,而图1中t ℃时两
者溶解度相等,而低于t℃时甲的溶解度小于乙,高于t℃时甲的溶解度大于乙,因此t大于20 ℃。故填:
甲,>。(3)A、甲溶解度随温度的升高而升高。氢氧化钠加入水中放热,甲溶解度升高,不会有晶体析出。错误。
B、乙溶解度随温度的升高而降低。氧化钙和水反应放热,乙溶解度降低,会有晶体析出。正确。
C、甲溶解度随温度的升高而升高。氯化钠溶于水温度几乎不变,乙溶解度几乎不变,不会有晶体析出。
错误。
D、乙溶解度随温度的升高而降低。硝酸铵溶于水吸热,乙溶解度升高,不会有晶体析出。错误。
故选B。
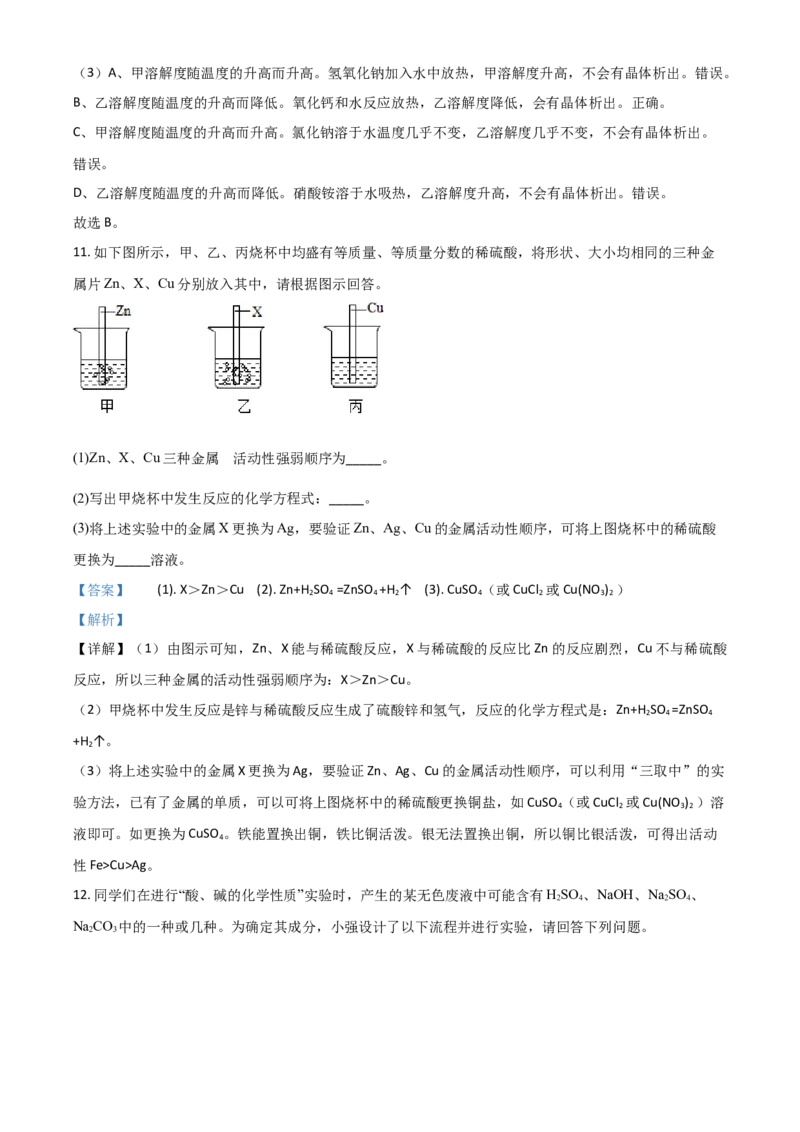
11. 如下图所示,甲、乙、丙烧杯中均盛有等质量、等质量分数的稀硫酸,将形状、大小均相同的三种金
属片Zn、X、Cu分别放入其中,请根据图示回答。
的
(1)Zn、X、Cu三种金属 活动性强弱顺序为_____。
(2)写出甲烧杯中发生反应的化学方程式:_____。
(3)将上述实验中的金属X更换为Ag,要验证Zn、Ag、Cu的金属活动性顺序,可将上图烧杯中的稀硫酸
更换为_____溶液。
【答案】 (1). X>Zn>Cu (2). Zn+H SO =ZnSO +H ↑ (3). CuSO (或CuCl 或Cu(NO ) )
2 4 4 2 4 2 3 2
【解析】
【详解】(1)由图示可知,Zn、X能与稀硫酸反应,X与稀硫酸的反应比Zn的反应剧烈,Cu不与稀硫酸
反应,所以三种金属的活动性强弱顺序为:X>Zn>Cu。
(2)甲烧杯中发生反应是锌与稀硫酸反应生成了硫酸锌和氢气,反应的化学方程式是:Zn+H SO =ZnSO
2 4 4
+H ↑。
2
(3)将上述实验中的金属X更换为Ag,要验证Zn、Ag、Cu的金属活动性顺序,可以利用“三取中”的实
验方法,已有了金属的单质,可以可将上图烧杯中的稀硫酸更换铜盐,如CuSO (或CuCl 或Cu(NO ) )溶
4 2 3 2
液即可。如更换为CuSO 。铁能置换出铜,铁比铜活泼。银无法置换出铜,所以铜比银活泼,可得出活动
4
性Fe>Cu>Ag。
12. 同学们在进行“酸、碱的化学性质”实验时,产生的某无色废液中可能含有HSO 、NaOH、NaSO 、
2 4 2 4
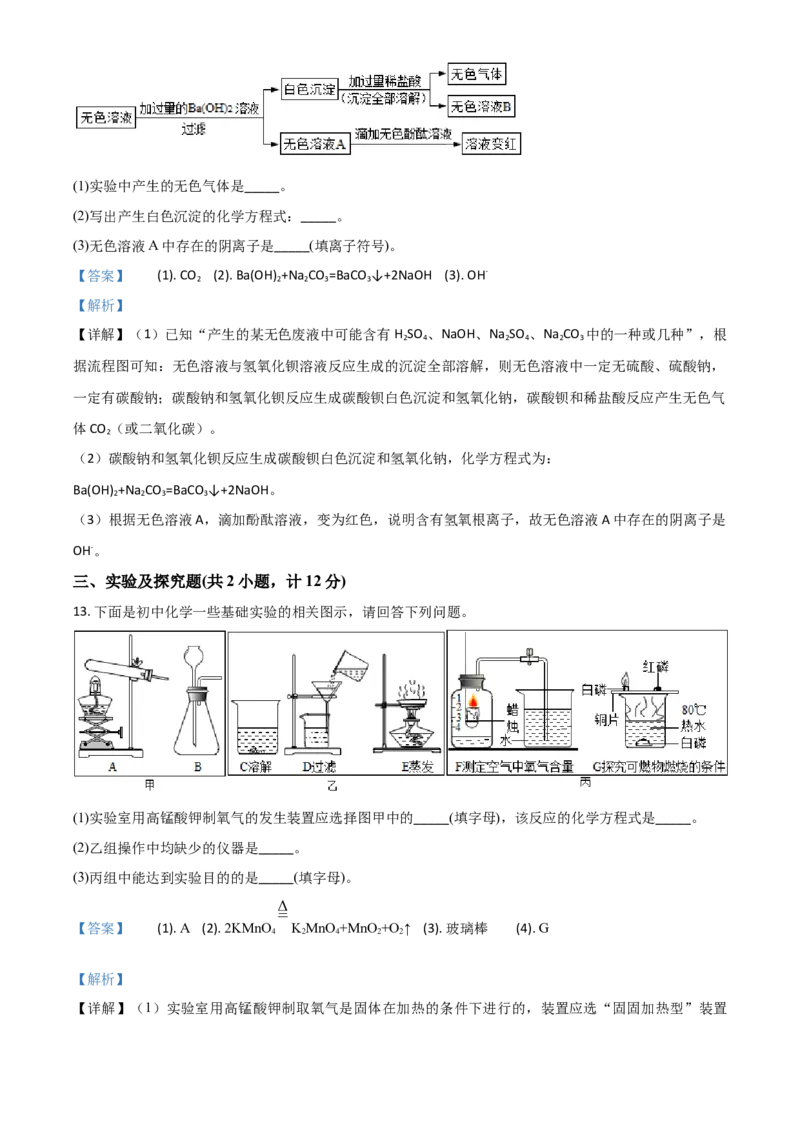
NaCO 中的一种或几种。为确定其成分,小强设计了以下流程并进行实验,请回答下列问题。
2 3(1)实验中产生的无色气体是_____。
(2)写出产生白色沉淀的化学方程式:_____。
(3)无色溶液A中存在的阴离子是_____(填离子符号)。
【答案】 (1). CO (2). Ba(OH) +Na CO =BaCO ↓+2NaOH (3). OH-
2 2 2 3 3
【解析】
【详解】(1)已知“产生的某无色废液中可能含有H SO 、NaOH、Na SO 、Na CO 中的一种或几种”,根
2 4 2 4 2 3
据流程图可知:无色溶液与氢氧化钡溶液反应生成的沉淀全部溶解,则无色溶液中一定无硫酸、硫酸钠,
一定有碳酸钠;碳酸钠和氢氧化钡反应生成碳酸钡白色沉淀和氢氧化钠,碳酸钡和稀盐酸反应产生无色气
体CO (或二氧化碳)。
2
(2)碳酸钠和氢氧化钡反应生成碳酸钡白色沉淀和氢氧化钠,化学方程式为:
Ba(OH) +Na CO =BaCO ↓+2NaOH。
2 2 3 3
(3)根据无色溶液A,滴加酚酞溶液,变为红色,说明含有氢氧根离子,故无色溶液A中存在的阴离子是
OH-。
三、实验及探究题(共2小题,计12分)
13. 下面是初中化学一些基础实验的相关图示,请回答下列问题。
(1)实验室用高锰酸钾制氧气的发生装置应选择图甲中的_____(填字母),该反应的化学方程式是_____。
(2)乙组操作中均缺少的仪器是_____。
(3)丙组中能达到实验目的的是_____(填字母)。
【答案】 (1). A (2). 2KMnO KMnO +MnO+O ↑ (3). 玻璃棒 (4). G
4 2 4 2 2
【解析】
【详解】(1)实验室用高锰酸钾制取氧气是固体在加热的条件下进行的,装置应选“固固加热型”装置A,高锰酸钾在加热的条件下分解生成锰酸钾、二氧化锰和氧气,反应的化学方程式为:2KMnO
4
KMnO +MnO+O ↑;故填:A;2KMnO KMnO +MnO+O ↑;
2 4 2 2 4 2 4 2 2
(2)乙组操作分别是溶解、过滤、蒸发,三个操作都要用到玻璃棒,玻璃棒在溶解时的作用是搅拌加速
溶解,在过滤时的作用是引流,在蒸发时的作用是搅拌散热防止因局部温度过高,造成液滴飞溅,故填:
玻璃棒;
的
(3)丙组中F是测定空气中氧气含量 实验,该实验不能用燃烧的蜡烛代替红磷,因为蜡烛在密闭的容
器中燃烧会生成二氧化碳和水,使容器内气体的体积没有减小,所以该实验不能达到实验目的;G实验中,
通过对比铜片上白磷燃烧、红磷不燃烧,可以得出燃烧需要温度达到可燃物的着火点的结论;通过对比铜
片上白磷燃烧、热水中白磷不燃烧,可以得出燃烧需要可燃物与空气(氧气)接触的结论,因此可以达到
实验目的。故填:G。
的
14. 小明做CO 通入澄清石灰水 实验时,因通入CO 时间较长,发现变浑浊的溶液又变澄清了,于是想
2 2
进一步探究,请你与他一起完成下列探究。
【提出问题】溶液又变澄清的原因是什么?
【查阅资料】(1)CaCO 可与CO 和HO发生反应:CaCO +CO+HO=Ca(HCO );
3 2 2 3 2 2 3 2
(2)CaCO 在825℃以上才能分解;
3
(3)酒精灯外焰的温度约为500℃
【讨论交流】(1)CO 使澄清石灰水变浑浊的化学方程式是______
2
(2)根据上述实验现象和相关资料分析,你认为相同温度下,Ca(HCO ) 的溶解度_____(填“大于”或“小
3 2
于”)CaCO 的溶解度,所以变浑浊的溶液又变澄清了。
3
(3)小明联想到老师讲过NaHCO 受热易分解的知识,他推测Ca(HCO ) 受热也会分解,于是又进行了下面
3 3 2
的实验。
【实验验证】(1)取适量变澄清的溶液于另一试管中,对其加热时,观察到溶液未沸腾前有无色气泡冒出,
同时溶液变浑浊。将试管静置、冷却至室温后,固体不消失,这说明小明的推测是_____(填“正确”或“不正
确”)的。
(2)取少量(1)中的上层清液于另一试管中,向其中滴加稀盐酸,无气泡生成。
(3)将(1)中试管内剩余物加热蒸干,得到白色固体,向其中加入稀盐酸,有大量气泡生成。
【实验分析】你认为上述(3)中得到的白色固体的成分应该是____(填字母)。A CaO B CaCO C Ca(HCO )
3 3 2
【拓展应用】(1)硬水中常含有较多Ca(HCO )、Mg(HCO ),日常生活中常采用______的方法降低其硬度。
3 2 3 2
(2)在家中,要去除水壶内的水垢,可选用____(填字母)。
A 纯碱溶液 B 食盐水 C 食醋
【答案】 (1). Ca(OH) +CO =CaCO ↓+H O (2). 大于 (3). 正确 (4). B (5). 煮沸 (6). C
2 2 3 2
【解析】
【详解】[讨论交流]
(1)二氧化碳和氢氧化钙反应生成碳酸钙和水,CO 使澄清石灰水变浑浊的化学方程式是
2
Ca(OH) +CO =CaCO ↓+H O 。
2 2 3 2
(2)CaCO 可与CO 和H O发生反应:CaCO +CO +H O=Ca(HCO ) ,相同温度下,Ca(HCO ) 的溶解度大
3 2 2 3 2 2 3 2 3 2
于CaCO 的溶解度,所以变浑浊的溶液又变澄清了。
3
[实验验证]
(1)取适量变澄清的溶液于另一试管中,对其加热时,观察到溶液未沸腾前有无色气泡冒出,同时溶液
变浑浊。说明有二氧化碳放出。
将试管静置、冷却至室温后,固体不消失,说明析出的不是Ca(HCO ) 说明有新的不溶于水的物质生成,这
3 2
说明小明的推测是正确的。
[实验分析]
A、氧化钙和水反应,所以白色固体不可能是CaO;
B、Ca(HCO ) 分解生成水、二氧化碳和碳酸钙,正确。
3 2
C、根据分析,沉淀不是原来的物质 Ca(HCO ) 。
3 2
故选B。
[拓展应用]
(1)日常生活中常采用煮沸的方法降低其硬度,煮沸可以将部分溶于水的钙镁离子转化为碳酸钙、氢氧
化镁沉淀。
(2)水垢的主要成分是碳酸钙、氢氧化镁等盐,用酸和其反应除去,要去除水壶内的水垢,用食醋。故
选C。
四、计算与分析题
15. 为测定某NaOH溶液中溶质的质量分数,取20 g该NaOH溶液于烧杯中,逐滴加入7.3%的稀盐酸至10
g时恰好完全反应。请完成下列分析与计算:
(1)常温下,恰好完全反应后溶液的pH=_____。
(2)计算NaOH溶液中溶质的质量分数。
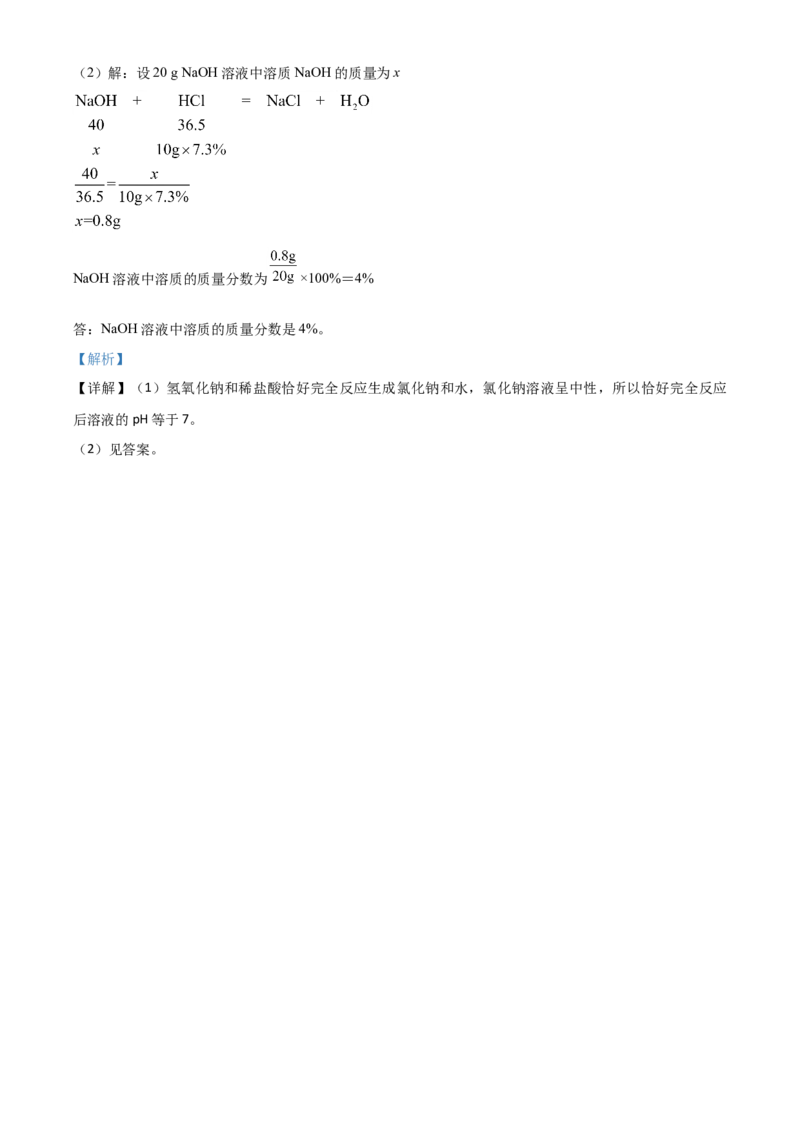
【答案】(1)7;(2)解:设20 g NaOH溶液中溶质NaOH的质量为x
NaOH溶液中溶质的质量分数为 ×100%=4%
答:NaOH溶液中溶质的质量分数是4%。
【解析】
【详解】(1)氢氧化钠和稀盐酸恰好完全反应生成氯化钠和水,氯化钠溶液呈中性,所以恰好完全反应
后溶液的pH等于7。
(2)见答案。