文档内容
2018年贵州省安顺市中考化学试卷
一、选择题(6小题,每题2分,共12分)
1.(2.00分)以下对自然资源利用的过程中只发生物理变化的是( )
A.铝土矿炼铝 B.液化气燃烧 C.木材制桌椅 D.海水提取镁
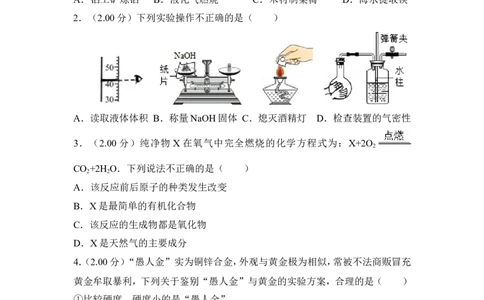
2.(2.00分)下列实验操作不正确的是( )
A.读取液体体积 B.称量NaOH固体 C.熄灭酒精灯 D.检查装置的气密性
3.(2.00 分)纯净物 X 在氧气中完全燃烧的化学方程式为:X+2O
2
CO +2H O.下列说法不正确的是( )
2 2
A.该反应前后原子的种类发生改变
B.X是最简单的有机化合物
C.该反应的生成物都是氧化物
D.X是天然气的主要成分
4.(2.00分)“愚人金”实为铜锌合金,外观与黄金极为相似,常被不法商贩冒充
黄金牟取暴利,下列关于鉴别“愚人金”与黄金的实验方案,合理的是( )
①比较硬度,硬度小的是“愚人金”
②灼烧,表面变色的是“愚人金”
③浸没在稀硫酸中,表面有气泡产生的是“愚人金”
④浸没在硫酸锌溶液中,表面附着白色物质的是“愚人金”
A.①③B.②④ C.①④ D.②③
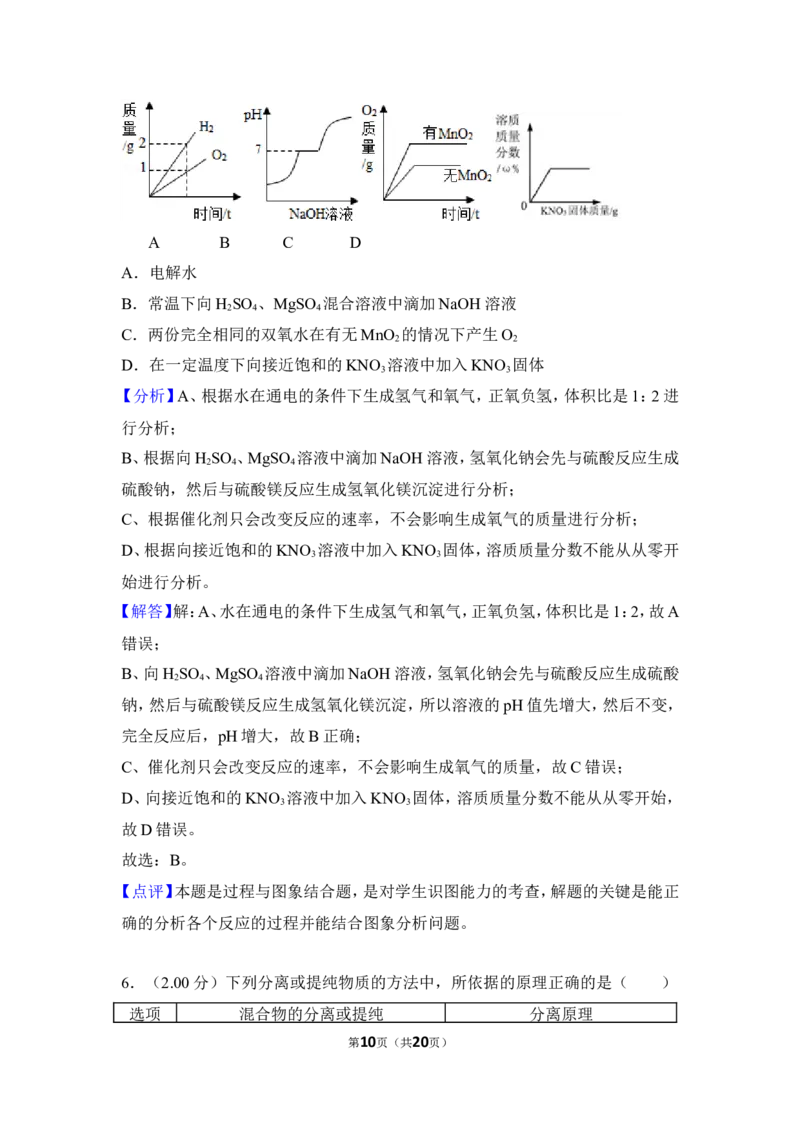
5.(2.00分)下列图象能正确反映其对应关系的是( )
第1页(共20页)A B C D
A.电解水
B.常温下向H SO 、MgSO 混合溶液中滴加NaOH溶液
2 4 4
C.两份完全相同的双氧水在有无MnO 的情况下产生O
2 2
D.在一定温度下向接近饱和的KNO 溶液中加入KNO 固体
3 3
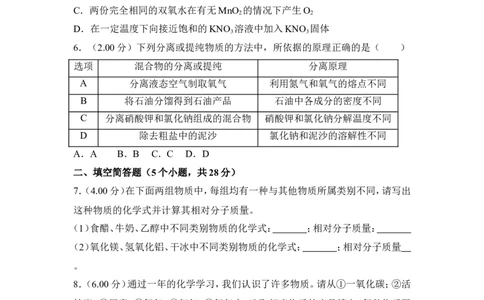
6.(2.00分)下列分离或提纯物质的方法中,所依据的原理正确的是( )
选项 混合物的分离或提纯 分离原理
A 分离液态空气制取氧气 利用氮气和氧气的熔点不同
B 将石油分馏得到石油产品 石油中各成分的密度不同
C 分离硝酸钾和氯化钠组成的混合物 硝酸钾和氯化钠分解温度不同
D 除去粗盐中的泥沙 氯化钠和泥沙的溶解性不同
A.A B.B C.C D.D
二、填空简答题(5个小题,共28分)
7.(4.00分)在下面两组物质中,每组均有一种与其他物质所属类别不同,请写出
这种物质的化学式并计算其相对分子质量。
(1)食醋、牛奶、乙醇中不同类别物质的化学式: ;相对分子质量:
(2)氧化镁、氢氧化铝、干冰中不同类别物质的化学式: ;相对分子质量
。
8.(6.00分)通过一年的化学学习,我们认识了许多物质。请从①一氧化碳;②活
性炭;③尿素;④氢气;⑤氦气;⑥氧气中,选取相应物质的序号填空(每种物质限
选一次)。
(1)用于急救病人的气体是 ;
(2)最清洁的燃料是 ;
(3)可用于冰箱除异味的是 ;
(4)可用作化肥的是 ;
(5)充入灯泡内通电能发出有色光的是 ;
第2页(共20页)(6)用于工业炼铁且有毒的气体是 。
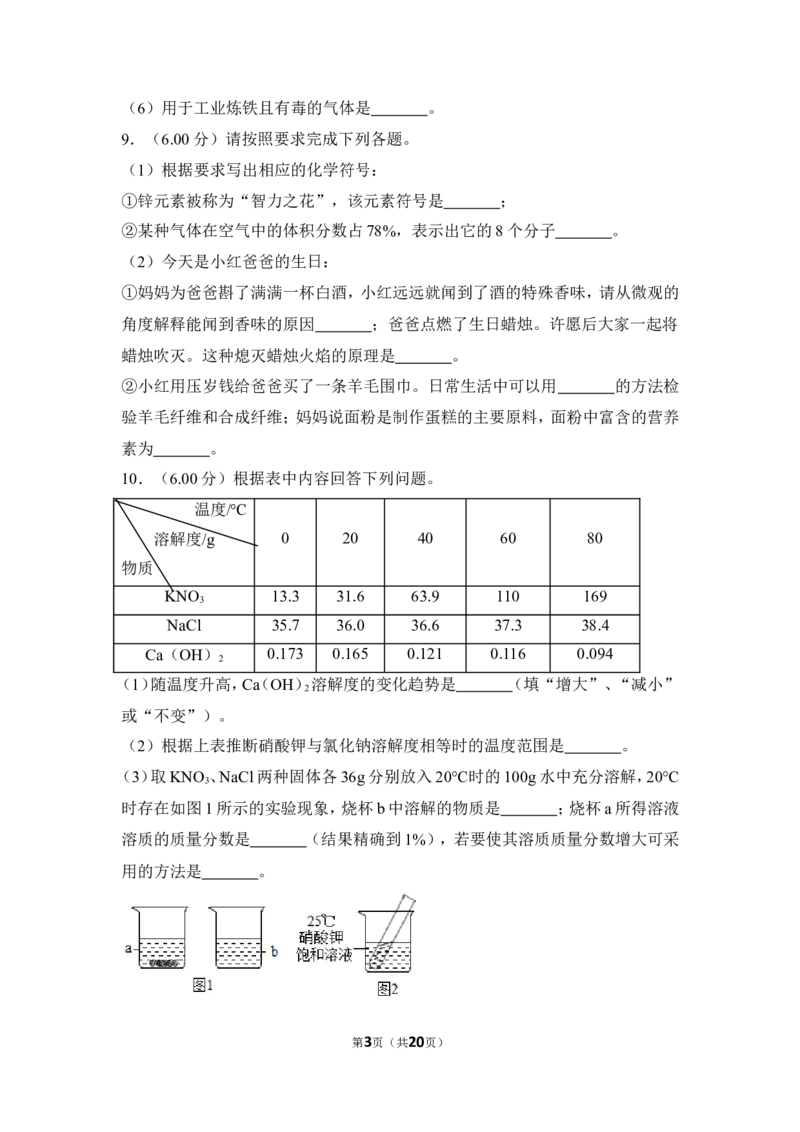
9.(6.00分)请按照要求完成下列各题。
(1)根据要求写出相应的化学符号:
①锌元素被称为“智力之花”,该元素符号是 ;
②某种气体在空气中的体积分数占78%,表示出它的8个分子 。
(2)今天是小红爸爸的生日:
①妈妈为爸爸斟了满满一杯白酒,小红远远就闻到了酒的特殊香味,请从微观的
角度解释能闻到香味的原因 ;爸爸点燃了生日蜡烛。许愿后大家一起将
蜡烛吹灭。这种熄灭蜡烛火焰的原理是 。
②小红用压岁钱给爸爸买了一条羊毛围巾。日常生活中可以用 的方法检
验羊毛纤维和合成纤维;妈妈说面粉是制作蛋糕的主要原料,面粉中富含的营养
素为 。
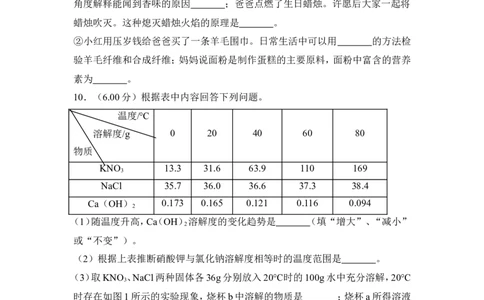
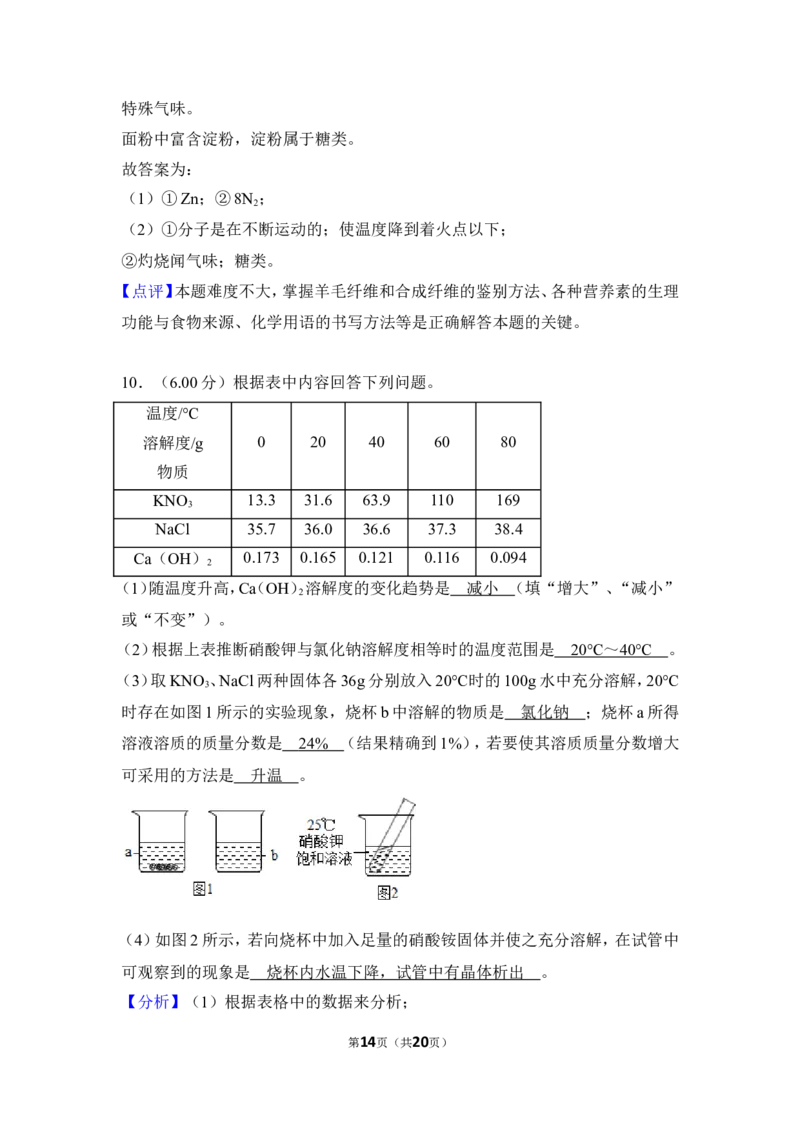
10.(6.00分)根据表中内容回答下列问题。
温度/℃
溶解度/g 0 20 40 60 80
物质
KNO 13.3 31.6 63.9 110 169
3
NaCl 35.7 36.0 36.6 37.3 38.4
Ca(OH) 0.173 0.165 0.121 0.116 0.094
2
(1)随温度升高,Ca(OH)溶解度的变化趋势是 (填“增大”、“减小”
2
或“不变”)。
(2)根据上表推断硝酸钾与氯化钠溶解度相等时的温度范围是 。
(3)取KNO 、NaCl两种固体各36g分别放入20℃时的100g水中充分溶解,20℃
3
时存在如图1所示的实验现象,烧杯b中溶解的物质是 ;烧杯a所得溶液
溶质的质量分数是 (结果精确到1%),若要使其溶质质量分数增大可采
用的方法是 。
第3页(共20页)(4)如图2所示,若向烧杯中加入足量的硝酸铵固体并使之充分溶解,在试管中
可观察到的现象是 。
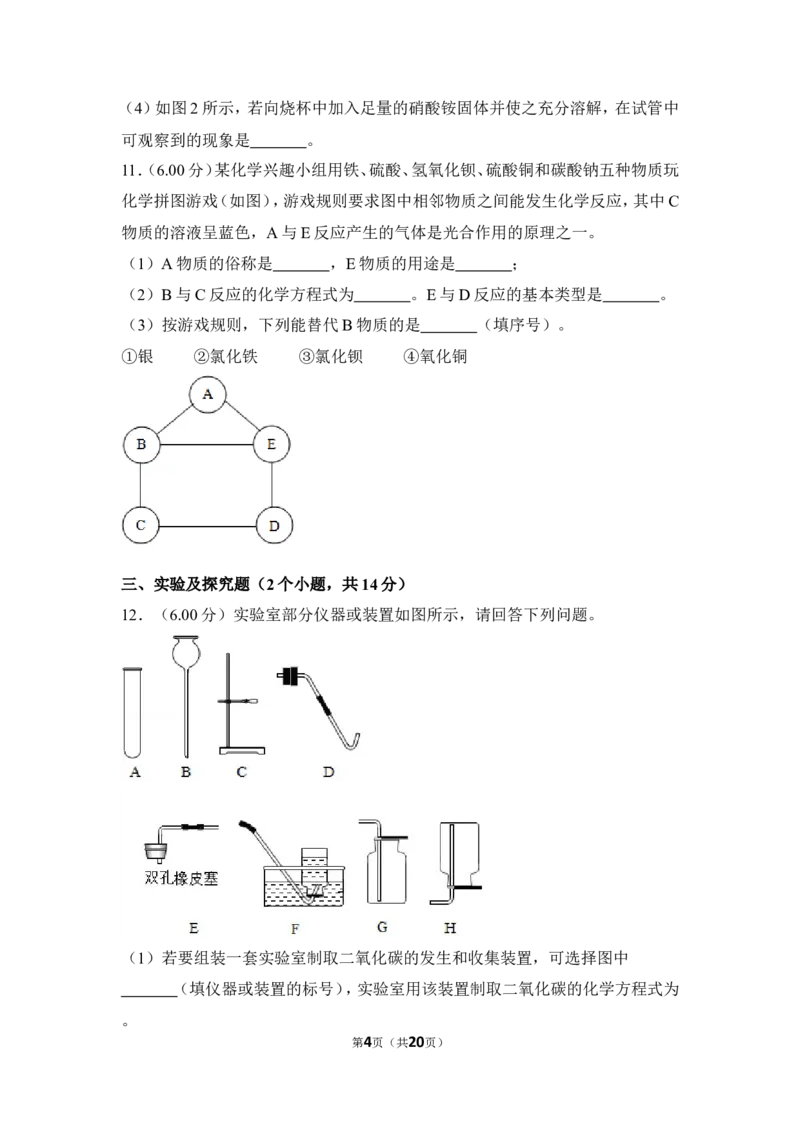
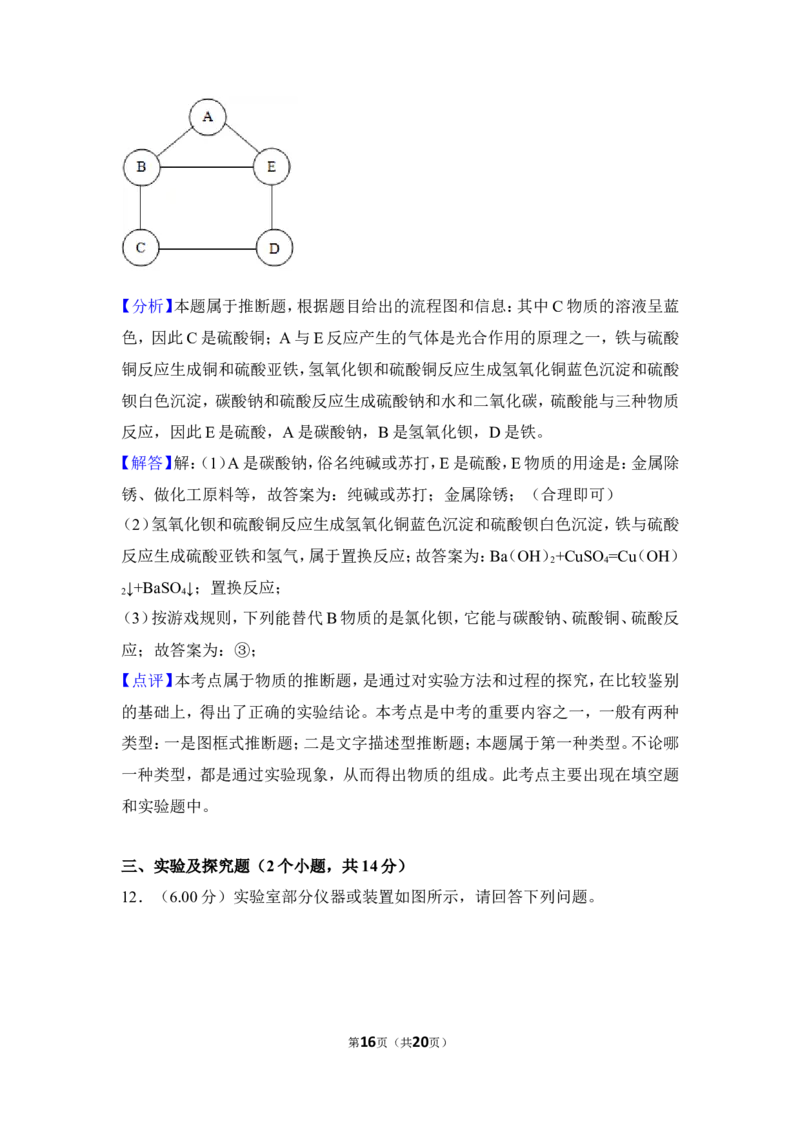
11.(6.00分)某化学兴趣小组用铁、硫酸、氢氧化钡、硫酸铜和碳酸钠五种物质玩
化学拼图游戏(如图),游戏规则要求图中相邻物质之间能发生化学反应,其中C
物质的溶液呈蓝色,A与E反应产生的气体是光合作用的原理之一。
(1)A物质的俗称是 ,E物质的用途是 ;
(2)B与C反应的化学方程式为 。E与D反应的基本类型是 。
(3)按游戏规则,下列能替代B物质的是 (填序号)。
①银 ②氯化铁 ③氯化钡 ④氧化铜
三、实验及探究题(2个小题,共14分)
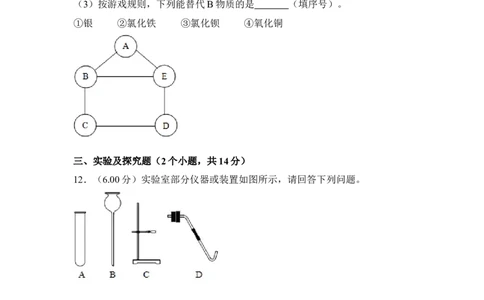
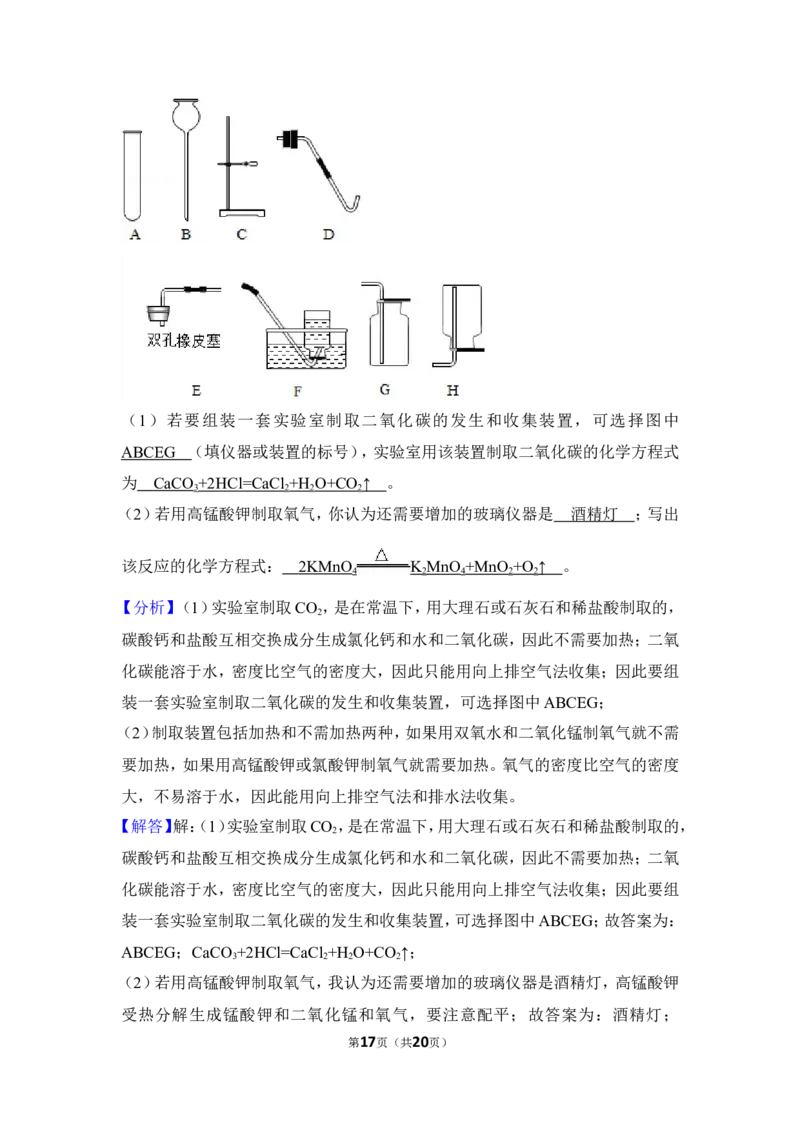
12.(6.00分)实验室部分仪器或装置如图所示,请回答下列问题。
(1)若要组装一套实验室制取二氧化碳的发生和收集装置,可选择图中
(填仪器或装置的标号),实验室用该装置制取二氧化碳的化学方程式为
。
第4页(共20页)(2)若用高锰酸钾制取氧气,你认为还需要增加的玻璃仪器是 ;写出该反
应的化学方程式: 。
13.(8.00分)氢化钙固体是登山运动员常用的能源提供剂。某探究小组的同学通
过查阅资料得知:氢化钙(CaH )遇水反应生成氢氧化钙和氢气。探究斯小组的同
2
学把一定量的CaH 加入Na CO 溶液中,充分反应后过滤,得到滤渣和滤液,经
2 2 3
检验滤渣的成分是碳酸钙。
【提出问题】滤液中溶质的成分是什么?
猜想一:NaOH 猜想二:NaOH、Ca(OH)
2
猜想三:NaOH、Na CO 猜想四:NaOH、Na CO 、Ca(OH)
2 3 2 3 2
经过讨论,大家一致认为猜想四不合理,请用化学方程式说明原因 。
【实验验证】
实验 现象 结论
猜想
(1)取少量滤液,向其中滴入少量碳酸钠溶液 无明显现象
不成立
(2)另取少量滤液,向其中加入足量稀盐酸 猜想三成立
【反思与拓展】
(1)写出氢化钙(CaH )与水反应的化学方程式 。
2
(2)若向NH Cl的溶液中加入一定量的CaH ,充分反应,产生的气体有氢气和
4 2
。
(3)登山运动员携带CaH 作为能源提供剂与携带氢气相比,其优点是
2
(写一条即可)。
四、计算题(只有一个小题,6分)
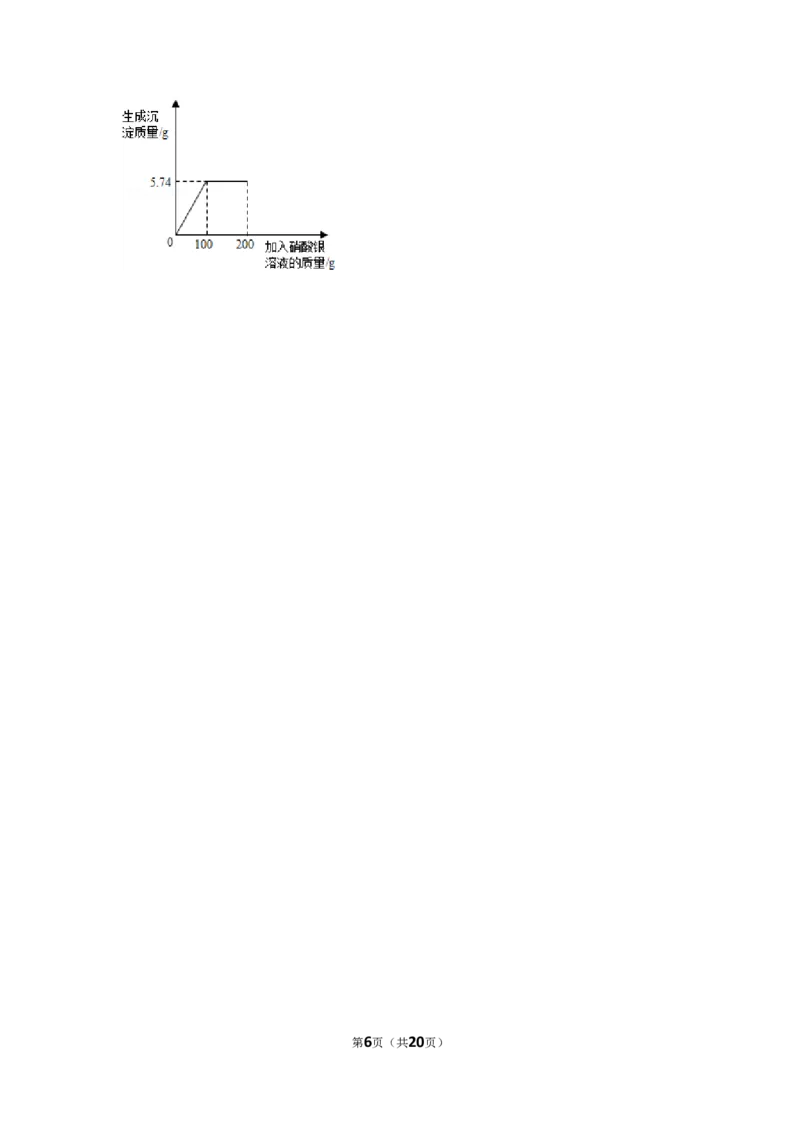
14.(6.00分)将含有可溶性杂质的某氯化镁样品3g溶于足量水中得到不饱和溶
液,再向所得溶液中逐滴滴入200g一定溶质质量分数的AgNO 溶液(杂质不含
3
镁元素且不与AgNO 溶液反应)。实验过程中,生成沉淀的质量与滴入AgNO 溶
3 3
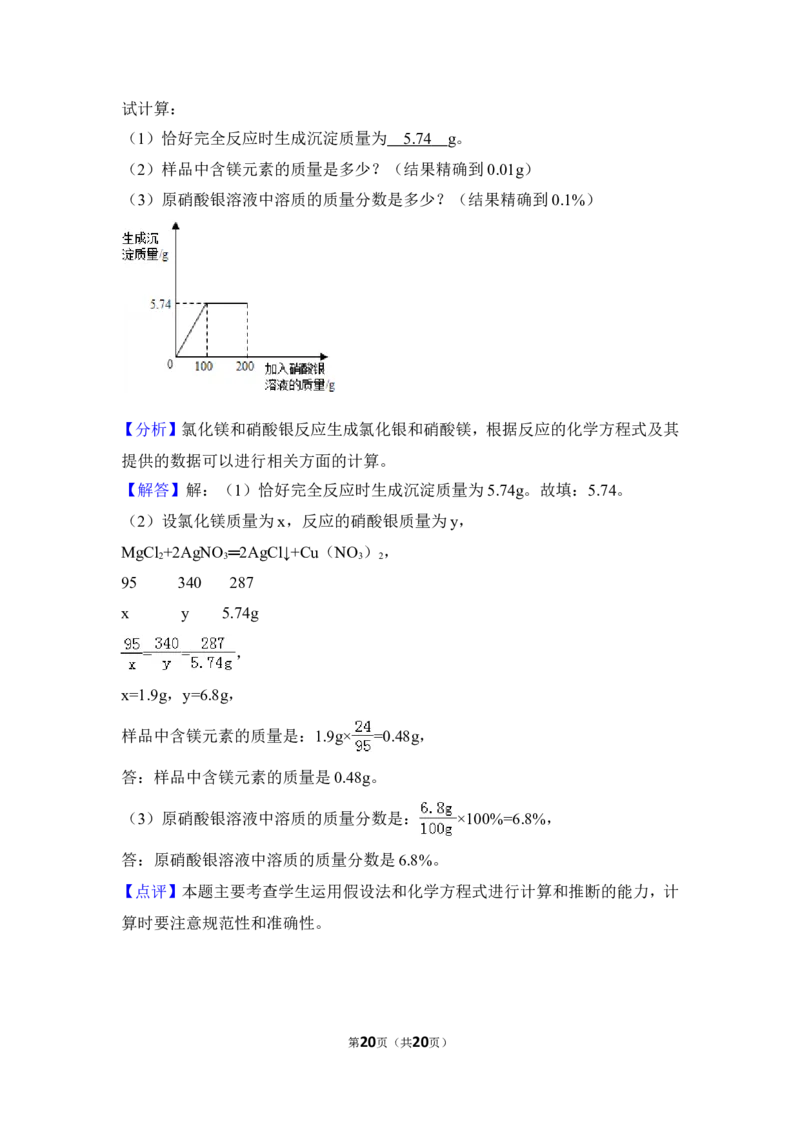
液的质量关系如图所示:
试计算:
(1)恰好完全反应时生成沉淀质量为 g。
(2)样品中含镁元素的质量是多少?(结果精确到0.01g)
(3)原硝酸银溶液中溶质的质量分数是多少?(结果精确到0.1%)
第5页(共20页)第6页(共20页)2018 年贵州省安顺市中考化学试卷
参考答案与试题解析
一、选择题(6小题,每题2分,共12分)
1.(2.00分)以下对自然资源利用的过程中只发生物理变化的是( )
A.铝土矿炼铝 B.液化气燃烧 C.木材制桌椅 D.海水提取镁
【分析】化学变化是指有新物质生成的变化,物理变化是指没有新物质生成的变
化,化学变化与物理变化的本质区别是有无新物质生成,据此抓住化学变化和物
理变化的区别结合事实进行分析判断即可。
【解答】解:A、铝土矿炼铝的过程中有新物质铝等生成,属于化学变化。
B、天然气燃烧的过程中有新物质二氧化碳和水生成,属于化学变化。
C、木材制桌椅的过程中只是形状发生改变,没有新物质生成,属于物理变化。
D、海水提取镁的过程中,有新物质镁等生成,属于化学变化。
故选:C。
【点评】本题难度不大,解答时要分析变化过程中是否有新物质生成,这里的新物
质是指和变化前的物质是不同种的物质,若没有新物质生成属于物理变化,若有
新物质生成属于化学变化。
2.(2.00分)下列实验操作不正确的是( )
A.读取液体体积 B.称量NaOH固体 C.熄灭酒精灯 D.检查装置的气密性
【分析】A.根据用量筒量取液体的方法考虑;
第7页(共20页)B.据称量固体时易潮解物品的称量方法分析;
C.根据酒精灯的使用分析;
D.根据装置气密性检查的方法考虑。
【解答】解:A.视线与凹液面最低处保持水平,故正确;
B.使用托盘天平时应将易潮解和腐蚀性强的药品放在玻璃器皿中称量,故错误
C.酒精灯的灯芯是活动的,所以在熄灭酒精灯时应该用灯帽盖灭,不能用嘴直接
吹灭,故操作正确
D.将导管一段浸入水中,用手紧握烧瓶外壁,有水柱上升,说明气密性良好。故
正确
故选:B。
【点评】化学实验的基本操作是做好化学实验的基础,学生要在平时的练习中多
操作,掌握操作要领,使操作规范。
3.(2.00 分)纯净物 X 在氧气中完全燃烧的化学方程式为:X+2O
2
CO +2H O.下列说法不正确的是( )
2 2
A.该反应前后原子的种类发生改变
B.X是最简单的有机化合物
C.该反应的生成物都是氧化物
D.X是天然气的主要成分
【分析】A、根据质量守恒定律,进行分析判断。
B、由质量守恒定律:反应前后,原子种类、数目均不变,进行分析判断。
C、氧化物是只含有两种元素且其中一种元素是氧元素的化合物。
D、根据天然气的主要成分,进行分析判断。
【解答】解:A、化学反应前后原子的种类不变,故选项说法错误。
B、由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式
X+2O CO +2H O,反应前碳、氢、氧原子个数分别为0、0、4,反应后的生
2 2 2
成物中碳、氢、氧原子个数分别为1、4、4,根据反应前后原子种类、数目不变,则
则每个X分子由1个碳原子和4个氢原子构成,则物质X的化学式为CH ,是最
4
第8页(共20页)简单的有机化合物,故选项说法正确。
C、生成物二氧化碳和水,均是由两种元素组成的且有一种是氧元素的化合物,均
属于氧化物,故选项说法正确。
D、天然气的主要成分是甲烷,故选项说法正确。
故选:A。
【点评】本题难度不大,掌握质量守恒定律(反应前后,原子种类、数目均不变)、
氧化物的特征、天然气的主要成分等是正确解答本题的关键。
4.(2.00分)“愚人金”实为铜锌合金,外观与黄金极为相似,常被不法商贩冒充
黄金牟取暴利,下列关于鉴别“愚人金”与黄金的实验方案,合理的是( )
①比较硬度,硬度小的是“愚人金”
②灼烧,表面变色的是“愚人金”
③浸没在稀硫酸中,表面有气泡产生的是“愚人金”
④浸没在硫酸锌溶液中,表面附着白色物质的是“愚人金”
A.①③B.②④ C.①④ D.②③
【分析】根据金属的性质进行分析,金的化学性质稳定,一般不与其他物质发生化
学反应,锌能与酸反应生成氢气,与盐溶液反应;铜能与氧气反应生成黑色氧化
铜;真假黄金的硬度都很大。
【解答】解:①比较硬度,二者的硬度都很大,故错误;
②灼烧,铜能够和氧气反应产生氧化铜,表面变黑色的是“愚人金”,故正确;
③浸没在稀硫酸中,锌能够和学生反应产生氢气,因此表面有气泡产生的是“愚
人金”,故正确;
④浸没在硫酸锌溶液中,三种金属都不能和硫酸锌反应,无法鉴别,故错误;
故选:D。
【点评】本题考查了常见金属的鉴别,在解此类题时,首先分析需要鉴别的物质的
性质,然后选择适当的试剂和方法,出现不同的现象即可鉴别。
5.(2.00分)下列图象能正确反映其对应关系的是( )
第9页(共20页)A B C D
A.电解水
B.常温下向H SO 、MgSO 混合溶液中滴加NaOH溶液
2 4 4
C.两份完全相同的双氧水在有无MnO 的情况下产生O
2 2
D.在一定温度下向接近饱和的KNO 溶液中加入KNO 固体
3 3
【分析】A、根据水在通电的条件下生成氢气和氧气,正氧负氢,体积比是1:2进
行分析;
B、根据向H SO 、MgSO 溶液中滴加NaOH溶液,氢氧化钠会先与硫酸反应生成
2 4 4
硫酸钠,然后与硫酸镁反应生成氢氧化镁沉淀进行分析;
C、根据催化剂只会改变反应的速率,不会影响生成氧气的质量进行分析;
D、根据向接近饱和的KNO 溶液中加入KNO 固体,溶质质量分数不能从从零开
3 3
始进行分析。
【解答】解:A、水在通电的条件下生成氢气和氧气,正氧负氢,体积比是1:2,故A
错误;
B、向H SO 、MgSO 溶液中滴加NaOH溶液,氢氧化钠会先与硫酸反应生成硫酸
2 4 4
钠,然后与硫酸镁反应生成氢氧化镁沉淀,所以溶液的pH值先增大,然后不变,
完全反应后,pH增大,故B正确;
C、催化剂只会改变反应的速率,不会影响生成氧气的质量,故C错误;
D、向接近饱和的KNO 溶液中加入KNO 固体,溶质质量分数不能从从零开始,
3 3
故D错误。
故选:B。
【点评】本题是过程与图象结合题,是对学生识图能力的考查,解题的关键是能正
确的分析各个反应的过程并能结合图象分析问题。
6.(2.00分)下列分离或提纯物质的方法中,所依据的原理正确的是( )
选项 混合物的分离或提纯 分离原理
第10页(共20页)A 分离液态空气制取氧气 利用氮气和氧气的熔点不同
B 将石油分馏得到石油产品 石油中各成分的密度不同
C 分离硝酸钾和氯化钠组成的混合物 硝酸钾和氯化钠分解温度不同
D 除去粗盐中的泥沙 氯化钠和泥沙的溶解性不同
A.A B.B C.C D.D
【分析】混合物的分离方法是指人们根据不同物质的性质的不同点,采用适当的
方式将混合物中各物质分离开来的科学方法,据此结合常见的分离的方法,进行
分析判断。
【解答】解:A、分离液态空气制取氧气,利用的是液态氮和液态氧沸点的不同,故
选项错误。
B、将石油分馏得到石油产品,利用的是石油中各成分的沸点不同,故选项错误。
C、分离硝酸钾和氯化钠组成的混合物,利用的是硝酸钾和氯化钠的溶解度不同,
故选项错误。
D、粗盐的主要成分是氯化钠,粗盐提纯是通过溶解(把不溶物与食盐初步分离)
过滤(把不溶物彻底除去)、蒸发(食盐从溶液中分离出来而得到食盐)得到精盐
的过程,利用的是氯化钠和泥沙的溶解性不同,故选项正确。
故选:D。
【点评】本题难度不大,了解常见的混合物分离的方法、原理并能灵活运用是正确
解答本题的关键。
二、填空简答题(5个小题,共28分)
7.(4.00分)在下面两组物质中,每组均有一种与其他物质所属类别不同,请写出
这种物质的化学式并计算其相对分子质量。
(1)食醋、牛奶、乙醇中不同类别物质的化学式: C H OH ;相对分子质量:
2 5
46 。
(2)氧化镁、氢氧化铝、干冰中不同类别物质的化学式: A (l OH ) ;相对分子
3
质量 7 8 。
【分析】(1)食醋、牛奶、乙醇中乙醇属于纯净物,另外两种物质属于混合物,结合
相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答。
第11页(共20页)(2)氧化镁、氢氧化铝、干冰中氢氧化铝属于碱,另外两种物质属于氧化物,结合
相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答。
【解答】解:(1)食醋、牛奶、乙醇中乙醇属于纯净物,另外两种物质属于混合物,
乙醇的化学式为C H OH;乙醇的相对分子质量为:12×2+1×5+16×5=46。
2 5
(2)氧化镁、氢氧化铝、干冰中氢氧化铝属于碱,另外两种物质属于氧化物,氢氧
化铝的化学式为Al(OH) ;氢氧化铝的相对分子质量为27+(16+1)×3=78。
3
故答案为:
(1)C H OH;46;
2 5
(2)Al(OH) ;78。
3
【点评】本题难度不大,掌握相对分子质量的计算方法、物质的分类方法、化学式
的书写是正确解答本题的关键。
8.(6.00分)通过一年的化学学习,我们认识了许多物质。请从①一氧化碳;②活
性炭;③尿素;④氢气;⑤氦气;⑥氧气中,选取相应物质的序号填空(每种物质限
选一次)。
(1)用于急救病人的气体是 ⑥ ;
(2)最清洁的燃料是 ④ ;
(3)可用于冰箱除异味的是 ② ;
(4)可用作化肥的是 ③ ;
(5)充入灯泡内通电能发出有色光的是 ⑤ ;
(6)用于工业炼铁且有毒的气体是 ① 。
【分析】物质的结构和组成决定物质的性质,物质的性质决定物质的用途,根据物
质的性质进行分析。
【解答】解:(1)氧气用于急救病人;
(2)氢气燃烧生成水,是最清洁的燃料;
(3)活性炭具有吸附性,可用于冰箱除异味;
(4)尿素可用作化肥;
(5)氦气充入灯泡内通电能发出有色光;
(6)一氧化碳具有还原性和可燃性,可用于工业炼铁且有毒。
故答案为:(1)⑥;(2)④;(3)②;(4)③;(5)⑤;(6)①。
第12页(共20页)【点评】本题难度不大,物质的性质决定物质的用途,掌握常见化学物质的性质和
用途是正确解答此类题的关键。
9.(6.00分)请按照要求完成下列各题。
(1)根据要求写出相应的化学符号:
①锌元素被称为“智力之花”,该元素符号是 Z n ;
②某种气体在空气中的体积分数占78%,表示出它的8个分子 8N 。
2
(2)今天是小红爸爸的生日:
①妈妈为爸爸斟了满满一杯白酒,小红远远就闻到了酒的特殊香味,请从微观的
角度解释能闻到香味的原因 分子是在不断运动的 ;爸爸点燃了生日蜡烛。许
愿后大家一起将蜡烛吹灭。这种熄灭蜡烛火焰的原理是 使温度降到着火点以下
。
②小红用压岁钱给爸爸买了一条羊毛围巾。日常生活中可以用 灼烧闻气味 的
方法检验羊毛纤维和合成纤维;妈妈说面粉是制作蛋糕的主要原料,面粉中富含
的营养素为 糖类 。
【分析】(1)①书写元素符号时应注意:①有一个字母表示的元素符号要大写;②
由两个字母表示的元素符号,第一个字母大写,第二个字母小写。
②在空气中占78%(体积百分含量)的气体是氮气,氮气是由氮分子构成的,它的
8个分子为8个氮分子。
(2)①闻到气味,可用分子是在不断的运动的进行分析解释;结合灭火的三种原
理,进行分析解答。
②根据羊毛纤维的主要成分是蛋白质,人体所需六大营养素的种类、食物来源进
行分析解答即可。
【解答】解:(1)①书写元素符号注意“一大二小”,锌的元素符号是Zn。
②在空气中占78%(体积百分含量)的气体是氮气,氮气是由氮分子构成的,它的
8个分子为8个氮分子,其分子符号为:8N 。
2
(2)①小红远远就闻到了酒的特殊香味,是因为酒精中含有的分子是在不断运动
的,向四周扩散,使小红闻到酒的特殊香味。
许愿后大家一起将蜡烛吹灭,将热量吹走,使温度降到着火点以下。
②羊毛纤维的主要成分是蛋白质,灼烧产生烧焦羽毛的气味,合成纤维灼烧产生
第13页(共20页)特殊气味。
面粉中富含淀粉,淀粉属于糖类。
故答案为:
(1)①Zn;②8N ;
2
(2)①分子是在不断运动的;使温度降到着火点以下;
②灼烧闻气味;糖类。
【点评】本题难度不大,掌握羊毛纤维和合成纤维的鉴别方法、各种营养素的生理
功能与食物来源、化学用语的书写方法等是正确解答本题的关键。
10.(6.00分)根据表中内容回答下列问题。
温度/℃
溶解度/g 0 20 40 60 80
物质
KNO 13.3 31.6 63.9 110 169
3
NaCl 35.7 36.0 36.6 37.3 38.4
Ca(OH) 0.173 0.165 0.121 0.116 0.094
2
(1)随温度升高,Ca(OH)溶解度的变化趋势是 减小 (填“增大”、“减小”
2
或“不变”)。
(2)根据上表推断硝酸钾与氯化钠溶解度相等时的温度范围是 20℃ ~ 40℃ 。
(3)取KNO 、NaCl两种固体各36g分别放入20℃时的100g水中充分溶解,20℃
3
时存在如图1所示的实验现象,烧杯b中溶解的物质是 氯化钠 ;烧杯a所得
溶液溶质的质量分数是 24% (结果精确到1%),若要使其溶质质量分数增大
可采用的方法是 升温 。
(4)如图2所示,若向烧杯中加入足量的硝酸铵固体并使之充分溶解,在试管中
可观察到的现象是 烧杯内水温下降,试管中有晶体析出 。
【分析】(1)根据表格中的数据来分析;
第14页(共20页)(2)根据表格提供的数据结合已有的知识进行分析解答;
(3)根据物质的溶解度、溶质质量分数的计算方法以及增大物质溶解度的方法来
分析;
(4)根据硝酸铵溶于水吸热以及硝酸钾的溶解度受温度影响来分析。
【解答】解:(1)通过分析溶解度表可知,随温度升高,硝酸钾溶解度的变化趋势是
减小;故填:减小;
(2)根据表格可以看出,在温度在20℃~40℃范围之内时,硝酸钾与氯化钠溶解
度相等,故填:20℃~40℃;
(3)20℃时,氯化钠的溶解度大于硝酸钾的溶解度,所以取KNO 、NaCl两种固体
3
各36g分别放入20℃时的100g水中充分溶解,20℃时有如图1所示的实验现象,
烧杯b中溶解的物质氯化钠;则烧杯a中溶解的是硝酸钾,此时硝酸钾溶液是饱
和溶液,其中溶质的质量分数为: ;因为硝酸钾的溶解
度随着温度的升高而增大,所以若要使其溶质质量分数增大可以升高温度;故填
氯化钠;24%;升温;
(4)硝酸铵溶于水,溶液温度降低,所以向烧杯中加入足量的硝酸铵使之充分溶
解,可观察到的现象是:烧杯内水温下降,试管中有晶体析出;故填:烧杯内水温
下降,试管中有晶体析出。
【点评】本题考查的是溶解度的影响因素以及溶解度的应用,完成此题,可以依据
已有的知识进行。
11.(6.00分)某化学兴趣小组用铁、硫酸、氢氧化钡、硫酸铜和碳酸钠五种物质玩
化学拼图游戏(如图),游戏规则要求图中相邻物质之间能发生化学反应,其中C
物质的溶液呈蓝色,A与E反应产生的气体是光合作用的原理之一。
(1)A物质的俗称是 纯碱或苏打 ,E物质的用途是 金属除锈 ;
(2)B与C反应的化学方程式为 B a( OH ) +CuSO =Cu( OH ) ↓+BaSO ↓ 。E与
2 4 2 4
D反应的基本类型是 置换反应 。
(3)按游戏规则,下列能替代B物质的是 ③ (填序号)。
①银 ②氯化铁 ③氯化钡 ④氧化铜
第15页(共20页)【分析】本题属于推断题,根据题目给出的流程图和信息:其中C物质的溶液呈蓝
色,因此C是硫酸铜;A与E反应产生的气体是光合作用的原理之一,铁与硫酸
铜反应生成铜和硫酸亚铁,氢氧化钡和硫酸铜反应生成氢氧化铜蓝色沉淀和硫酸
钡白色沉淀,碳酸钠和硫酸反应生成硫酸钠和水和二氧化碳,硫酸能与三种物质
反应,因此E是硫酸,A是碳酸钠,B是氢氧化钡,D是铁。
【解答】解:(1)A是碳酸钠,俗名纯碱或苏打,E是硫酸,E物质的用途是:金属除
锈、做化工原料等,故答案为:纯碱或苏打;金属除锈;(合理即可)
(2)氢氧化钡和硫酸铜反应生成氢氧化铜蓝色沉淀和硫酸钡白色沉淀,铁与硫酸
反应生成硫酸亚铁和氢气,属于置换反应;故答案为:Ba(OH)+CuSO =Cu(OH)
2 4
↓+BaSO ↓;置换反应;
2 4
(3)按游戏规则,下列能替代B物质的是氯化钡,它能与碳酸钠、硫酸铜、硫酸反
应;故答案为:③;
【点评】本考点属于物质的推断题,是通过对实验方法和过程的探究,在比较鉴别
的基础上,得出了正确的实验结论。本考点是中考的重要内容之一,一般有两种
类型:一是图框式推断题;二是文字描述型推断题;本题属于第一种类型。不论哪
一种类型,都是通过实验现象,从而得出物质的组成。此考点主要出现在填空题
和实验题中。
三、实验及探究题(2个小题,共14分)
12.(6.00分)实验室部分仪器或装置如图所示,请回答下列问题。
第16页(共20页)(1)若要组装一套实验室制取二氧化碳的发生和收集装置,可选择图中
ABCEG (填仪器或装置的标号),实验室用该装置制取二氧化碳的化学方程式
为 CaCO +2HCl=CaCl +H O+CO ↑ 。
3 2 2 2
(2)若用高锰酸钾制取氧气,你认为还需要增加的玻璃仪器是 酒精灯 ;写出
该反应的化学方程式: 2KMnO K MnO +MnO +O ↑ 。
4 2 4 2 2
【分析】(1)实验室制取CO ,是在常温下,用大理石或石灰石和稀盐酸制取的,
2
碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;二氧
化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;因此要组
装一套实验室制取二氧化碳的发生和收集装置,可选择图中ABCEG;
(2)制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需
要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热。氧气的密度比空气的密度
大,不易溶于水,因此能用向上排空气法和排水法收集。
【解答】解:(1)实验室制取CO ,是在常温下,用大理石或石灰石和稀盐酸制取的,
2
碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;二氧
化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;因此要组
装一套实验室制取二氧化碳的发生和收集装置,可选择图中ABCEG;故答案为:
ABCEG;CaCO +2HCl=CaCl +H O+CO ↑;
3 2 2 2
(2)若用高锰酸钾制取氧气,我认为还需要增加的玻璃仪器是酒精灯,高锰酸钾
受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;故答案为:酒精灯;
第17页(共20页)2KMnO K MnO +MnO +O ↑;
4 2 4 2 2
【点评】本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时
也考查了化学方程式的书写等,综合性比较强。气体的制取装置的选择与反应物
的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关。
本考点是中考的重要考点之一,主要出现在实验题中。
13.(8.00分)氢化钙固体是登山运动员常用的能源提供剂。某探究小组的同学通
过查阅资料得知:氢化钙(CaH )遇水反应生成氢氧化钙和氢气。探究斯小组的同
2
学把一定量的CaH 加入Na CO 溶液中,充分反应后过滤,得到滤渣和滤液,经
2 2 3
检验滤渣的成分是碳酸钙。
【提出问题】滤液中溶质的成分是什么?
猜想一:NaOH 猜想二:NaOH、Ca(OH)
2
猜想三:NaOH、Na CO 猜想四:NaOH、Na CO 、Ca(OH)
2 3 2 3 2
经过讨论,大家一致认为猜想四不合理,请用化学方程式说明原因 N a CO +Ca
2 3
( OH ) ═CaCO ↓+2NaOH 。
2 3
【实验验证】
实验 现象 结论
猜想 二
(1)取少量滤液,向其中滴入少量碳酸钠溶液 无明显现象
不成立
猜想三成
(2)另取少量滤液,向其中加入足量稀盐酸 产生气泡
立
【反思与拓展】
(1)写出氢化钙(CaH )与水反应的化学方程式 CaH +2H O=Ca( OH ) +2H ↑ 。
2 2 2 2 2
(2)若向NH Cl的溶液中加入一定量的CaH ,充分反应,产生的气体有氢气和
4 2
氨气 。
(3)登山运动员携带CaH 作为能源提供剂与携带氢气相比,其优点是 携带方
2
便 (写一条即可)。
【分析】碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,和稀盐酸反应生成
氯化钠、水和二氧化碳;
氢化钙和水反应生成氢氧化钙和氢气,氢氧化钙和氯化铵反应生成氯化钙、水和
第18页(共20页)氨气。
【解答】解:【提出问题】
经过讨论,大家一致认为猜想四不合理,这是因为碳酸钠和氢氧化钙反应生成碳
酸钙和氢氧化钠,反应的化学方程式为:Na CO +Ca(OH)═CaCO ↓+2NaOH。
2 3 2 3
故填:Na CO +Ca(OH) ═CaCO ↓+2NaOH。
2 3 2 3
【实验验证】
(1)取少量滤液,向其中滴入少量碳酸钠溶液,无明显现象,说明溶液中不含有氢
氧化钙;
(2)另取少量滤液,向其中加入足量稀盐酸,产生气泡,说明溶液中含有碳酸钠,
实验过程如下所示:
实验 现象 结论
(1)取少量滤液,向其中滴入少量碳酸钠溶液 无明显现象 猜想二不成立
(2)另取少量滤液,向其中加入足量稀盐酸 产生气泡 猜想三成立
【反思与拓展】
(1)氢化钙(CaH )与水反应的化学方程式为:CaH +2H O=Ca(OH)+2H ↑。
2 2 2 2 2
故填:CaH +2H O=Ca(OH) +2H ↑。
2 2 2 2
(2)若向NH Cl的溶液中加入一定量的CaH ,充分反应,产生的气体有氢气和氯
4 2
化铵与氢氧化钙反应生成的氨气。
故填:氨气。
(3)登山运动员携带CaH 作为能源提供剂与携带氢气相比,其优点是携带方便、
2
安全。
故填:携带方便。
【点评】本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条
件进行分析、判断,从而得出正确的结论。
四、计算题(只有一个小题,6分)
14.(6.00分)将含有可溶性杂质的某氯化镁样品3g溶于足量水中得到不饱和溶
液,再向所得溶液中逐滴滴入200g一定溶质质量分数的AgNO 溶液(杂质不含
3
镁元素且不与AgNO 溶液反应)。实验过程中,生成沉淀的质量与滴入AgNO 溶
3 3
液的质量关系如图所示:
第19页(共20页)试计算:
(1)恰好完全反应时生成沉淀质量为 5.7 4 g。
(2)样品中含镁元素的质量是多少?(结果精确到0.01g)
(3)原硝酸银溶液中溶质的质量分数是多少?(结果精确到0.1%)
【分析】氯化镁和硝酸银反应生成氯化银和硝酸镁,根据反应的化学方程式及其
提供的数据可以进行相关方面的计算。
【解答】解:(1)恰好完全反应时生成沉淀质量为5.74g。故填:5.74。
(2)设氯化镁质量为x,反应的硝酸银质量为y,
MgCl +2AgNO ═2AgCl↓+Cu(NO ) ,
2 3 3 2
95 340 287
x y 5.74g
= = ,
x=1.9g,y=6.8g,
样品中含镁元素的质量是:1.9g× =0.48g,
答:样品中含镁元素的质量是0.48g。
(3)原硝酸银溶液中溶质的质量分数是: ×100%=6.8%,
答:原硝酸银溶液中溶质的质量分数是6.8%。
【点评】本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计
算时要注意规范性和准确性。
第20页(共20页)