文档内容
高三期末质量检测 化学
高三期末质量监测 化学
说明:
本解答给出的非选择题答案仅供参考,若考生的回答与本答案不同,但只要合理,可参照评
分标准酌情给分。
一、选择题:本题共 15 分,每小题 3 分,共 45 分。在每小题给出的四个选项中,只有一项是符合
题目要求的。
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
答案 B A A B C B C C B C D A C D A
严肃认真 高度负责 公平公正
给分有理 扣分有据 宽严适度
二、非选择题:本题共 4 小题,共 55 分。
16.(14分,除特殊标注外,每空2分)
题号 参考答案 评分细则
B(1分) 此空答案唯一
Ⅰ.(1) 浓硫酸(1分) “浓H
2
SO
4
(溶液)”给分;
“H SO ”不给分
2 4
(2) 水浴加热 答案合理即可
△ 完全正确得2分,===写成→扣1分,
Cr O +3CCl 2CrCl +3COCl
2 3 4 3 2
(3) 漏写“△”扣1分,配平错误或任一
化学式错误不给分
将生成的CrCl 排入装置C 被收集,并将COCl 完全排入装 “收集产物”1分,“尾气处理”1
(4) 3 2
置E被充分吸收 分
5abM 完全正确得2分,未化简不扣分,
Ⅱ(. 1) 12m 5abM
写“ %”扣1分
12m
使过量H O 完全分解 合理表述即可
(2) 2 2
偏低 此空答案唯一,“低”不给分
17.(13分,除特殊标注外,每空2分)
题号 参考答案 评分细则
C(1分) 此空答案唯一
(1) 烧杯、漏斗、玻璃棒 完全正确得2分,少写给1分,有错
写不给分
2SnS+O +2H O===2SnO +2H S 完全正确得2分,===写成→扣1分,
(2) 2 2 2 2
配平错误或任一化学式错误不给分
表诉不唯一,合理表述即可,但表达
K (FeAsO )
由Fe3+浓度和K (FeAsO )可得c(AsO3)= sp 4 意思正确,内容表述不完整,酌情扣
sp 4 4 c(Fe3)
1分,求Co2+形成沉淀时的最大浓度
(3) =1×10-15mol/L,由Co2+浓度可得Q[Co (AsO ) ]= 也得分
3 4 2
c3(Co2+)·c2(AsO3)≤10-33<K [Co (AsO ) ],故“富砷渣”
4 sp 3 4 2
中不含Co (AsO ) ,该同学观点错误
3 4 2
高三期末质量监测化学试题参考答案 第 1 页 共 10 页高三期末质量检测 化学
完全正确得2分,===写成→扣1分,
3Co2++MnO+7H O===3Co(OH) ↓+MnO +5H+
4 2 3 2 漏写“↓”扣1分,配平错误或任一
化学式错误不给分,写化学方程式不
(4)
给分
ZnSO 和K SO 完全正确得2分,少写给1分,有错
4 2 4
写不给分,写汉字不给分
(5) Co O 此空答案唯一,写汉字不给分
3 4
18.(14分,除特殊标注外,每空2分)
题号 参考答案 评分细则
-206kJ/mol(1分) 此空答案唯一,不写负号、不写单位
(1) 不给分
低温(1分) 此空答案唯一
①D ①此空答案唯一
(2)
②增大 ②此空答案唯一
①CO ①此空答案唯一,写汉字不给分
2
②0.4mol ②此空答案唯一,不写单位扣1分
(3)
②7.03 此空答案唯一
③减小 ③此空答案唯一
19.(14分,每空2分)
题号 参考答案 评分细则
酯基、醚键 完全正确得2分,写对1个给1分
(1)
C H O I “C H IO ”给分
9 13 4 9 13 4
(2) 取代反应 “取代”给2分
完全正确得2分,→写成===不扣分,
(3) 不写条件扣1分,任一化学式错误不
+
催化剂 给分,
正确即可,交叉处可连接
(4)
任写一种,完全正确得2分,可用键
(5)
线式表示
或
完全正确得2分,一步1分,
(6)
m-CPBA CH 3 ONa 其他合理答案给分
CH Cl
2 2
严肃认真 高度负责 公平公正
给分有理 扣分有据 宽严适度
请化学老师上课讲评试卷时,提醒学生认真审题、规范作答。
及时纠正学生此次答题上所存在的一些小问题!
高三期末质量监测化学试题参考答案 第 2 页 共 10 页高三期末质量检测 化学
高三期末质量监测 化学
一、选择题
1.【答案】B
【立意】结合我国馆藏文物的知识,考查常见材料的分类与性质,检验对有机高分子材料、硅酸盐材料、
金属化合物材料的辨析能力,体现化学与传统文化的联系。
【思路】清代瓷器的釉料主要成分为硅酸盐,硅酸钠不耐强酸的腐蚀,A项不符合题意;纸的主要成分为
纤维素,纤维素属于糖类,B项符合题意;棉布的主要成分是纤维素(属于糖类),点燃时产生烧纸的气味,
蛋白质(如丝绸)点燃时才会产生烧焦羽毛的气味,C项不符合题意;铜绿的主要成分是碱式碳酸铜,不是
氧化铜,D项不符合题意。
2.【答案】A
【立意】考查化学用语的规范表达,涵盖离子空间结构判断、原子书写规则、分子电子式、有机物命名,
检验化学用语书写的准确性与严谨性。
【思路】根据价层电子对互斥模型可推知SO2的空间结构为正四面体形,A项正确;中子数为125的铅原
4
子表示为207Pb,B项错误;CO 的电子式为OCO,C项错误;有机物命名时要从距官能团最近的
82 2
一端开始编号, 的正确命名为3-甲基-1-丁烯,D项错误。
3.【答案】A
【立意】基于陌生氧化还原反应,考查电子转移情况、物质结构与性质,检验对阿伏加德罗常数的理解与
应用能力。
【思路】1个OH-中有10个电子,所以1molOH-中所含电子的数目为10N ,A项错误;1个N H 中含5
A 2 4
个σ键,32gN H 的物质的量为1mol,所含σ键的数目为5N ,B项正确;反应中Cu元素由+2价被还原
2 4 A
为+1价,生成1molCu O时转移2mole-,C项正确;H O中只有O原子满足8电子稳定结构,1molH O
2 2 2
中含有N 个O原子,D项正确。
A
4.【答案】B
【立意】通过同类型物质性质的比较,考查键角、氢键、水解规律、酸性强弱的影响因素,检验对性质的
探究与推理能力。
【思路】比较键角时先比较中心原子杂化方式,然后比较孤电子对,孤电子对对成键电子对的斥力更大,
孤电子对越多键角越小,键角:SO >SO ,则键角:H O+>H O,A项正确;水结冰时所有水分子之间全
3 2 3 2
部以氢键形成空间网状结构,水分子之间间距增大,密度减小,CCl 变为固体时,分子间距离变小,密度
4
变大,B项错误;PCl 中Cl的电负性大,Cl显负价,所以水解生成HCl,NF 中F的电负性大,F显负价,
3 3
所以水解生成HF,C项正确;F的电负性大于Cl的电负性,F的吸电子能力大于Cl的吸电子能力,所以
酸性:CF COOH>CCl COOH,酸性:F—SO H>Cl—SO H,D项正确。
3 3 3 3
5.【答案】C
【立意】通过陌生离子方程式的考查,检验对守恒关系的掌握能力。
【思路】Pb比铜活泼,Pb粉加入硫酸铜饱和溶液中置换出铜单质,生成的二价铅结合硫酸根离子产生硫
0.028 L
酸铅沉淀,A项错误;n(Cl )= =0.00125mol,0.001molFeI 中含0.002molI-、0.001molFe2+,
2 2
22.4 L/mol
I-先被氧化,I-完全氧化需0.001molCl ,剩余0.00025molCl 可氧化0.0005molFe2+,Fe2+未完全反应,但
2 2
选项方程式中Fe2+被完全氧化,B项错误;甘氨酸中的氨基与盐酸反应,离子方程式正确,C项正确;FeO
溶于稀硝酸,稀硝酸氧化亚铁离子,会有NO和Fe3+生成,反应的离子方程式为
3FeO+10H++NO===3Fe3++5H O+NO↑,D项错误。
3 2
6.【答案】B
【立意】考查晶胞结构与相关计算,以及元素周期表相关知识。
高三期末质量监测化学试题参考答案 第 3 页 共 10 页高三期末质量检测 化学
【思路】Zn和Cu元素均位于周期表ds区,A项正确;由图可知,晶体中距离Zn原子最近且等距的S原
1 3 3
子有4个,B项错误;根据1号、3号原子的位置,可知2号原子的分数坐标为( , , ),C项正确;
4 4 8
1 1 1 1
Cu原子位于顶点、面上和体心,个数为8× +4× +1=4,Zn原子位于棱上和面心,个数 为4× +2×=2,
8 2 2 4
1
Sn原子位于面上,个数为4× =2,S原子位于晶胞内部,个数为8,则该晶体的密度为
2
M (6446521192328) g 4.41032
= = g/cm3,D项正确。
V N aa2a1030 cm3 N a3
A A
7.【答案】C
【立意】通过“价-类”二维图,考查硫、氯及其化合物的性质,涉及性质比较与氧化还原反应的推断。
【思路】a为HCl、b为Cl 、c为ClO 、d为HClO 、e为HClO、a'为H S、b'为S、c'为SO 、d'为
2 2 4 2 2
SO 、e'为H SO 。H S、SO 均有还原性,可被HClO氧化,A项正确;酸性:HClO >H SO >HClO,
3 2 4 2 2 4 2 4
B 项 正 确 ; Cl 没 有 漂 白 性 , C 项 错 误 ; ClO 和 SO 在 水 中 反 应 的 化 学 方 程 式 为
2 2 2
2ClO +5SO +6H O===2HCl+5H SO ,D项正确。
2 2 2 2 4
8.【答案】C
【立意】通过实验装置的设计,考查乙炔与溴水的反应、氨气的实验室制备、滴定实验、非金属性验证实
验,检验对实验原理的应用能力。
【思路】用水和电石反应制得的乙炔中含有H S、PH 等杂质,杂质能与溴单质发生氧化还原反应使溴水
2 3
褪色,不能证明乙炔可使溴水褪色,A项不符合题意;氨气密度比空气小,应使用向下排空气法收集,导
气管应伸入试管底部,B项不符合题意;使用聚四氟乙烯活塞的滴定管耐酸碱的腐蚀,可以盛装酸性或碱
性溶液,C项符合题意;需要通过最高价氧化物对应水化物的酸性比较元素的非金属性,不能通过氢化物
的酸性比较,D项不符合题意。
9.【答案】B
【立意】通过实验方案、现象与结论的对应关系,考查溴乙烷消去反应产物检验、浓硫酸与蔗糖反应实验、
氧化铁的还原与产物检验、K 比较,检验实验现象的分析能力与对反应原理的理解。
sp
【思路】乙醇具有挥发性,挥发出的乙醇也能使酸性KMnO 溶液褪色,因此酸性KMnO 溶液褪色不能证
4 4
明是产生了乙烯,A项不符合题意;向蔗糖中加入浓硫酸,蔗糖膨胀变黑,这是因为浓硫酸具有脱水性,
将蔗糖中的H、O按2∶1脱去,生成碳,有刺激性气体生成,说明产生了SO ,是因为浓硫酸具有强氧化
2
性,与碳发生反应生成SO 、CO 和H O,所以说明浓硫酸具有脱水性和强氧化性,B项符合题意;若CO
2 2 2
未将氧化铁完全反应,将适量反应后的固体(含Fe)溶于稀盐酸时,氧化铁与稀盐酸反应生成氯化铁和水,
而Fe可以和氯化铁反应生成氯化亚铁,滴加硫氰化钾溶液时,溶液不变红色,故Fe O 不一定被CO完全
2 3
还原,C项不符合题意;未给出FeCl 和CuCl 的浓度,无法比较K [Fe(OH) ]、K [Cu(OH) ]的大小,D
3 2 sp 3 sp 2
项不符合题意。
10.【答案】C
【立意】通过陌生配合物的结构,考查还原性物质与配合物的性质和原子结构。
【思路】合成过程中邻苯二甲腈和Fe2+反应,Fe2+易被氧化,需要在还原性氛围中进行,A项正确;邻苯
二甲腈分子中所有原子共平面,所以有14个原子共平面,B项正确;由题中信息“具有平面结构的铁酞
菁”可知C、N原子均为sp2杂化,C项错误;基态Fe2+价层电子的轨道表示式为 ,D项
正确。
11.【答案】D
【立意】通过电化学制备有机物装置,考查电解池原理的应用,包括电极判断、电极反应式书写、产物产
量计算、交换膜性质判断。
高三期末质量监测化学试题参考答案 第 4 页 共 10 页高三期末质量检测 化学
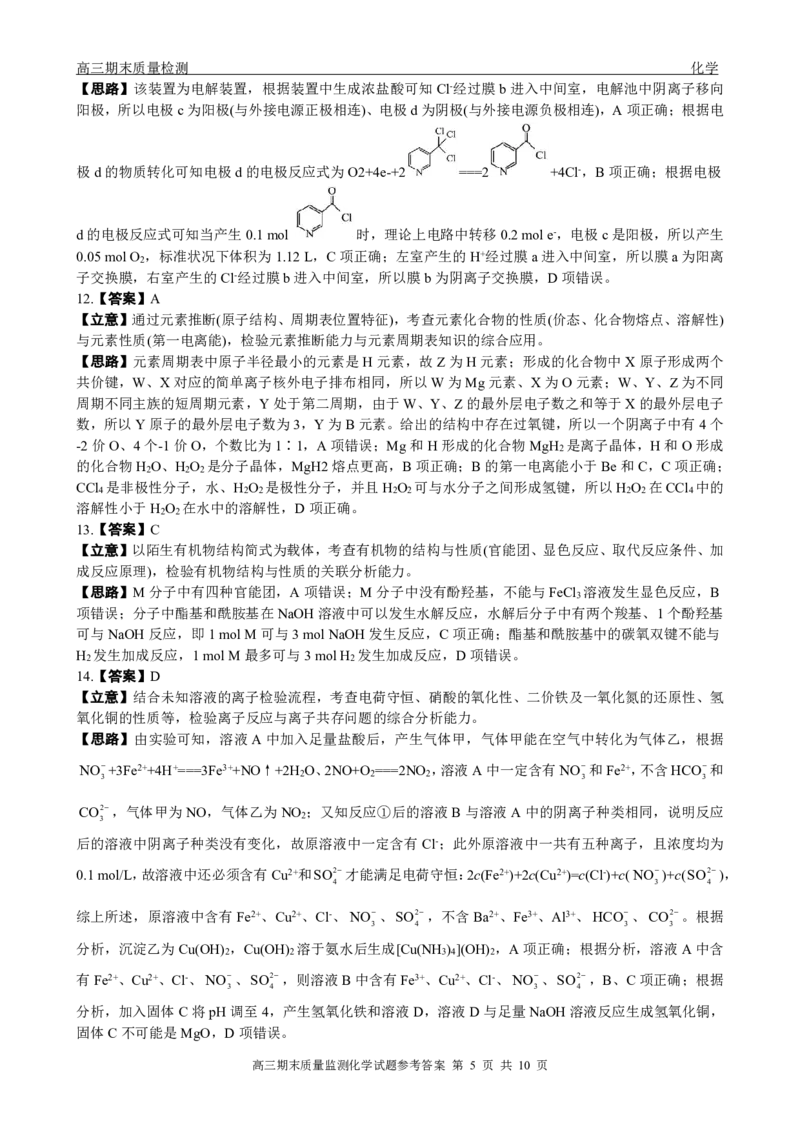
【思路】该装置为电解装置,根据装置中生成浓盐酸可知Cl-经过膜b进入中间室,电解池中阴离子移向
阳极,所以电极c为阳极(与外接电源正极相连)、电极d为阴极(与外接电源负极相连),A项正确;根据电
极d的物质转化可知电极d的电极反应式为O2+4e-+2 ===2 +4Cl-,B项正确;根据电极
d的电极反应式可知当产生0.1mol 时,理论上电路中转移0.2mole-,电极c是阳极,所以产生
0.05molO ,标准状况下体积为1.12L,C项正确;左室产生的H+经过膜a进入中间室,所以膜a为阳离
2
子交换膜,右室产生的Cl-经过膜b进入中间室,所以膜b为阴离子交换膜,D项错误。
12.【答案】A
【立意】通过元素推断(原子结构、周期表位置特征),考查元素化合物的性质(价态、化合物熔点、溶解性)
与元素性质(第一电离能),检验元素推断能力与元素周期表知识的综合应用。
【思路】元素周期表中原子半径最小的元素是H元素,故Z为H元素;形成的化合物中X原子形成两个
共价键,W、X对应的简单离子核外电子排布相同,所以W为Mg元素、X为O元素;W、Y、Z为不同
周期不同主族的短周期元素,Y处于第二周期,由于W、Y、Z的最外层电子数之和等于X的最外层电子
数,所以Y原子的最外层电子数为3,Y为B元素。给出的结构中存在过氧键,所以一个阴离子中有4个
-2价O、4个-1价O,个数比为1∶1,A项错误;Mg和H形成的化合物MgH 是离子晶体,H和O形成
2
的化合物H O、H O 是分子晶体,MgH2熔点更高,B项正确;B的第一电离能小于Be和C,C项正确;
2 2 2
CCl 是非极性分子,水、H O 是极性分子,并且H O 可与水分子之间形成氢键,所以H O 在CCl 中的
4 2 2 2 2 2 2 4
溶解性小于H O 在水中的溶解性,D项正确。
2 2
13.【答案】C
【立意】以陌生有机物结构简式为载体,考查有机物的结构与性质(官能团、显色反应、取代反应条件、加
成反应原理),检验有机物结构与性质的关联分析能力。
【思路】M分子中有四种官能团,A项错误;M分子中没有酚羟基,不能与FeCl 溶液发生显色反应,B
3
项错误;分子中酯基和酰胺基在NaOH溶液中可以发生水解反应,水解后分子中有两个羧基、1个酚羟基
可与NaOH反应,即1molM可与3molNaOH发生反应,C项正确;酯基和酰胺基中的碳氧双键不能与
H 发生加成反应,1molM最多可与3molH 发生加成反应,D项错误。
2 2
14.【答案】D
【立意】结合未知溶液的离子检验流程,考查电荷守恒、硝酸的氧化性、二价铁及一氧化氮的还原性、氢
氧化铜的性质等,检验离子反应与离子共存问题的综合分析能力。
【思路】由实验可知,溶液A中加入足量盐酸后,产生气体甲,气体甲能在空气中转化为气体乙,根据
NO+3Fe2++4H+===3Fe3++NO↑+2H O、2NO+O ===2NO ,溶液A中一定含有NO和Fe2+,不含HCO和
3 2 2 2 3 3
CO2,气体甲为NO,气体乙为NO ;又知反应①后的溶液B与溶液A中的阴离子种类相同,说明反应
3 2
后的溶液中阴离子种类没有变化,故原溶液中一定含有Cl-;此外原溶液中一共有五种离子,且浓度均为
0.1mol/L,故溶液中还必须含有Cu2+和SO2才能满足电荷守恒:2c(Fe2+)+2c(Cu2+)=c(Cl-)+c(NO)+c(SO2),
4 3 4
综上所述,原溶液中含有Fe2+、Cu2+、Cl-、NO、SO2,不含Ba2+、Fe3+、Al3+、HCO、CO2。根据
3 4 3 3
分析,沉淀乙为Cu(OH) ,Cu(OH) 溶于氨水后生成[Cu(NH ) ](OH) ,A项正确;根据分析,溶液A中含
2 2 3 4 2
有Fe2+、Cu2+、Cl-、NO、SO2,则溶液B中含有Fe3+、Cu2+、Cl-、NO、SO2,B、C项正确;根据
3 4 3 4
分析,加入固体C将pH调至4,产生氢氧化铁和溶液D,溶液D与足量NaOH溶液反应生成氢氧化铜,
固体C不可能是MgO,D项错误。
高三期末质量监测化学试题参考答案 第 5 页 共 10 页高三期末质量检测 化学
15.【答案】A
【立意】以草酸钙和水的反应为背景,考查对水溶液中离子浓度平衡图像的分析,包含三大守恒、读图能
力、水的电离程度,检验化学平衡原理的应用能力。
【思路】CaC O 体系中存在一系列平衡,当通入HCl时,pH降低,CaC O 转化为HC O和H C O ,pH
2 4 2 4 2 4 2 2 4
越小H C O 含量越高,所以①②③分别代表C O2、H C O 、HC O与pH变化的关系,B点酸性比较
2 2 4 2 4 2 2 4 2 4
强,已经通入HCl,所以溶液中的电荷守恒为c(H+)+2c(Ca2+)=2c(C O2)+c(HC O)+c(OH-)+c(Cl-),A项
2 4 2 4
错误;C点为曲线①③交点,说明pH=4.2时,c(HC O)=c(C O2),H C O 的
2 4 2 4 2 2 4
c(H)c(C O2)
K = 2 4 =c(H+)=10-4.2,B点为曲线①②交点,说明pH=2.77时,c(H C O )=c(C O2),
a2 c(HC O) 2 2 4 2 4
2 4
c2(H)c(C O2) 105.54 105.54
K ·K = 2 4 =c2(H+)=10-5.54,H C O 的K = = =c(H+)=10-1.34,A点为曲线②③交
a1 a2 2 2 4 a1
c(H C O ) K 104.2
2 2 4 a2
点,此时c(HC O)=c(H C O ),c(H+)=K =10-1.34mol/L,pH=1.34,B项正确;HC O的水解常数
2 4 2 2 4 a1 2 4
K 11014
K = w = =10-12.66、H C O 的K =10-4.2,所以NaHC O 溶液中HC O的电离程度大于水解程度,
h K 101.34 2 2 4 a2 2 4 2 4
a1
c(HC O)>c(C O2)>c(H C O ),C项正确;A点溶液显酸性,B、C点酸性减弱,水的电离程度增大,
2 4 2 4 2 2 4
C点之后才得到饱和盐溶液,因此水的电离程度:A<B<C,D项正确。
二、非选择题
16.(14分)
【答案】
Ⅰ.
(1)b(1分) 浓硫酸(1分)
(2)水浴加热(2分,答案合理即可)
△
(3)Cr O +3CCl 2CrCl +3COCl (2分)
2 3 4 3 2
(4)将生成的CrCl 排入装置C被收集,并将COCl 完全排入装置E被充分吸收(2分)
3 2
5abM
Ⅱ.(1) (2分) (2)使过量H O 完全分解(2分) 偏低(2分)
2 2
12m
【思路】
Ⅰ.
(1)干燥管在使用时一般是粗口进气体、细口出气体,因此与c口相连接的是b口;因为CrCl 易水解,
3
所以装置B、C前后都要防止水蒸气进入,故X的作用为干燥N ,可选择浓硫酸。
2
(2)CCl 易挥发,所以可以采用水浴加热的方法提供稳定的CCl 气流。
4 4
△
(3)利用原子守恒可以写出Cr O 和CCl 制备无水CrCl 的化学方程式:Cr O +3CCl 2CrCl +3COCl 。
2 3 4 3 2 3 4 3 2
(4)反应结束后还需要持续通入N ,将生成的CrCl 排入装置C被收集,并将COCl 完全排入装置E被
2 3 2
充分吸收。
Ⅱ.
(1)由原子个数和得失电子数目守恒可得关系式:2CrCl ~2CrO2~3I ~6Na S O ,滴定消耗bmLa
3 4 2 2 2 3
高三期末质量监测化学试题参考答案 第 6 页 共 10 页高三期末质量检测 化学
mol/L硫代硫酸钠溶液,则无水三氯化铬的质量分数为
2 250 mL
ab103 mol M g/mol
6 20.00 mL 5abM
×100%= %。
m g 12m
(2)加热使过量H O 完全分解,以免在酸性条件下,H O 将CrO2还原为Cr3+;若步骤ⅱ中未继续加热
2 2 2 2 2 7
一段时间,由于过量H O 的存在,在后面的酸性条件下会将CrO2还原为Cr3+,则滴定时消耗标准溶液
2 2 2 7
Na S O 体积减小,测定的CrCl 质量分数偏低。
2 2 3 3
17.(13分)
【答案】
(1)C(1分) 烧杯、漏斗、玻璃棒(2分)
(2)2SnS+O +2H O===2SnO +2H S(2分)
2 2 2 2
K (FeAsO )
(3)由 Fe3+浓度和 K (FeAsO )可得 c( AsO3 )= sp 4 =1×10-15 mol/L,由 Co2+浓度可得
sp 4 4 c(Fe3)
Q[Co (AsO ) ]=c3(Co2+)·c2(AsO3)≤10-33<K [Co (AsO ) ],故“富砷渣”中不含Co (AsO ) ,该同学观点错误
3 4 2 4 sp 3 4 2 3 4 2
(2分,答案合理即可)
(4)3Co2++MnO+7H O===3Co(OH) ↓+MnO +5H+(2分) ZnSO 和K SO (2分)
4 2 3 2 4 2 4
(5)Co O (2分)
3 4
【思路】
(1)根据图像可知超过70℃时锡的浸出率非常低、钴和锌的浸出率增大不多,故选C项;实验室中过滤
操作需要用到的玻璃仪器为烧杯、漏斗、玻璃棒。
(2)根据化合价升降相等、电荷守恒、原子守恒可以写出反应的化学方程式:2SnS+O +2H O===2SnO +2H S。
2 2 2 2
K (FeAsO )
(3)由Fe3+浓度和K (FeAsO )可得c(AsO3 )= sp 4 =1×10-15mol/L,由Co2+浓度可得
sp 4 4 c(Fe3)
Q[Co (AsO ) ]=c3(Co2+)·c2(AsO3)≤10-33<K [Co (AsO ) ],故“富砷渣”中不含Co (AsO ) ,该同学观点错误。
3 4 2 4 sp 3 4 2 3 4 2
(4)“氧化沉钴”中Co2+发生氧化还原反应的离子方程式为3Co2++MnO+7H O===3Co(OH) ↓+MnO +5H+;
4 2 3 2
最终得到的“除钴液”中含有的金属离子主要是除砷时与加入ZnO调pH时引入的Zn2+、加入KMnO “氧化
4
沉钴”时引入的K+[c(Fe3+)<1×10-5mol/L,已沉淀完全],而阴离子是在酸浸时引入的,因此其中主要的盐
有ZnSO 和K SO 。
4 2 4
(5)由图可知,CoC O ·2H O[M=183g/mol]的质量为18.3g,其物质的量为0.1mol,B点对应物质的质
2 4 2
量为14.7g,与其起始物质的质量相比减少18.3g-14.7g=3.6g,为结晶水的质量,故B点物质为CoC O ,
2 4
继续加热得到钴的氧化物,根据钴原子守恒,C点8.03g固体中有0.1mol钴,质量为5.9g,O的质量为
8.03g-5.9g=2.13g,n(Co)∶n(O)≈3∶4,所以C点剩余固体的成分是Co O 。
3 4
18.(14分)
【答案】
(1)-206kJ/mol(1分) 低温(1分)
(2)①D(2分)
(2)②增大(2分)
(3)①CO (2分)
2
(3)②0.4mol(2分) 7.03(2分)
(3)③减小(2分)
【思路】
(1)由盖斯定律可知,反应ⅲ=反应ⅱ-反应ⅰ,ΔH =ΔH -ΔH =(-165-41)kJ·mol−1=-206kJ·mol−1;反应ⅲ为放
3 2 1
热、熵减的反应,在低温下有利于反应自发进行。
高三期末质量监测化学试题参考答案 第 7 页 共 10 页高三期末质量检测 化学
(2)
①容器内反应后气体物质的量减少,容器内气体压强减小,所以容器内压强不发生变化时达到平衡状态,
A项不符合题意;混合气体的物质的量发生改变,所以气体平均摩尔质量达到平衡前会发生变化,B项不
符合题意;反应ⅰ、ⅱ消耗的H 和CO 的物质的量不相等,故达到平衡前H 和CO 的物质的量之比发生改
2 2 2 2
变,C项不符合题意;因为是在恒容容器中发生反应,容器体积不变,容器内的物质全部都是气态,所以
混合气体的密度不是变化量,D项符合题意。
②反应ⅰ是吸热反应,平衡后升高温度时v 、v 均增大,平衡正向移动,v 增大更多,即k 、k 均增大,
正 逆 正 正 逆
k 增大更多,所以k -k 的差值增大。
正 正 逆
(3)
①反应ⅰ为吸热反应,反应ⅱ、ⅲ均为放热反应,升高温度,反应ⅰ正向移动,反应ⅱ、ⅲ逆向移动,则随温度
的升高,n(CO)增大、n(CH )减小,即b表示CH 、c表示CO,则a表示CO 。
4 4 2
②T℃平衡时n(H )=1.2mol,即n (H )=(2-1.2)mol=0.8mol,n(H O)=0.6mol,根据H原子守恒得n(CH )=0.1
2 消耗 2 2 4
mol,根据C、O原子守恒可知此时n(CO)=0.4mol,n(CO )=0.5mol,则此时反应ⅲ的平衡常数
2
0.6 0.1
K 9 9 7.03。
0.4 1.2
( )3
9 9
③保持温度不变缩小容器体积,反应ⅱ、ⅲ均正向移动,n(H )减小、n(H O)增大,反应 i 的平衡常数
2 2
c(H O)c(CO) n(H O) n(CO)
K= 2 ,温度不变时K不改变, 2 增大,所以 减小。
c(H )c(CO ) n(H ) n(CO )
2 2 2 2
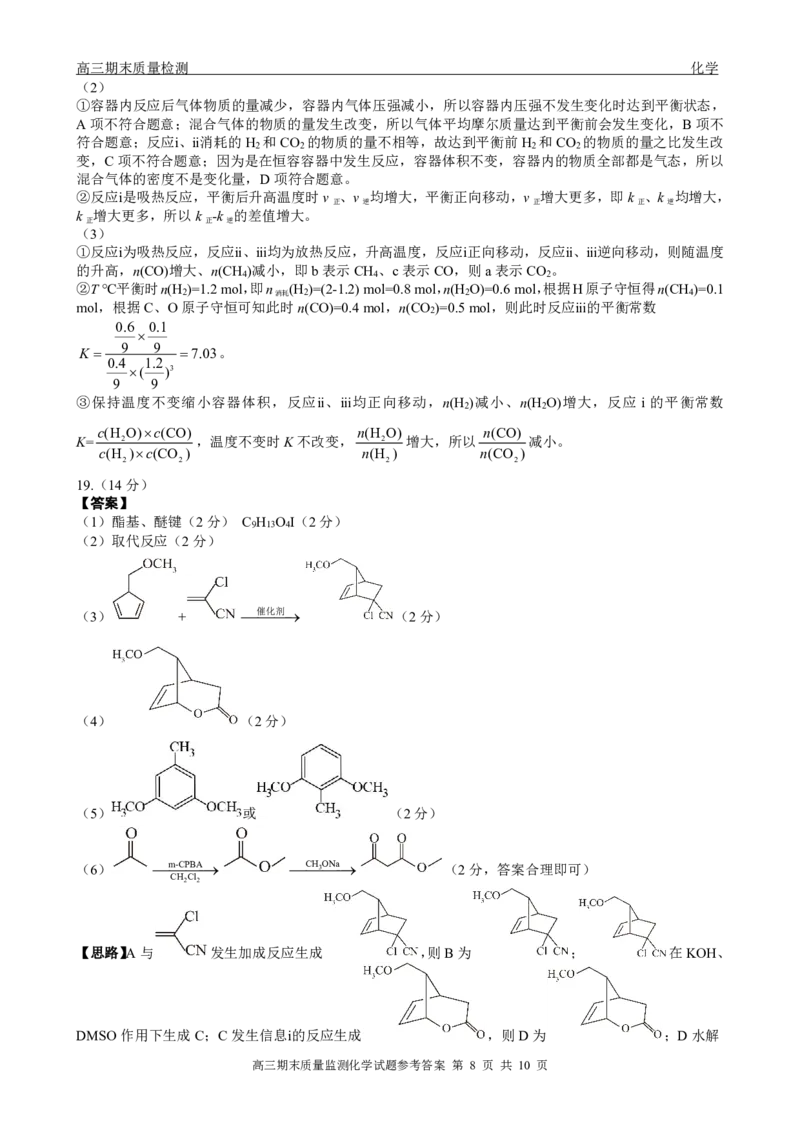
19.(14分)
【答案】
(1)酯基、醚键(2分) C H O I(2分)
9 13 4
(2)取代反应(2分)
(3) + 催化剂 (2分)
(4) (2分)
(5) 或 (2分)
(6) m-CPBA CH 3 ONa (2分,答案合理即可)
CH Cl
2 2
【思路】A与 发生加成反应生成 ,则B为 ; 在KOH、
DMSO作用下生成C;C发生信息ⅰ的反应生成 ,则D为 ;D水解
高三期末质量监测化学试题参考答案 第 8 页 共 10 页高三期末质量检测 化学
生成E;E在KI 、H O条件下生成F;F与 发生取代反应生成G;G在n-Bm SmH、
3 2 3
AlBN条件下生成H。
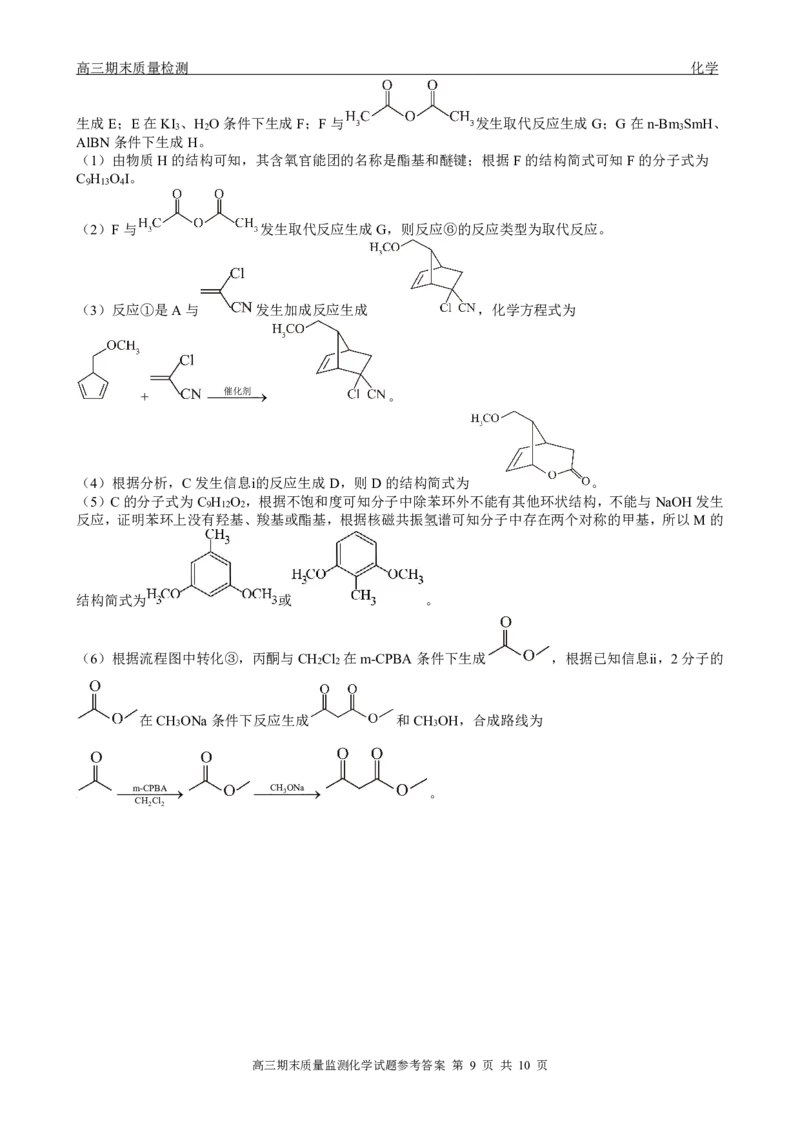
(1)由物质H的结构可知,其含氧官能团的名称是酯基和醚键;根据F的结构简式可知F的分子式为
C H O I。
9 13 4
(2)F与 发生取代反应生成G,则反应⑥的反应类型为取代反应。
(3)反应①是A与 发生加成反应生成 ,化学方程式为
+ 催化剂 。
(4)根据分析,C发生信息ⅰ的反应生成D,则D的结构简式为 。
(5)C的分子式为C H O ,根据不饱和度可知分子中除苯环外不能有其他环状结构,不能与NaOH发生
9 12 2
反应,证明苯环上没有羟基、羧基或酯基,根据核磁共振氢谱可知分子中存在两个对称的甲基,所以M的
结构简式为 或 。
(6)根据流程图中转化③,丙酮与CH Cl 在m-CPBA条件下生成 ,根据已知信息ⅱ,2分子的
2 2
在CH ONa条件下反应生成 和CH OH,合成路线为
3 3
m-CPBA CH 3 ONa 。
CH Cl
2 2
高三期末质量监测化学试题参考答案 第 9 页 共 10 页高三期末质量检测 化学
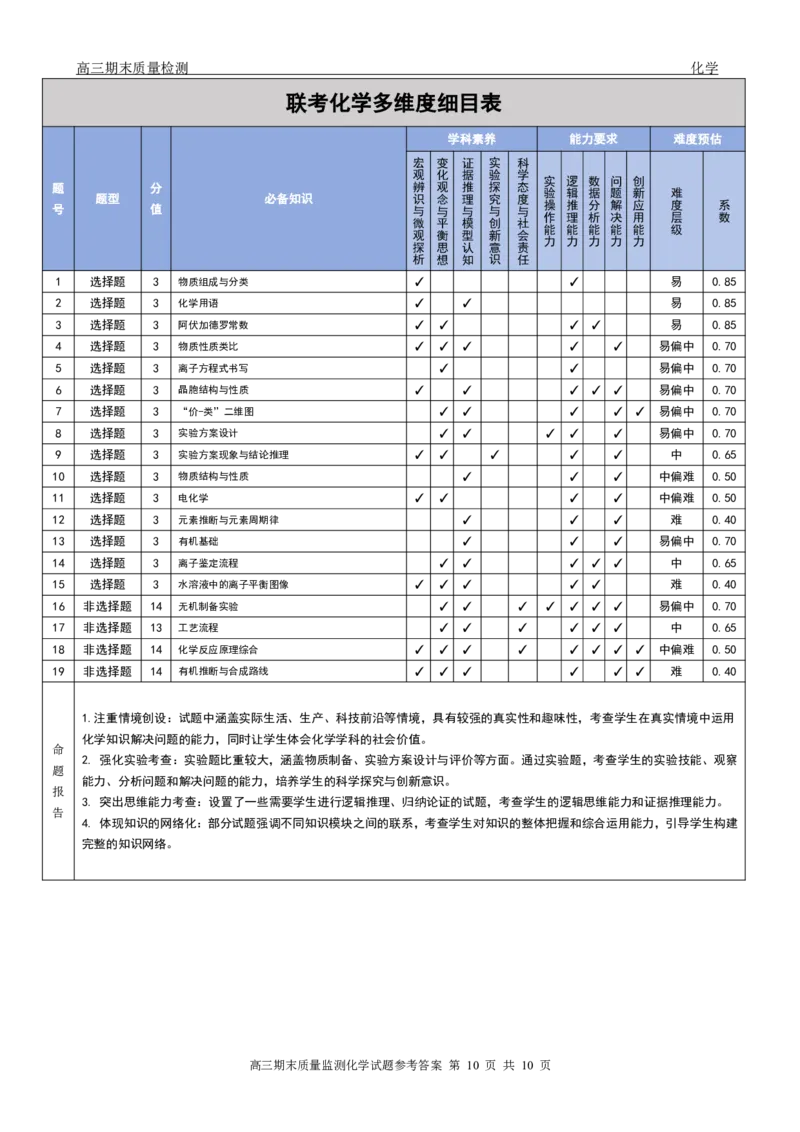
联考化学多维度细目表
学科素养 能力要求 难度预估
宏 变 证 实 科
观 化 据 验 学
实 逻 数 问 创
题 分 辨 观 推 探 态 验 辑 据 题 新 难
题型 必备知识 识 念 理 究 度
操 推 分 解 应 度 系
号 值 与 与 与 与 与
作 理 析 决 用 层 数
微 平 模 创 社
能 能 能 能 能 级
观 衡 型 新 会
力 力 力 力 力
探 思 认 意 责
析 想 知 识 任
1 选择题 3 物质组成与分类 ✓ ✓ 易 0.85
2 选择题 3 化学用语 ✓ ✓ 易 0.85
3 选择题 3 阿伏加德罗常数 ✓ ✓ ✓ ✓ 易 0.85
4 选择题 3 物质性质类比 ✓ ✓ ✓ ✓ ✓ 易偏中 0.70
5 选择题 3 离子方程式书写 ✓ ✓ 易偏中 0.70
6 选择题 3 晶胞结构与性质 ✓ ✓ ✓ ✓ ✓ 易偏中 0.70
7 选择题 3 “价-类”二维图 ✓ ✓ ✓ ✓ ✓ 易偏中 0.70
8 选择题 3 实验方案设计 ✓ ✓ ✓ ✓ ✓ 易偏中 0.70
9 选择题 3 实验方案现象与结论推理 ✓ ✓ ✓ ✓ ✓ 中 0.65
10 选择题 3 物质结构与性质 ✓ ✓ ✓ 中偏难 0.50
11 选择题 3 电化学 ✓ ✓ ✓ ✓ 中偏难 0.50
12 选择题 3 元素推断与元素周期律 ✓ ✓ ✓ 难 0.40
13 选择题 3 有机基础 ✓ ✓ ✓ 易偏中 0.70
14 选择题 3 离子鉴定流程 ✓ ✓ ✓ ✓ ✓ 中 0.65
15 选择题 3 水溶液中的离子平衡图像 ✓ ✓ ✓ ✓ ✓ 难 0.40
16 非选择题 14 无机制备实验 ✓ ✓ ✓ ✓ ✓ ✓ ✓ 易偏中 0.70
17 非选择题 13 工艺流程 ✓ ✓ ✓ ✓ ✓ ✓ 中 0.65
18 非选择题 14 化学反应原理综合 ✓ ✓ ✓ ✓ ✓ ✓ ✓ ✓ 中偏难 0.50
19 非选择题 14 有机推断与合成路线 ✓ ✓ ✓ ✓ ✓ ✓ 难 0.40
1.注重情境创设:试题中涵盖实际生活、生产、科技前沿等情境,具有较强的真实性和趣味性,考查学生在真实情境中运用
化学知识解决问题的能力,同时让学生体会化学学科的社会价值。
命
2. 强化实验考查:实验题比重较大,涵盖物质制备、实验方案设计与评价等方面。通过实验题,考查学生的实验技能、观察
题
能力、分析问题和解决问题的能力,培养学生的科学探究与创新意识。
报
3. 突出思维能力考查:设置了一些需要学生进行逻辑推理、归纳论证的试题,考查学生的逻辑思维能力和证据推理能力。
告
4. 体现知识的网络化:部分试题强调不同知识模块之间的联系,考查学生对知识的整体把握和综合运用能力,引导学生构建
完整的知识网络。
高三期末质量监测化学试题参考答案 第 10 页 共 10 页