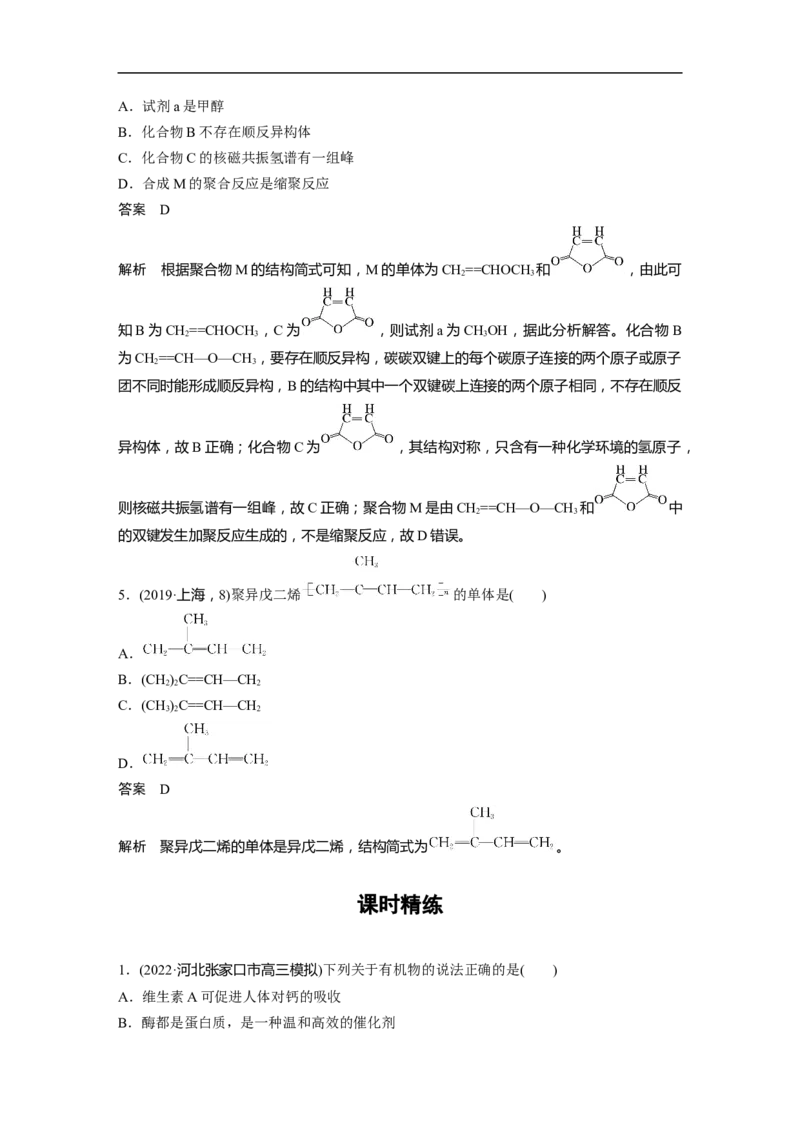
文档内容
第 64 讲 生命中的基础有机化学物质 合成有机高分子
复习目标 1.了解糖类、核酸、油脂、氨基酸和蛋白质的组成、结构特点、主要化学性质
及应用。2.了解糖类、氨基酸和蛋白质在生命过程中的作用,了解脱氧核糖核酸、核糖核酸
的生物功能。3.了解合成高分子的组成与结构特点,能依据简单合成高分子的结构分析其链
节和单体。4.了解加聚反应和缩聚反应的含义。5.了解合成高分子在高新技术领域的应用以
及在发展经济、提高生活质量方面的贡献。
考点一 糖类 核酸 油脂
1.糖类
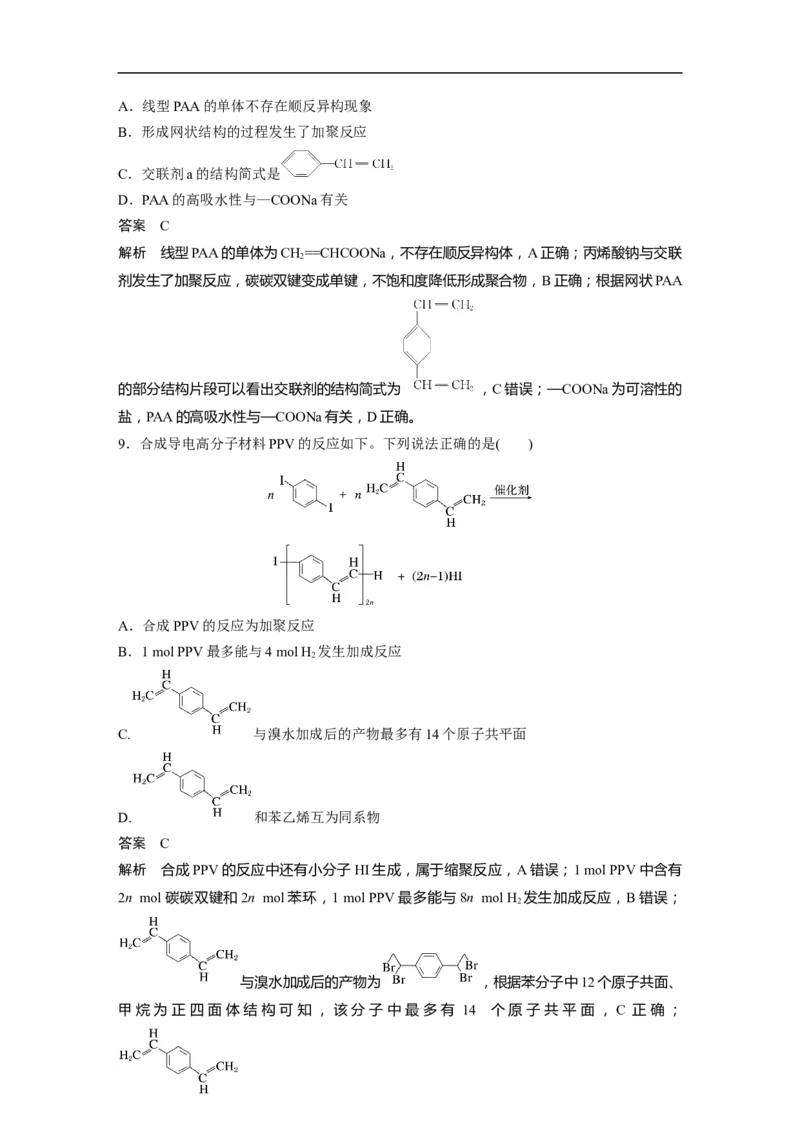
(1)糖类的概念和分类
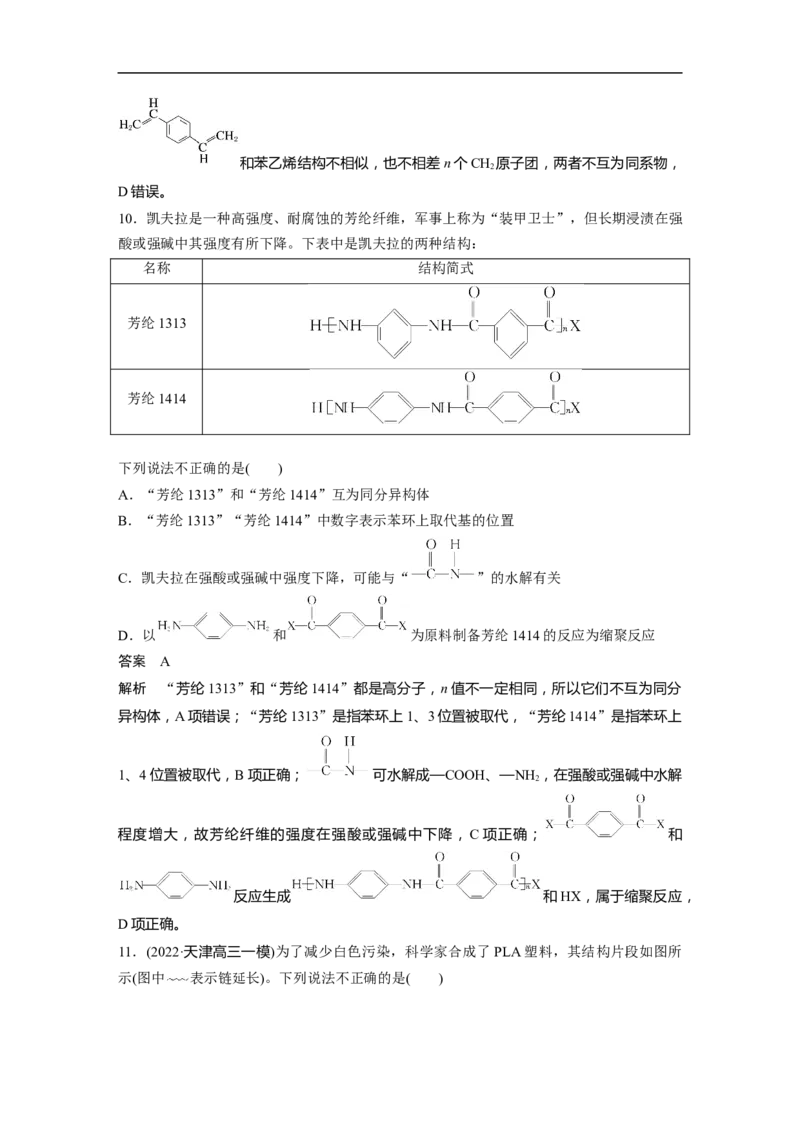
①概念:从分子结构上看,糖类可以定义为多羟基醛、多羟基酮和它们的脱水缩合物。
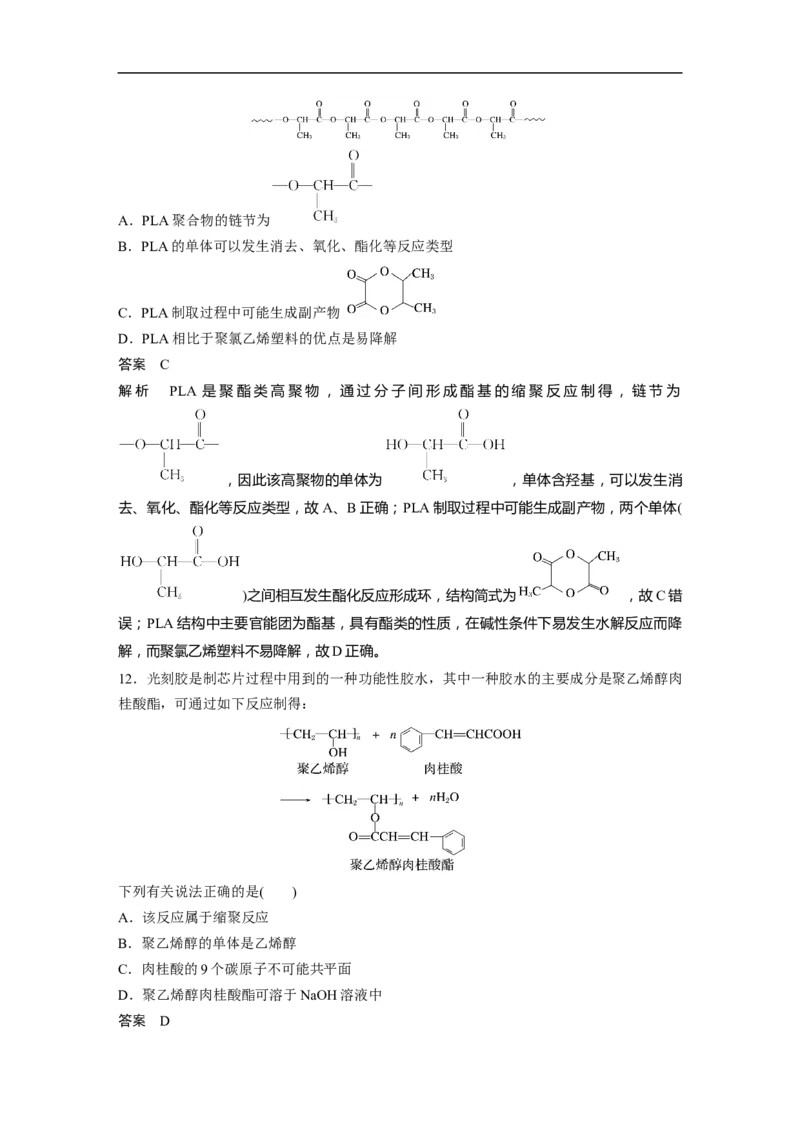
②组成:碳、氢、氧三种元素。大多数糖类化合物的通式为C (H O) ,所以糖类也叫碳水化
m 2 n
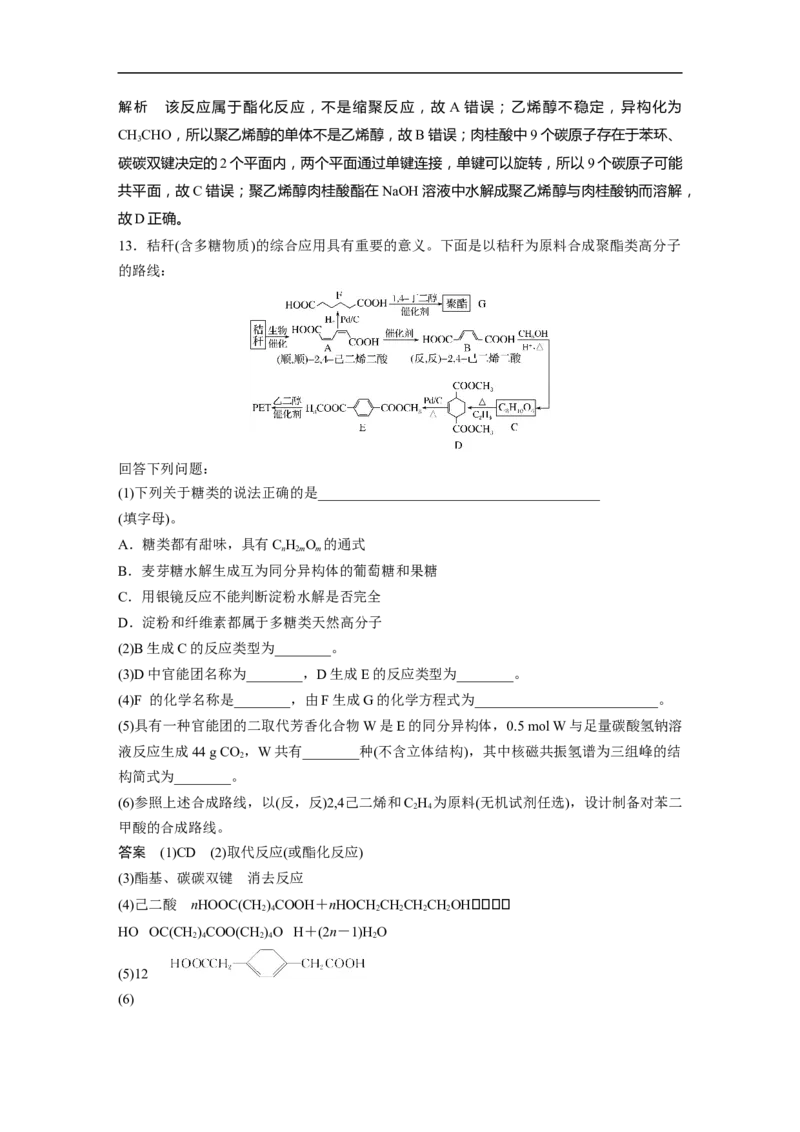
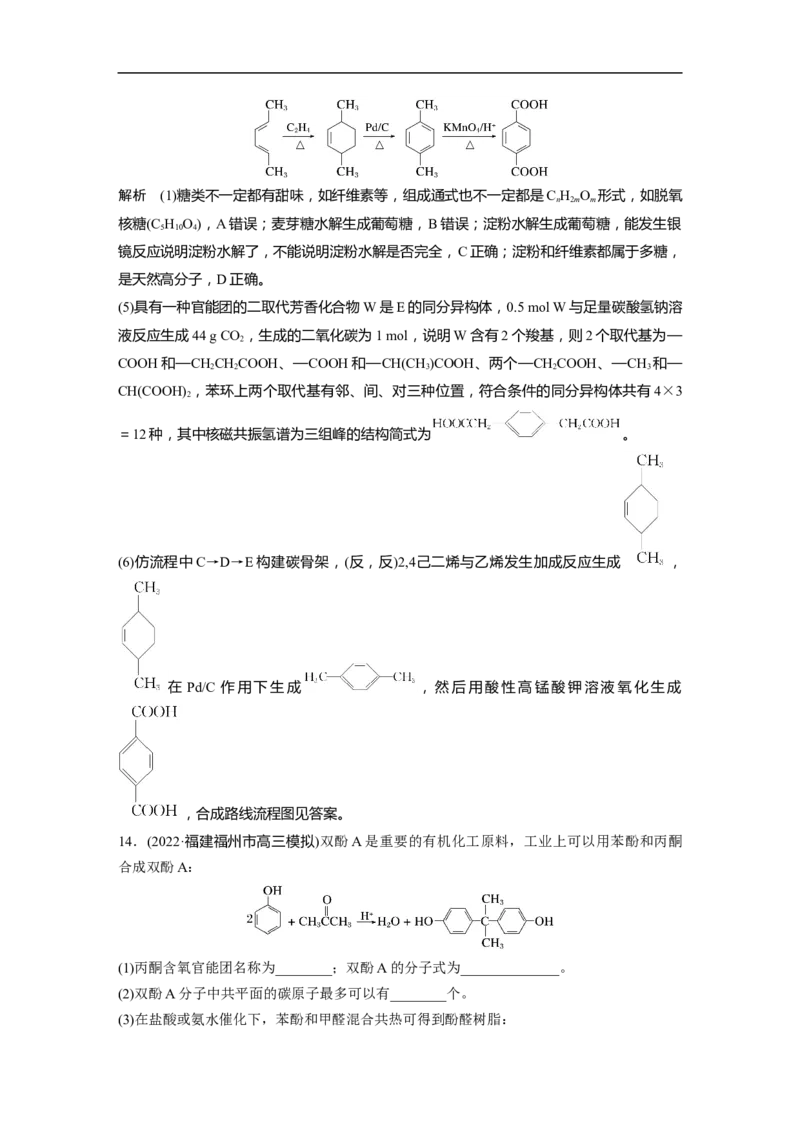
合物。
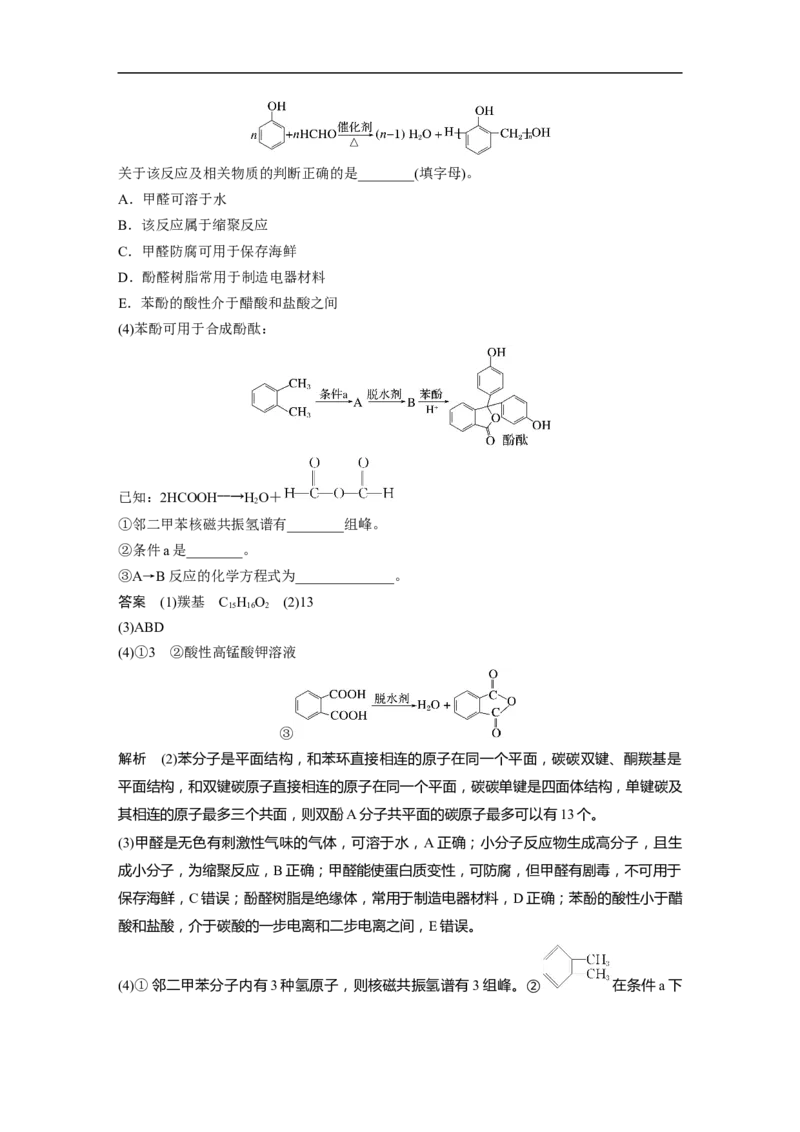
③分类
(2)单糖
① 葡 萄 糖 : 多 羟 基 醛 CHOH(CHOH) CHO , 它 与 果 糖 [ 多 羟 基 酮
2 4
]互为同分异构体。
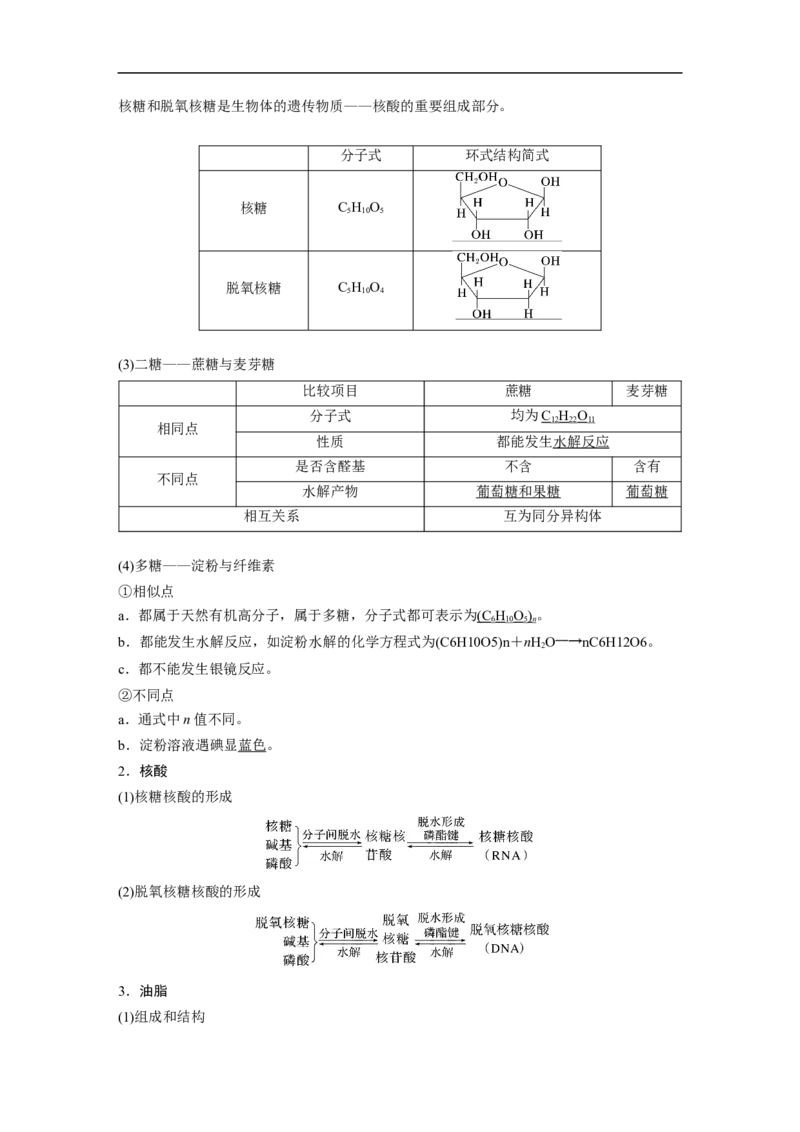
②戊糖——核糖、脱氧核糖核糖和脱氧核糖是生物体的遗传物质——核酸的重要组成部分。
分子式 环式结构简式
核糖 C H O
5 10 5
脱氧核糖 C H O
5 10 4
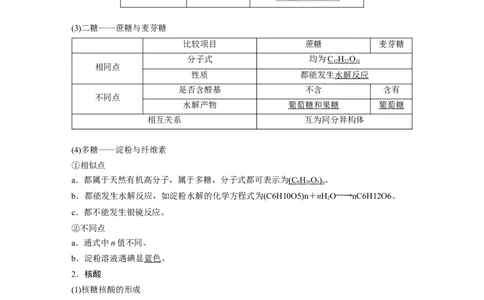
(3)二糖——蔗糖与麦芽糖
比较项目 蔗糖 麦芽糖
分子式 均为C H O
12 22 11
相同点
性质 都能发生水解反应
是否含醛基 不含 含有
不同点
水解产物 葡萄糖和果糖 葡萄糖
相互关系 互为同分异构体
(4)多糖——淀粉与纤维素
①相似点
a.都属于天然有机高分子,属于多糖,分子式都可表示为(C H O)。
6 10 5 n
b.都能发生水解反应,如淀粉水解的化学方程式为(C6H10O5)n+nHO――→nC6H12O6。
2
c.都不能发生银镜反应。
②不同点
a.通式中n值不同。
b.淀粉溶液遇碘显蓝色。
2.核酸
(1)核糖核酸的形成
(2)脱氧核糖核酸的形成
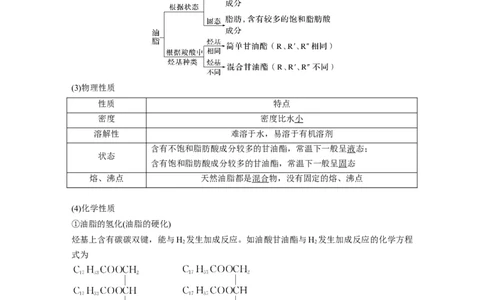
3.油脂
(1)组成和结构油脂是高级脂肪酸与甘油反应所生成的酯,由C、H、O三种元素组成,其结构可表示为
(2)分类
(3)物理性质
性质 特点
密度 密度比水小
溶解性 难溶于水,易溶于有机溶剂
含有不饱和脂肪酸成分较多的甘油酯,常温下一般呈液态;
状态
含有饱和脂肪酸成分较多的甘油酯,常温下一般呈固态
熔、沸点 天然油脂都是混合物,没有固定的熔、沸点
(4)化学性质
①油脂的氢化(油脂的硬化)
烃基上含有碳碳双键,能与H 发生加成反应。如油酸甘油酯与H 发生加成反应的化学方程
2 2
式为
+3H――→ 。
2
经硬化制得的油脂叫人造脂肪,也称硬化油。
②水解反应
a.酸性条件下
如硬脂酸甘油酯在酸性溶液中的水解反应方程式为
+3HO
2+ 3C H COOH。
17 35
b.碱性条件下——皂化反应
如硬脂酸甘油酯在氢氧化钠溶液中的水解反应方程式为
+3NaOH――→
+ 3C H COONa。
17 35
碱性条件下其水解程度比酸性条件下水解程度大。
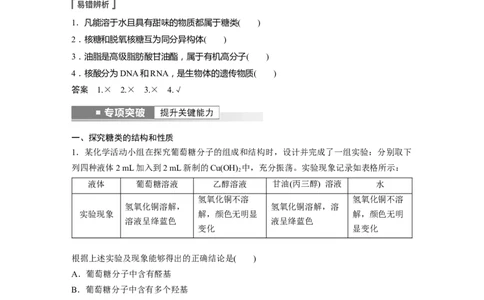
1.凡能溶于水且具有甜味的物质都属于糖类( )
2.核糖和脱氧核糖互为同分异构体( )
3.油脂是高级脂肪酸甘油酯,属于有机高分子( )
4.核酸分为DNA和RNA,是生物体的遗传物质( )
答案 1.× 2.× 3.× 4.√
一、探究糖类的结构和性质
1.某化学活动小组在探究葡萄糖分子的组成和结构时,设计并完成了一组实验:分别取下
列四种液体2 mL加入到2 mL新制的Cu(OH) 中,充分振荡。实验现象记录如表格所示:
2
液体 葡萄糖溶液 乙醇溶液 甘油(丙三醇) 溶液 水
氢氧化铜不溶 氢氧化铜不溶
氢氧化铜溶解, 氢氧化铜溶解,溶
实验现象 解,颜色无明显 解,颜色无明
溶液呈绛蓝色 液呈绛蓝色
变化 显变化
根据上述实验及现象能够得出的正确结论是( )
A.葡萄糖分子中含有醛基
B.葡萄糖分子中含有多个羟基
C.葡萄糖的分子式是C H O
6 12 6
D.葡萄糖分子中碳链呈锯齿形
答案 B
解析 乙醇是一元醇,不能与新制的氢氧化铜反应,氢氧化铜也不溶于水中;而甘油是三
(多)元醇,能溶解氢氧化铜并得到绛蓝色溶液,当向葡萄糖溶液中加入新制的氢氧化铜时,
也得到了相同的现象,故可得出结论:在葡萄糖的结构中含有多个羟基,B项正确;实验中
未加热,没有砖红色沉淀生成,故不能证明醛基的存在。
2.棉籽和甜菜中含有棉籽糖。一定条件下,一分子棉籽糖水解生成一分子蔗糖和一分子半乳糖(半乳糖是一种单糖,和葡萄糖互为同分异构体)。
(1)棉籽糖属于哪一类糖?(选答“单糖”“二糖”或“三糖”)
(2)写出棉籽糖的化学式。
(3)如果使1 mol棉籽糖完全水解,各水解产物物质的量分别是多少?
答案 (1)三糖 (2)C H O (3)1 mol半乳糖,1 mol葡萄糖,1 mol果糖。
18 32 16
3.为了检验淀粉的水解程度,甲、乙、丙三位同学分别设计并完成了如下三个实验,得出
了相应的结论。
甲:淀粉液――→水解液――――――→中和液――→溶液不变蓝。
结论:淀粉完全水解。
乙:淀粉液――→水解液――――→无银镜现象。
结论:淀粉没有水解。
丙:淀粉液――→水解液
。
结论:淀粉完全水解。
请分别判断以上三位学生的结论是否正确?说明理由。
答案 甲的结论不正确,因为加入NaOH溶液呈碱性后,加入碘水,I 与NaOH溶液发生反
2
应,没有I 存在,不能证明淀粉是否存在;乙的结论不正确,乙实验方案中未用碱中和作催
2
化剂的酸,银镜反应须在碱性条件下才能发生;丙的结论正确,该方案中,中和液能发生银
镜反应,说明淀粉已经水解,加入碘水无现象,说明已无淀粉存在,故淀粉已完全水解。
二、油脂的结构与性质
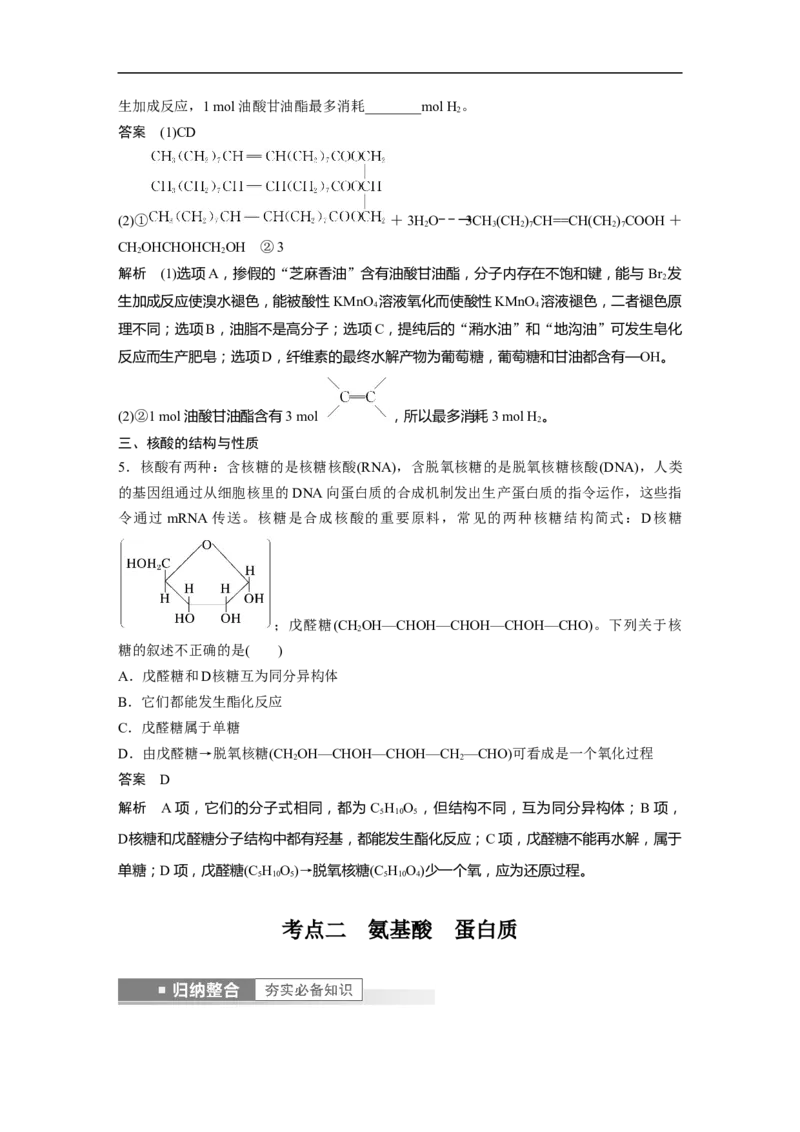
4.地沟油,泛指在生活中存在的各类劣质油,如回收的食用油、反复使用的炸油等。地沟
油最大来源为城市大型饭店下水道的隔油池。长期食用可能会引发癌症,对人体的危害极大。
根据以上信息和相关知识回答下列问题:
(1)下列说法正确的是________(填字母)。
A.掺假的“芝麻香油”能使溴水和酸性KMnO 溶液褪色,其原理相同
4
B.淀粉和油脂都是高分子
C.可将“潲水油”和“地沟油”分离提纯后来生产肥皂
D.纤维素的最终水解产物与油脂水解产生的甘油含有某种相同的官能团
(2)“地沟油”常常含有油酸甘油酯,在微生物作用下水解生成的不饱和脂肪酸中的碳碳双
键在日光作用下被空气中的氧气氧化生成有臭味的醛或酮,这种过程称为“酸败”。
①试写出油酸甘油酯[ ,—R为CH(CH)CH==CH(CH )CH—]“酸败”过程中
3 2 7 2 6 2
水解的化学方程式:________________________。
②工业上为了延缓不饱和油脂的“酸败”,通常采取的一种措施是在Ni催化作用下与H 发
2生加成反应,1 mol油酸甘油酯最多消耗________mol H。
2
答案 (1)CD
(2)① +3HO――→3CH(CH)CH==CH(CH )COOH+
2 3 2 7 2 7
CHOHCHOHCH OH ②3
2 2
解析 (1)选项A,掺假的“芝麻香油”含有油酸甘油酯,分子内存在不饱和键,能与 Br 发
2
生加成反应使溴水褪色,能被酸性KMnO 溶液氧化而使酸性KMnO 溶液褪色,二者褪色原
4 4
理不同;选项B,油脂不是高分子;选项C,提纯后的“潲水油”和“地沟油”可发生皂化
反应而生产肥皂;选项D,纤维素的最终水解产物为葡萄糖,葡萄糖和甘油都含有—OH。
(2)②1 mol油酸甘油酯含有3 mol ,所以最多消耗3 mol H 。
2
三、核酸的结构与性质
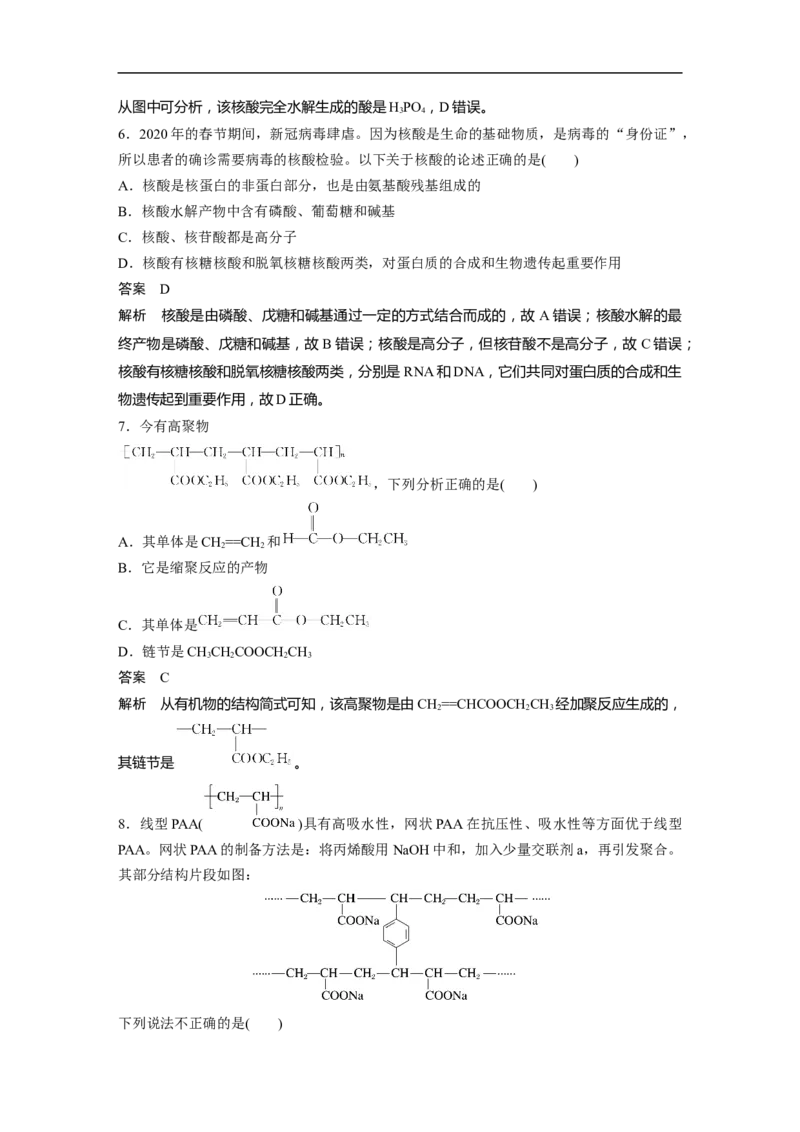
5.核酸有两种:含核糖的是核糖核酸(RNA),含脱氧核糖的是脱氧核糖核酸(DNA),人类
的基因组通过从细胞核里的DNA向蛋白质的合成机制发出生产蛋白质的指令运作,这些指
令通过 mRNA传送。核糖是合成核酸的重要原料,常见的两种核糖结构简式:D核糖
;戊醛糖(CHOH—CHOH—CHOH—CHOH—CHO)。下列关于核
2
糖的叙述不正确的是( )
A.戊醛糖和D核糖互为同分异构体
B.它们都能发生酯化反应
C.戊醛糖属于单糖
D.由戊醛糖→脱氧核糖(CHOH—CHOH—CHOH—CH —CHO)可看成是一个氧化过程
2 2
答案 D
解析 A项,它们的分子式相同,都为C H O ,但结构不同,互为同分异构体;B项,
5 10 5
D核糖和戊醛糖分子结构中都有羟基,都能发生酯化反应;C项,戊醛糖不能再水解,属于
单糖;D项,戊醛糖(C H O)→脱氧核糖(C H O)少一个氧,应为还原过程。
5 10 5 5 10 4
考点二 氨基酸 蛋白质1.氨基酸的结构与性质
(1)氨基酸的组成与结构
羧酸分子烃基上的氢原子被氨基取代得到的化合物称为氨基酸。蛋白质水解后得到的几乎都
是α氨基酸,其通式为 ,官能团为 — NH 和— COOH 。
2
(2)氨基酸的化学性质
①两性
氨基酸分子中既含有酸性基团 — COOH ,又含有碱性基团 — NH ,因此,氨基酸是两性化合
2
物。
如甘氨酸与HCl、NaOH反应的化学方程式分别为
+HCl―→ ;
+NaOH
―→ +HO。
2
②成肽反应
两个氨基酸分子(可以相同,也可以不同),在酸或碱的存在下加热,通过一分子的氨基与另
一分子的羧基间脱去一分子水,缩合形成含肽键( )的化合物,称为成肽反应。
两分子氨基酸脱水形成二肽,如:
+
―→ +HO。
2
多种氨基酸分子间脱水以肽键相互结合,可形成蛋白质。
2.蛋白质的结构与性质
(1)组成与结构
①蛋白质含有C、H、O、N、S等元素。
②蛋白质是由氨基酸通过缩聚反应生成的,蛋白质属于天然有机高分子。
(2)蛋白质的性质(3)酶
①大部分酶是一种蛋白质,具有蛋白质的性质。
②酶是一种生物催化剂,催化作用具有以下特点:
a.条件温和,不需加热;
b.具有高度的专一性;
c.具有高效催化作用。
1.棉、麻、羊毛及合成纤维完全燃烧都只生成CO 和HO( )
2 2
2.食用花生油和鸡蛋清都能发生水解反应( )
3.蚕丝、帛的主要成分均是蛋白质,属于天然高分子( )
4.用灼烧的方法可以区分蚕丝和人造纤维( )
5.蛋白质水解的条件是酸、碱或酶( )
答案 1.× 2.√ 3.√ 4.√ 5.√
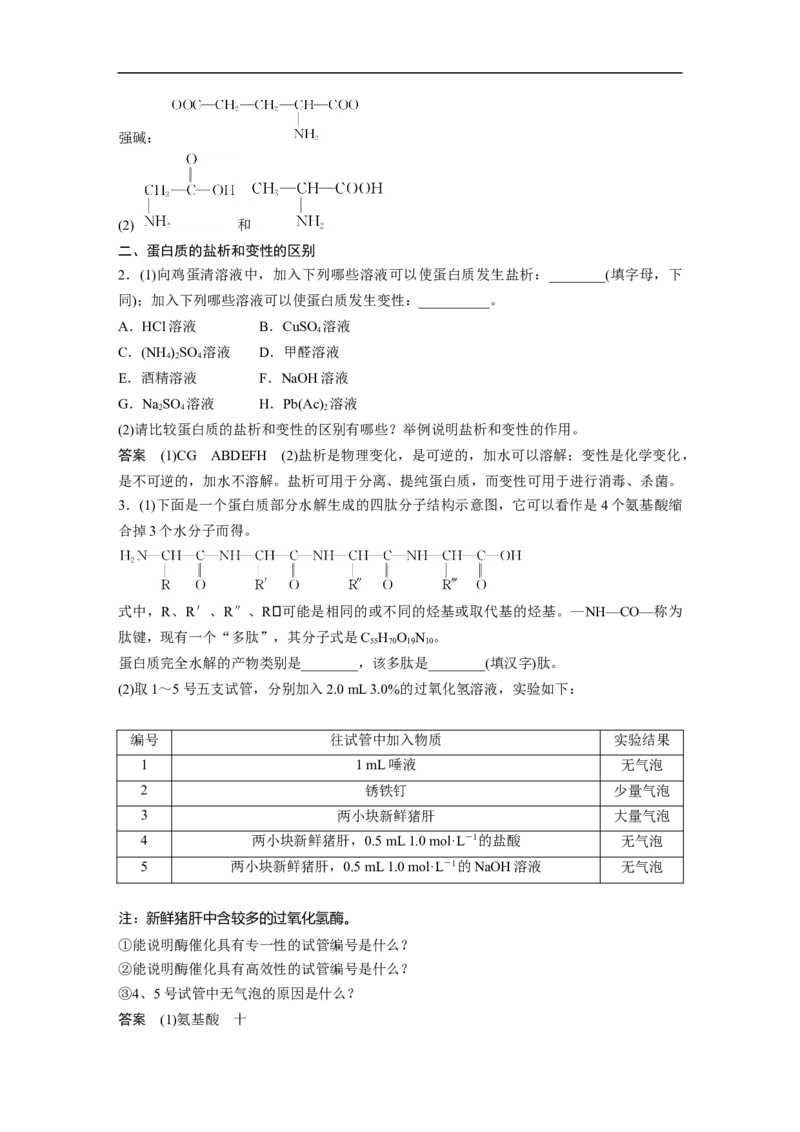
一、氨基酸的两性和成肽反应
1.(1)分别写出谷氨酸在强酸或强碱性条件下,粒子存在形式的结构简式。
(2)一种二肽的结构简式为
,写出合成这种二肽的氨基酸的结构简式。
答案 (1)强酸:强碱:
(2) 和
二、蛋白质的盐析和变性的区别
2.(1)向鸡蛋清溶液中,加入下列哪些溶液可以使蛋白质发生盐析:________(填字母,下
同);加入下列哪些溶液可以使蛋白质发生变性:__________。
A.HCl溶液 B.CuSO 溶液
4
C.(NH )SO 溶液 D.甲醛溶液
4 2 4
E.酒精溶液 F.NaOH溶液
G.NaSO 溶液 H.Pb(Ac) 溶液
2 4 2
(2)请比较蛋白质的盐析和变性的区别有哪些?举例说明盐析和变性的作用。
答案 (1)CG ABDEFH (2)盐析是物理变化,是可逆的,加水可以溶解;变性是化学变化,
是不可逆的,加水不溶解。盐析可用于分离、提纯蛋白质,而变性可用于进行消毒、杀菌。
3.(1)下面是一个蛋白质部分水解生成的四肽分子结构示意图,它可以看作是4个氨基酸缩
合掉3个水分子而得。
式中,R、R′、R″、R可能是相同的或不同的烃基或取代基的烃基。—NH—CO—称为
肽键,现有一个“多肽”,其分子式是C H O N 。
55 70 19 10
蛋白质完全水解的产物类别是________,该多肽是________(填汉字)肽。
(2)取1~5号五支试管,分别加入2.0 mL 3.0%的过氧化氢溶液,实验如下:
编号 往试管中加入物质 实验结果
1 1 mL唾液 无气泡
2 锈铁钉 少量气泡
3 两小块新鲜猪肝 大量气泡
4 两小块新鲜猪肝,0.5 mL 1.0 mol·L-1的盐酸 无气泡
5 两小块新鲜猪肝,0.5 mL 1.0 mol·L-1的NaOH溶液 无气泡
注:新鲜猪肝中含较多的过氧化氢酶。
①能说明酶催化具有专一性的试管编号是什么?
②能说明酶催化具有高效性的试管编号是什么?
③4、5号试管中无气泡的原因是什么?
答案 (1)氨基酸 十(2)①1,3 ②2,3 ③在强酸或强碱性条件下,过氧化氢酶(蛋白质)发生变性。
考点三 合成高分子
1.基本概念
(1)单体:能够进行聚合反应形成高分子的低分子化合物。
(2)链节:高分子中化学组成相同、可重复的最小单位。
(3)聚合度:高分子链中含有的链节数目。
如:
2.合成高分子的两个基本反应
(1)加聚反应:由含有不饱和键的化合物分子以加成反应的形式结合成高分子的反应。
(2)缩聚反应:单体分子间缩合 脱去小分子 ( 如 H O 、 HX 等 ) 生成高分子的反应。
2
3.高分子的分类及性质特点
高分子――→
高分子材料――→
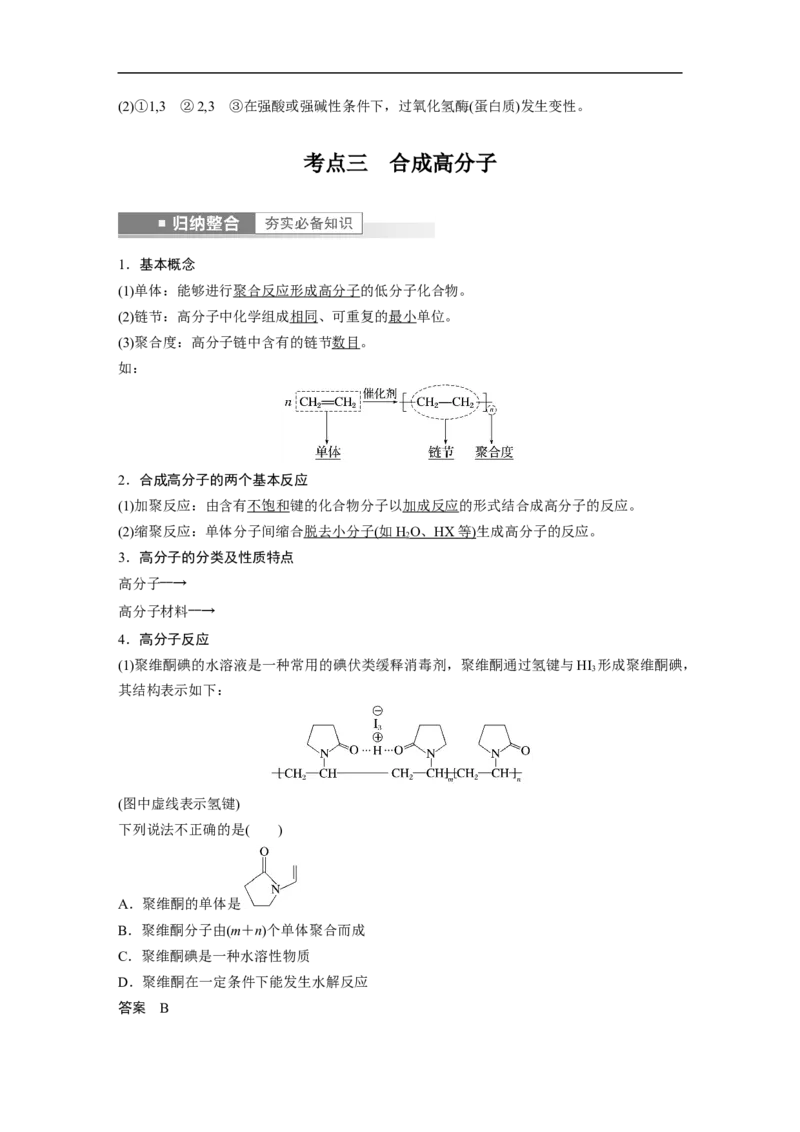
4.高分子反应
(1)聚维酮碘的水溶液是一种常用的碘伏类缓释消毒剂,聚维酮通过氢键与HI 形成聚维酮碘,
3
其结构表示如下:
(图中虚线表示氢键)
下列说法不正确的是( )
A.聚维酮的单体是
B.聚维酮分子由(m+n)个单体聚合而成
C.聚维酮碘是一种水溶性物质
D.聚维酮在一定条件下能发生水解反应
答案 B(2)橡胶树是热带植物,在我国海南已大面积种植。从橡胶树的胶乳中可提取天然橡胶,天
然橡胶的成分是聚异戊二烯,其结构简式为 。
回答下列问题: 天然橡胶能溶于汽油的根本原因是_______________________________,
天然橡胶加入适当的硫进行硫化后,其结构由__________变成__________,因而硫化橡胶
__________(填“能”或“不能”)溶于汽油。
答案 天然橡胶是线型结构 线型结构 网状结构 不能
1.丙烯和聚丙烯都能使溴的四氯化碳溶液褪色( )
2.加聚反应的原子利用率为100%( )
3.聚合度就是链节的个数( )
4.高分子不溶于任何溶剂,但对环境都会产生污染( )
答案 1.× 2.√ 3.× 4.×
一、加聚反应、缩聚反应方程式的书写方法
1.完成下列方程式。
(1)nCH==CH—CH ――→ 。
2 3
(2)nCH==CH—CH===CH――→
2 2
CH—CH==CH—CH 。
2 2
(3)n ――→
。
(4)nHOCH —CHOH+nHOOC—COOH
2 2
+(2n-1)H O;
2
nHOCH —CH—COOH
2 2
+(n-1)H O。
2
(5)nHN—CH COOH――→
2 2
+(n-1)H O;
2nHNCH COOH+ ――→
2 2
+(2n-1)H O]。
2
(6)nHCHO+n ――→ ( n - 1)H O +
2
。
(1)加聚反应方程式的书写
①单烯烃型单体加聚时,“断开双键,键分两端,添上括号,右下写n”。
②二烯烃型单体加聚时,“单变双,双变单,破两头,移中间,添上括号,右下写n”。
③含有一个双键的两种单体聚合时,“双键打开,中间相连,添上括号,右下写n”。
(2)缩聚物结构简式的书写
书写缩合聚合物(简称缩聚物)结构简式时,与加成聚合物(简称加聚物)结构简式写法有点不
同,缩聚物结构简式要在方括号外侧写出链节余下的端基原子或原子团,而加聚物的端基不
确定,通常用横线“—”表示。
(3)缩聚反应方程式的书写
①各单体物质的量与缩聚物结构简式的下角标一般要一致。
②注意生成的小分子的物质的量:由一种单体进行缩聚反应,生成的小分子物质的量一般为
n-1;由两种单体进行缩聚反应,生成的小分子物质的量一般为2n-1。
二、高聚物单体的推断
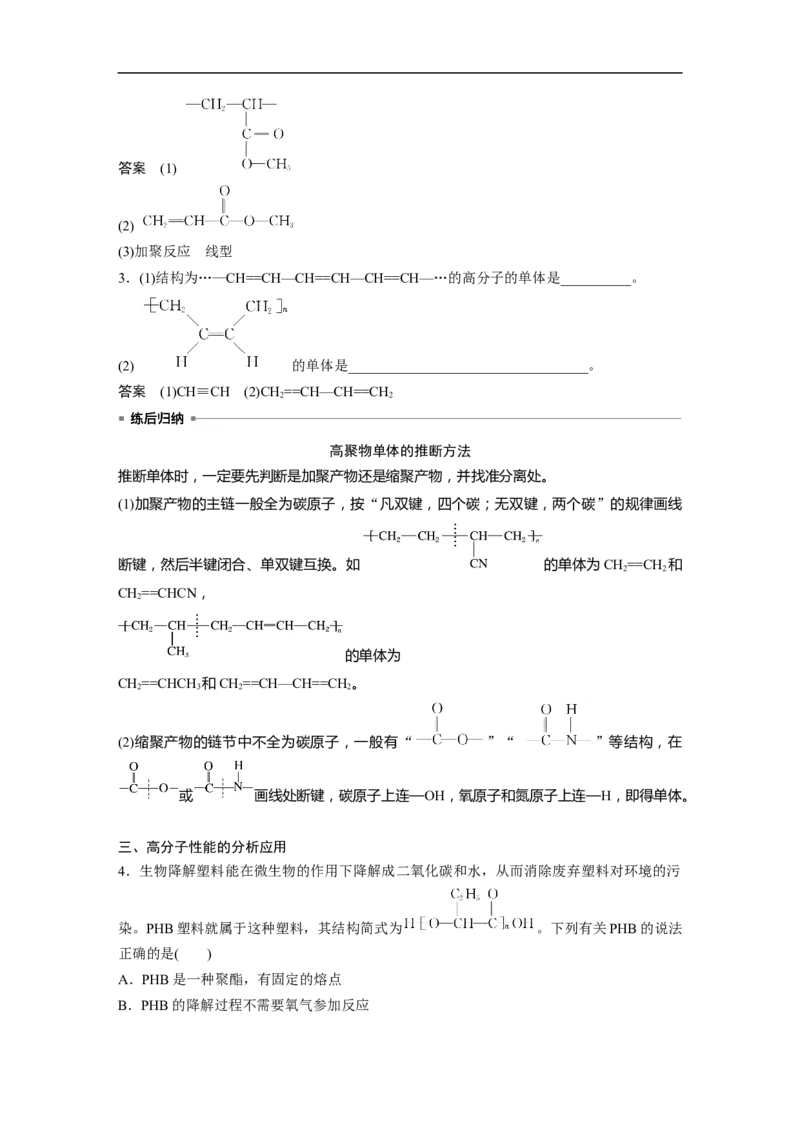
2.现有高聚物
回答下列问题:
(1)其链节是________________。
(2)其单体是________________。
(3)该反应为________________,它是一种__________(填“体型”或“线型”)高分子。答案 (1)
(2)
(3)加聚反应 线型
3.(1)结构为…—CH==CH—CH==CH—CH==CH—…的高分子的单体是__________。
(2) 的单体是__________________________________。
答案 (1)CH≡CH (2)CH ==CH—CH==CH
2 2
高聚物单体的推断方法
推断单体时,一定要先判断是加聚产物还是缩聚产物,并找准分离处。
(1)加聚产物的主链一般全为碳原子,按“凡双键,四个碳;无双键,两个碳”的规律画线
断键,然后半键闭合、单双键互换。如 的单体为CH==CH 和
2 2
CH==CHCN,
2
的单体为
CH==CHCH 和CH==CH—CH==CH。
2 3 2 2
(2)缩聚产物的链节中不全为碳原子,一般有“ ”“ ”等结构,在
或 画线处断键,碳原子上连—OH,氧原子和氮原子上连—H,即得单体。
三、高分子性能的分析应用
4.生物降解塑料能在微生物的作用下降解成二氧化碳和水,从而消除废弃塑料对环境的污
染。PHB塑料就属于这种塑料,其结构简式为 。下列有关PHB的说法
正确的是( )
A.PHB是一种聚酯,有固定的熔点
B.PHB的降解过程不需要氧气参加反应C.合成PHB的单体是CHCHCH(OH)COOH
3 2
D.通过加聚反应可以制得PHB
答案 C
解析 是高分子,属于混合物,没有固定的熔点;PHB是聚酯类高分
子,通过缩聚反应制得;其降解过程是先水解生成2羟基丁酸,然后被氧化为CO 和HO。
2 2
5.聚乳酸(PLA)是以有机酸乳酸为原料生产的新型聚酯材料,性能胜于现有的塑料聚乙烯、
聚丙烯、聚苯乙烯等材料,是新世纪最有发展前途的新型包装材料,是环保材料中的一颗明
星。聚乳酸可以玉米为原料发酵生产,利用聚乳酸制成生物降解性发泡材料。该材料的强度,
压缩应力、缓冲性、耐药性等与聚苯乙烯塑料相同,经焚烧后不污染环境,还可肥田。下列
说法不正确的是( )
A.聚乳酸使用后能被自然界中的微生物完全降解,最终生成二氧化碳和水,不污染环境
B.聚乳酸适用于吹塑、热塑等各种加工方法,加工方便,应用十分广泛
C.聚乳酸(PLA)是一种对环境友好的天然高分子聚酯材料
D.聚乳酸是以淀粉发酵(或化学合成)得到的,以乳酸为基本原料制备的一种聚酯材料
答案 C
解析 聚乳酸(PLA)经焚烧后不污染环境,是一种对环境友好的合成高分子聚酯材料,故C
错误。
1.(2021·山东,7)某同学进行蔗糖水解实验,并检验产物中的醛基,操作如下:向试管Ⅰ中
加入1 mL 20%蔗糖溶液,加入3滴稀硫酸,水浴加热5分钟。打开盛有10% NaOH溶液的
试剂瓶,将玻璃瓶塞倒放,取1 mL溶液加入试管Ⅱ,盖紧瓶塞;向试管Ⅱ中加入5滴2%
CuSO 溶液。将试管Ⅱ中反应液加入试管Ⅰ,用酒精灯加热试管Ⅰ并观察现象。实验中存在
4
的错误有几处( )
A.1 B.2 C.3 D.4
答案 B
解析 第1处错误:利用新制的氢氧化铜检验蔗糖水解生成的葡萄糖中的醛基时,溶液需保
持弱碱性,否则作水解催化剂的酸会与氢氧化铜反应,导致实验失败,题干实验过程中蔗糖
水解后溶液未冷却且未碱化;第2处错误:NaOH溶液具有强碱性,不能用玻璃瓶塞,否则
NaOH与玻璃塞中的SiO 反应生成具有黏性的NaSiO,会导致瓶盖无法打开。
2 2 3
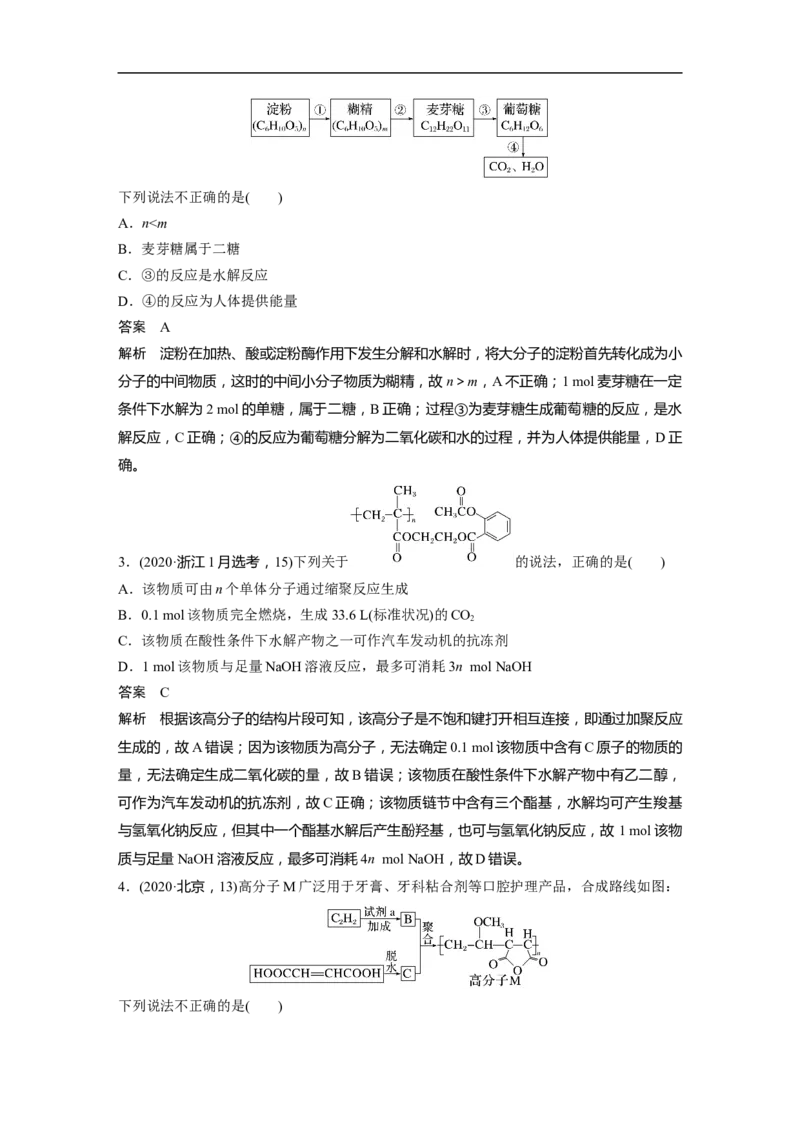
2.(2020·北京,8)淀粉在人体内的变化过程如图:下列说法不正确的是( )
A.n