文档内容
威海市 2015 年初中学业考试
化学试题(含答案全解全析)
可能用到的相对原子质量:H—1 O—16 S—32 Fe—56
一、选择(本题包括10小题,每小题2分,共20分。每小题只有一个选项符合题意。)
1.碳—12、碳—13、碳—14都是碳元素的原子,它们的主要差别在于( )
A.电子数目不同 B.中子数目不同 C.质子数目不同 D.化学性质不同
2.汤姆森和卢瑟福都对现代原子结构理论作出了巨大贡献。下列关于原子构成的论述中,不
属于他们两人共同观点的是( )
A.原子很小,但可以再分 B.原子是构成物质的基本粒子
C.原子中的电子带负电荷 D.原子由原子核和核外电子构成
3.远到恒星、行星,近到树木、花草,物质世界一刻不停地发生着变化。下列过程发生了化学变
化的是( )
①烘烤食物 ②钢铁生锈 ③擦燃一根火柴 ④干冰升华 ⑤瓷碗碎了 ⑥杜鹃开花 ⑦
沙子变成沙雕 ⑧化石燃料的形成
A.①②③⑥⑧ B.①②③④⑥⑧
C.④⑤⑦ D.①②③⑤⑥⑦⑧
4.一定温度下,一定质量的氢氧化钠固体溶于水制成溶液。下列有关的量不随水的质量改变
而改变的是( )
A.溶质质量分数 B.溶液的pH
C.氢氧化钠的溶解度 D.最多能吸收二氧化碳的质量
5.对构成物质的分子、原子和离子的认识,下列说法正确的是( )
A.构成分子的原子能保持该物质的化学性质
B.原子得失电子变成离子后,元素的种类发生了变化
C.两种原子的质量之比等于它们的相对原子质量之比
D.离子之间存在着相互作用,分子间没有相互作用
6.在①糖类 ②油脂 ③蛋白质 ④维生素 ⑤纤维素 ⑥无机盐 ⑦水 ⑧二氧化碳中,
属于人体必需营养素的有( )
A.①②③④⑥⑦ B.①②③⑥⑦
C.①②③④⑤⑥⑦ D.①②③④⑤⑥⑦⑧
7.当代社会几乎离不开化石燃料。关于人类使用化石燃料的“利”与“弊”,下列说法正确
的是( )
A.只有“利”而无“弊”。因为人类的生活和生产根本就离不开化石燃料,也离不开以化石
燃料为原料生产的塑料、橡胶、纤维、药物、化肥、农药等
B.只有“弊”而无“利”。因为化石燃料燃烧产生很多有害物质,导致气候变暖、酸雨、空气
中可吸入颗粒物含量急剧上升
C.“弊”大于“利”。虽然化石燃料为人类提供了能源和物质,但使用化石燃料带来了严重的
环境问题
D.“利”大于“弊”。虽然使用化石燃料带来了一定的环境问题,但化石燃料是当今社会重要的能源和物质资源,只要合理利用,可以趋利避害
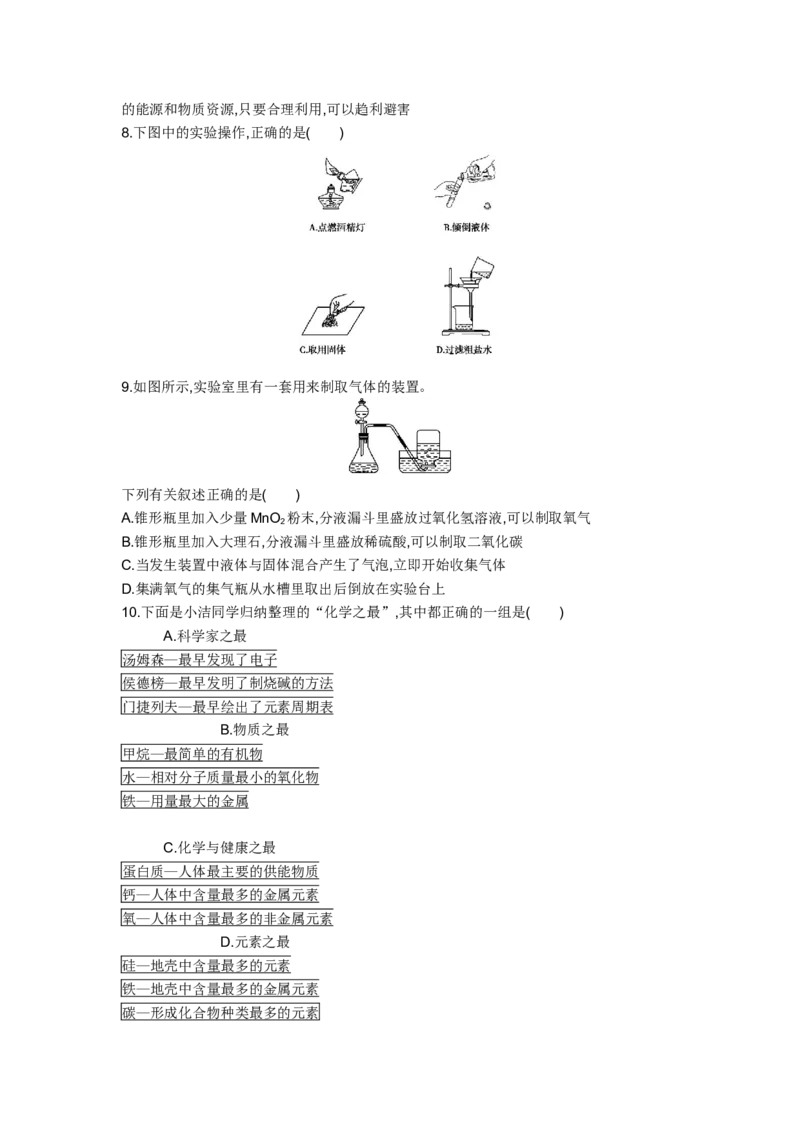
8.下图中的实验操作,正确的是( )
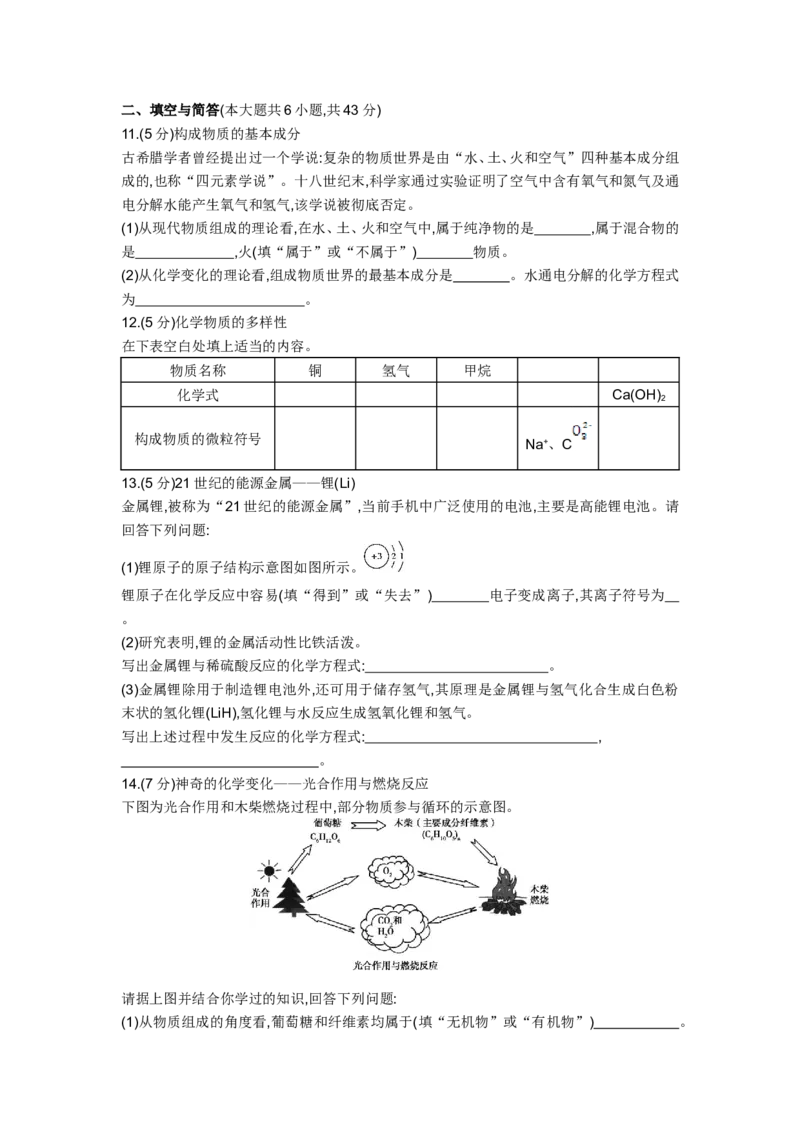
9.如图所示,实验室里有一套用来制取气体的装置。
下列有关叙述正确的是( )
A.锥形瓶里加入少量MnO 粉末,分液漏斗里盛放过氧化氢溶液,可以制取氧气
2
B.锥形瓶里加入大理石,分液漏斗里盛放稀硫酸,可以制取二氧化碳
C.当发生装置中液体与固体混合产生了气泡,立即开始收集气体
D.集满氧气的集气瓶从水槽里取出后倒放在实验台上
10.下面是小洁同学归纳整理的“化学之最”,其中都正确的一组是( )
A.科学家之最
汤姆森—最早发现了电子
侯德榜—最早发明了制烧碱的方法
门捷列夫—最早绘出了元素周期表
B.物质之最
甲烷—最简单的有机物
水—相对分子质量最小的氧化物
铁—用量最大的金属
C.化学与健康之最
蛋白质—人体最主要的供能物质
钙—人体中含量最多的金属元素
氧—人体中含量最多的非金属元素
D.元素之最
硅—地壳中含量最多的元素
铁—地壳中含量最多的金属元素
碳—形成化合物种类最多的元素二、填空与简答(本大题共6小题,共43分)
11.(5分)构成物质的基本成分
古希腊学者曾经提出过一个学说:复杂的物质世界是由“水、土、火和空气”四种基本成分组
成的,也称“四元素学说”。十八世纪末,科学家通过实验证明了空气中含有氧气和氮气及通
电分解水能产生氧气和氢气,该学说被彻底否定。
(1)从现代物质组成的理论看,在水、土、火和空气中,属于纯净物的是 ,属于混合物的
是 ,火(填“属于”或“不属于”) 物质。
(2)从化学变化的理论看,组成物质世界的最基本成分是 。水通电分解的化学方程式
为 。
12.(5分)化学物质的多样性
在下表空白处填上适当的内容。
物质名称 铜 氢气 甲烷
化学式 Ca(OH)
2
构成物质的微粒符号
Na+、C
13.(5分)21世纪的能源金属——锂(Li)
金属锂,被称为“21世纪的能源金属”,当前手机中广泛使用的电池,主要是高能锂电池。请
回答下列问题:
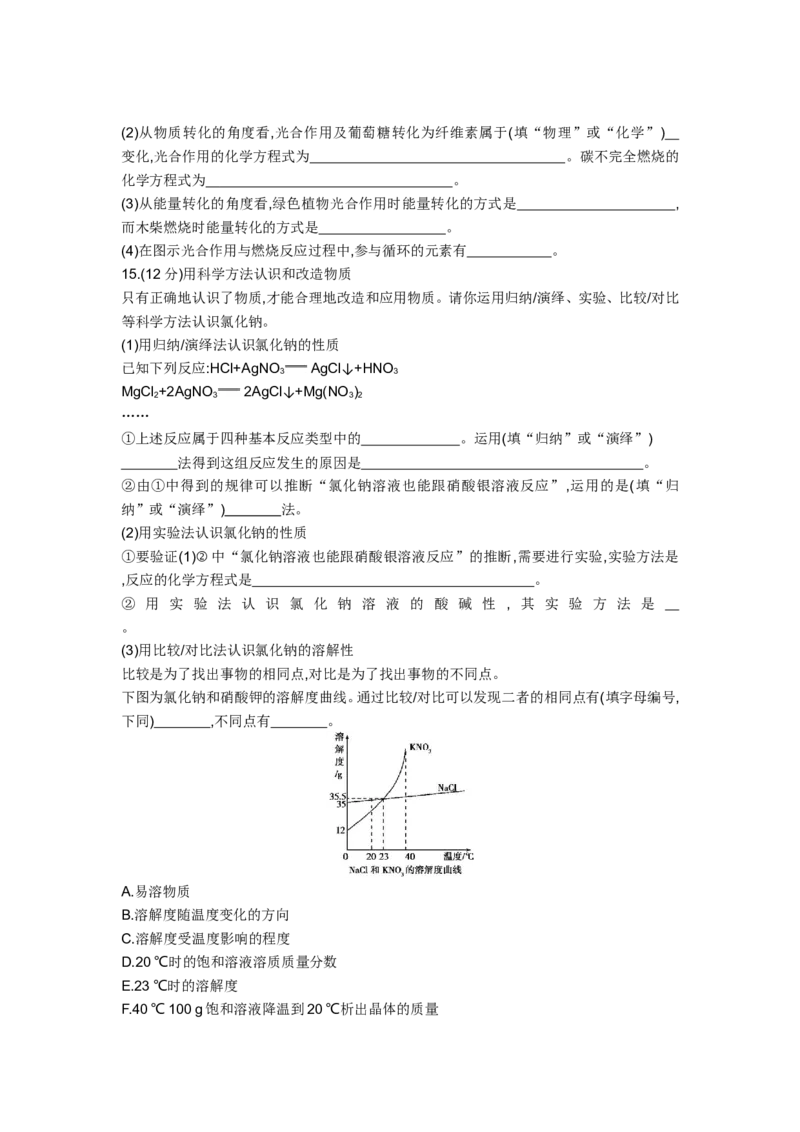
(1)锂原子的原子结构示意图如图所示。
锂原子在化学反应中容易(填“得到”或“失去”) 电子变成离子,其离子符号为
。
(2)研究表明,锂的金属活动性比铁活泼。
写出金属锂与稀硫酸反应的化学方程式: 。
(3)金属锂除用于制造锂电池外,还可用于储存氢气,其原理是金属锂与氢气化合生成白色粉
末状的氢化锂(LiH),氢化锂与水反应生成氢氧化锂和氢气。
写出上述过程中发生反应的化学方程式: ,
。
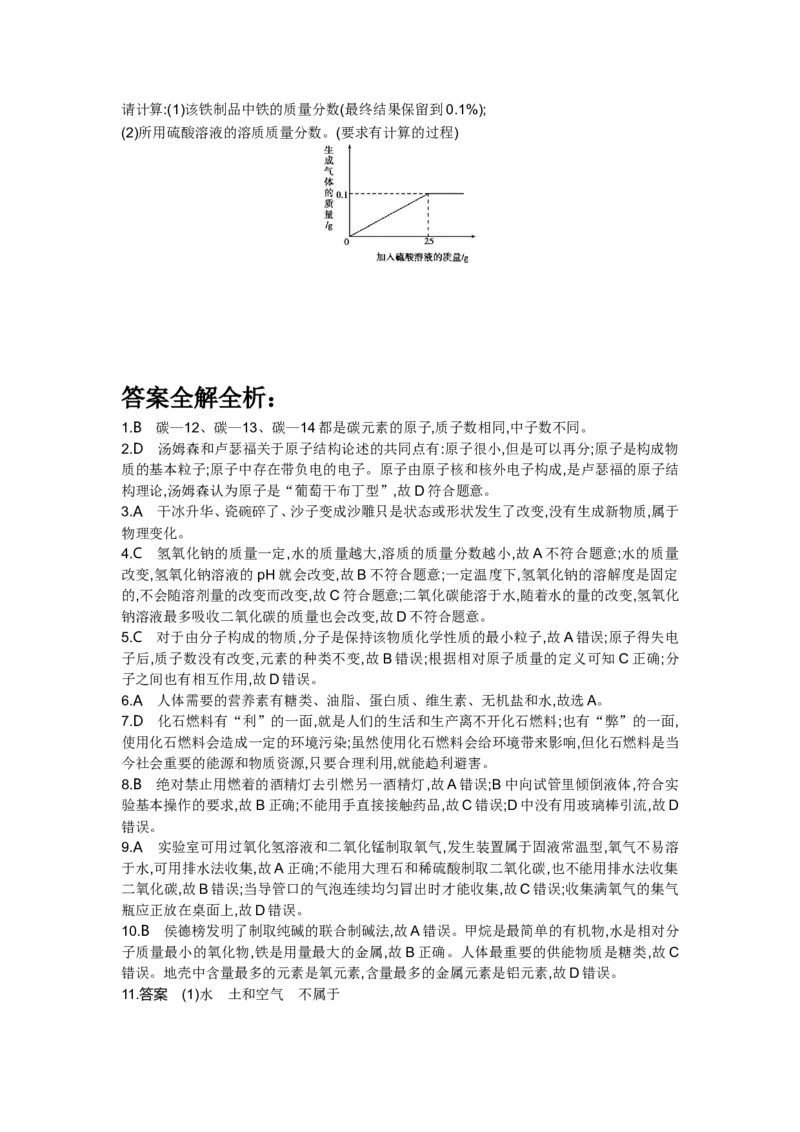
14.(7分)神奇的化学变化——光合作用与燃烧反应
下图为光合作用和木柴燃烧过程中,部分物质参与循环的示意图。
请据上图并结合你学过的知识,回答下列问题:
(1)从物质组成的角度看,葡萄糖和纤维素均属于(填“无机物”或“有机物”) 。(2)从物质转化的角度看,光合作用及葡萄糖转化为纤维素属于(填“物理”或“化学”)
变化,光合作用的化学方程式为 。碳不完全燃烧的
化学方程式为 。
(3)从能量转化的角度看,绿色植物光合作用时能量转化的方式是 ,
而木柴燃烧时能量转化的方式是 。
(4)在图示光合作用与燃烧反应过程中,参与循环的元素有 。
15.(12分)用科学方法认识和改造物质
只有正确地认识了物质,才能合理地改造和应用物质。请你运用归纳/演绎、实验、比较/对比
等科学方法认识氯化钠。
(1)用归纳/演绎法认识氯化钠的性质
已知下列反应:HCl+AgNO AgCl↓+HNO
3 3
MgCl +2AgNO 2AgCl↓+Mg(NO )
2 3 3 2
……
①上述反应属于四种基本反应类型中的 。运用(填“归纳”或“演绎”)
法得到这组反应发生的原因是 。
②由①中得到的规律可以推断“氯化钠溶液也能跟硝酸银溶液反应”,运用的是(填“归
纳”或“演绎”) 法。
(2)用实验法认识氯化钠的性质
①要验证(1)②中“氯化钠溶液也能跟硝酸银溶液反应”的推断,需要进行实验,实验方法是
,反应的化学方程式是 。
② 用 实 验 法 认 识 氯 化 钠 溶 液 的 酸 碱 性 , 其 实 验 方 法 是
。
(3)用比较/对比法认识氯化钠的溶解性
比较是为了找出事物的相同点,对比是为了找出事物的不同点。
下图为氯化钠和硝酸钾的溶解度曲线。通过比较/对比可以发现二者的相同点有(填字母编号,
下同) ,不同点有 。
A.易溶物质
B.溶解度随温度变化的方向
C.溶解度受温度影响的程度
D.20 ℃时的饱和溶液溶质质量分数
E.23 ℃时的溶解度
F.40 ℃ 100 g饱和溶液降温到20 ℃析出晶体的质量(4)用两种重要的实验法——“蒸馏法和结晶法”改造物质
从古希腊炼金士到今天的化学工作者,都用到了两种重要的实验法——蒸馏法和结晶法。证
明氯化钠溶于水没有新物质生成,可采用蒸馏法和结晶法中的 。在生活生产中通过
蒸馏法获得物质的一个事例是 ,通过结晶法获得物质的一个事例是 。
16.(9分)铁生锈探秘
为探究铁生锈的原因,化学兴趣小组的同学进行了下图所示的四个实验。实验结果显示,B、D
实验中铁生了锈,而A、C实验中没有明显的现象。仔细分析这4个实验,回答下列问题:
(1)评价方案
对照实验指除了一个变量以外,其他的量都保持不变的实验。该实验方案中采用了对照实验
的方法。请指出其中的对照实验(填ABCD实验代号)和变量。
第①组对照实验 ,变量 。
第②组对照实验 ,变量 。
第③组对照实验 ,变量 。
(2)解释数据
实验时,每隔一段时间测量导管内水面上升的高度,结果如下表所示(表中所列数据为导管中
水面上升的高度/cm)。
时间/小时
0 0.5 1.0 1.5 2.0 2.5 3.0
编号
A 0 0 0 0 0 0 0
B 0 0 0 0.3 0.8 2.0 3.5
C 0 0 0 0 0 0 0
D 0 0.4 1.2 3.4 5.6 7.6 9.8
导致B、D实验装置中导管内水面上升的原因是
。
(3)获得结论
根据本实验,你认为导致铁生锈的物质有 ;能加快铁生锈的物质是
。
三、计算
17.(7分)测定铁制品中铁的质量分数
铁是常用的金属材料。兴趣小组的同学对某铁制品中铁的质量分数进行了测定。
称取3 g铁屑,缓慢加入一定溶质质量分数的硫酸溶液,直到过量(假设除铁以外的物质都不
与硫酸反应),实验数据如图所示。请计算:(1)该铁制品中铁的质量分数(最终结果保留到0.1%);
(2)所用硫酸溶液的溶质质量分数。(要求有计算的过程)
答案全解全析:
1.B 碳—12、碳—13、碳—14都是碳元素的原子,质子数相同,中子数不同。
2.D 汤姆森和卢瑟福关于原子结构论述的共同点有:原子很小,但是可以再分;原子是构成物
质的基本粒子;原子中存在带负电的电子。原子由原子核和核外电子构成,是卢瑟福的原子结
构理论,汤姆森认为原子是“葡萄干布丁型”,故D符合题意。
3.A 干冰升华、瓷碗碎了、沙子变成沙雕只是状态或形状发生了改变,没有生成新物质,属于
物理变化。
4.C 氢氧化钠的质量一定,水的质量越大,溶质的质量分数越小,故A不符合题意;水的质量
改变,氢氧化钠溶液的pH就会改变,故B不符合题意;一定温度下,氢氧化钠的溶解度是固定
的,不会随溶剂量的改变而改变,故C符合题意;二氧化碳能溶于水,随着水的量的改变,氢氧化
钠溶液最多吸收二氧化碳的质量也会改变,故D不符合题意。
5.C 对于由分子构成的物质,分子是保持该物质化学性质的最小粒子,故A错误;原子得失电
子后,质子数没有改变,元素的种类不变,故B错误;根据相对原子质量的定义可知C正确;分
子之间也有相互作用,故D错误。
6.A 人体需要的营养素有糖类、油脂、蛋白质、维生素、无机盐和水,故选A。
7.D 化石燃料有“利”的一面,就是人们的生活和生产离不开化石燃料;也有“弊”的一面,
使用化石燃料会造成一定的环境污染;虽然使用化石燃料会给环境带来影响,但化石燃料是当
今社会重要的能源和物质资源,只要合理利用,就能趋利避害。
8.B 绝对禁止用燃着的酒精灯去引燃另一酒精灯,故A错误;B中向试管里倾倒液体,符合实
验基本操作的要求,故B正确;不能用手直接接触药品,故C错误;D中没有用玻璃棒引流,故D
错误。
9.A 实验室可用过氧化氢溶液和二氧化锰制取氧气,发生装置属于固液常温型,氧气不易溶
于水,可用排水法收集,故A正确;不能用大理石和稀硫酸制取二氧化碳,也不能用排水法收集
二氧化碳,故B错误;当导管口的气泡连续均匀冒出时才能收集,故C错误;收集满氧气的集气
瓶应正放在桌面上,故D错误。
10.B 侯德榜发明了制取纯碱的联合制碱法,故A错误。甲烷是最简单的有机物,水是相对分
子质量最小的氧化物,铁是用量最大的金属,故B正确。人体最重要的供能物质是糖类,故C
错误。地壳中含量最多的元素是氧元素,含量最多的金属元素是铝元素,故D错误。
11.答案 (1)水 土和空气 不属于(2)元素(或原子) 2H O O ↑+2H ↑
2 2 2
解析 (1)在水、土、火和空气中,属于纯净物的是水,属于混合物的是土和空气,火不属于物质。
(2)元素(或原子)是组成物质世界的最基本成分;水通电分解为氢气和氧气,化学方程式为
2H O 2H ↑+O ↑。
2 2 2
12.答案 (5分,每空0.5分)
物质名称 碳酸钠 氢氧化钙
化学式 Cu H CH NaCO
2 4 2 3
构成物质的微粒符号 Cu H
2
CH
4
Ca2+、OH-
解析 铜的化学式为Cu,构成铜的微粒是铜原子;氢气的化学式为H ,构成氢气的微粒是氢分
2
子;甲烷的化学式为CH ,构成甲烷的微粒是甲烷分子;Na+和C 构成的物质是碳酸钠,化学
4
式为Na CO ;Ca(OH) 的名称为氢氧化钙,其构成微粒是Ca2+和OH-。
2 3 2
评析 本题主要考查化学式的书写和构成物质的微粒符号,难度不大,属于基础题。
13.答案 (5分,每空1分)(1)失去 Li+
(2)2Li+H SO Li SO +H ↑
2 4 2 4 2
(3)2Li+H 2LiH LiH+H O LiOH+H ↑
2 2 2
解析 (1)锂原子的最外层有1个电子,容易失去电子变成离子,锂离子的符号为Li+。
(2)锂和稀硫酸反应生成硫酸锂和氢气,化学方程式为2Li+H SO Li SO +H ↑。
2 4 2 4 2
(3)根据化学方程式的书写规则,写出化学方程式:2Li+H 2LiH、LiH+H O LiOH+H ↑。
2 2 2
14.答案 (7分,每空1分)(1)有机物
(2)化学 6CO +6H O C H O +6O
2 2 6 12 6 2
2C+O 2CO
2
(3)光能转化成化学能(或内能) 化学能(或内能)转化成热能(光能)
(4)C、H、O(或碳、氢、氧)(少答1种得0.5分,只答一种或多答、错答不得分)
解析 (1)葡萄糖和纤维素都含有碳元素,都属于有机物。
(2)光合作用及葡萄糖转化为纤维素,都有新物质生成,都属于化学变化;光合作用的化学方程
式为6CO +6H O C H O +6O 。碳不完全燃烧的化学方程式为2C+O 2CO。(3)光
2 2 6 12 6 2 2
合作用时光能转化为化学能(或内能);木柴燃烧时化学能(或内能)转化为热能(光能)。(4)光合
作用和燃烧反应过程中都涉及C、H、O三种元素。
15.答案 (12分,每空1分)(1)①复分解反应 归纳 氯离子和银离子结合生成难溶于水的
氯化银(或两种化合物相互交换成分,生成难溶于水的物质) ②演绎
(2)①向氯化钠溶液中滴加硝酸银溶液,观察现象
NaCl+AgNO AgCl↓+NaNO
3 3
②向氯化钠溶液中滴加紫色石蕊试液,观察现象(或:用玻璃棒蘸取氯化钠溶液滴在pH试纸
上,将试纸显示的颜色与标准比色卡对照,读出溶液的pH)
(3)ABE CDF
(4)结晶法 制蒸馏水(或分离液态空气或石油分馏) 海水晒盐
解析 (1)①两个反应都是两种化合物相互交换成分,生成另外两种化合物,属于复分解反应;通过归纳法发现,这两个反应之所以发生,都是因为氯离子和银离子结合生成难溶于水的氯化
银。②运用①中的规律,推断出氯化钠溶液能和硝酸银溶液反应,同样有氯化银沉淀生成,运用
的是演绎法。
(2)①要验证氯化钠溶液能和硝酸银溶液反应,只需向氯化钠溶液中滴加硝酸银溶液,观察是
否有白色沉淀生成即可;反应的化学方程式为AgNO +NaCl AgCl↓+NaNO 。②要认识氯
3 3
化钠溶液的酸碱性,可以向氯化钠溶液中滴加紫色石蕊试液,观察颜色变化情况;或用玻璃棒
蘸取氯化钠溶液,滴在pH试纸上,然后与标准比色卡比较,读出氯化钠溶液的pH。
(3)20 ℃时氯化钠和硝酸钾的溶解度都大于10 g,故两者都属于易溶物质,故A是相同点;二者
的溶解度都随温度升高而增大,故B是相同点;硝酸钾的溶解度受温度影响较大,而氯化钠的
溶解度受温度影响较小,故C是不同点;20 ℃时氯化钠和硝酸钾的溶解度不同,所以该温度下
饱和溶液的溶质质量分数不同,故D是不同点;23 ℃时氯化钠和硝酸钾的溶解度都是35.5 g,
故E是相同点;40 ℃时100 g饱和溶液降温到20 ℃,因为氯化钠的溶解度受温度影响小,硝
酸钾的溶解度受温度影响大,所以析出晶体的质量不同,故F是不同点。
(4)证明氯化钠溶于水没有生成新物质,可以用结晶法,把氯化钠溶液中的水蒸发掉,得到氯化
钠晶体;通过蒸馏法得到物质的事例有制取蒸馏水、分离液态空气制取氧气、石油分馏等;通
过结晶法得到物质的事例有海水晒盐等。
评析 本题主要考查的是研究化学的方法,归纳/演绎法、比较/对比法,有新意,注重对获取信
息、知识的灵活运用能力的考查。
16.答案 (9分,每空1分)
(1)①AB 水(或H O) ②BC 空气(或氧气或O ) ③BD 食盐(或氯化钠或NaCl)(本题
2 2
答案为AD,食盐水,也可)
(2)铁生锈消耗了氧气,使锥形瓶内气体压强小于瓶外的大气压
(3)水和氧气(或空气)(同时存在) 食盐(或氯化钠或NaCl)
解析 (1)A、B两个实验中的变量只有水(一个与水接触,一个没有与水接触);B、C两个实验
中的变量只有氧气(空气)(一个与空气接触,一个没有与空气接触);B、D两个实验中的变量只
有氯化钠(一个与氯化钠接触,一个没有与氯化钠接触);A、D两个实验中的变量只有食盐水
(一个与食盐水接触,一个没有与食盐水接触)。
(2)B、D实验装置内铁生锈消耗了氧气,使锥形瓶内的压强小于外界大气压,导致导管内水面
上升。
(3)通过实验A、B、C证明铁与水、氧气接触会生锈,通过实验B、D证明有食盐存在的情况下
铁生锈更快。
评析 本题主要考查的是探究实验中的对比实验法。只要知道对比实验的特点(除一个量不
同外,其余条件完全相同),就不难解答。
17.答案 (7分)由题图知,反应中生成氢气的质量为0.1 g,恰好完全反应时消耗硫酸溶液的
质量为25 g。
设3 g铁屑中含铁的质量为x,参加反应的硫酸的质量为y。
Fe+H SO FeSO +H ↑(1分)
2 4 4 2
56 98 2
x y 0.1 g
= (1分)x= =2.8 g(1分)
则铁制品中含铁的质量分数= ×100%≈93.3%。(1分)
= (1分)
y= =4.9 g(1分)
则硫酸溶液的溶质质量分数= ×100%=19.6%。(1分)
答:该铁制品中铁的质量分数约为93.3%,所用硫酸溶液的溶质质量分数为19.6%。
说明:(1)本题若根据质量守恒定律列出综合算式或用其他计算方法,只要合理,可参考上述评
分标准酌情给分。
(2)化学方程式书写错误,本题不给分。但化学方程式书写正确而因相对分子质量计算有误,其
他计算正确,只扣1分。
解析 从题中图像看出,铁与稀硫酸反应生成氢气的质量为0.1 g,根据化学方程式计算求出
铁的质量和反应的硫酸的质量,进一步求出最终答案。
评析 本题是一道典型的图像式计算题。主要考查分析图像得到数据和根据化学方程式进
行计算的能力。