文档内容
绝密★启用前
2024 年中考押题预测卷 01【广东卷】
化 学
(考试时间:60分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必用黑色字迹的签字笔或钢笔在答题卡上填写自己的准考证号、姓名、班级、试
室号、座位号。
2.选择题每小题选出答案后,用2B铅笔把答题卡上对应题目选项的答案信息点涂黑,如需改动,用
橡皮擦干净后,再选涂其它答案,答案不能答在试卷上。
3.非选择题必须用黑色字迹钢笔或签字笔作答,答案必须写在答题卡各题目指定区域内相应位置
上;如需改动,先划掉原来的答案,然后再写上新的答案;不准使用铅笔和涂改液,不按以上要求作答的
答案无效。
4.考生务必保持答题卡的整洁。考试结束时,将答题卡交回。
5.可能用到的相对原子质量:H 1 C 12 O 16 Na 23 Cl 35.5 Ca 40 Fe 56
一、选择题:本大题共 15小题,每小题3分,共45分。在每小题列出的四个选项中,只有
一个是符合题目要求的。
1.物质世界是在不断变化的。下列过程中,属于化学变化的是
A.浇水成冰 B.火箭发射 C.纸剪窗花 D.风力发电
2.低碳生活,从点滴做起。下列行为不符合“低碳”理念的是
A.购物自备购物袋 B.按需取餐不浪费 C.少用一次性木筷 D.教室人空未关灯
3.下列材料中,属于复合材料的是
A.钢 B.玻璃 C.玻璃钢 D.有机玻璃
4.中国丝绸历史悠久,古代染坊常用一种“碱剂”处理丝绸,可使丝绸质感柔软。“碱剂”的主要成分
是一种盐,这种盐是
A.纯碱 B.生石灰 C.酒精 D.苛性钠
5.在配制稀硫酸并制备氢气的实验中,下列装置和实验操作正确并规范的是
A.量取浓硫酸 B.稀释浓硫酸 C.制取氢气 D.干燥氢气
6.“平衡膳食要会看标签”,某品牌纯牛奶标签如下表所示,下列说法正确的是
规格:250 mL/盒项目 每100
mL
能量 277 kJ
蛋白质 3.2 g
脂肪 3.8 g
碳水化合物 4.8 g
钠 53 mg
钙 100 mg
A.该牛奶中的“钠”指的是钠单质 B.该牛奶中的“钙”可预防大脖子病
C.仅饮用该牛奶可满足均衡营养的需要 D.饮用1盒该牛奶可补充蛋白质8 g
7.一种有趣的钟表式元素周期表如题7图所示。下列关于元素说法中正确的是
A.5∶00对应元素的质子数是5
B.2∶00时针对应的元素属于金属元素
C.9∶00对应元素的离子符号为F+
D.10∶00对应的元素易与其他元素形成化合物
8.下列跨学科实践活动中,涉及的知识解释错误的是
选项 实践活动 知识解释
A 用双氧水自制简易供氧器 双氧水中含有氧气
B 调查家用燃料的使用 天然气的主要成分为甲烷
查阅科学家探索物质组成与结构的历
C 原子不是最小粒子
程
D 用醋在鸡蛋壳表面刻画字样 蛋壳成分能与醋酸发生化学反应
9.端午节是中华民族重要的传统节日,民间有插艾草的习俗。艾草中含有丰富的黄酮类物质,其中矢车
菊黄素的化学式为C H O。下列关于矢车菊黄素的说法不正确的是
18 16 8
A.由碳、氢、氧三种元素组成 B.相对分子质量为360 g
C.碳元素的质量分数最大 D.1个分子中含有42个原子
10.学生承担家务是劳动教育的方式之一。下列家务劳动的过程中,利用降低温度到着火点以下来灭火的
原理的是
A.用水浇灭家庭聚会的篝火 B.旋转燃气炉开关熄灭炉火
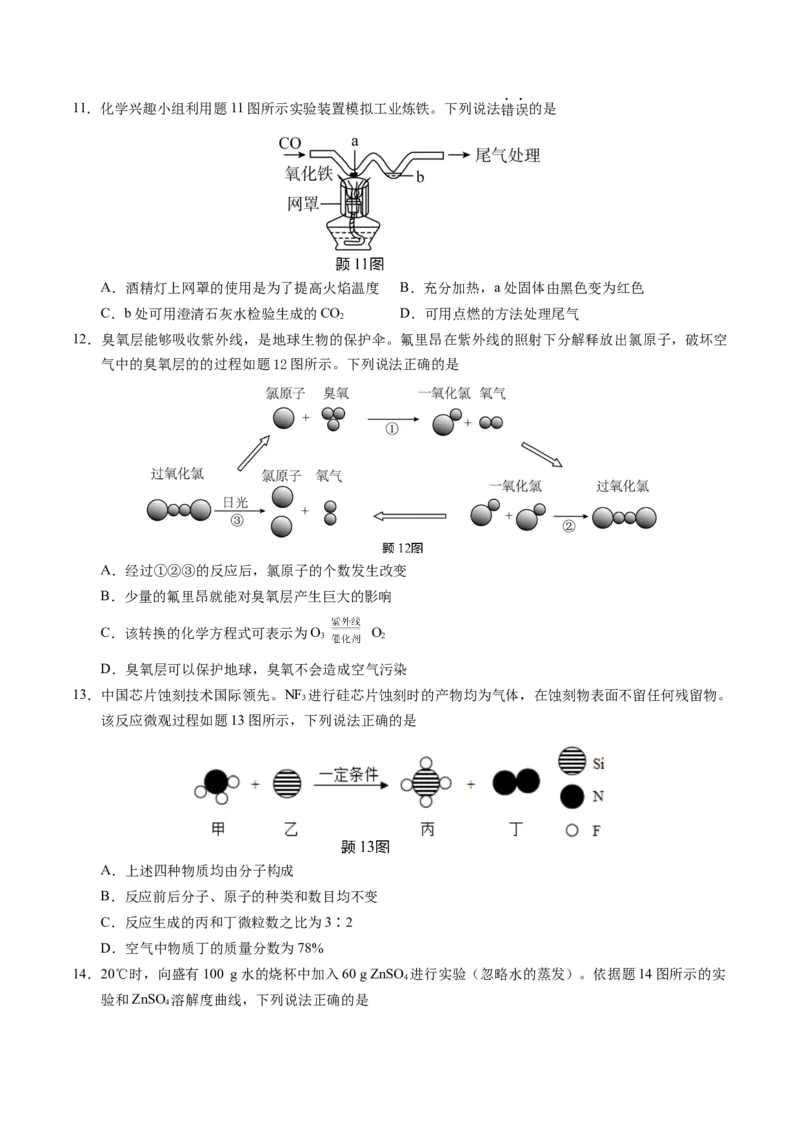
C.盖上锅盖熄灭锅中的油火 D.移除炉灶内木柴熄灭灶火11.化学兴趣小组利用题11图所示实验装置模拟工业炼铁。下列说法错误的是
A.酒精灯上网罩的使用是为了提高火焰温度 B.充分加热,a处固体由黑色变为红色
C.b处可用澄清石灰水检验生成的CO D.可用点燃的方法处理尾气
2
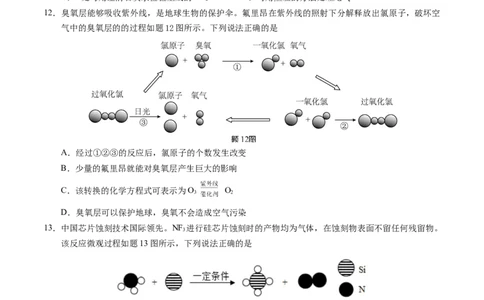
12.臭氧层能够吸收紫外线,是地球生物的保护伞。氟里昂在紫外线的照射下分解释放出氯原子,破坏空
气中的臭氧层的的过程如题12图所示。下列说法正确的是
A.经过①②③的反应后,氯原子的个数发生改变
B.少量的氟里昂就能对臭氧层产生巨大的影响
C.该转换的化学方程式可表示为O O
3 2
D.臭氧层可以保护地球,臭氧不会造成空气污染
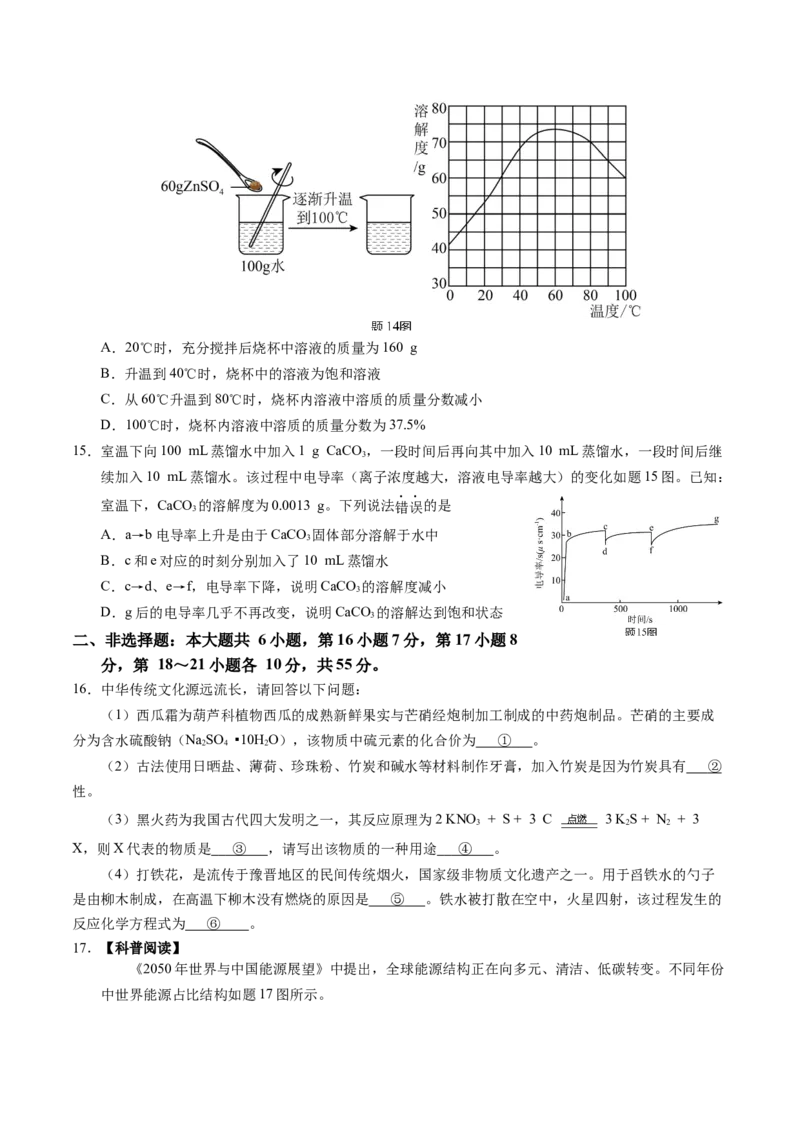
13.中国芯片蚀刻技术国际领先。NF 进行硅芯片蚀刻时的产物均为气体,在蚀刻物表面不留任何残留物。
3
该反应微观过程如题13图所示,下列说法正确的是
A.上述四种物质均由分子构成
B.反应前后分子、原子的种类和数目均不变
C.反应生成的丙和丁微粒数之比为3∶2
D.空气中物质丁的质量分数为78%
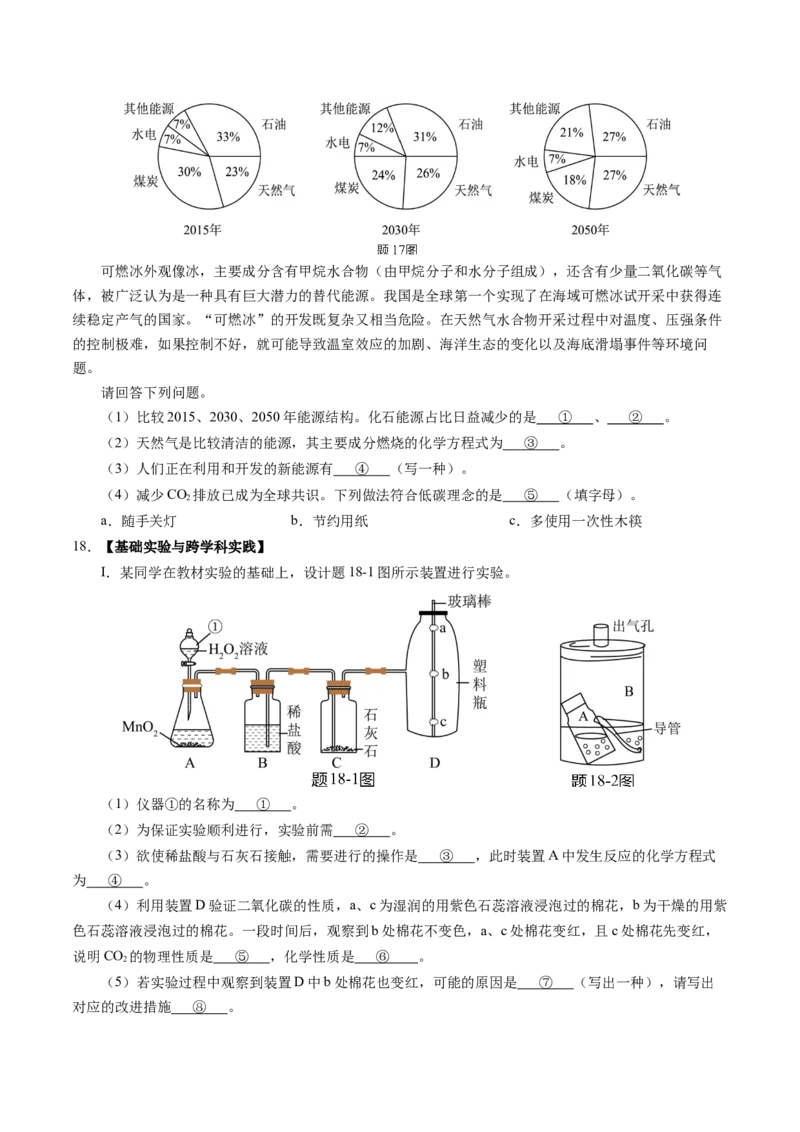
14.20℃时,向盛有100 g水的烧杯中加入60 g ZnSO 进行实验(忽略水的蒸发)。依据题14图所示的实
4
验和ZnSO 溶解度曲线,下列说法正确的是
4A.20℃时,充分搅拌后烧杯中溶液的质量为160 g
B.升温到40℃时,烧杯中的溶液为饱和溶液
C.从60℃升温到80℃时,烧杯内溶液中溶质的质量分数减小
D.100℃时,烧杯内溶液中溶质的质量分数为37.5%
15.室温下向100 mL蒸馏水中加入1 g CaCO ,一段时间后再向其中加入10 mL蒸馏水,一段时间后继
3
续加入10 mL蒸馏水。该过程中电导率(离子浓度越大,溶液电导率越大)的变化如题15图。已知:
室温下,CaCO 的溶解度为0.0013 g。下列说法错误的是
3
A.a→b电导率上升是由于CaCO 固体部分溶解于水中
3
B.c和e对应的时刻分别加入了10 mL蒸馏水
C.c→d、e→f,电导率下降,说明CaCO 的溶解度减小
3
D.g后的电导率几乎不再改变,说明CaCO 的溶解达到饱和状态
3
二、非选择题:本大题共 6小题,第16小题7分,第17小题8
分,第 18~21小题各 10分,共55分。
16.中华传统文化源远流长,请回答以下问题:
(1)西瓜霜为葫芦科植物西瓜的成熟新鲜果实与芒硝经炮制加工制成的中药炮制品。芒硝的主要成
分为含水硫酸钠(NaSO ▪10H O),该物质中硫元素的化合价为 ① 。
2 4 2
(2)古法使用日晒盐、薄荷、珍珠粉、竹炭和碱水等材料制作牙膏,加入竹炭是因为竹炭具有 ②
性。
(3)黑火药为我国古代四大发明之一,其反应原理为2 KNO + S + 3 C 3 K S + N + 3
3 2 2
X,则X代表的物质是 ③ ,请写出该物质的一种用途 ④ 。
(4)打铁花,是流传于豫晋地区的民间传统烟火,国家级非物质文化遗产之一。用于舀铁水的勺子
是由柳木制成,在高温下柳木没有燃烧的原因是 ⑤ 。铁水被打散在空中,火星四射,该过程发生的
反应化学方程式为 ⑥ 。
17.【科普阅读】
《2050年世界与中国能源展望》中提出,全球能源结构正在向多元、清洁、低碳转变。不同年份
中世界能源占比结构如题17图所示。可燃冰外观像冰,主要成分含有甲烷水合物(由甲烷分子和水分子组成),还含有少量二氧化碳等气
体,被广泛认为是一种具有巨大潜力的替代能源。我国是全球第一个实现了在海域可燃冰试开采中获得连
续稳定产气的国家。“可燃冰”的开发既复杂又相当危险。在天然气水合物开采过程中对温度、压强条件
的控制极难,如果控制不好,就可能导致温室效应的加剧、海洋生态的变化以及海底滑塌事件等环境问
题。
请回答下列问题。
(1)比较2015、2030、2050年能源结构。化石能源占比日益减少的是 ① 、 ② 。
(2)天然气是比较清洁的能源,其主要成分燃烧的化学方程式为 ③ 。
(3)人们正在利用和开发的新能源有 ④ (写一种)。
(4)减少CO 排放已成为全球共识。下列做法符合低碳理念的是 ⑤ (填字母)。
2
a.随手关灯 b.节约用纸 c.多使用一次性木筷
18.【基础实验与跨学科实践】
Ⅰ.某同学在教材实验的基础上,设计题18-1图所示装置进行实验。
(1)仪器①的名称为 ① 。
(2)为保证实验顺利进行,实验前需 ② 。
(3)欲使稀盐酸与石灰石接触,需要进行的操作是 ③ ,此时装置A中发生反应的化学方程式
为 ④ 。
(4)利用装置D验证二氧化碳的性质,a、c为湿润的用紫色石蕊溶液浸泡过的棉花,b为干燥的用紫
色石蕊溶液浸泡过的棉花。一段时间后,观察到b处棉花不变色,a、c处棉花变红,且c处棉花先变红,
说明CO 的物理性质是 ⑤ ,化学性质是 ⑥ 。
2
(5)若实验过程中观察到装置D中b处棉花也变红,可能的原因是 ⑦ (写出一种),请写出
对应的改进措施 ⑧ 。ⅠI.题18-2图是一台简易制氧机,A瓶中装有“茶垢净”(遇到热水后会产生氧气)、二氧化锰和
水,氧气可从B瓶盖子上 的出气孔排出,供人呼吸。A瓶的导管伸入B瓶水中的目的是 ⑨ 。
19.【科学探究】
生态富民是我国实现高质量发展的重要路径。近年来,我国一些地区创新采用了“渔光互补”发
展模式,化学实践小组的同学们对渔光互补的工作模式、鱼塘水的成分等产生了浓厚的兴趣,他们在
老师的指导下展开了项目式学习活动。
任务一:了解渔光互补模式
【信息检索】同学们上网查阅资料,了解到“渔光互补”是在水面上方架设光伏板发电,下方的水域
则用于水产养殖,形成“上可发电,下可养鱼”的发展模式。
【分析交流】
(1)光伏发电过程中能量的转化为 ① 。
任务二:检测分析鱼塘水质
【听取介绍】同学们来到“XX渔光互补示范园”参观,据专家介绍,水产养殖过程中需保证合适的
水温、溶氧量和酸碱度。
【检测水质】
(2)同学们用pH试纸对鱼塘水的酸碱度进行了检测,具体操作是 ② 。
【小组讨论】
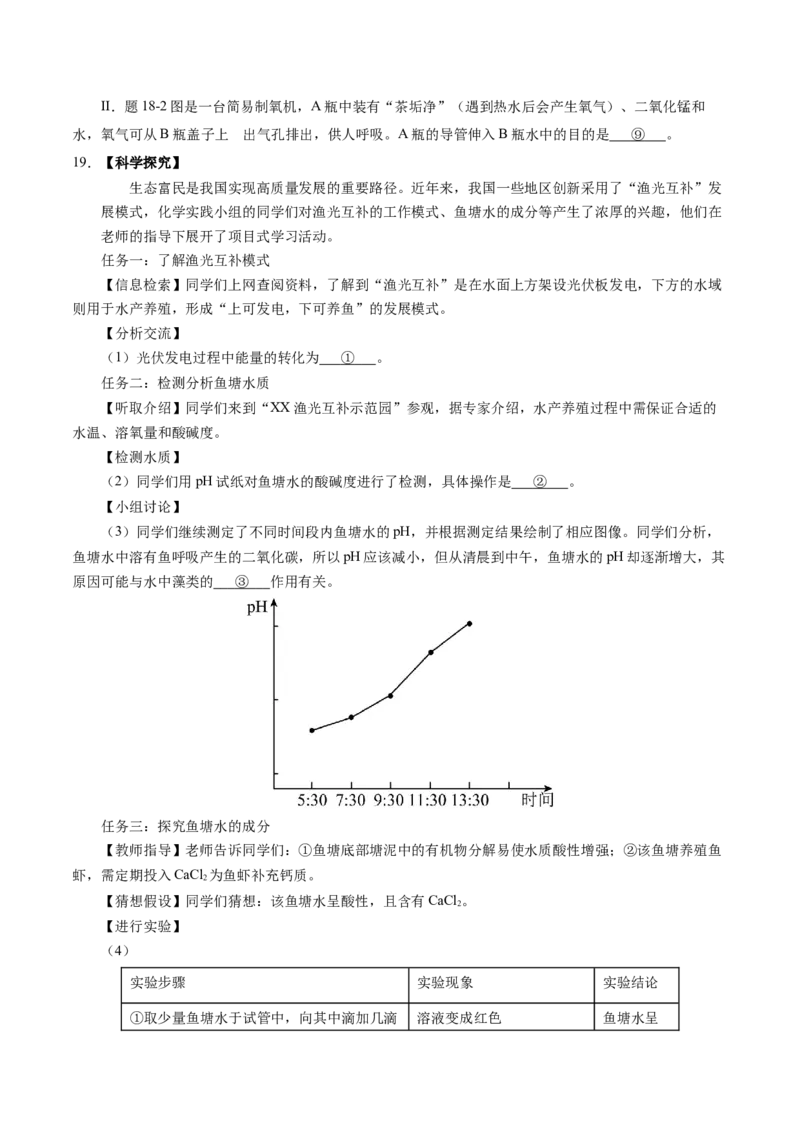
(3)同学们继续测定了不同时间段内鱼塘水的pH,并根据测定结果绘制了相应图像。同学们分析,
鱼塘水中溶有鱼呼吸产生的二氧化碳,所以pH应该减小,但从清晨到中午,鱼塘水的pH却逐渐增大,其
原因可能与水中藻类的 ③ 作用有关。
任务三:探究鱼塘水的成分
【教师指导】老师告诉同学们:①鱼塘底部塘泥中的有机物分解易使水质酸性增强;②该鱼塘养殖鱼
虾,需定期投入CaCl 为鱼虾补充钙质。
2
【猜想假设】同学们猜想:该鱼塘水呈酸性,且含有CaCl 。
2
【进行实验】
(4)
实验步骤 实验现象 实验结论
①取少量鱼塘水于试管中,向其中滴加几滴 溶液变成红色 鱼塘水呈④ 。 酸性
②另取少量鱼塘水于试管中,向其中滴加足 ⑤ ,一段时间后产生 且含有
量NaCO 溶液。 白色沉淀 CaCl
2 3 2
【反思评价】
(5)步骤②中产生白色沉淀所发生反应的化学方程式为 ⑥ 。
(6)有同学对实验结论提出了质疑,理由是 ⑦ ,同学们改进方案后重新进行实验,得出了正
确的结论。
任务四:展示项目研究成果
【成果分享】
(7)同学们通过实践活动,了解到“渔光互补”是一项具有发展潜力的高效生产模式,他们设计了
板报进行宣传,请你与他们共同完成板报内容 ⑧ 。
20.某化工厂以废金属(主要成分为Fe和Cu,表面有少量油污)为原料回收海绵铜,并制备氯化铁的工
艺流程如题20图所示。
已知:NaNO 易溶于水且不与氢氧化钠反应,在“氧化”中起催化作用,该反应的化学方程式为:4
2
FeCl + 4 HCl + O 4 FeCl + 2 HO。
2 2 3 2
回答下列问题:
(1)废金属回收利用是保护金属资源的有效途径之一,它有利于 ① 。
(2)“洗涤”的目的是去除废金属表面的油污,试剂X最好选用 ② (填标号)。
a.水 b.氢氧化钠溶液 c.稀硫酸
(3)“酸浸”中发生反应的化学方程式为 ③ 。
(4)在“氧化”过程中,反应前后化合价发生变化的元素有 ④ (写元素符号)。
(5)向“滤渣乙”中加入适量盐酸,发生的化学反应方程式为 ⑤ 。最后得到的溶液为 ⑥
色。
(6)现有100 t含铁为28%的废金属,利用上述流程制备FeCl 溶液,若过程中铁元素无损失,最后
3得到的FeCl 溶液中FeCl 的质量为 ⑦ t。
3 3
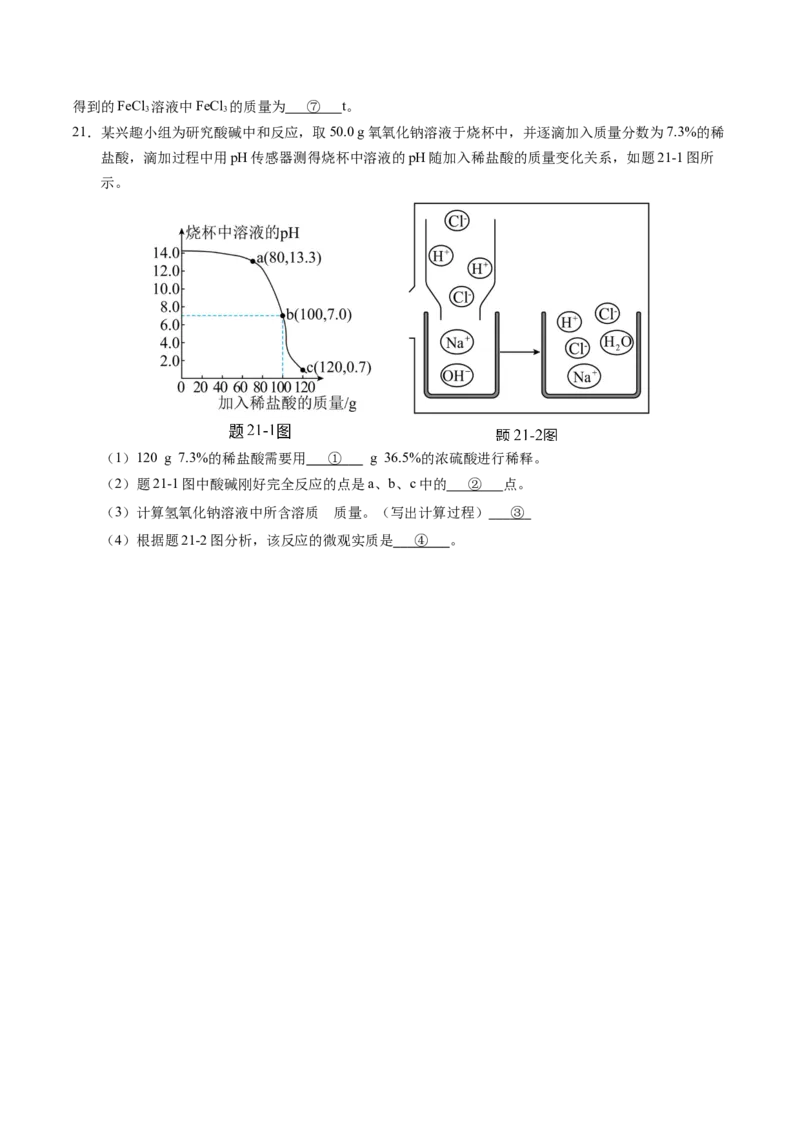
21.某兴趣小组为研究酸碱中和反应,取50.0 g氧氧化钠溶液于烧杯中,并逐滴加入质量分数为7.3%的稀
盐酸,滴加过程中用pH传感器测得烧杯中溶液的pH随加入稀盐酸的质量变化关系,如题21-1图所
示。
(1)120 g 7.3%的稀盐酸需要用 ① g 36.5%的浓硫酸进行稀释。
(2)题21-1图中酸碱刚好完全反应的点是a、b、c中的 ② 点。
(3)计算氢氧化钠溶液中所含溶质 的质量。(写出计算过程) ③
(4)根据题21-2图分析,该反应的微观实质是 ④ 。