文档内容
绝密★启用前 C. 活性炭可以吸附水中色素和异味 D. 溶液都是均一、稳定的
2024 年中考押题预测卷 01【苏州卷】 7.硒被医药界和营养学界尊称为“生命的火种”,享有“长寿元素”、“抗癌之王”、“心脏守护神”、
“天然解毒剂”等美誉。如图,甲是硒的原子结构示意图,乙是硒元素在元素周期表中的信息。下列相
化 学 关说法中,不合理的是
(考试时间:90分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,
用橡皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.考试结束后,将本试卷和答题卡一并交回。 A.硒原子的原子核内有34个质子
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Si-28 S-32 Cl-35.5 Cu-64 Br-80 B.硒原子在化学反应中易失去电子
C.硒原子的相对原子质量为78.96
一、选择题(本题20小题,每小题只有一个选项符合题意。每小题2分,共40分) D.硒元素是一种非金属元素
1.2024年世界环境日中国主题“全面推进美丽中国建设”。下列做法不符合该主题的是 8.下列说法正确的是
A.煤炭脱硫处理 B.积极植树造林 A.内壁沾有碘的试管可用酒精清洗
C.滥用化石燃料 D.垃圾分类投放 B.亚硝酸钠(NaNO )可用于烹调食物
2
2.苏州吴文化创造了辉煌的历史。下列吴文化不涉及化学变化的是 C.焚烧聚乙烯塑料会产生刺激性气味的气体
A. 玉器打磨 B. 黏土烧瓷 C. 铁矿炼铁 D. 粮食酿酒 D.测定溶液的pH前,可先将pH试纸用水湿润
3. 化学用语是学习化学的重要工具。下列化学用语表示正确的是 9.某冶炼厂处理尾气时有下列转化,下列说法不正确的是
A. 尿素:氧化铁:FeO B. CO(NH)
2 2
C. 钙离子:Ca+2 D. 两个氧原子:O
2
4.运用乳化原理清洗物品的是
A. 清水洗手 B. 汽油洗油污 C. 盐酸除水垢 D. 洗洁精洗餐具
5.“粗盐中难溶性杂质的去除”涉及的实验操作中不正确的是 A.转化①是氧化反应
B.甲、乙、丁属于氧化物
C.乙中氮元素的化合价为+4价
D.转化②中,参加反应的乙与生成丙的分子个数之比为2:1
A.溶解粗盐 B.过滤杂质
10.分析推理是化学学习中最常用的思维方法,下列说法正确的是
A. 离子是带电荷的粒子,则带电荷的粒子一定是离子
B. 氧化物中一定含有氧元素,则含有氧元素 的化合物一定是氧化物
C. 燃烧有发光放热现象出现,则有发光放热现象的变化一定是燃烧
D. 碱性溶液能使酚酞溶液变红,则能使酚酞溶液变红的溶液一定呈碱性
11.茶叶中含茶氨酸(化学式为C H ON)、锌等多种成分,茶树适宜在pH为5-6的土壤中生长。下列说法
2 14 3 2
C.蒸发结晶 D.熄灭酒精灯 错误的是
A. 茶氨酸属于有机物 B. 茶氨酸中碳、氢元素的质量比为12:7
C. 1个茶氨酸分子中含有1个氮分子 D. 茶树不宜在碱性土壤中生长
12.要使如图装置中的小气球鼓起来且一段时间后未恢复到原大小,则图中的固体和液体可以是
6.下列关于水和溶液的说法错误的是
A. 水是一种最常见的溶剂 B. 水中加入蔗糖后形成溶液,导电性明显增强………………
○
………………
外
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
………………
○
………………
内
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
C 鉴别H 和CH 分别点燃,在火焰上方罩一个干冷烧杯
2 4
D 鉴别NaCl和NaSO 溶液 取样,滴加Mg(NO ) 溶液,观察现象
2 4 3 2
此
A. A B. B C. C D. D
16. 某化学兴趣小组的同学利用如图微型实验装置进行探究实验。先挤压右侧滴管,使液体A与固体D接
卷
①石灰石和稀盐酸 ②镁和稀硫酸 ③固体氧氧化钠和水 触,产生大量气泡,同时微热燃烧管,观察到纸屑先于木屑燃烧,然后挤压左侧滴管滴下液体,也产生
只
A. ①②③ B. 只有①② C. 只有①③ D. 只有②③ 气泡,同时纸屑和木屑均熄灭。下列说法不正确的是
13.实验小组借助传感器对稀NaOH溶液与稀盐酸的反应进行研究。三颈烧瓶中盛放溶液X,用恒压漏斗
装
匀速滴加另一种溶液,并用磁力搅拌器不断搅拌。实验装置和测定结果如图。下列说法正确的是
订
不
密
A. 该实验可证明木屑的着火点高于纸屑
封
B. 该装置的优点有:操作简单、节约药品、现象明显
A. X溶液能使酚酞变红 C. 实验过程中产生的CO,可以通入足量的氢氧化钠溶液中进行反应
B. 0~40s溶液中H+数量不断增加 D. 液体B和固体C可以是稀盐酸和石灰石(或大理石)
C. 60s时溶液中存在的离子有Na+、Cl-、OH- 17. 化学兴趣小组利用如图所示实验装置模拟工业炼铁。下列说法错误的是
D. 可以用硝酸银验证M点时氢氧化钠和盐酸是否恰好完全反应
14.电导率是衡量溶液导电能力大小的物理量,在相同条件下,电导率与离子浓度(单位体积内的离子数)成
正比,利用数据传感技术测定溶液电导率可辅助探究复分解反应。对如图所示实验分析不正确的是
18. CuSO 和NaC1的溶解度曲线如图所示。下列说法正确的是
4
A. P点时溶液中的阳离子有Na+、H+
B. M到N时,氢氧化钠溶液过量,溶液呈碱性
C. P到M电导率减小是因为溶液中离子数量逐渐减少 A. CuSO 4 的溶解度一定大于NaCl的溶解度
D. N点时溶液中的离子数大于P点 B. 升高温度可以降低NaCl的溶解度
15. 下列实验方案中,能达到目的的是 C. T℃时,等质量NaCl和CuSO 4 两种溶液溶质的质量分数一定相等
D. 将等质量T℃时的NaCl和CuSO 饱和溶液均升温至80℃后,两种溶液溶质的质量分数仍然相等 4
选项 实验目的 实验方案
19. 下列物质的转化在给定条件下均能实现的是
通过盛有NaOH溶液的洗气瓶,再通过盛有 A. Fe FeCl 3 Fe(OH) 3
A 除去CO 中的HCl气体
2
浓硫酸的洗气瓶
B. CuOCuSO
4
溶液Cu(OH)
2
C. NaCl溶液NaHCONaOH
3
B 除去MgCl 2 溶液中的少量盐酸 加入过量MgO后过滤 D. BaCl 2 溶液BaCO 3 Ba(NO 3 ) 2 溶液
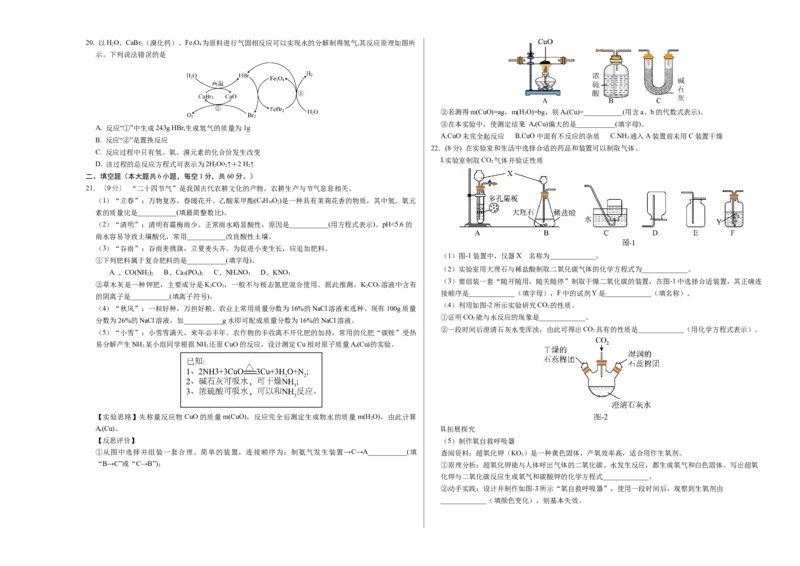
试题 第211页(共612页) 试题 第212页(共612页)20. 以HO、CaBr (溴化钙)、Fe O 为原料进行气固相反应可以实现水的分解制得氢气,其反应原理如图所
2 2 3 4
示。下列说法错误的是
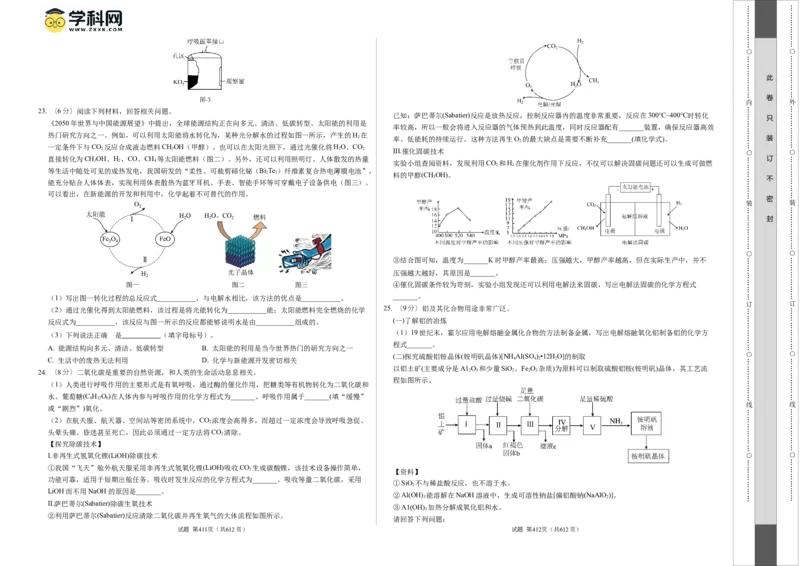
②若测得m(CuO)=ag,m(HO)=bg,则A(Cu)=___________(用含a、b的代数式表示)。
2 r
③在本实验中,使测定结果 A(Cu)偏大的是___________(填字母)。
A. 反应“①”中生成243g HBr,生成氢气的质量为1g r
A.CuO未完全起反应 B.CuO中混有不反应的杂质 C.NH 通入A装置前未用C装置干燥
B. 反应“②”是置换反应 3
22.(8分) 在实验室和生活中选择合适的药品和装置可以制取气体。
C. 反应过程中只有氢、氧、溴元素的化合价发生改变
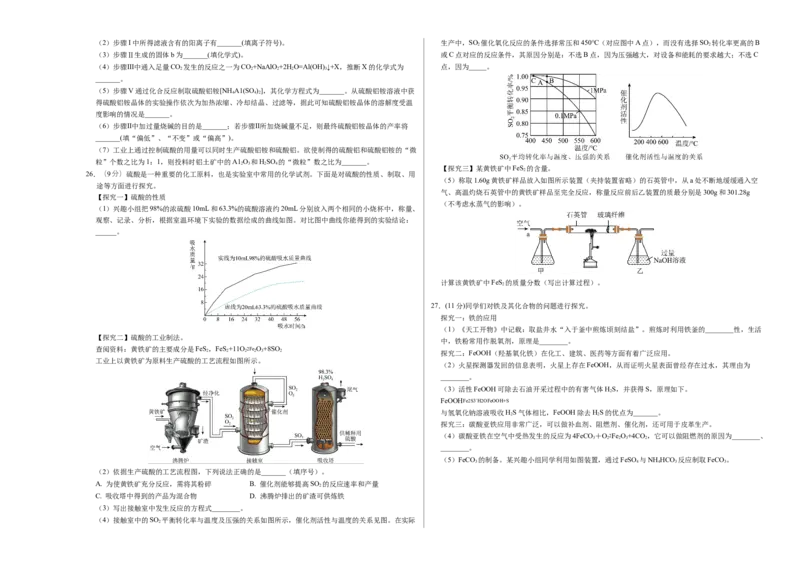
I.实验室制取CO 气体并验证性质
D. 该过程的总反应方程式可表示为2HOO↑+2 H ↑ 2
2 2 2
二、填空题(本大题共6小题,每空1分,共60分。)
21.(9分) “二十四节气”是我国古代农耕文化的产物,农耕生产与节气息息相关。
(1)“立春”:万物复苏,春暖花开。乙酸苯甲酯(C H O)是一种具有茉莉花香的物质,其中氢、氧元
9 10 2
素的质量比是___________(填最简整数比)。
(2)“清明”:清明有霜梅雨少。正常雨水略显酸性,原因是___________(用方程式表示)。pH<5.6的
雨水容易导致土壤酸化,常用___________改良酸性土壤。
(3)“谷雨”:谷雨麦挑旗,立夏麦头齐。为促进小麦生长,应追加肥料。
(1)图-1装置中,仪器X 的名称为_____________。
①下列肥料属于复合肥料的是___________(填字母)。
(2)实验室用大理石与稀盐酸制取二氧化碳气体的化学方程式为_____________。
A 、CO(NH) B、Ca (PO ) C、NH NO D、KNO
2 2 3 4 2 4 3 3
(3)要组装一套“随开随用,随关随停”制取干燥二氧化碳的装置,在图-1中选择合适装置,其正确连
②草木灰是一种钾肥,主要成分是KCO ,一般不与铵态氮肥混合使用。据此推测,KCO 溶液中含有
2 3 2 3
接顺序是_____________(填字母),F中的试剂Y是_____________(填名称)。
的阴离子是___________(填离子符号)。
(4)利用如图-2所示实验研究CO 的性质。
(4)“秋风”:一粒好种,万担好粮。农业上常用质量分数为16%的NaCl溶液来选种。现有100g质量 2
①证明CO 能与水反应的现象是_____________。
分数为26%的NaCl溶液,加___________g水即可配成质量分数为16%的NaCl溶液。 2
②一段时间后澄清石灰水变浑浊,由此可得出CO 具有的性质是_____________(用化学方程式表示)。
(5)“小雪”:小雪雪满天,来年必丰年。农作物的丰收离不开化肥的加持,常用的化肥“碳铵”受热 2
易分解产生NH 某小组同学根据NH 还原CuO的反应,设计测定Cu相对原子质量A(Cu)的实验。
3. 3 r
【实验思路】先称量反应物CuO的质量m(CuO),反应完全后测定生成物水的质量 m(HO),由此计算
2
A(Cu)。 Ⅱ.拓展探究
r
【反思评价】 (5)制作氧自救呼吸器
①从图中选择并组装一套合理、简单的装置,连接顺序为:制氨气发生装置→C→A___________(填 查阅资料:超氧化钾(KO )是一种黄色固体,产氧效率高,适合用作生氧剂。
2
“B→C”或“C→B”); ①原理分析:超氧化钾能与人体呼出气体的二氧化碳、水发生反应,都生成氧气和白色固体。写出超氧
化钾与二氧化碳反应生成氧气和碳酸钾的化学方程式_____________。
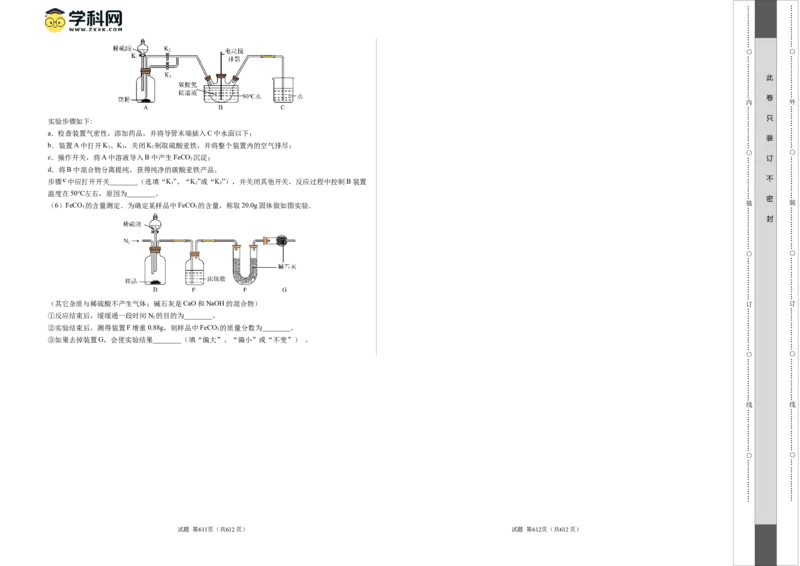
②动手实践:设计并制作如图-3所示“氧自救呼吸器”,使用一段时间后,观察到生氧剂由
_____________(填颜色变化),则基本失效。………………
○
………………
外
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
………………
○
………………
内
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
此
卷
23. (6分)阅读下列材料,回答相关问题。
已知:萨巴蒂尔(Sabatier)反应是放热反应,控制反应器内的温度非常重要,反应在300℃~400℃时转化
只
《2050年世界与中国能源展望》中提出,全球能源结构正在向多元、清洁、低碳转型。太阳能的利用是
率较高,所以一般会将进入反应器的气体预热到此温度,同时反应器配有_______装置,确保反应器高效
热门研究方向之一。例如,可以利用太阳能将水转化为,某种光分解水的过程如图一所示,产生的H 在
2 率、低能耗的持续运行。这种方法再生O 的最大缺点是需要不断补充_______(填化学式)。 装
2
一定条件下与CO 反应合成液态燃料CHOH(甲醇)。也可以在太阳光照下,通过光催化将HO、CO
2 3 2 2 III.催化固碳技术
直接转化为CHOH、H、CO、CH 等太阳能燃料(图二)。另外,还可以利用照明灯、人体散发的热量 订 3 2 4 实验小组查阅资料,发现利用CO 和H 在催化剂作用下反应,不仅可以解决固碳问题还可以生成可做燃
2 2
等生活中随处可见的成热发电,我国研发的“柔性、可裁剪碲化铋(BiTe)纤维素复合热电薄膜电池”,
2 3 料的甲醇(CHOH)。
3 不
能充分贴合人体体表,实现利用体表散热为蓝牙耳机、手表、智能手环等可穿戴电子设备供电(图三)。
可以看出,在新能源的开发和利用中,化学起着不可替代的作用。
密
封
③结合图可知,温度为_______K时甲醇产率最高;压强越大,甲醇产率越高,但在实际生产中,并不 是
压强越大越好,其原因是_______。
④催化固碳条件较为苛刻,实验小组发现还可以利用电解法来固碳,写出电解法固碳的化学方程式
(1)写出图一转化过程的总反应式___________,与电解水相比,该方法的优点是___________。 _______。
(2)通过光催化得到太阳能燃料,该过程是将光能转化为___________能;太阳能燃料完全燃烧的化学 25. (9分)铝及其化合物用途非常广泛。
反应式为___________,该反应与图一所示的反应都能够说明水是由___________组成的。 (一)了解铝的冶炼
(3)下列说法正确 的是 (填字母标号)。 (1)19世纪末,霍尔应用电解熔融金属化合物的方法制备金属,写出电解熔融氧化铝制备铝的化学方
程式_______。
A. 能源结构向多元、清洁、低碳转型 B. 太阳能的利用是当今世界热门的研究方向之一
(二)探究硫酸铝铵晶体(铵明矾晶体)[NH Al(SO )•12H O]的制取
C. 生活中的废热无法利用 D. 化学与新能源开发密切相关 4 4 2 2
以铝土矿(主要成分是A1 O 和少量SiO、Fe O 杂质)为原料可以制取硫酸铝铵(铵明矾)晶体,其工艺流
24. (8分)二氧化碳是重要的自然资源,和人类的生命活动息息相关。 2 3 2 2 3
程如图所示。
(1)人类进行呼吸作用的主要形式是有氧呼吸,通过酶的催化作用,把糖类等有机物转化为二氧化碳和
水。葡萄糖(C H O)在人体内参与呼吸作用的化学方程式为_______。呼吸作用属于_______(填“缓慢”
6 12 6
或“剧烈”)氧化。
(2)在航天服、航天器、空间站等密闭系统中,CO 浓度会高得多,而超过一定浓度会导致呼吸急促、
2
头晕头痛、昏迷甚至死亡,因此必须通过一定方法将CO 清除。
2
【探究除碳技术】
I.非再生式氢氧化锂(LiOH)除碳技术
①我国“飞天”舱外航天服采用非再生式氢氧化锂(LiOH)吸收CO 生成碳酸锂,该技术设备操作简单,
2 【资料】
功能可靠,适用于短期出舱任务。吸收时发生反应的化学方程式为_______。吸收等量二氧化碳,采用
①SiO 不与稀盐酸反应,也不溶于水。
2
LiOH而不用NaOH的原因是_______。
②Al(OH) 能溶解在NaOH溶液中,生成可溶性钠盐[偏铝酸钠(NaAlO )]。
3 2
II.萨巴蒂尔(Sabatier)除碳生氧技术
③A1(OH) 加热分解成氧化铝和水。
3
②利用萨巴蒂尔(Sabatier)反应清除二氧化碳并再生氧气的大体流程如图所示。
请回答下列问题:
试题 第411页(共612页) 试题 第412页(共612页)(2)步骤I中所得滤液含有的阳离子有_______(填离子符号)。 生产中,SO 催化氧化反应的条件选择常压和450℃(对应图中A点),而没有选择SO 转化率更高的B
2 2
(3)步骤Ⅱ生成的固体b为_______(填化学式)。 或C点对应的反应条件,其原因分别是:不选B点,因为压强越大,对设备和能耗的要求越大;不选C
(4)步骤Ⅲ中通入足量CO 发生的反应之一为CO+NaAlO+2H O=Al(OH) ↓+X,推断X的化学式为 点,因为_____。
2 2 2 2 3
_______。
(5)步骤V通过化合反应制取硫酸铝铵[NH A1(SO )],其化学方程式为_______。从硫酸铝铵溶液中获
4 4 2
得硫酸铝铵晶体的实验操作依次为加热浓缩、冷却结晶、过滤等,据此可知硫酸铝铵晶体的溶解度受温
度影响的情况是_______。
(6)步骤Ⅱ中加过量烧碱的目的是_______;若步骤Ⅱ所加烧碱量不足,则最终硫酸铝铵晶体的产率将
_______(填“偏低”、“不变”或“偏高”)。
(7)工业上通过控制硫酸的用量可以同时生产硫酸铝铵和硫酸铝。欲使制得的硫酸铝和硫酸铝铵的“微
粒”个数之比为1:1,则投料时铝土矿中的A1 O 和HSO 的“微粒”数之比为_______。
2 3 2 4
【探究三】某黄铁矿中FeS 的含量。
2
26.(9分)硫酸是一种重要的化工原料,也是实验室中常用的化学试剂。下面是对硫酸的性质、制取、用
(5)称取1.60g黄铁矿样品放入如图所示装置(夹持装置省略)的石英管中,从a处不断地缓缓通入空
途等方面进行探究。
气、高温灼烧石英管中的黄铁矿样品至完全反应,称量反应前后乙装置的质最分别是300g和301.28g
【探究一】硫酸的性质
(不考虑水蒸气的影响)。
(1)兴趣小组把98%的浓硫酸10mL和63.3%的硫酸溶液约20mL分别放入两个相同的小烧杯中,称量、
观察、记录、分析,根据室温环境下实验的数据绘成的曲线如图。对比图中曲线你能得到的实验结论:
______。
计算该黄铁矿中FeS 的质量分数(写出计算过程)。
2
27.(11分)同学们对铁及其化合物的问题进行探究。
探究一:铁的应用
(1)《天工开物》中记载:取盐井水“入于釜中煎炼顷刻结盐”。煎炼时利用铁釜的________性,生活
【探究二】硫酸的工业制法。
中,铁粉常用作脱氧剂,原理是________。
查阅资料:黄铁矿的主要成分是FeS,FeS+11O 2Fe O+8SO
2 2 2 2 3 2 探究二:FeOOH(羟基氧化铁)在化工、建筑、医药等方面有着广泛应用。
工业上以黄铁矿为原料生产硫酸的工艺流程如图所示。
(2)火星探测器发回的信息表明,火星上存在FeOOH,从而证明火星表面曾经存在过水,其理由为
________。
(3)活性FeOOH可除去石油开采过程中的有害气体HS,并获得S,原理如下。
2
FeOOHFe2S3`H2OFeOOH+S
与氢氧化钠溶液吸收HS气体相比,FeOOH除去HS的优点为_______。
2 2
探究三:碳酸亚铁应用非常广泛,可以做补血剂、阻燃剂、催化剂,还可用于皮革生产。
(4)碳酸亚铁在空气中受热发生的反应为4FeCO+O2Fe O+4CO ,它可以做阻燃剂的原因为________、
3 2 2 3 2
________。
(5)FeCO 的制备。某兴趣小组同学利用如图装置,通过FeSO 与NH HCO 反应制取FeCO。
3 4 4 3 3
(2)依据生产硫酸的工艺流程图,下列说法正确的是_______(填序号)。
A. 为使黄铁矿充分反应,需将其粉碎 B. 催化剂能够提高SO 的反应速率和产量
2
C. 吸收塔中得到的产品为混合物 D. 沸腾炉排出的矿渣可供炼铁
(3)写出接触室中发生反应的方程式________。
(4)接触室中的SO 平衡转化率与温度及压强的关系如图所示,催化剂活性与温度的关系见图。在实际
2………………
○
………………
外
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
………………
○
………………
内
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
此
卷
只
实验步骤如下:
a.检查装置气密性,添加药品,并将导管末端插入C中水面以下;
装
b.装置A中打开K、K,关闭K 制取硫酸亚铁,并将整个装置内的空气排尽;
1 3 2
c.操作开关,将A中溶液导入B中产生FeCO 3 沉淀; 订
d.将B中混合物分离提纯,获得纯净的碳酸亚铁产品。
不
步骤 中应打开开关________(选填“K”、“K”或“K”),并关闭其他开关,反应过程中控制B装置
1 2 3
温度在50℃左右,原因为________。
密
(6)FeCO 的含量测定.为确定某样品中FeCO 的含量,称取20.0g固体做如图实验.
3 3
封
(其它杂质与稀硫酸不产生气体;碱石灰是CaO和NaOH的混合物)
①反应结束后,缓缓通一段时间N 的目的为________。
2
②实验结束后,测得装置F增重0.88g,则样品中FeCO 的质量分数为________。
3
③如果去掉装置G,会使实验结果________(填“偏大”、“偏小”或“不变”) 。
试题 第611页(共612页) 试题 第612页(共612页)