文档内容
2024 年中考第二次模拟考试(包头卷)
化 学
(考试时间:50分钟 试卷满分:40分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
4.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 O-16 Ca-40 Cl-35.5
一、选择题(本大题共6小题,每小题2分,共12分。每小题给出的四个选项中,只有一个选项最符合题
目的要求)
1.今年我国环境日的主题是“建设人与自然和谐共生的现代化”。下列生活方式符合这一理念的是(
)
A.提倡无纸化办公 B.生活垃圾直接填埋
C.多开燃油私家车 D.常使用一次性餐具
【答案】A
【详解】A、提倡无纸化办公,能节约纸张,减少树木的砍伐,该选项符合题意;
B、直接填埋生活垃圾,会污染土壤,该选项不符合题意;
C、燃油会污染空气,该选项不符合题意;
D、常使用一次性餐具,会增加树木的砍伐,该选项不符合题意。
故选A。
2.项目式化学小组同学制作了简易净水器(如下图),下列有关分析合理的是( )A.石英砂能吸附水中的悬浮杂质 B.活性炭能除去水中的色素和异味
C.烧杯中得到的水是软水 D.该净水器可用于淡化海水
【答案】B
【详解】A、石英砂间存在空隙,起过滤作用,活性炭具有吸附性,能吸附色素和异味,故A不合理;
B、活性炭具有吸附性,能除去水中的色素和异味,故B合理;
C、该净化过程不能除去河水中可溶性钙、镁化合物,得到的水不是软水,故C不合理;
D、该净水器不能出去水中的可溶性杂质,不可用于淡化海水,故D不合理;
故选:B。
3.2023杭州亚运会开幕式,主火炬塔历史性地采用了废碳再生的“零碳甲醇(CHOH)”作为燃料。“零碳
3
甲醇”是利用工业尾气中排放的废弃二氧化碳以及焦炉气中的氢气来合成零碳甲醇,从而实现工业尾
气中二氧化碳循环利用,其微观示意图如图(图中的分子恰好完全反应)。下列说法错误的是( )
A.生成物丙中碳元素的质量分数为37.5%
B.生成物丙和丁的质量比为1:1
C.该反应有助于实现“碳中和”
D.该反应的化学方程式为3H+CO CHOH+H O
2 2 3 2
【答案】B
【详解】A、根据微观示意图可知,丙的化学式为CHOH,碳元素的质量分数为
3
=37.5%,故A不符合题意;B、根据微观示意图可知,该反应的化学方程式为 ,生成物丙和丁的质量
比为32:18,故B符合题意;
C、该反应将二氧化碳转化为甲醇,有助于实现“碳中和”,故C不符合题意;
D、综上分析,化学方程式书写正确,故D不符合题意;
故选B。
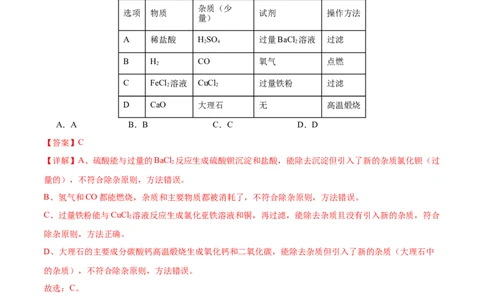
4.除去下列物质中的少量杂质,所用试剂和操作方法都正确的是( )
杂质(少
选项 物质 试剂 操作方法
量)
A 稀盐酸 HSO 过量BaCl 溶液 过滤
2 4 2
B H CO 氧气 点燃
2
C FeCl 溶液 CuCl 过量铁粉 过滤
2 2
D CaO 大理石 无 高温煅烧
A.A B.B C.C D.D
【答案】C
【详解】A、硫酸能与过量的BaCl 反应生成硫酸钡沉淀和盐酸,能除去沉淀但引入了新的杂质氯化钡(过
2
量的),不符合除杂原则,方法错误。
B、氢气和CO都能燃烧,杂质和主要物质都被消耗了,不符合除杂原则,方法错误。
C、过量铁粉能与CuCl 溶液反应生成氯化亚铁溶液和铜,再过滤,能除去杂质且没有引入新的杂质,符合
2
除杂原则,方法正确。
D、大理石的主要成分碳酸钙高温煅烧生成氧化钙和二氧化碳,能除去杂质但引入了新的杂质(大理石中
的杂质),不符合除杂原则,方法错误。
故选:C。
5.我国研制的航天员舱外服为航天员成功进行太空行走提供了可靠的保证,太空中已经留下了“中国人
的脚印”,舱外服内含有与氢氧化钠性质相似的氢氧化锂(LiOH)。下列有关氢氧化锂的说法正确的是
( )
A.其水溶液能使无色酚酞试液变红 B.不能与硫酸铜溶液反应生成蓝色沉淀
C.其水溶液不能与二氧化碳发生反应 D.其水溶液能与氧化铁发生反应
【答案】A
【详解】A、无色酚酞试液遇碱变红,氢氧化锂是一种可溶性碱,其水溶液能使无色酚酞试液变红色,故选项说法正确。
B、氢氧化锂能和硫酸铜溶液反应生成氢氧化铜蓝色沉淀,故选项说法不正确。
C、氢氧化锂与氢氧化钠性质相似,氢氧化锂和二氧化碳反应生成碳酸锂和水,故选项说法不正确。
D、碱不与金属氧化物反应,则氢氧化锂不能和氧化铁发生反应,故选项说法不正确。
故选:A。
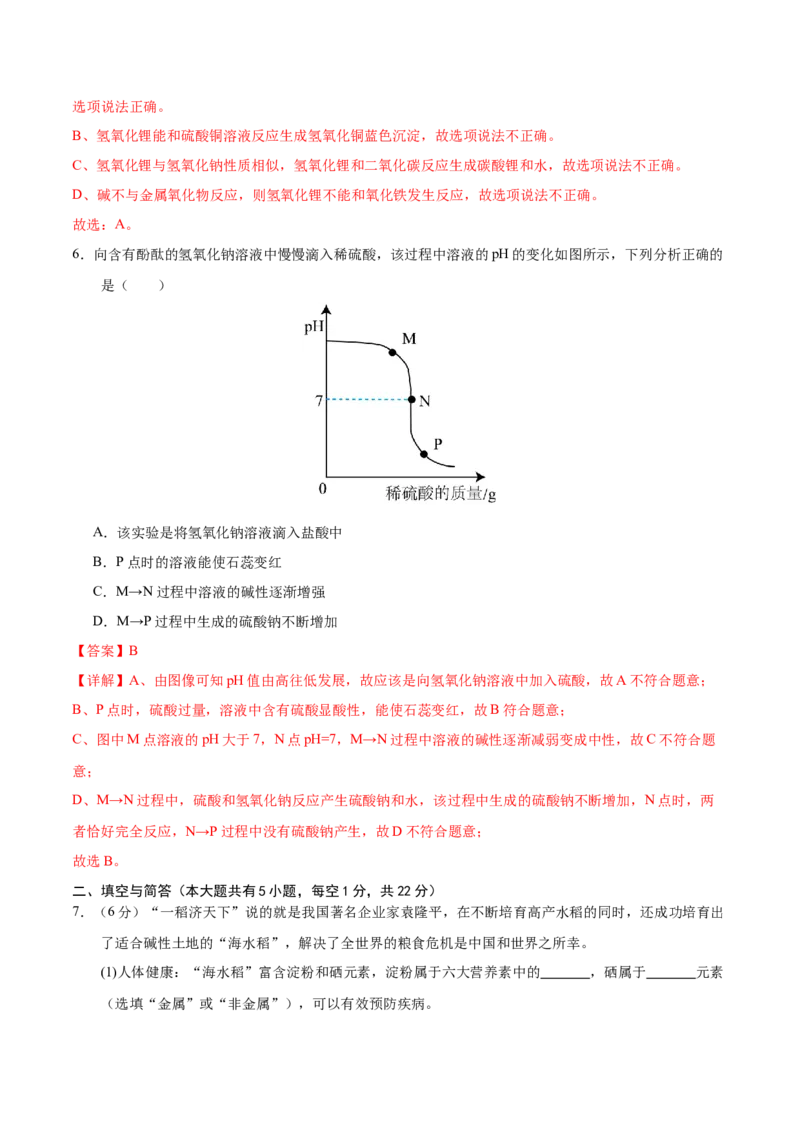
6.向含有酚酞的氢氧化钠溶液中慢慢滴入稀硫酸,该过程中溶液的pH的变化如图所示,下列分析正确的
是( )
A.该实验是将氢氧化钠溶液滴入盐酸中
B.P点时的溶液能使石蕊变红
C.M→N过程中溶液的碱性逐渐增强
D.M→P过程中生成的硫酸钠不断增加
【答案】B
【详解】A、由图像可知pH值由高往低发展,故应该是向氢氧化钠溶液中加入硫酸,故A不符合题意;
B、P点时,硫酸过量,溶液中含有硫酸显酸性,能使石蕊变红,故B符合题意;
C、图中M点溶液的pH大于7,N点pH=7,M→N过程中溶液的碱性逐渐减弱变成中性,故C不符合题
意;
D、M→N过程中,硫酸和氢氧化钠反应产生硫酸钠和水,该过程中生成的硫酸钠不断增加,N点时,两
者恰好完全反应,N→P过程中没有硫酸钠产生,故D不符合题意;
故选B。
二、填空与简答(本大题共有5小题,每空1分,共22分)
7.(6分)“一稻济天下”说的就是我国著名企业家袁隆平,在不断培育高产水稻的同时,还成功培育出
了适合碱性土地的“海水稻”,解决了全世界的粮食危机是中国和世界之所幸。
(1)人体健康:“海水稻”富含淀粉和硒元素,淀粉属于六大营养素中的 ,硒属于 元素
(选填“金属”或“非金属”),可以有效预防疾病。(2)粮食高产:“庄稼好不好全靠施肥巧不巧”,常见的化肥有 等,其中
中碳的化合价为 ,属于复合肥的是 。
(3)绿色环保:稻草是一种宝贵的资源,其主要成分纤维素在催化剂和水的作用下会产生葡萄糖,葡萄
糖再与酒化酶作用转化成乙醇,其中反应为 请写出X的化学式 。因
此从能源分类来看属于 资源(选填“可再生”或“不可再生”)。
【答案】(1) 糖类 非金属
(2) +4 KNO /硝酸钾
3
(3) CO 可再生
2
【详解】(1)淀粉属于六大营养素中的糖类;硒元素名称带“石”字旁,属于非金属元素,故填:糖类;
非金属;
(2) 中钾元素化合价为+1价,氧元素化合价为-2价,设碳元素化合价为x,根据化合物中正负化
合价代数为0,则有(+1)×2+ x+(-2)×3=0,得x=+4价;
中含有N、P、K中的钾元素,属于钾肥,Ca(HPO ) 中含有N、P、K中的磷元素,属于磷肥,
2 4 2
KNO 中含有N、P、K中的钾元素和氮元素,属于复合肥;
3
故填:+4或+4价;KNO 或硝酸钾;
3
(3)根据质量守恒定律,反应前后原子的种类、数目不变,反应前C、H、O的原子个数分别为6、12、
6,反应后C、H、O的原子个数分别为4、12、2,则2X中含有2个碳原子和4个氧原子,X的化学式为
CO;
2
稻草通过一系列反应能转化为乙醇,说明乙醇属于可再生能源;
故填:CO;可再生。
2
8.(3分)甲、乙两种固体物质的溶解度曲线如图所示。(1)M点表示t℃时,固体甲和乙的 。
1
(2)t ℃时,将60克甲物质加入到50克水中,充分溶解后,所得溶液的质量是 克。
2
(3)若固体甲中含有少量乙物质,可采用 的方法提纯甲。
【答案】(1)溶解度相同
(2)80
(3)降温结晶
【详解】(1)由图可知,M为甲乙溶解度的交点,表示在t℃,固体甲和乙的溶解度相同;
1
(2)t℃时,甲物质的溶解度是60克,在t℃,在100克水中最多能够溶解60克甲物质,将60克甲物质
2 2
加入到50克水中,充分溶解后,溶解的甲物质质量为60g÷2=30g,所得溶液的质量是30+50克=80克;
(3)甲的溶解度受温度影响较大,乙的溶解度受温度影响较小,所以甲中含有少量的乙,可采用降温结
晶的方法提纯甲。
9.(5分)根据下列图示装置回答问题。
(1)仪器①的名称为 。
(2)实验室制 和 均可使用的气体发生装置是 (填字母)。用该装置制取 时,发生反
应的化学方程式为 。
(3)能用C装置收集的气体,其密度应该比空气 。
(4)若装置D中的白磷燃烧,则试管中的气体为 。
【答案】(1)锥形瓶(2) B
(3)小
(4)氧气或空气
【详解】(1)仪器①的名称为锥形瓶;
(2)实验室制取氧气可采用过氧化氢溶液和二氧化锰混合,制取二氧化碳选用大理石或石灰石与稀盐酸
反应,都是固液常温型,故发生装置都能选B;
过氧化氢在二氧化锰的催化下分解生成氧气和水,化学方程式为: ;
(3)能用C装置向下排空气法收集的气体,其密度应该比空气小;
(4)燃烧的三要素为:可燃物、与氧气(或空气)接触、温度达到白磷的着火点,若装置D中的白磷燃
烧,则试管中的气体为氧气或空气。
10.(3分)为了从硝酸锌和硝酸银的混合溶液中回收银,设计了如下的实验方案:
(1)步骤①中可观察到有固体析出,溶液颜色由 。
(2)溶液乙中的金属离子为 (填离子符号)。
(3)写出步骤②发生反应的化学方程式: 。
【答案】(1)无色变为蓝色
(2)Zn2+、Cu2+
(3)Cu+2AgNO =Cu(NO)+2Ag
3 3 2
【详解】(1)根据金属活动性顺序Zn>Cu>Ag,步骤①向硝酸锌和硝酸银的混合溶液中,加入过量的铜
粉,铜不能和硝酸锌反应,铜和硝酸银反应生成硝酸铜和银,可观察到溶液由无色变为蓝色;
(2)根据金属活动性顺序Zn>Cu>Ag,步骤①向硝酸锌和硝酸银的混合溶液中,加入过量的铜粉,铜不
能和硝酸锌反应,铜和硝酸银反应生成硝酸铜和银,溶液乙中含有硝酸锌和硝酸铜,则溶液乙中的金属离
子为Zn2+、Cu2+;
(3)固体甲中含有银和过量的铜,根据除杂的原则,除去杂质且不能引入新的杂质,则步骤②可加入足
量的硝酸银,铜和硝酸银反应生成硝酸铜和银,过滤可得到铜,化学方程式为:。
11.(5分)兴趣小组的同学在学习了金属的化学性质后,把一小块钠放入硫酸铜溶液中,观察到有气泡
冒出。但未观察到红色固体,而是看到了有蓝色沉淀产生,并进行了如下探究。
【查阅资料】钠是一种活泼金属,常温下能与氧气、水等物质发生反应:
钠与水反应的化学方程式为 。
【提出问题】钠与硫酸铜溶液反应后溶液中溶质的成分是什么?
【做出猜想】猜想I:NaSO
2 4
猜想Ⅱ:NaSO 、NaOH
2 4
猜想Ⅲ: 。
猜想IV:NaSO 、NaOH、CuSO
2 4 4
小林认为猜想Ⅳ一定不成立,其原因是 (用化学方程式表示)。
【实验探究】
实验 实验操作 实验现象 实验结论
猜想Ⅲ不成
实验1 取反应后的溶液于试管中,观察溶液颜色 溶液为无色
立
实验2 向实验1所取的溶液中滴入氯化钡溶液 猜想Ⅱ成立
溶液变为红
实验3 另取反应后的溶液于试管中,向其中滴加少量无色酚酞溶液 猜想Ⅱ成立
色
【讨论分析】
(1)同学们认为实验2不合理,其原因是 。
(2)金属钠在储存过程中意外着火时 (选填“能”或“不能”)用水来扑灭。
【答案】 NaSO 、CuSO
2 4 4
生成白色固体 猜想I中加入BaCl 也会产生白色沉淀 不能
2
【详解】[做出猜想]由于钠能与水反应生成氢氧化钠和氢气,而氢氧化钠能与硫酸铜反应生成硫酸钠和氢
氧化铜沉淀,则若恰好反应,溶液中的溶质为硫酸钠,若钠过量,则溶液中的溶质为氢氧化钠和硫酸钠,
若硫酸铜过量,则溶液中的溶质为硫酸钠和硫酸铜,则猜想Ⅲ为硫酸钠和硫酸铜。
由于氢氧化钠能与硫酸铜反应,则猜想Ⅳ一定不成立,反应的化学方程式为。
[实验探究]由于硫酸钠能与氯化钡反应生成硫酸钡沉淀和氯化钠,则现象为有白色沉淀产生。
[讨论分析](1)由于猜想Ⅰ中加入BaCl 也会产生白色沉淀,则不能说明猜想Ⅱ成立,则实验2不合理。
2
(2)由于钠能与水反应,则金属钠在储存过程中意外着火时,不能用水来扑灭。
三、计算题(本大题共1个小题,共6分)
12.(6分)某化学兴趣小组为测定反应后溶液的溶质质量分数,进行如下实验:
①称取20g碳酸钙,平均分成两份,并分别将第一份加工成块状第二份加工成粉末状;
②将两份样品分别投入两个锥形瓶中,分别加入相同溶质质量分数的稀盐酸各100克恰好完全反应,
测得生成二氧化碳的质量与反应时间的关系如下图所示:
请回答:
(1)每份样品充分反应后,生成二氧化碳的质量为 g。
(2)向其中一个锥形瓶中再加水5.4克,求加水后此锥形瓶中溶液的溶质质量分数?
【答案】(1)4.4
(2)解:设生成的CaCl 的质量为x,
2
x=11.1g
向其中一个锥形瓶中再加水5.4克,此时锥形瓶内溶液的质量为(100g+10g)-4.4g+5.4g=111g;
故锥形瓶内溶液溶质质量分数为 ×100%=10%
答:锥形瓶内溶液溶质质量分数为10%。【详解】(1)根据图示,每份样品充分反应后,生成二氧化碳的质量为4.4g;
(2)见答案。