文档内容
2024 年中考第三次模拟考试(安徽卷)
化 学
注意事项:
1、化学试卷共二大题17小题,满分40分物理和化学的考试时间共120分钟。
2、试卷包括“试题卷"和“答题卷"两部分请务必在“答题卷”上答题,在“试题卷"上答题是无效的。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Ca-40
一、本大题包括12小题,每小题1分,共12分。每小题的4个备选答案中只有一个答案符合题意。
1.文房四宝“笔墨纸砚”是中华文化的瑰宝。下列关于笔墨纸砚的制作工艺中,涉及到化学变化的是(
)
A.竹作笔杆羊毛为毫 B.杂木烧炭集烟成墨
C.浆压薄片晾干成纸 D.开石磨光雕刻成砚
【答案】B
【详解】A、竹作笔杆羊毛为毫过程是形状改变,没有新物质生成,属于物理变化;
B、杂木烧炭集烟成墨过程中,有新物质碳单质生成,属于化学变化;
C、浆压薄片晾干成纸过程是形状改变,没有新物质生成,属于物理变化;
D、开石磨光雕刻成砚过程是形状改变,没有新物质生成,属于物理变化。
故选B。
2.“构建生命共同体”理念体现人与自然和谐共生。下列做法与该理念不相符的是
A.全民义务植树活动 B.就地焚烧青稞秸秆
C.生活废水处理后排放 D.倡导“低碳”出行
【答案】B
【详解】A、全民义务植树活动,可增加空气进化的能力,有利于改善环境,与理念相符,故A不符合题
意;
B、就地焚烧青稞秸秆,会产生大量严惩和有害气体,不利于保护环境,与理念不相符,故B符合题意;
C、生活废水处理后排放,减少水体污染,有利于保护环境,与理念相符,故C不符合题意;
D、“低碳”出行可减少二氧化碳的排放,节约能源的使用,有利于保护环境,与理念相符,故D不符合
题意;
故选B。3.规范的实验操作可以减少不必要的麻烦,避免一些危险和提高实验的成功率,下列实验操作规范的是
A.向试管中塞进橡胶塞 B.倾倒二氧化碳气体 C.称量NaOH固体 D.氢气的验纯
A.A B.B C.C D.D
【答案】D
【详解】A、向试管中塞橡胶塞应慢慢转动着着塞进试管口,切不可把试管直立放在桌上使劲塞橡胶塞,
以免压破试管,图示操作错误,不符合题意;
B、倾倒二氧化碳气体时,应用玻璃片盖住集气瓶口的大部分,图示操作错误,不符合题意;
C、氢氧化钠固体具有腐蚀性,应放在玻璃器皿中称量,图示操作错误,不符合题意;
D、氢气验纯:将收集到的一试管氢气用拇指堵住试管口,管口朝下靠近火焰,松开拇指,听到尖锐的爆
鸣声说明氢气不纯,声音很小说明氢气较纯,图示操作正确,符合题意。
故选:D。
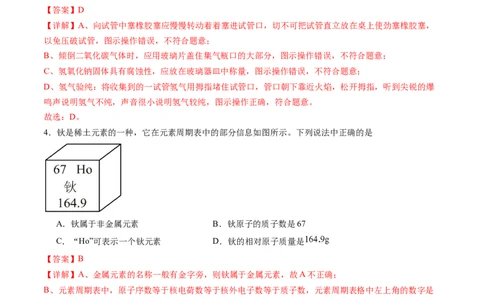
4.钬是稀土元素的一种,它在元素周期表中的部分信息如图所示。下列说法中正确的是
A.钬属于非金属元素 B.钬原子的质子数是67
C.“Ho”可表示一个钬元素 D.钬的相对原子质量是
【答案】B
【详解】A、金属元素的名称一般有金字旁,则钬属于金属元素,故A不正确;
B、元素周期表中,原子序数等于核电荷数等于核外电子数等于质子数,元素周期表格中左上角的数字是
原子序数,等于质子数,故B正确;
C、“Ho”可表示一个钬原子,故C不正确;
D、相对原子质量的单位为1,则钬元素的相对原子质量为164.9,故D不正确。
故选B。
5.螃蟹味道鲜美,营养丰富,蟹肉中含有的烟酸(化学式:C HNO )是人体必需的13中维生素之一,具有
6 5 2
扩张血管的作用。下列说法中正确的是
A.一个烟酸分子中含有1个NO 分子
2
B.123g烟酸中含氧元素的质量为64gC.烟酸中碳元素的质量分数最高
D.烟酸中氮、氧元素的质量比为1:2
【答案】C
【详解】A、一个烟酸分子是由6个碳原子、5个氢原子、1个氮原子、2个氧原子构成,没有二氧化氮分
子,故错误;
B、物质中元素的质量= = =32g,故错误;
C、元素质量分数= ,烟酸中各元素的质量比为:碳元素:
氢元素:氮元素:氧元素=(12×6):(1×5):14:(16×2)=72:5:14:32,由此可见碳元素质量分数最大,
故正确;
D、烟酸中氮元素:氧元素=14:(16×2)=7:16,故错误。
故选C。
6.三氧化二碳(C O)是某星球大气的成分之一,其化学性质与一氧化碳相似。下列关于三氧化二碳的说法
2 3
中不正确的是
A.三氧化二碳的密度比空气大
B.三氧化二碳在一定条件下能还原氧化铁
C.三氧化二碳具有可燃性
D.三氧化二碳中碳元素的化合价为+2
【答案】D
【详解】A、三氧化二碳的相对分子质量为12×2+16×3=72,空气的平均相对分子质量为29,72大于29,
则三氧化二碳的密度比空气大,故选项说法正确;
B、一氧化碳具有还原性,三氧化二碳的化学性质与一氧化碳相似,所以在一定条件下能还原氧化铁,故
选项说法正确;
C、一氧化碳具有可燃性,三氧化二碳的化学性质与一氧化碳相似,所以三氧化二碳具有可燃性,故选项
说法正确;
D、氧元素显﹣2价,设碳元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:2x+(﹣2)
×3=0,则x=+3价,故选项说法错误。
故选D。
7.“人造树叶”是一种新型材料。光照时,CO 和HO在“人造树叶”的催化下反应,其微观图示如下,
2 2
下列说法错误的是A.该反应前后原子的个数不变
B.由图可知,乙醇的化学式为C HOH
2 5
C.参加反应的CO 和HO的分子个数比为1:1
2 2
D.该反应可以缓解温室效应,又能产生燃料,并释放O
2
【答案】C
【详解】A、根据质量守恒定律可知,化学反应前后,原子的种类和个数不变,故A正确;
B、由图可知,1个乙醇分子中含有2个碳原子、1个氧原子和6个氢原子,则化学式为C HOH,故B正
2 5
确;
C、由图可知,该反应为HO和CO 在“人造树叶”的催化下反应生成乙醇和O,反应的化学方程式为:
2 2 2
,则参加反应的CO 和HO的分子个数比为2:3,故C错误;
2 2
D、该反应能消耗二氧化碳,则能缓解温室效应,且该反应能生成氧气和乙醇,乙醇为燃料,故D正确。
故选C。
8.下列实验操作不能达到实验目的是
选
实验目的 实验操作
项
A 鉴别O 和CO 分别将燃着的木条伸入集气瓶中,观察现象
2 2
B 检验人体呼出气体中是否含CO 将气体通入澄清石灰水中,观察现象
2
C 除去CuO粉末中少量C粉 加入稀盐酸,过滤
D 分离KCl和MnO 的混合物 取样,加水溶解、过滤、洗涤、蒸发
2
A.A B.B C.C D.D
【答案】C
【详解】A、氧气具有助燃性,能够使燃着的木条燃烧更旺,二氧化碳不燃烧也不支持燃烧,分别将燃着
的木条伸入集气瓶中,使燃着的木条燃烧更旺的是氧气,木条熄灭的是二氧化碳,选项正确;
B、二氧化碳能够与澄清石灰水中的氢氧化钙反应生成碳酸钙沉淀和水,碳酸钙沉淀使澄清石灰水变浑浊,
所以将气体通入澄清石灰水中,观察现象能够检验人体呼出气体中是否含CO,选项正确;
2
C、碳粉不与稀盐酸反应,氧化铜能够与稀盐酸反应生成氯化铜和水,会将欲保留的氧化铜反应掉,不符
合除杂原则,选项错误;D、氯化钾易溶于水,二氧化锰不溶于水,取样,加水溶解、过滤、洗涤、蒸发能够分离KCl和MnO 的
2
混合物,选项正确,故选C。
9.宏观辨识与微观探析是化学学科的核心素养之一,下列对宏观事实的微观解释错误的是
选项 宏观事实 微观解释
A 氧气经压缩可以储存在钢瓶中 压强增大,分子间的间隔变小
B 过氧化氢分解生成水和氧气 化学反应前后原子的种类改变
C 水和过氧化氢的化学性质不同 构成二者的分子不同
D 氢氧化钠和氢氧化钙溶液具有相似的化学性质 两种溶液中都含有OH-
A.A B.B C.C D.D
【答案】B
【详解】A、压强增大,分子间的间隔变小,故可将氧气经压缩储存在钢瓶中,该选项正确;
B、根据质量守恒定律,化学反应前后原子的种类和数目都不变,过氧化氢分解生成水和氧气,该反应过
程中,分子的种类发生变化,原子的种类不变,该选项错误;
C、水和过氧化氢的化学性质不同,是由于构成二者的分子不同,不同种分子化学性质不同,该选项正确;
D、氢氧化钠和氢氧化钙溶液具有相似的化学性质,是由于两种溶液中都含有OH-,该选项正确;
故选B。
10.下列物质的用途与其性质的对应关系不正确的是
选
A B C D
项
物 金刚
铜丝 盐酸 活性炭
质 石
用 玻璃
导线 除铁锈 去异味
途 刀
性 硬度
导电性 挥发性 吸附性
质 大
A.A B.B C.C D.D
【答案】C
【详解】A、铜丝具有导电性,可用作导线,对应关系正确,不符合题意;
B、金刚石硬度大,可用于玻璃刀,对应关系正确,不符合题意;
C、盐酸具有酸性,能与金属氧化物反应,铁锈的主要成分是氧化铁,因此可用盐酸除铁锈,与挥发性无
关,对应关系不正确,符合题意;
D、活性炭具有吸附性,可吸附色素和异味,可用于去异味,对应关系正确,不符合题意;
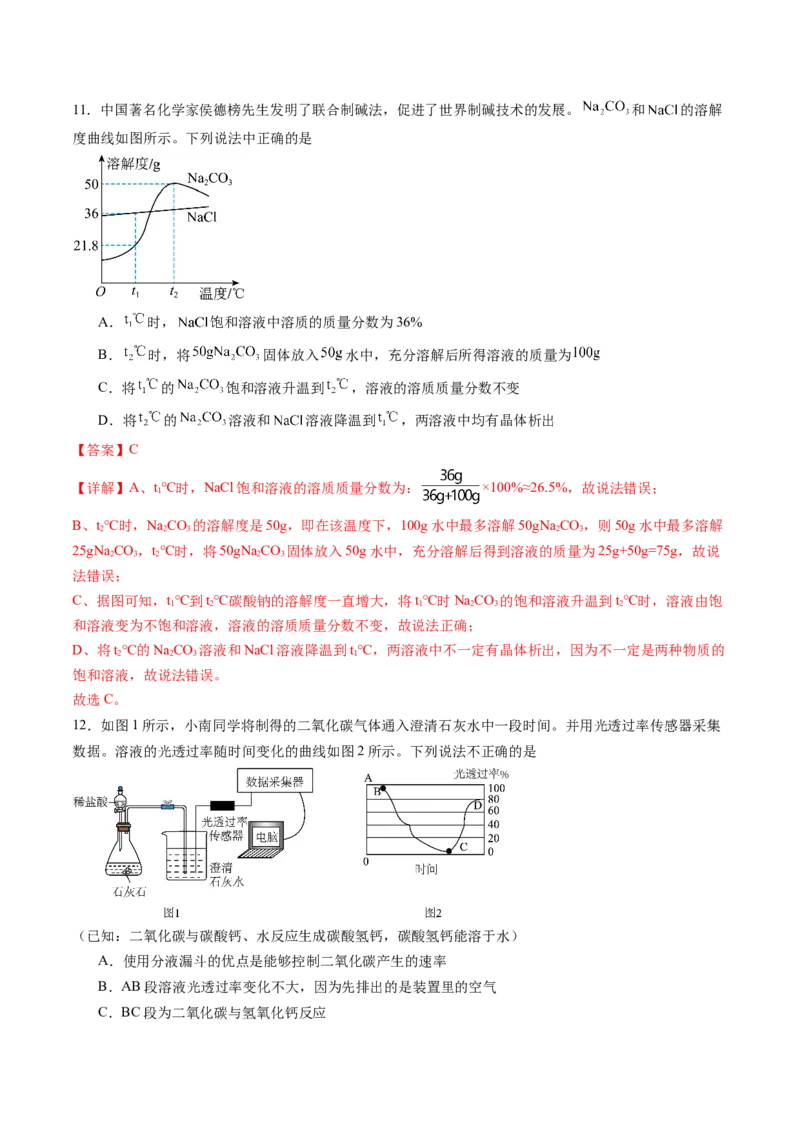
故选:C。11.中国著名化学家侯德榜先生发明了联合制碱法,促进了世界制碱技术的发展。 和 的溶解
度曲线如图所示。下列说法中正确的是
A. 时, 饱和溶液中溶质的质量分数为36%
B. 时,将 固体放入 水中,充分溶解后所得溶液的质量为
C.将 的 饱和溶液升温到 ,溶液的溶质质量分数不变
D.将 的 溶液和 溶液降温到 ,两溶液中均有晶体析出
【答案】C
【详解】A、t℃时,NaCl饱和溶液的溶质质量分数为: ×100%≈26.5%,故说法错误;
1
B、t℃时,NaCO 的溶解度是50g,即在该温度下,100g水中最多溶解50gNaCO,则50g水中最多溶解
2 2 3 2 3
25gNaCO,t℃时,将50gNaCO 固体放入50g水中,充分溶解后得到溶液的质量为25g+50g=75g,故说
2 3 2 2 3
法错误;
C、据图可知,t℃到t℃碳酸钠的溶解度一直增大,将t℃时NaCO 的饱和溶液升温到t℃时,溶液由饱
1 2 1 2 3 2
和溶液变为不饱和溶液,溶液的溶质质量分数不变,故说法正确;
D、将t℃的NaCO 溶液和NaCl溶液降温到t℃,两溶液中不一定有晶体析出,因为不一定是两种物质的
2 2 3 1
饱和溶液,故说法错误。
故选C。
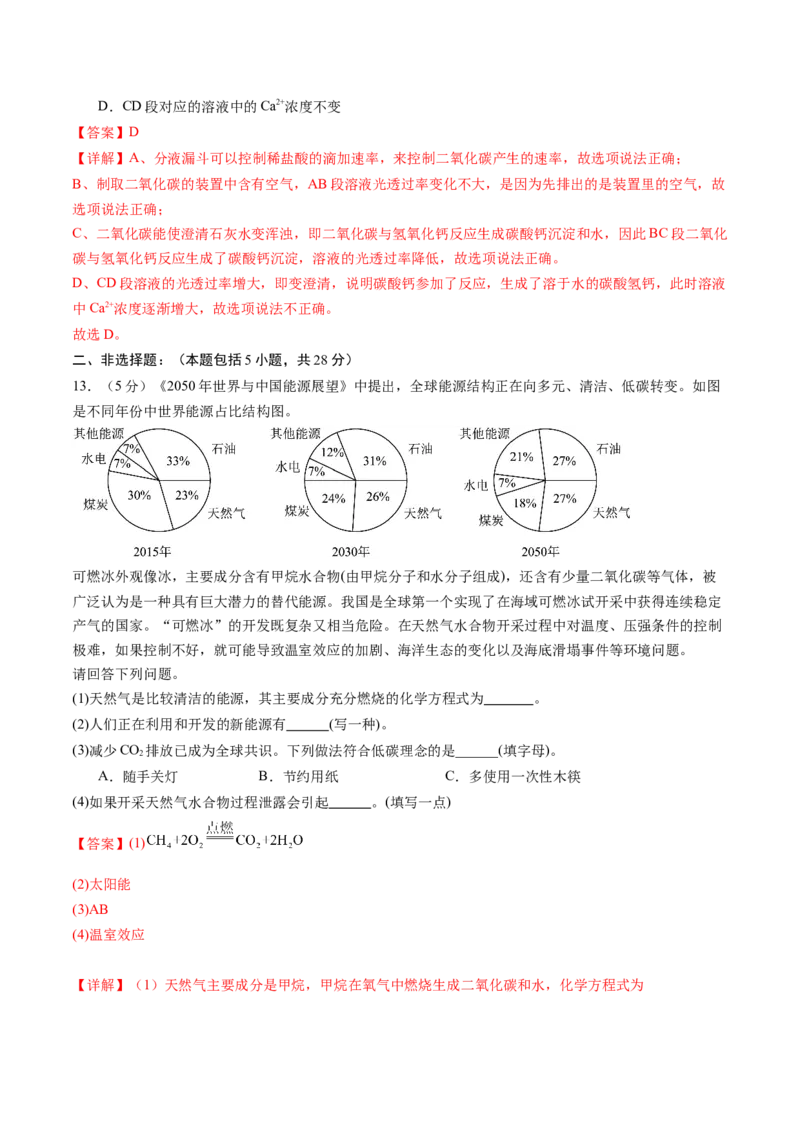
12.如图1所示,小南同学将制得的二氧化碳气体通入澄清石灰水中一段时间。并用光透过率传感器采集
数据。溶液的光透过率随时间变化的曲线如图2所示。下列说法不正确的是
(已知:二氧化碳与碳酸钙、水反应生成碳酸氢钙,碳酸氢钙能溶于水)
A.使用分液漏斗的优点是能够控制二氧化碳产生的速率
B.AB段溶液光透过率变化不大,因为先排出的是装置里的空气
C.BC段为二氧化碳与氢氧化钙反应D.CD段对应的溶液中的Ca2+浓度不变
【答案】D
【详解】A、分液漏斗可以控制稀盐酸的滴加速率,来控制二氧化碳产生的速率,故选项说法正确;
B、制取二氧化碳的装置中含有空气,AB段溶液光透过率变化不大,是因为先排出的是装置里的空气,故
选项说法正确;
C、二氧化碳能使澄清石灰水变浑浊,即二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,因此BC段二氧化
碳与氢氧化钙反应生成了碳酸钙沉淀,溶液的光透过率降低,故选项说法正确。
D、CD段溶液的光透过率增大,即变澄清,说明碳酸钙参加了反应,生成了溶于水的碳酸氢钙,此时溶液
中Ca2+浓度逐渐增大,故选项说法不正确。
故选D。
二、非选择题:(本题包括5小题,共28分)
13.(5分)《2050年世界与中国能源展望》中提出,全球能源结构正在向多元、清洁、低碳转变。如图
是不同年份中世界能源占比结构图。
可燃冰外观像冰,主要成分含有甲烷水合物(由甲烷分子和水分子组成),还含有少量二氧化碳等气体,被
广泛认为是一种具有巨大潜力的替代能源。我国是全球第一个实现了在海域可燃冰试开采中获得连续稳定
产气的国家。“可燃冰”的开发既复杂又相当危险。在天然气水合物开采过程中对温度、压强条件的控制
极难,如果控制不好,就可能导致温室效应的加剧、海洋生态的变化以及海底滑塌事件等环境问题。
请回答下列问题。
(1)天然气是比较清洁的能源,其主要成分充分燃烧的化学方程式为 。
(2)人们正在利用和开发的新能源有 (写一种)。
(3)减少CO 排放已成为全球共识。下列做法符合低碳理念的是______(填字母)。
2
A.随手关灯 B.节约用纸 C.多使用一次性木筷
(4)如果开采天然气水合物过程泄露会引起 。(填写一点)
【答案】(1)
(2)太阳能
(3)AB
(4)温室效应
【详解】(1)天然气主要成分是甲烷,甲烷在氧气中燃烧生成二氧化碳和水,化学方程式为;
(2)人们正在利用和开发的新能源有太阳能、风能、氢能、生物质能等;
(3)A、随手关灯,有利于节约电能,符合低碳理念,符合题意;
B、节约用纸,有利于节约资源,符合低碳理念,符合题意;
C、多使用一次性木筷,会造成资源浪费,不利于保护环境,不符合低碳理念,不符合题意。
故选:AB;
(4)如果开采天然气水合物过程泄露会引起温室效应。
14.(6分)如图是实验室制取气体的常用装置。
(1)仪器a的名称 。
(2)写出一个用装置A制取O 的化学方程式 。
2
(3)实验室可选用装置B或装置C制取CO,若选用装置C作为发生装置,与装置B相比较,装置C的主要
2
优点 。
(4)收集CO 时,用燃着的木条来验满,是利用CO 的化学性质。
2 2
(5)若某气体只能用D装置收集,则该气体可能具有的性质为 (填序号)。
①常温下能与空气中的某物质反应
②密度与空气的密度接近且难溶于水
③能与水反应
【答案】(1)锥形瓶
(2)
(3)可以控制反应的速率
(4)既不能燃烧、又不能支持燃烧
(5)①②
【详解】(1)由图可知,氧气a为锥形瓶;
(2)A为固体加热型发生装置,管口有棉花团,应选用高锰酸钾制氧,高锰酸钾加热生成锰酸钾、二氧化
锰和氧气,故化学方程式为: ;(3)C装置可以利用注入器控制滴加液体的速率,从而控制反应的速率,产生平稳的气流;
(4)二氧化碳既不能燃烧、又不能支持燃烧,所以二氧化碳验满时可以用燃着的木条放在瓶口;
(5)D装置为排水法收集装置,能采用排水法收集说明该气体难溶于水,不与水反应;只能用排水法收集,
说明不能采用排空气法收集,可能是气体的密度与空气过于接近,或是与空气中成分发生反应。
故选①②。
15.(5分)兴趣小组的同学利用某废镍材料(含有金属Ni及少量Fe、Cu)回收镍,设计流程如下图所示
(部分产物略去)。
(1)过滤时,玻璃棒的作用是 。
(2)“酸浸”时加入过量稀硫酸的目的是 。
(3)过氧化氢具有氧化性,“氧化”时发生反应的化学方程式为 ,则
X的化学式是 。
(4)依据上述流程判断Ni、Fe、Cu的金属活动性由强到弱的顺序为 。
(5)已知Fe3+和Ni2+开始沉淀和完全沉淀时的pH如下表。“除铁”过程中加入NaOH溶液的目的是通过调节
溶液的pH使Fe3+完全沉淀而Ni2+不沉淀,则pH的范围是 。
开始沉淀时的pH 完全沉淀时的pH
Fe3+ 2.7 3.2
Ni2+ 7.2 8.7
【答案】(1)引流
(2)将镍、铁完全反应
(3)H O
2
(4)Fe>Ni>Cu
(5)3.2~7.2
【详解】(1)过滤时,玻璃棒的作用为引流;
(2)“酸浸”时加入过量稀硫酸,是为了将镍和铁完全反应;
(3)依据质量守恒定律,反应前后,原子的种类和个数不变,等号左边有2Fe、3S、4H和14O,等号右
边除2X外,有2Fe、3S和12O,则2X中含有4H和2O,则X的化学式为HO;
2
(4)结合流程可知,加入向滤液Ⅱ加入铁粉能置换出镍,则说明铁比镍活泼,在金属活动性顺序中,铁>
氢>铜,则金属活动性顺序铁>镍>铜;
(5)由于Fe3+完全沉淀时pH为3.2,而Ni2+开始沉淀时的pH为7.2,则若想使Fe3+完全沉淀而Ni2+不沉淀,pH的范围为3.2~7.2。
16.(6+3分)某学习小组对铁锈蚀进行探究
【提出问题】铁锈蚀与哪些因素有关?
【查阅资料】资料1:氯化钙固体可作干燥剂。 资料2:常温常压下,H 的密度是 d g/mL。
2
资料3:一定条件下,碳可加快铁的锈蚀,但碳本身不参加反应。
【设计与实验】
实验一:取四枚相同的洁净无锈铁钉分别放入试管,进行下图实验,现象如表。
试 一周后现
管
象
A 铁钉表面有一层铁锈
B 铁钉表面无明显变化
C 铁钉表面无明显变化
D 铁钉表面有较厚铁锈
(1)对比A、B、C试管中实验现象,说明铁锈蚀与空气中的 发生化学反应。
(2)试管B中植物油的作用是 。
(3)铁锈蚀后应及时除锈,但铝制品不需要除锈的原因是 。
实验二:小组设计了如图装置,检查气密性,将5g铁粉和2g的碳粉加入三颈烧瓶,t 时刻加入2 mLNaC1
1
溶液后,再将一只装有5mL稀盐酸的注射器插到烧瓶上,采集数据。
(4)如图对三颈烧瓶检查装置气密性,应先封闭左右支管口,然后进行的操作和结果为: 。
(5)据图分析,对比AB段和BC段说明 。
(6)分析t-t 时刻压强突然变大的原因是 。
3 4
实验三:测定剩余固体中铁锈的含量
将实验二烧瓶中剩余物质过滤、洗涤、干燥,得mg固体,连接如图装置,检查气密性,加入固体与足量
稀盐酸进行实验。【若正确回答下列问题加3分,总分不超过40分】
(7)完全反应后,常温常压下测得生成气体体积为VmL,则该剩余固体中铁锈的质量分数表达式为
。
【反思与评价】
(8)与实验一试管D对比,实验二铁锈蚀明显更快的原因可能是 (写一点即可)
【答案】(1)氧气和水
(2)隔绝氧气,防止氧气溶于水
(3)常温下,铝在空气中与氧气反应,生成一层致密的氧化膜覆盖在铝的表面,防止铝进一步被氧化
(4)向上拉注射器活塞,松手后,注射器恢复原来位置,则说明该装置气密性良好
(5)NaCl会加快铁的锈蚀
(6)铁与盐酸反应产生氢气
(7)
(8)使用铁粉和加入碳粉,加快了铁锈蚀的速率
【详解】(1)A中铁钉与氧气和水接触,生锈;B中铁钉只与蒸馏水接触,不生锈;C铁钉只与氧气接触,
不生锈。对比ABC 可以得出,铁锈蚀与空气中的氧气和水发生化学反应;
(2)氧气不易溶于水,为了减小实验误差,可以往试管B中,加入植物油,隔绝氧气,防止其溶于水;
(3)铁锈蚀后应及时除锈的原因是铁锈疏松多孔,能吸附氧气和水蒸气,会加快铁的锈蚀,因此铁锈蚀
后应及时除锈;
常温下,铝在空气中与氧气反应,生成一层致密的氧化膜覆盖在铝的表面,防止铝进一步被氧化,所以铝
制品不需要除锈;
(4)如图对三颈烧瓶检查装置气密性,应先封闭左右支管口,向上拉注射器活塞,松手后,注射器恢复
原来位置,则说明该装置气密性良好;
(5)对比AB段和BC段说明加氯化钠溶液前,铁锈蚀慢,加入氯化钠后,压强下降的多,铁锈蚀快,即
NaCl会加快铁的锈蚀;
(6)铁锈蚀消耗氧气,装置内压强减小,注射器内盐酸被吸入烧瓶,铁与盐酸反应产生较多氢气,所以t
3
时刻压强突然变大,该反应的化学方程式为Fe+2HCl=FeCl +H ↑;
2 2
(7)生成氢气质量=VmL×dg/mL=Vdg,设铁的质量为x,
, ,解得x=28Vdg;
由于一定条件下,碳可加快铁的锈蚀,但碳本身不参加反应,所以mg固体中仍含有2g碳粉。所以铁锈质量=mg-2g-28Vdg。因此,该固体中铁锈质量分数表达式为: ;
(9)实验一是铁钉,实验二是铁粉,增大了反应物之间的接触面积,且加入了碳粉,加速了铁的锈蚀,
实验二铁锈蚀明显更快的原因是使用铁粉和加入碳粉,加快了铁锈蚀的速率。
17.(6分)氮化镁( )是制造特殊陶瓷的原料,可用镁条在氮气中燃烧获得,其主要反应为
。
(1)若用36kg镁,最多可得到氮化镁的质量是多少?(根据化学方程式进行计算)
(2)空气中氮气的含量远大于氧气的含量,而镁条在空气中燃烧产物主要是氧化镁,原因是 。
【答案】(1)解:设最多可得到氮化镁的质量为x
答:最多可得到氮化镁的质量为50kg。
(2)氧气化学性质比氮气更活泼,镁条更容易与氧气发生反应
【详解】(1)见答案;
(2)空气中氮气的含量远大于氧气的含量,而镁条在空气中燃烧产物主要是氧化镁,原因是氧气化学性
质比氮气更活泼,镁条更容易与氧气发生反应。