文档内容
2024 年中考第一次模拟考试(无锡卷)
化 学
(考试时间:100分钟 试卷满分:80分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Mg-24 Cl-35.5 Fe-56 Cu-64
一、单项选择题(本大题包括20小题,每小题有四个选项,其中只有一个选项符合题意,请将符合题意的
选项代号填在相应位置上。1~10题每小题1分,11~20题每小题2分,共30分)
1.2023年8月24日,日本政府将福岛核电站污水(含有高浓度放射性且难以消除的物质)排入大海。这
个决定挑战了人类良知的底线,震惊了整个世界。对于此次事件,下列说法正确的是
A.核废水和普通的海水没有区别,可以直接排入大海
B.核废水的排放入海会对整个海洋环境造成严重破坏,应慎重考虑
C.对于核废水,我们可以通过肥皂水来加以鉴别
D.核废水可通过沉淀、过滤、吸附、消毒进行净化为自然界的天然水
2.下列物质混合,充分搅拌后能形成无色溶液的是
A.植物油与水 B.碘与酒精 C.面粉与水 D.食盐与水
3.“一带一路”是跨越时空的宏伟构思,赋予古丝绸之路崭新的时代内涵。古丝绸之路将中国的发明和
技术传送到国外。下列不涉及化学变化的是
A.蚕丝织布 B.使用火药 C.炼制丹药 D.冶炼金属
4.下列化学用语正确的是
A.保持氧气化学性质的最小粒子:O B.氧化铁:FeO
C.2个镁离子:2Mg2+ D.60个碳原子:C
60
5.镍具有很好的可塑性、耐腐蚀性和磁性,因此广泛用于飞机、雷达等各种军工制造业。如图是镍元素
的原子结构示意图及其在元素周期表中的相关信息。下列说法错误的是
A.镍原子质子数为28
B.镍原子核外有4个电子层
C.镍原子结构示意图中m=28,n=16
D.镍原子在化学反应中易得到电子形成阴离子
6.树状分类法是日常生活和科学研究中常用的一种方法。如图所示的是一种树状分类的运用实例。下表
所列的分类与图示分类相符的是
选
甲 乙 丙 丁 图示
项二氧化碳与氢氧 盐酸与氧化铁反 硫酸铜与氢
A 复分解反应
化钠反应 应 氧化钠反应
B 化合物 氧化物 酸 碱
C 溶液 石灰水 食盐水 蒸馏水
D 盐酸的用途 金属除锈 制造药物 与铁反应
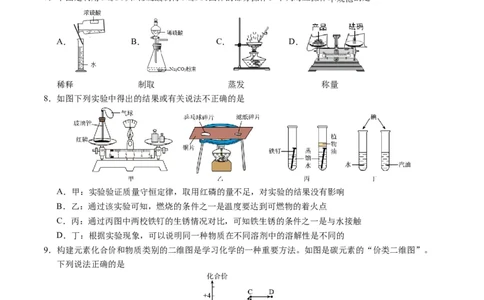
7.下图是利用NaCO 和稀硫酸制得NaSO 固体的部分操作。下列对应操作不规范的是
2 3 2 4
A. B. C. D.
稀释 制取 蒸发 称量
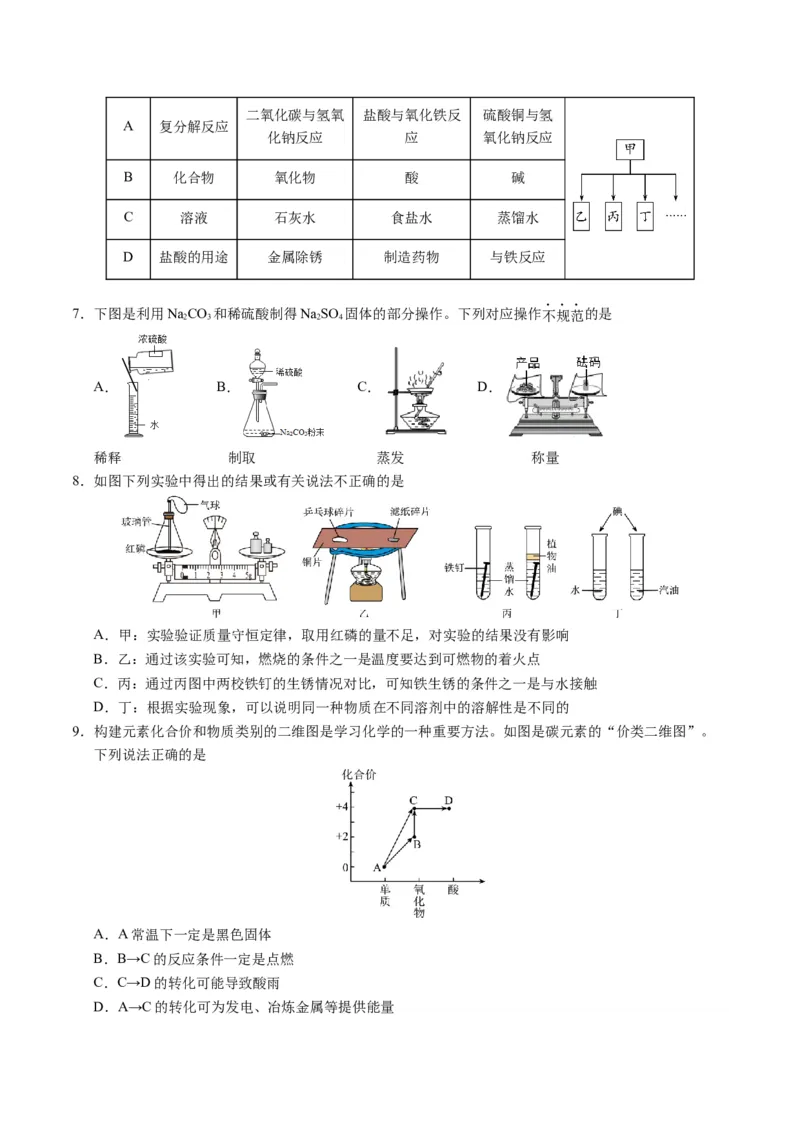
8.如图下列实验中得出的结果或有关说法不正确的是
A.甲:实验验证质量守恒定律,取用红磷的量不足,对实验的结果没有影响
B.乙:通过该实验可知,燃烧的条件之一是温度要达到可燃物的着火点
C.丙:通过丙图中两校铁钉的生锈情况对比,可知铁生锈的条件之一是与水接触
D.丁:根据实验现象,可以说明同一种物质在不同溶剂中的溶解性是不同的
9.构建元素化合价和物质类别的二维图是学习化学的一种重要方法。如图是碳元素的“价类二维图”。
下列说法正确的是
A.A常温下一定是黑色固体
B.B→C的反应条件一定是点燃
C.C→D的转化可能导致酸雨
D.A→C的转化可为发电、冶炼金属等提供能量10.“宏观-微观-符号”三重表征是化学独特的表示物质及其变化的方法。下图是金属钠投入水中所发生
反应的微观示意图。下列叙述正确的是
A.钠原子在该反应过程中得到电子
B.氢氧化钠由氢氧化钠分子构成
C.该反应的化学方程式是
D.参加反应的物质的微粒个数比为1:1
11.在给定条件下,下列物质间的转化能一步实现的是
A. B.C HOH CO
2 5 2
C. D.
12.化学学习者常用化学学科观念去认识和理解世界,下列说法错误的是
A.变化与守恒:某物质在氧气中充分燃烧后生成CO 和HO,推知该物质中含有碳、氢、氧元素
2 2
B.模型与推理:碱溶液能使酚酞溶液变红,NaOH是碱,可知 NaOH 溶液能使酚酞溶液变红
C.宏观与微观:金刚石和石墨物理性质差异很大,是因为构成它们的碳原子排列方式不同
D.探究与创新:将燃着的镁条伸入充满CO 的集气瓶中,镁条继续燃烧,瓶壁出现黑色物质,可推
2
知 CO 在一定条件下可以支持燃烧
2
13.胰蛋白酶是我国自主研发新冠疫苗的原料之一,其中一种胰蛋白酶的化学式为 。下列关于
这种胰蛋白酶的说法正确的是
A.胰蛋白酶由四种非金属元素组成的化合物
B.胰蛋白酶完全燃烧只生成 和
C.胰蛋白酶中氢、氧元素的质量比为5:4
D.胰蛋白酶由6个碳原子、15个氢原子、12个氧原子、3个磷原子构成
14.某化学兴趣小组的同学利用如图微型实验装置进行探究实验。先挤压右侧滴管,使液体A与固体D接
触,产生大量气泡,同时微热燃烧管,观察到纸屑先于木屑燃烧,然后挤压左侧滴管滴下液体,也产
生气泡,同时纸屑和木屑均熄灭。下列说法不正确的是
A.该实验可证明木屑的着火点高于纸屑
B.该装置的优点有:操作简单、节约药品、现象明显
C.实验过程中产生的CO,可以通入足量的氢氧化钠溶液
中进行反应
D.液体B和固体C可以是稀盐酸和石灰石(或大理石)
15.下列各组离子在pH=1的溶液中能大量共存的是
A.Cu2+、OH-、Cl-、Ba2+ B. 、K+、Na+、
C. 、 、Na+、Cl- D.Ag+、 、Cl-、Na+16.下列实验操作中能达到实验目的是
选项 实验目的 实验方案
A 除去CO 中的CO 通入过量O,点燃
2 2
B 分离硝酸钾与氯化钠 溶解、过滤、蒸发
C 鉴别(NH )SO 固体和NH NO 固体 分别加入熟石灰研磨,闻气味
4 2 4 4 3
检验氢氧化钠溶液中是否含有少量的碳酸
D 取样,加入适量稀盐酸
钠
17.化学小组的同学欲探究某固体混合物A的成分,已知A中可能含有NaCl、CaCO 、CuSO 、(NH )SO
3 4 4 2 4
四种物质中的两种或多种,按下图所示进行探究实验,根据实验过程和图示信息,以下推理结果不正
确的是
A.气体B是NH B.滤液F中一定含CaCl
3 2
C.白色沉淀G是BaSO D.A中肯定不存在CuSO 和NaCl
4 4
18.煤化工废水中含有NaCl、NaSO 、NaNO ,这三种盐的溶解度曲线如图所示。下列有关说法正确的是
2 4 3
A.与NaNO 相比,NaCl更适合通过饱和溶液降温结晶得到
3
B.a℃时,NaNO 的饱和溶液,溶质的质量分数为80%
1 3
C.a℃,NaCl和NaSO 的饱和溶液,溶质质量分数相等
1 2 4
D.40℃时,NaSO 的饱和溶液,升温到60℃变为不饱和溶液
2 4
19.一定质量的CH 可与常见物质M反应(M为黑色固体,其中有一种元素的化合价为+2价),同时放
4
出少量热量;将所得产物Cu O与O 反应又生成M,同时放出较多热量。其反应原理如下图所示,
2 2
“→”代表反应生成。下列说法正确的是
①Cu O中Cu元素化合价为-1价
2
②根据上面的反应,理论上反应每生成44gCO,同时生成36gHO
2 2
③根据上面的反应,理论上每144gCu O参与反应,最终消耗32gO
2 2④M中铜元素的质量分数比Cu O中的低
2
⑤以上两个反应有一个是化合反应,有一个是分解反应
⑥在上述反应中参加循环的物质有两种
A.②④⑥ B.①③⑥ C.②③⑤ D.③④⑥
20.现有MgCO 和BaCO 组成的固体混合物5 g,将其加入50 g某浓度的稀盐酸中恰好完全反应,得到不
3 3
饱和溶液的质量为52.8 g,则下列说法中,不正确的是
A.过程中产生CO 总质量为2.2g B.Mg、Ba元素的质量之和为2g
2
C.所用盐酸的质量分数为7.3% D.所得溶液中溶质的质量为6.65g
二、非选择题:本大题包括8小题,共50分。
21.(5分)“化”说五味。
(1)酸:酸脆爽口的醋溜黄瓜深受人们喜爱。食醋中因含有大量的 ,所以食醋呈酸性。
(2)甜:食物的甜味主要来自于糖类,糖类物质 (选填“一定”或“不一定”)有甜味。
(3)苦:鱼胆胆汁中含有具有苦味且难溶于水的胆汁酸。在沾有胆汁的鱼肉上涂抹白酒可去除苦味,
说明物质的溶解性与 (选填“溶质”或“溶剂”)的种类有关。
(4)辣:辣椒最适宜在pH6.2~7.2的土壤中种植,若某地区土壤pH=5.2,想种植辣椒,可撒
降低土壤酸性。
(5)咸:食盐主要成分为氯化钠,它由 (填“分子”、“原子”或“离子”)构成。
22.(4分)水是生命之源,可由多种途径获得水。
I.空气制水机能充分利用大气中的水分制出饮用水,其工作原理如下:
(1)①中可阻挡直径 (填“大于”或“小于”)滤孔直径的物质。
(2)③中需吸附色素和异味,常用的物质是 。
II.蒸馏法和膜分离法(如图)是两种常用的海水淡化方法。
(3)图中,加压后钠离子、镁离子等不能通过反渗透膜。
①图中微粒属于原子团的是 。
②一段时间后装置左侧海水中溶质的质量分数会 (填“增大”、“减小”或“不变”)。
23.(4分)化学就在我们身边,人类的生活离不开化学。
(1)葡萄糖酸锌(化学式为 )口服液可用于补锌。组成葡萄糖酸锌的元素中,属于常量元
素的是 (填元素符号)。
(2)郁铭芳院士是我国化纤领域奠基人,他纺出了我国第一根合成纤维。下列属于合成纤维的是
_______(填字母)。
A.涤纶B.蚕丝 C.腈纶 D.尼龙
(3)2021年9月我国科学家利用 人工合成了淀粉,其中关键一步是用 制取甲醇(化学式为),其反应的微观示意图如下。
①该反应的化学方程式是 。
②甲、乙、丙、丁四种物质中,属于有机物的是 。
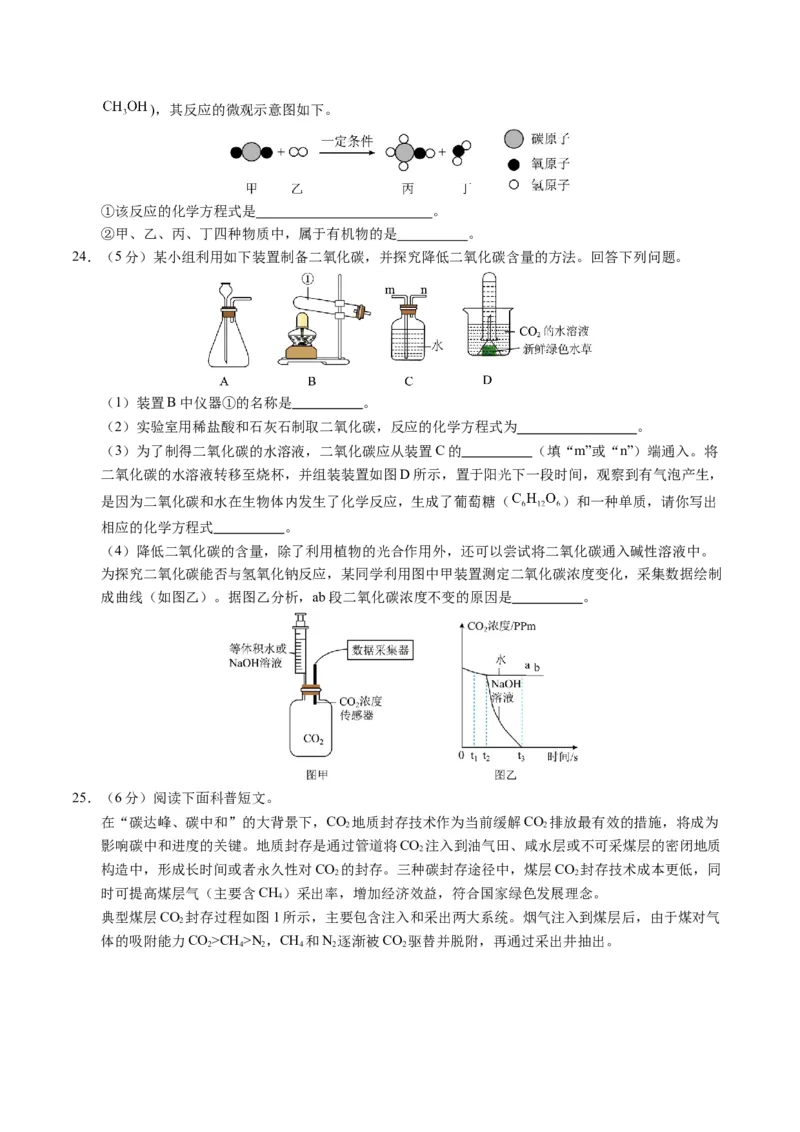
24.(5分)某小组利用如下装置制备二氧化碳,并探究降低二氧化碳含量的方法。回答下列问题。
(1)装置B中仪器①的名称是 。
(2)实验室用稀盐酸和石灰石制取二氧化碳,反应的化学方程式为 。
(3)为了制得二氧化碳的水溶液,二氧化碳应从装置C的 (填“m”或“n”)端通入。将
二氧化碳的水溶液转移至烧杯,并组装装置如图D所示,置于阳光下一段时间,观察到有气泡产生,
是因为二氧化碳和水在生物体内发生了化学反应,生成了葡萄糖( )和一种单质,请你写出
相应的化学方程式 。
(4)降低二氧化碳的含量,除了利用植物的光合作用外,还可以尝试将二氧化碳通入碱性溶液中。
为探究二氧化碳能否与氢氧化钠反应,某同学利用图中甲装置测定二氧化碳浓度变化,采集数据绘制
成曲线(如图乙)。据图乙分析,ab段二氧化碳浓度不变的原因是 。
25.(6分)阅读下面科普短文。
在“碳达峰、碳中和”的大背景下,CO 地质封存技术作为当前缓解CO 排放最有效的措施,将成为
2 2
影响碳中和进度的关键。地质封存是通过管道将CO 注入到油气田、咸水层或不可采煤层的密闭地质
2
构造中,形成长时间或者永久性对CO 的封存。三种碳封存途径中,煤层CO 封存技术成本更低,同
2 2
时可提高煤层气(主要含CH)采出率,增加经济效益,符合国家绿色发展理念。
4
典型煤层CO 封存过程如图1所示,主要包含注入和采出两大系统。烟气注入到煤层后,由于煤对气
2
体的吸附能力CO>CH >N ,CH 和N 逐渐被CO 驱替并脱附,再通过采出井抽出。
2 4 2 4 2 2研究人员为了找吸附能力最强的煤,对不同的煤在相同条件下吸附CO 的能力进行研究,结果如图2
2
所示。然而,煤层CO 封存也涉及多种安全风险。如CO 注入后,易引发地质体结构失稳,导致CO
2 2 2
泄露,使土壤、水酸化,破坏周围的生态环境,对人类健康产生影响。
依据文章内容回答下列问题。
(1)CO 地质封存的途径主要有煤层封存、 。
2
(2)图1中,通常是先将CO 由气态压缩成超临界流体再注入。从微观角度分析,这一过程中发生变
2
化的是 。
(3)判断下列说法是否正确(填“对”或“错”)。
①煤层CO 封存成本较低,同时可实现煤层气高效采收。 。
2
②CO 对环境的危害是形成酸雨。 。
2
(4)对比图2中的四条曲线,得出的结论是: 。
26.(8分)某兴趣小组利用废镍材料(含有金属Ni及少量Fe、Ag、Fe O)探究相关物质的性质并回收
2 3
镍,设计流程如图所示。
资料:a.HO 溶液可将Fe2+转化为Fe3+。
2 2
b.Fe2+、Fe3+、Ni2+转化为对应的氢氧化物沉淀时,溶液pH有如图关系:
(1)废镍材料“粉碎”的目的是 。
(2)“酸浸”中发生的反应化学方程式除 、 、还有
(填化学方程式),该反应属于 反应(填基本反应类型);X是 (填名称)。
(3)在“转化1”中,加入试剂先后顺序是______(填字母)。
A.先加HO 溶液,再加NaOH溶液 B.先加NaOH溶液,再加HO 溶液
2 2 2 2
(4)在“转化1”中,加NaOH溶液调节pH为 (填范围),操作A是 。
(5)Ni、Fe、Ag三种金属的活动性由强到弱的顺序为 。
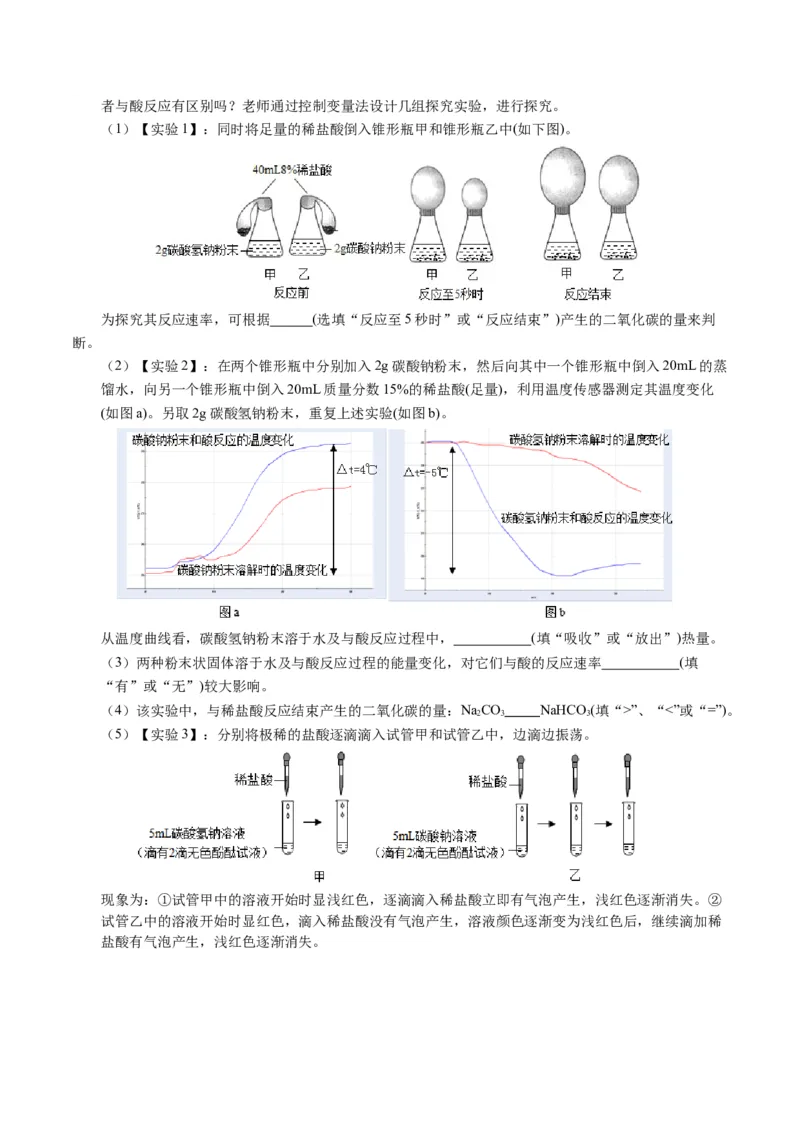
27.(7分)碳酸钠、碳酸氢钠是我们初中化学中两种常见的碳酸盐,它们与酸反应的情形非常相似。两者与酸反应有区别吗?老师通过控制变量法设计几组探究实验,进行探究。
(1)【实验1】:同时将足量的稀盐酸倒入锥形瓶甲和锥形瓶乙中(如下图)。
为探究其反应速率,可根据 (选填“反应至5秒时”或“反应结束”)产生的二氧化碳的量来判
断。
(2)【实验2】:在两个锥形瓶中分别加入2g碳酸钠粉末,然后向其中一个锥形瓶中倒入20mL的蒸
馏水,向另一个锥形瓶中倒入20mL质量分数15%的稀盐酸(足量),利用温度传感器测定其温度变化
(如图a)。另取2g碳酸氢钠粉末,重复上述实验(如图b)。
从温度曲线看,碳酸氢钠粉末溶于水及与酸反应过程中, (填“吸收”或“放出”)热量。
(3)两种粉末状固体溶于水及与酸反应过程的能量变化,对它们与酸的反应速率 (填
“有”或“无”)较大影响。
(4)该实验中,与稀盐酸反应结束产生的二氧化碳的量:NaCO NaHCO (填“>”、“<”或“=”)。
2 3 3
(5)【实验3】:分别将极稀的盐酸逐滴滴入试管甲和试管乙中,边滴边振荡。
现象为:①试管甲中的溶液开始时显浅红色,逐滴滴入稀盐酸立即有气泡产生,浅红色逐渐消失。②
试管乙中的溶液开始时显红色,滴入稀盐酸没有气泡产生,溶液颜色逐渐变为浅红色后,继续滴加稀
盐酸有气泡产生,浅红色逐渐消失。【反思】在【实验3】碳酸钠溶液中逐滴滴入稀盐酸,为何刚开始没有气泡产生?研究小组查阅资料,
绘制出微观示意图。
①结合图示,用化学方程式解释刚开始没有气泡的原因 。
②相同浓度的碳酸氢钠溶液和碳酸钠溶液的碱性:碳酸氢钠 碳酸钠(填“>”、“<”或“=”)。
28.(11分)金属铁及其制品是现代生活中不可缺少的材料和工具,在生产和生活中的应用极为广泛。请
用所学化学知识回答下列问题:
I.铁与铁的化合物
(1)金属在生产和生活中有着广泛的用途,铁是目前世界上使用最多的金属。下图是铁原子的结构
示意图,其最外层电子数为 。
(2)铁的化合物在现代更多领域发挥着重要作用其中碳酸亚铁(FeCO)不溶于水,可作补血剂,服用
3
后与胃酸反应生成的物质被人体吸收,能促进血红蛋白的生成,写出碳酸亚铁与胃酸反应的化学方程
式 。
Ⅱ.钢铁的冶炼
《天工开物》中记载的“炒钢法”,该方法的生产过程如图所示。
资料:潮泥灰主要成分是石灰石。
(3)在炼铁炉中鼓入的空气与矿物逆流而行的目的是 。
(4)不断翻炒液态生铁,是为了降低 元素的含量。
III.金属的锈蚀
(5)铁生锈的原理:
写出Fe(OH) 转化为Fe(OH) 的化学方程式 。
2 3
(6)某小组同学利用手持数据采集器,测定铁钉与不同溶液(浓度相等)接触生锈时氧气浓度的变化,
装置及数据如图:①实验所用三种溶液中,铁钉接触到 溶液(填化学式)更容易生锈。
②根据三条曲线都是“先陡后缓”的现象。关于铁生锈快慢的问题,你能得出的结论是 。
IV.拓展:测定还原性铁粉的组成
还原性铁粉中含有少量FexCy,小组同学在老师的指导下进行以下实验。
【资料】:①Fe,FexCy在加热时与O 反应能生成相应氧化物。
2
②FexCy不与酸反应。
③碱石灰的主要成分是氧化钙与氢氧化钠的混合物
【实验1】:取29.80g样品,加入足量稀HSO ,充分反应后生成1.00gH 。
2 4 2
【实验2】:另取29.80g样品,按如图进行实验。
实验后A中固体全部变为红棕色,装置B的质量增加了0.44g。
(7)A中红棕色固体的化学式是 。
(8)FeC 中,x:y= 。
x y
(9)若用空气(过量)替代O 进行实验,测得x:y的值 (填偏大、偏小或不变),可能的原因
2
是 。