文档内容
2024 年中考第三次模拟考试(无锡卷)
化 学
(考试时间:100分钟 试卷满分:80分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
4.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 S-32 Cl-35.5 Ca-40
一、选择题(本题包括 20小题,每小题只有1个选项符合题意。1~10题每小题1分,11~20题每小题2分,
共30分)
1.下列物质属于氧化物的是
A.O B.Mg(OH) C.NaSO D.CuO
2 2 2 4
2.我国明代《本草纲目》记载了烧酒的制造工艺:“凡酸坏之酒,皆可蒸烧”,“以烧酒复烧二次价值
倍也”。这里用到的实验方法可用于分离
A.植物油和水 B.食盐水和泥沙
C.酒精和水 D.硝酸钾和硫酸钠
3.“垃圾分类工作就是新时尚”。废旧报纸应投入的垃圾箱是
A. B. C. D.
4.草木灰的主要成分为碳酸钾,碳酸钾属于
A.酸 B.碱 C.盐 D.氧化物
5.下列仪器中不可加热的是
A.试管 B.烧杯 C.量筒 D.蒸发皿
6.下列能反映水在空气中放置时发生变化的微观图示的是:注:(图中 表示氧原子, 表示氢原子)。
A. B. C. D.
7.下列化学用语表达正确的是
A.一氧化碳:CoB.硝酸铵中的阳离子:
C.2个氢原子:2H
D.氧化镁中镁元素的化合价:
8.下列有关CO 实验的图示正确的是( )
2
A.制取CO B.收集CO C.验证CO 已集满 D.验证CO 能与水反应
2 2 2 2
9.下列物质的名称、俗称、化学式表示正确的是
A.乙醇、酒精、CHCOOH B.氢氧化钙、消石灰、Ca(OH)
3 2
C.氢氧化钠、纯碱、NaCO D.氧化钙、石灰石、Ca
2 3
10.《茉莉花》是一首脍炙人口的苏南民歌。茉莉花香气的成分有多种,乙酸苯甲酯(C H O) 是其中的一
9 10 2
种。下列关于乙酸苯甲酯的说法正确的是
A.乙酸苯甲酯的相对分子质量为150g
B.乙酸苯甲酯由碳、氢、氧三种元素组成
C.乙酸苯甲酯中碳、氢、氧三种元素质量比为9: 10: 2
D.乙酸苯甲酯分子由碳原子、氢原子、氧分子构成
11.下列叙述正确的是
A.用小苏打治疗胃酸过多 B.用氢氧化钠改良酸性土壤
C.用铁桶长时间存放硫酸铜溶液 D.用食盐水除去热水瓶中的水垢
12.下列物质的转化在给定条件下均能实现的是
A. B.
C. D.
13.镁在国防工业中应用广泛,镁元素的相关信息如下图所示,下列有关说法正确的是
A.镁属于非金属元素
B.镁的相对原子质量是24.31g
C.镁原子得到两个电子变为Mg2+
D.镁原子的质子数是12
14.下列实验操作能达到实验目的的是
选项 物质 目的 主要实验操作A H、CH 鉴别 点燃,在火焰上方罩一个干冷的烧杯,观察现象
2 4
NaOH溶液中混有
B 除杂 加入适量的CaCl 溶液,振荡、静置、过滤
2
NaCO
2 3
NaCO 溶液中是否含
2 3
C 检验 取样,滴加BaCl 溶液,观察现象
2
有NaSO
2 4
KNO 和Ba(NO ) 先加入过量的KCO 溶液,搅拌、静置、过滤、洗涤,再分别
3 3 2 2 3
D 分离
的混合溶液 向滤液、滤渣中加入适量的稀硝酸,搅拌
15.如图为MgCl 、KCl和MgSO 的溶解度曲线。下列说法正确的是
2 4
A.T℃时,溶解度:S(MgCl )>S(KCl)>S(MgSO )
2 2 4
B.T℃时,将MgSO 、MgCl 固体各30.0g分别溶于50.0g水,则形成MgSO 饱和溶液和MgCl 不饱和溶
2 4 2 4 2
液,前者溶液的溶质质量分数大于后者
C.T℃时,将KCl、MgSO 的饱和溶液分别降温到T℃,两种溶液中均有晶体析出
3 4 2
D.T℃时,将等质量的KCl、MgSO 饱和溶液分别升温到T℃,要使两种溶液均达到饱和,加入的对应
1 4 3
溶质质量相等
16.下列各组溶液,不用其他试剂就不能鉴别出来的是
A.CuCl 、NaOH、MgCl 、HCl
2 2
B.BaCl 、HCl、KCO、HNO
2 2 3 3
C.Ba(OH)、NaCO、KSO 、HNO
2 2 3 2 4 3
D.MgSO 、NaOH、Ba(NO )、HCl
4 3 2
17.经研究发现,利用催化剂可有效消除室内装修材料释放的甲醛。该反应的微观示意图如图所示,下列
有关说法不正确的是
A.生成物中丙、丁的质量比为1:1B.该反应一定有元素的化合价发生变化
C.反应前后催化剂的质量、化学性质均未发生改变
D.1个甲醛分子由1个碳原子、2个氢原子、1个氧原子构成
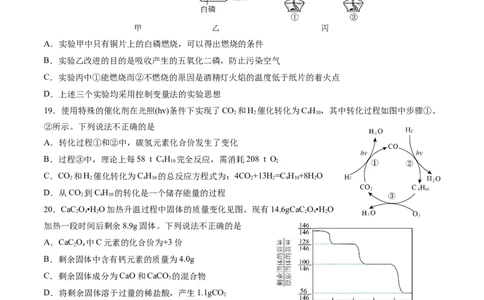
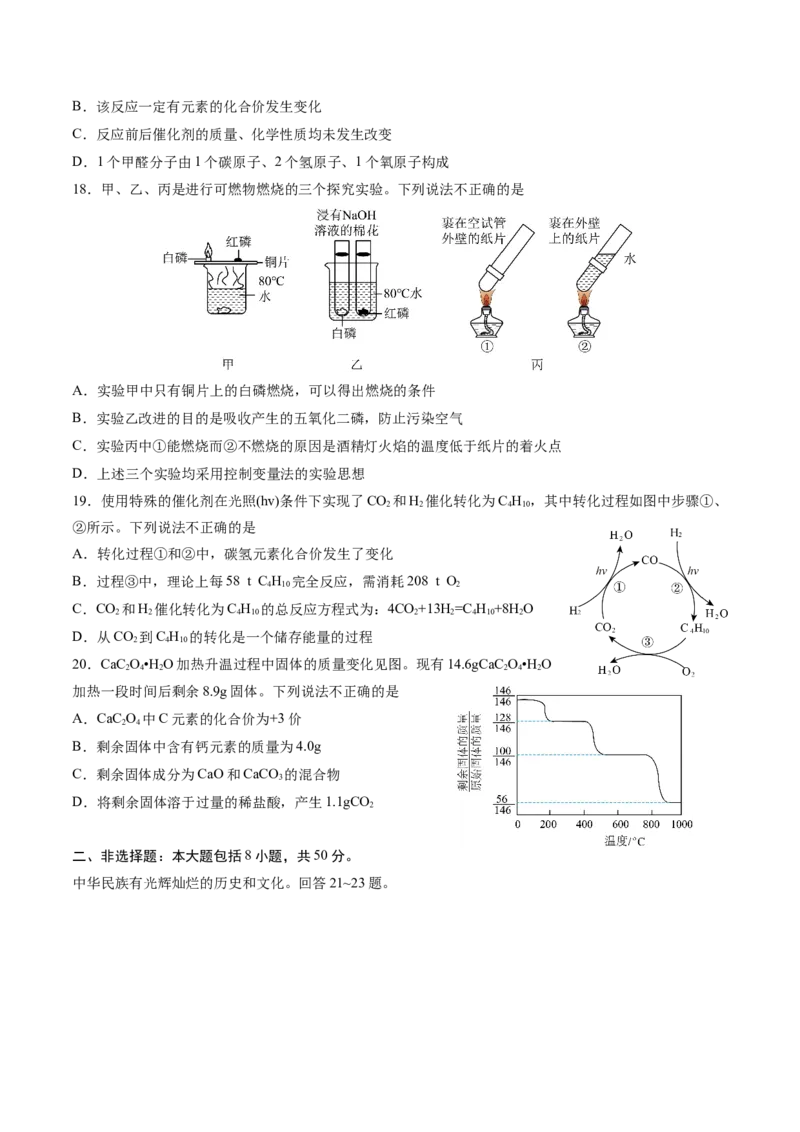
18.甲、乙、丙是进行可燃物燃烧的三个探究实验。下列说法不正确的是
A.实验甲中只有铜片上的白磷燃烧,可以得出燃烧的条件
B.实验乙改进的目的是吸收产生的五氧化二磷,防止污染空气
C.实验丙中①能燃烧而②不燃烧的原因是酒精灯火焰的温度低于纸片的着火点
D.上述三个实验均采用控制变量法的实验思想
19.使用特殊的催化剂在光照(hv)条件下实现了CO 和H 催化转化为C H ,其中转化过程如图中步骤①、
2 2 4 10
②所示。下列说法不正确的是
A.转化过程①和②中,碳氢元素化合价发生了变化
B.过程③中,理论上每58 t C H 完全反应,需消耗208 t O
4 10 2
C.CO 和H 催化转化为C H 的总反应方程式为:4CO+13H =C H +8H O
2 2 4 10 2 2 4 10 2
D.从CO 到C H 的转化是一个储存能量的过程
2 4 10
20.CaC O•H O加热升温过程中固体的质量变化见图。现有14.6gCaC O•H O
2 4 2 2 4 2
加热一段时间后剩余8.9g固体。下列说法不正确的是
A.CaC O 中C元素的化合价为+3价
2 4
B.剩余固体中含有钙元素的质量为4.0g
C.剩余固体成分为CaO和CaCO 的混合物
3
D.将剩余固体溶于过量的稀盐酸,产生1.1gCO
2
二、非选择题:本大题包括8小题,共50分。
中华民族有光辉灿烂的历史和文化。回答21~23题。21.(2分)战国•曾侯乙编钟属于青铜制品。青铜是一种合金,所谓青铜是铜与锡或铅等元素按一定比例
熔铸而成的,颜色呈青,故名青铜。
①加入锡或铅可以 (填“升高”或“降低”)“熔铸”时所需温度。
②通过X射线衍射法检测某铜器表面锈蚀物质的组成为Cu (OH) (CO)。称取73.8g该物质加热使其完全分
x y 3 2
解为三种氧化物,将产物依次用足量的浓硫酸和碱石灰吸收,分别增重了9.0g和8.8g,则该物质的化学式
为 。
22.(2分)秦朝•兵马俑被誉为“世界第八大奇迹”。
①兵马俑用黏土烧制而成的。某种黏土的主要成分为Al Si O(OH) ,将其用氧化物的形式表示为
2 2 5 4
aAl O•bSiO •cH O,则a:b:c= (最简整数比)。
2 3 2 2
②兵马俑彩绘中发现了绝美的“中国紫”,“中国紫”主要成分是硅酸铜钡(BaCuSi O),其中铜元素和硅
2 x
元素的化合价分别为+2价和+4价,则x的值为 。
23.(6分)(1)宋•王希孟《千里江山图》所用纸张为宣纸。
①宣纸的制作过程中会将植物的茎浸泡在水中,加入生石灰、草木灰(主要成分是KCO)、纯碱,写出其
2 3
中发生的一个复分解反应的化学方程式 。
②绘画所用毛笔的笔杆常用竹管制作。竹管的主要成分为纤维素,其化学式为(C H O),纤维素
6 10 5 n
(填“是”或“不是”)高分子化合物。
(2)宋•沈子藩《梅鹊图》所用缂丝中含有桑蚕丝。
①桑蚕丝是一种天然的动物蛋白质纤维,其在催化剂作用下水解的最终产物是 。
②人造丝的主要成分是纤维素。鉴别桑蚕丝和人造丝的方法是 (写出操作、现象和结论)。
24.(6分)氢气是一种极具发展潜力的清洁高效的二次能源,其生产和储存是科学研究的重要方向。目
前制氢的方法主要有化石能源制氢和电解水制氢。氢气的储存有物理储氢和化学储氢。物理储氢包括加压
储氢和吸附储氢。由化石能源制得的H 中含有CO,利用液氮的低温可将CO液化分离,从而获得纯净的
2
氢气。储氢、释氢、用氢过程中涉及的部分物质转化如图1所示:
(1)利用液氮的低温能将H 与CO分离,说明氢气的沸点比CO的沸点 。
2(2)物理储氢:高压气态储氢是广泛应用的储氢技术,即通过高压将氢气液化至氢瓶中加以储存。高压将
氢气液化过程中,发生的改变是 (从微观角度解释)。该技术的优点在于其充装释放氢气速度
快,但其缺点是 。
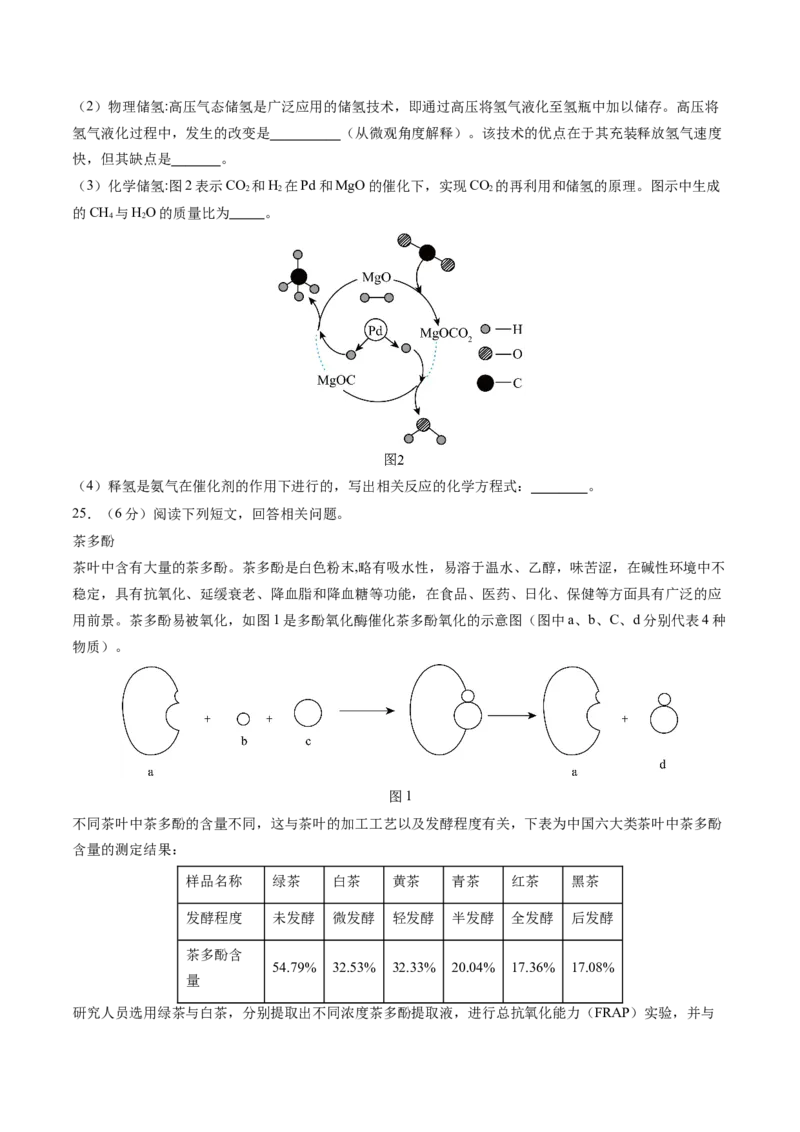
(3)化学储氢:图2表示CO 和H 在Pd和MgO的催化下,实现CO 的再利用和储氢的原理。图示中生成
2 2 2
的CH 与HO的质量比为 。
4 2
(4)释氢是氨气在催化剂的作用下进行的,写出相关反应的化学方程式: 。
25.(6分)阅读下列短文,回答相关问题。
茶多酚
茶叶中含有大量的茶多酚。茶多酚是白色粉末,略有吸水性,易溶于温水、乙醇,味苦涩,在碱性环境中不
稳定,具有抗氧化、延缓衰老、降血脂和降血糖等功能,在食品、医药、日化、保健等方面具有广泛的应
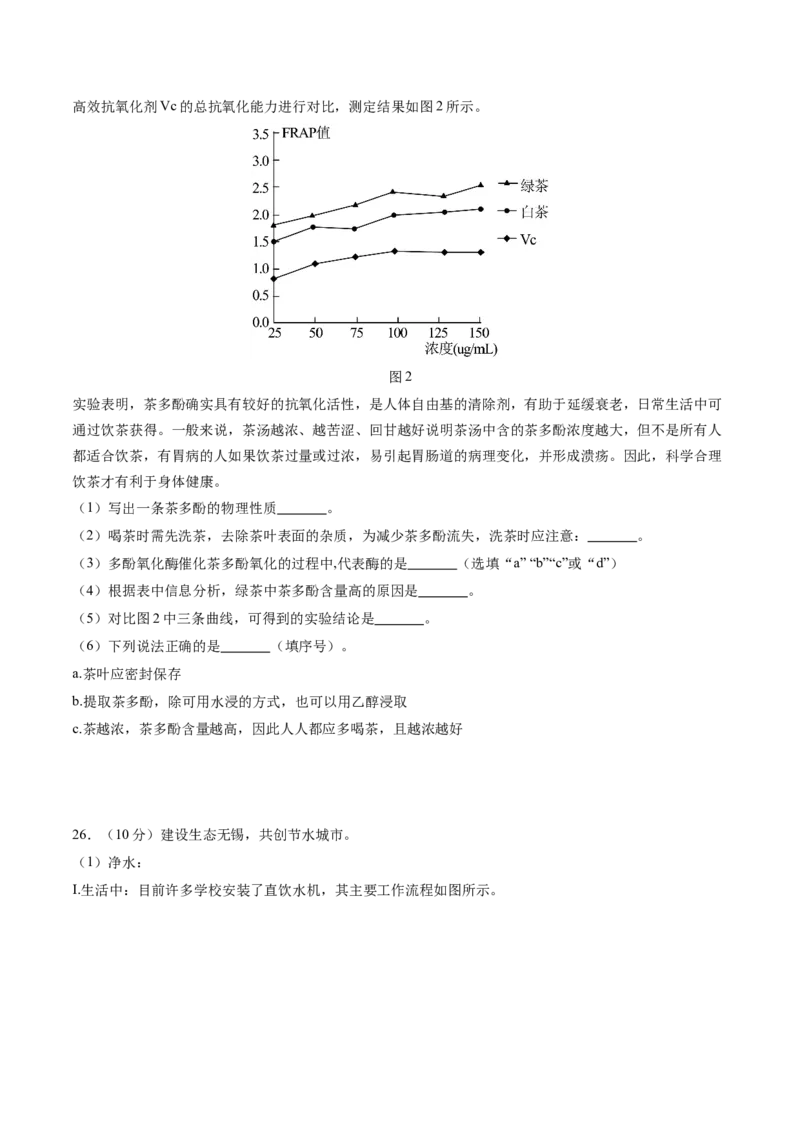
用前景。茶多酚易被氧化,如图1是多酚氧化酶催化茶多酚氧化的示意图(图中a、b、C、d分别代表4种
物质)。
图1
不同茶叶中茶多酚的含量不同,这与茶叶的加工工艺以及发酵程度有关,下表为中国六大类茶叶中茶多酚
含量的测定结果:
样品名称 绿茶 白茶 黄茶 青茶 红茶 黑茶
发酵程度 未发酵 微发酵 轻发酵 半发酵 全发酵 后发酵
茶多酚含
54.79% 32.53% 32.33% 20.04% 17.36% 17.08%
量
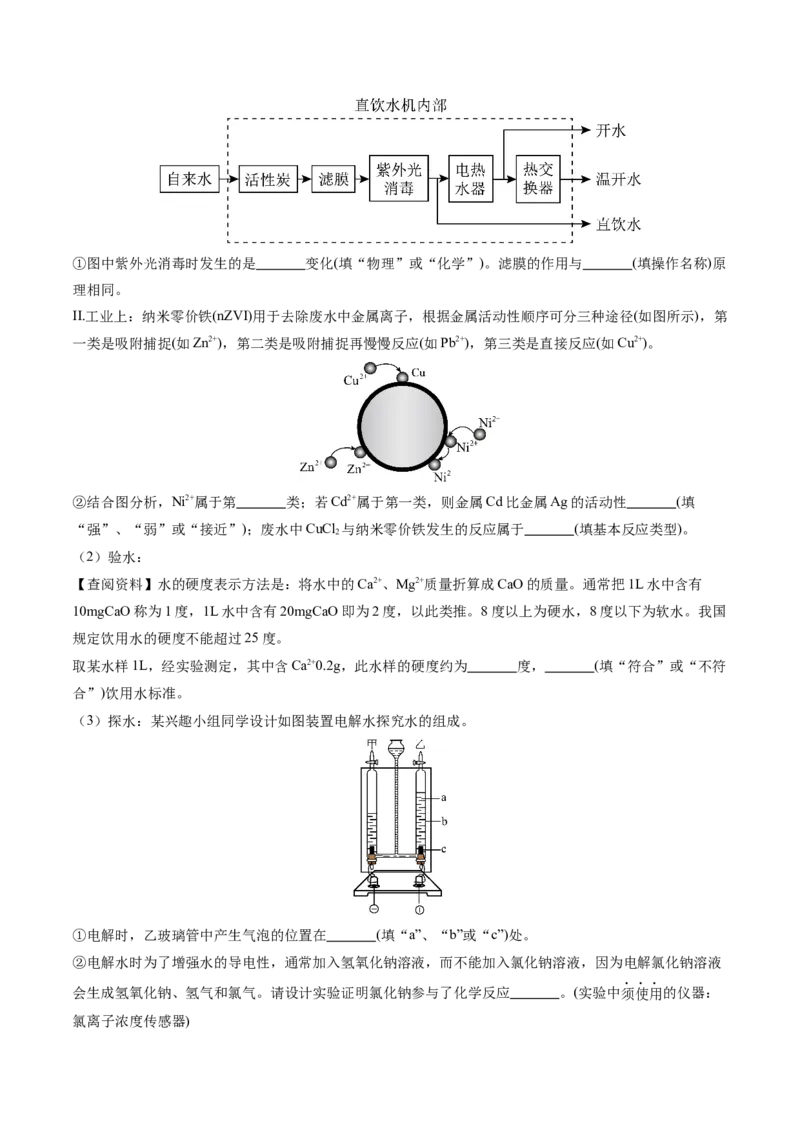
研究人员选用绿茶与白茶,分别提取出不同浓度茶多酚提取液,进行总抗氧化能力(FRAP)实验,并与高效抗氧化剂Vc的总抗氧化能力进行对比,测定结果如图2所示。
图2
实验表明,茶多酚确实具有较好的抗氧化活性,是人体自由基的清除剂,有助于延缓衰老,日常生活中可
通过饮茶获得。一般来说,茶汤越浓、越苦涩、回甘越好说明茶汤中含的茶多酚浓度越大,但不是所有人
都适合饮茶,有胃病的人如果饮茶过量或过浓,易引起胃肠道的病理变化,并形成溃疡。因此,科学合理
饮茶才有利于身体健康。
(1)写出一条茶多酚的物理性质 。
(2)喝茶时需先洗茶,去除茶叶表面的杂质,为减少茶多酚流失,洗茶时应注意: 。
(3)多酚氧化酶催化茶多酚氧化的过程中,代表酶的是 (选填“a” “b”“c”或“d”)
(4)根据表中信息分析,绿茶中茶多酚含量高的原因是 。
(5)对比图2中三条曲线,可得到的实验结论是 。
(6)下列说法正确的是 (填序号)。
a.茶叶应密封保存
b.提取茶多酚,除可用水浸的方式,也可以用乙醇浸取
c.茶越浓,茶多酚含量越高,因此人人都应多喝茶,且越浓越好
26.(10分)建设生态无锡,共创节水城市。
(1)净水:
I.生活中:目前许多学校安装了直饮水机,其主要工作流程如图所示。①图中紫外光消毒时发生的是 变化(填“物理”或“化学”)。滤膜的作用与 (填操作名称)原
理相同。
II.工业上:纳米零价铁(nZVI)用于去除废水中金属离子,根据金属活动性顺序可分三种途径(如图所示),第
一类是吸附捕捉(如Zn2+),第二类是吸附捕捉再慢慢反应(如Pb2+),第三类是直接反应(如Cu2+)。
②结合图分析,Ni2+属于第 类;若Cd2+属于第一类,则金属Cd比金属Ag的活动性 (填
“强”、“弱”或“接近”);废水中CuCl 与纳米零价铁发生的反应属于 (填基本反应类型)。
2
(2)验水:
【查阅资料】水的硬度表示方法是:将水中的Ca2+、Mg2+质量折算成CaO的质量。通常把1L水中含有
10mgCaO称为1度,1L水中含有20mgCaO即为2度,以此类推。8度以上为硬水,8度以下为软水。我国
规定饮用水的硬度不能超过25度。
取某水样1L,经实验测定,其中含Ca2+0.2g,此水样的硬度约为 度, (填“符合”或“不符
合”)饮用水标准。
(3)探水:某兴趣小组同学设计如图装置电解水探究水的组成。
①电解时,乙玻璃管中产生气泡的位置在 (填“a”、“b”或“c”)处。
②电解水时为了增强水的导电性,通常加入氢氧化钠溶液,而不能加入氯化钠溶液,因为电解氯化钠溶液
会生成氢氧化钠、氢气和氯气。请设计实验证明氯化钠参与了化学反应 。(实验中须使用的仪器:
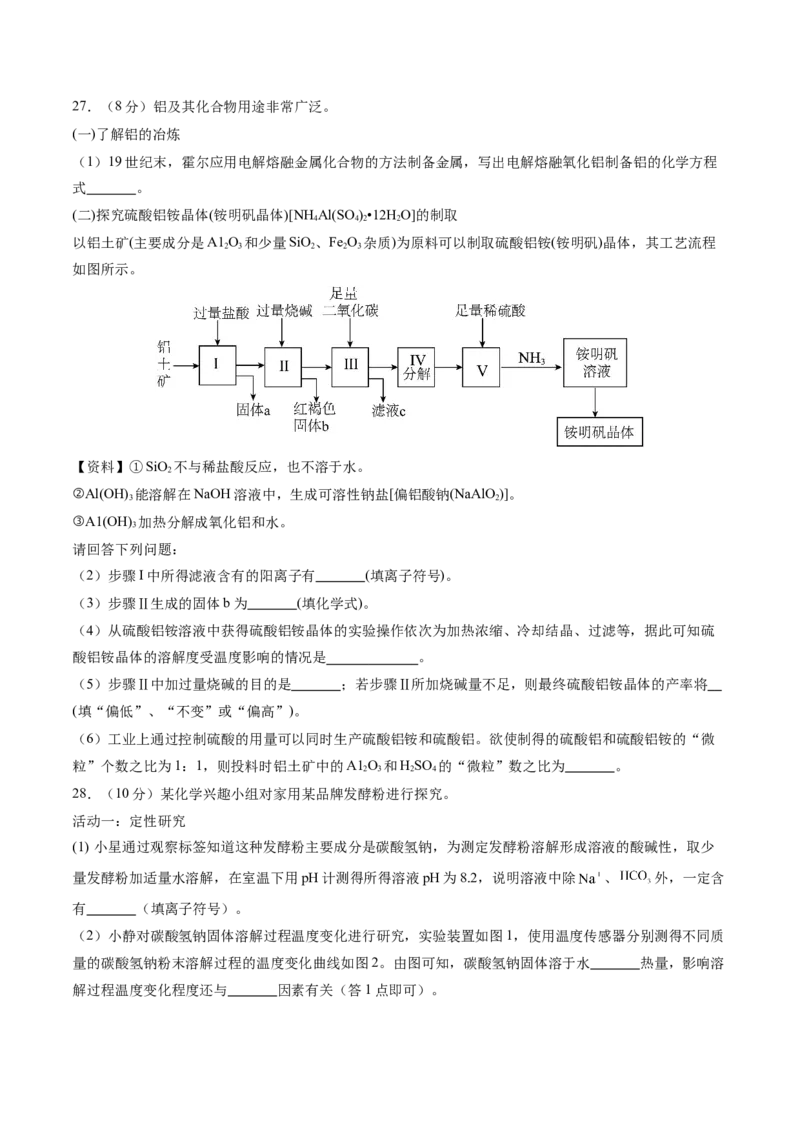
氯离子浓度传感器)27.(8分)铝及其化合物用途非常广泛。
(一)了解铝的冶炼
(1)19世纪末,霍尔应用电解熔融金属化合物的方法制备金属,写出电解熔融氧化铝制备铝的化学方程
式 。
(二)探究硫酸铝铵晶体(铵明矾晶体)[NH Al(SO )•12H O]的制取
4 4 2 2
以铝土矿(主要成分是A1 O 和少量SiO、Fe O 杂质)为原料可以制取硫酸铝铵(铵明矾)晶体,其工艺流程
2 3 2 2 3
如图所示。
【资料】①SiO 不与稀盐酸反应,也不溶于水。
2
②Al(OH) 能溶解在NaOH溶液中,生成可溶性钠盐[偏铝酸钠(NaAlO )]。
3 2
③A1(OH) 加热分解成氧化铝和水。
3
请回答下列问题:
(2)步骤I中所得滤液含有的阳离子有 (填离子符号)。
(3)步骤Ⅱ生成的固体b为 (填化学式)。
(4)从硫酸铝铵溶液中获得硫酸铝铵晶体的实验操作依次为加热浓缩、冷却结晶、过滤等,据此可知硫
酸铝铵晶体的溶解度受温度影响的情况是 。
(5)步骤Ⅱ中加过量烧碱的目的是 ;若步骤Ⅱ所加烧碱量不足,则最终硫酸铝铵晶体的产率将
(填“偏低”、“不变”或“偏高”)。
(6)工业上通过控制硫酸的用量可以同时生产硫酸铝铵和硫酸铝。欲使制得的硫酸铝和硫酸铝铵的“微
粒”个数之比为1:1,则投料时铝土矿中的A1 O 和HSO 的“微粒”数之比为 。
2 3 2 4
28.(10分)某化学兴趣小组对家用某品牌发酵粉进行探究。
活动一:定性研究
(1) 小星通过观察标签知道这种发酵粉主要成分是碳酸氢钠,为测定发酵粉溶解形成溶液的酸碱性,取少
量发酵粉加适量水溶解,在室温下用pH计测得所得溶液pH为8.2,说明溶液中除 、 外,一定含
有 (填离子符号)。
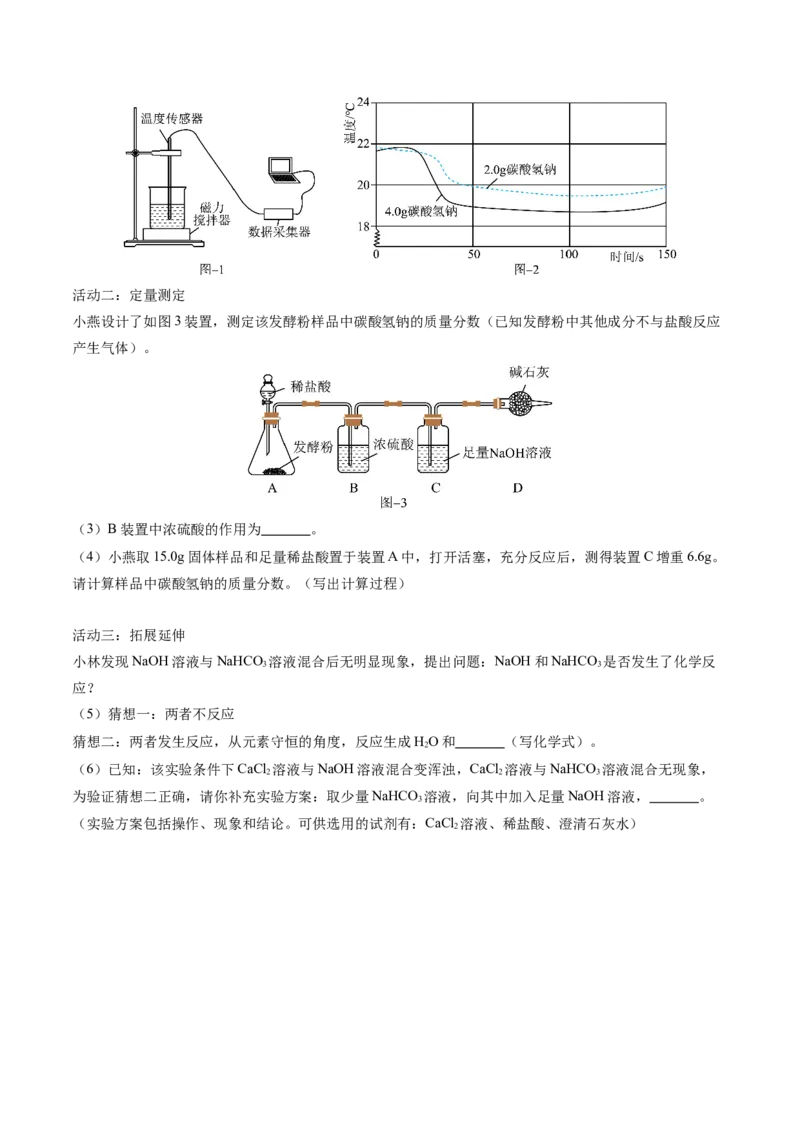
(2)小静对碳酸氢钠固体溶解过程温度变化进行研究,实验装置如图1,使用温度传感器分别测得不同质
量的碳酸氢钠粉末溶解过程的温度变化曲线如图2。由图可知,碳酸氢钠固体溶于水 热量,影响溶
解过程温度变化程度还与 因素有关(答1点即可)。活动二:定量测定
小燕设计了如图3装置,测定该发酵粉样品中碳酸氢钠的质量分数(已知发酵粉中其他成分不与盐酸反应
产生气体)。
(3)B装置中浓硫酸的作用为 。
(4)小燕取15.0g固体样品和足量稀盐酸置于装置A中,打开活塞,充分反应后,测得装置C增重6.6g。
请计算样品中碳酸氢钠的质量分数。(写出计算过程)
活动三:拓展延伸
小林发现NaOH溶液与NaHCO 溶液混合后无明显现象,提出问题:NaOH和NaHCO 是否发生了化学反
3 3
应?
(5)猜想一:两者不反应
猜想二:两者发生反应,从元素守恒的角度,反应生成HO和 (写化学式)。
2
(6)已知:该实验条件下CaCl 溶液与NaOH溶液混合变浑浊,CaCl 溶液与NaHCO 溶液混合无现象,
2 2 3
为验证猜想二正确,请你补充实验方案:取少量NaHCO 溶液,向其中加入足量NaOH溶液, 。
3
(实验方案包括操作、现象和结论。可供选用的试剂有:CaCl 溶液、稀盐酸、澄清石灰水)
2