文档内容
二诊化学试题解析
1.【答案】C
【解析】A.制曲是以谷物(比如小麦)为基质,通过一定温度,湿度,通风等条件下,吸引空气中的
微生物在基质上繁殖,从而进一步产生各种酶,A涉及化学变化,A不符合题意。
B.发酵过程中,淀粉在淀粉酶作用下分解成低聚糖,B涉及化学变化,B不符合题意。
C.蒸馏是利用酒精,水和其他物质的沸点不同进行分离,C为物理变化,C符合题意。
D.陈酿是白酒储存一定时间让酒体内物质进一步发生物理和化学变化,使得酒体口感更醇和,风格
更协调等,D不符合题意。
2.【答案】C
【解析】A.基态B原子价层电子的轨道表示式为 ,A不符合题意。
B.HF为共价化合物,B不符合题意。
C.BF 空间结构为平面三角形,为非极性分子,C符合题意。
3
D.H O价层电子对为4对,其中2对为孤电子对,所以分子空间结构为V形,D不符合题意。
2
3.【答案】A
【解析】A.二氧化硅熔点高与可用于制造光导纤维,无对应关系,A符合题意。
B.碳酸氢铵受热产生大量气体,可用作食品膨松剂,B不符合题意。
C.食品抗氧化剂利用物质的还原性,C不符合题意。
D.铁与浓硝酸发生钝化,表面形成致密氧化膜阻止铁与硝酸进一步反应,D不符合题意。
4.【答案】B
【解析】B.定容后摇匀操作为盖好瓶塞,反复上下颠倒,摇匀。其余操作正确。
5.【答案】D
【解析】A.分子式为C H NO ,A不符合题意。
18 27 2
B.分子中含有3个手性碳原子( ),B不符合题意。
C.分子不饱和度为6,同分异构体不可能有2个苯环,C不符合题意。
D.分子含有酰胺基,所以能与盐酸反应,也能与NaOH溶液反应,D符合题意。
6.【答案】D
【解析】A.1.8gH O的物质的量为0.1mol,中子为0.8N ,A不符合题意。
2 A
B.常温常压,V 大于22.4L/mol,B不符合题意。
m
C.ClO−会发生水解,ClO−的数目小于0.1N ,C不符合题意。
A
D.反应每生成1molN H ,转移电子数为2N ,D符合题意。
2 4 A
7.【答案】A
【解析】A.Cu与浓硫酸可得CuSO ,Fe与CuSO 可得Cu,Cu与O 可得CuO,CuO与硫酸可得CuSO
4 4 2 4,
A符合题意。
B.NO与O 可以反应得NO ,NO 与H O反应可得NO,NO与NH 可得N ,N 不能直接得到NO ,
2 2 2 2 3 2 2 2
B不符合题意。
C.S与O 可得SO ,SO 与H S可得S,S不能直接得SO ,C不符合题意。
2 2 2 2 3
D.FeCl 与Fe可得FeCl ,FeCl 与Cl 可得FeCl ,FeCl 与氨水可得Fe(OH) ,Fe(OH) 不能直接得
3 2 2 2 3 3 3 3
到FeCl ,D不符合题意。
2
18.【答案】D
【解析】A.H S为气体或水溶液为弱酸不能拆,A不符合题意。
2
B.用FeCl 溶液制备Fe(OH) 胶体,应该为FeCl 在沸水中发生水解,B不符合题意。
3 3 3
C.过量Na SO 与H+反应生成HSO-,即3SO2+Cl +H O SO2+2Cl−+2HSO-,C不符合题意。
2 3 3 3 2 2 4 3
9.【答案】B
【解析】A.根据元素质量守恒,m=n-1,A不符合题意。
B.聚乳酸分子中有羟基,羧基,酯基共3种官能团,B符合题意。
C.聚乳酸可用于手术缝合线,具有良好的生物相容性和生物可吸收性,来自选修3教材高分子材料
章节P ,C不符合题意。
139
D.乳酸发生分子内脱水可生成内酯或者丙烯酸,而不是烯烃,D不符合题意。
10.【答案】C
【解析】根据信息推出元素W,X,Y,Z,Q分别为H,C,N,F,Al。
A.电负性:F>C>H,A不符合题意。
B.相对分子质量N >H ,单质沸点:N >H ,B不符合题意。
2 2 2 2
C.正确的为Al>N>F,C符合题意。
D.第一电离能:F>N>C,D不符合题意。
11.【答案】D
【解析】A.18-冠-6分子中含有饱和碳原子,所有原子不可能共平面,A不符合题意。
B.L-精氨酸中含“=NH”结构的N为sp2杂化,B不符合题意。
C.根据题目信息,18-冠-6为环状配体,L-精氨酸为客体,C不符合题意。
D.P中阴阳离子之间存在离子键,阴阳离子内部均存在配位键,阳离子内部18-冠-6的3个O原子
与N—H之间存在氢键,D符合题意。
12.【答案】A
【解析】A.Cu(NH ) SO 为离子化合物,根据相似相溶规律,乙醇极性小于水,A符合题意。
3 4 4
B.向I 的CCl 溶液中加入浓KI溶液,因发生I +I− I −,导致I 在KI溶液溶液中溶解度增大,
2 4 2 3 2
故不能说明I 在CCl 中溶解度小于在水中溶解度,B不符合题意。
2 4
C.红棕色气体可能是HNO 分解产生的NO ,C不符合题意。
3 2
D.AgOH溶于氨水,但没有证明可溶于强碱,不能证明AgOH体现两性,D不符合题意。
13.【答案】B
【解析】A.适当升高温度可以加快浸取速率,但是不宜温度过高,以防H O 分解,A不符合题意。
2 2
B.NaClO与盐酸会产生污染气体Cl ,B符合题意。
2
C.NaOH作用是除去没有完全沉淀的Fe3+,C不符合题意。
D.Li CO 溶解度随温度升高而减小,洗涤时时用热水可以减少溶解损耗,D不符合题意。
2 3
14.【答案】B
【解析】A.b极发生氧化反应,b极为阳极,b连接电源正极,A不符合题意。
B.a表面的反应历程只有非极性键的断裂,没有非极性键的形成,B符合题意。
C.阴极反应式:CO +N +6H++6e− CO(NH ) +H O,C不符合题意。
2 2 2 2 2
D.每转移4mol电子,右侧溶液既要考虑逸出O 还要考虑迁移走的H+,相当于质量减少2molH O,
2 2
D不符合题意。
15.【答案】A
【解析】A.随pH增大,Cr3+先转化为Cr(OH) ,后续Cr(OH) 转化为[Cr(OH) ]−,Cr(OH) 的量先增加
3 3 4 3
后减少,溶液中c(Cr3+)与c([Cr(OH) ]−)的总浓度先减小后增大,A符合题意;
4
B.根据K 、K 可计算a点pH=5,d点pH=11.2,差值为6.2,B不符合题意;
1 2
C.根据K 、K 可计算K=1031.4,C不符合题意。
1 2
D.假设可以完全溶解,c([Cr(OH) ]-)=0.1mol/L,反应后剩余c(OH-)=1mol/L,Q=c([Cr(OH) ]
4 4
2-)∶c(OH-)=0.1<10-0.4,即可以完全溶解,D不符合题意;
16.(14分)
(1)根据图示,仪器a的名称为三颈烧瓶。冷凝管中冷凝水应从下口进,上口出,即c口通入。
(2)Br−具有较强的还原性,浓硫酸具有强氧化性,二者反应生成Br 的水溶液为橙色,故原因是2NaBr
2
+3H SO (浓) Br +SO ↑+2H O+2NaHSO 或2HBr+H SO (浓) Br +SO ↑+2H O。
2 4 2 2 2 4 2 4 2 2 2
(3)反应生成了HBr和SO ,会污染环境,故装置B的主要作用是吸收挥发的HBr和SO ,防止污染
2 2
空气。
(4)三颈烧瓶中含有可能未反应完的H SO 和生成的NaHSO 、HBr等酸性物质,故用饱和NaHCO
2 4 4 3
溶液进行洗涤的目的是除去粗产品中的H SO 、NaHSO 等酸性物质。
2 4 4
(5)反应物20.6gNaBr为0.2mol,7.4g正丁醇为0.1mol,NaBr过量,故正溴丁烷的产率为
8.2g
100%≈59.9%。
0.1mol137g/mol
(6)根据正丁醇和正溴丁烷的沸点可知,正溴丁烷蒸馏完全后会馏出正丁醇,结合二者在水中的溶解
性可知,最后的馏出液溶于水即证明蒸馏完全。故用试管接取最后几滴馏出液,加入少量蒸馏水
并振荡,若无油珠出现,说明蒸馏完全。
(7)根据正溴丁烷结构简式,纯净的正溴丁烷只有四种不同化学环境的氢原子,即核磁共振氢谱只有
四组峰,而图谱中有5组峰,说明还含有杂质
17.(15分)
(1)“还原”后滤液中含有Cu2+和少量Zn2+、HAsO ,“置换”步骤中,过量铁粉置换出Cu单质,
2
故“滤渣1”的主要成分是Fe、Cu。
(2)根据流程信息,“还原”步骤生成溶解度较小的HAsO ,故AsO3发生反应的离子方程式是AsO3
2 4 4
+HSO-+2H+ HAsO ↓+SO2+H O。
3 2 4 2
(3)“置换”步骤所得溶液中含有Fe2+、Zn2+、HAsO 。“氧化沉砷”步骤生成FeAsO ,故加入H O
2 4 2 2
的目的是氧化Fe2+和HAsO ,使二者反应生成FeAsO 。
2 4
(4)K [Zn(OH) ]=c(Zn2+)×c2(OH−)=1.2×10−17,pH=8.5 时,c(OH−)=10−5.5 mol•L−1。c(Zn2+)=
sp 2
1.2×1017
=1.2×10−6mol•L−1。锌是两性金属,pH过高,Zn(OH) 会溶解生成[Zn(OH) ]2−。
(105.5)2 2 4
(5)“还原”步骤生成SO2,“调pH”步骤又引入了Na+,故“废液”中含有的溶质主要为Na SO 。
4 2 4
(6)①测定As O 晶体结构的常用仪器是X射线衍射仪。
2 3
②砷华由As O 分子类似金刚石的结构堆积而成,故砷华的晶体类型是分子晶体。
4 6
8×396
③根据砷华晶胞结构可知,一个晶胞中含有8个As O 分子,砷华的密度= =
4 6 (1.110-7)3N
A
g•cm−3。
18.(13分)
(1)焓变ΔH=产物生成焓之和-反应物生成焓之和,故ΔH =-31.1×2-0-0=-62.2kJ•mol-1。该
1
反应为放热、熵减反应,在低温下自发进行。
(2)①该反应为放热反应,温度越高,分解产生气体压强越大,故T <T 。
1 2
1
②K = ,故K ∶K =p ∶p =3或3:1。
p p(O ) p1 p2 平2 平1
2
(3)从状态Ⅰ到状态Ⅱ的过程ΔS>0,说明反应向左移动,气体质量及压强增加,A选项正确;从状态Ⅱ
到状态Ⅲ升温,平衡逆向移动,产生更多气体,根据质量守恒,m(Ⅰ)>m(Ⅲ),B选项错误。状态
Ⅱ到状态Ⅲ,温度更高,v(Ⅱ)<v(Ⅲ);状态Ⅲ到状态Ⅳ,因反应体系中只有O ,温度不变,K 不
2 p
变,O 浓度和压强均不变,v(Ⅲ)=v(Ⅳ),故v(Ⅱ)<v(Ⅳ),C选项正确。从状态Ⅲ到状态Ⅳ有Ag O
2 2
3分解产生Ag和O ,由于不知起始Ag的质量,因此无法确定两种状态Ag质量的关系,D选项
2
错误。
(4)乙醇催化氧化反应在该条件下不是可逆反应,故不能从平衡移动的角度思考。混合气体以固定流
速通过Ag/Ag O催化剂,主要考虑反应速率对反应的影响。
2
①根据4Ag(s)+O (g) 2Ag O(s) ΔH <0,升高温度,反应逆向移动分解为Ag和O ,起氧化
2 2 1 2
作用的Ag O减少,催化效率下降。
2
②延长了混合气体与催化剂的接触时间,提高了催化氧化反应的转化率。
19.(13分)
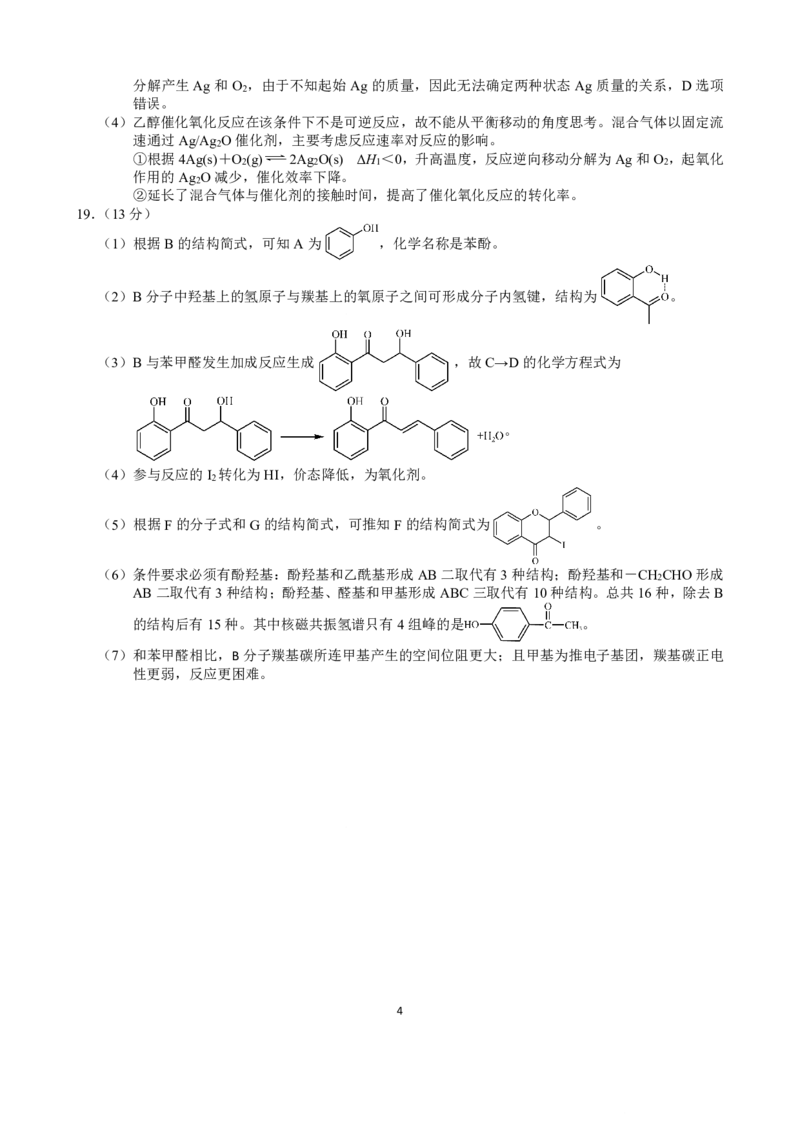
(1)根据B的结构简式,可知A为 ,化学名称是苯酚。
(2)B分子中羟基上的氢原子与羰基上的氧原子之间可形成分子内氢键,结构为 。
(3)B与苯甲醛发生加成反应生成 ,故C→D的化学方程式为
。
(4)参与反应的I 转化为HI,价态降低,为氧化剂。
2
(5)根据F的分子式和G的结构简式,可推知F的结构简式为 。
(6)条件要求必须有酚羟基:酚羟基和乙酰基形成AB二取代有3种结构;酚羟基和-CH CHO形成
2
AB二取代有3种结构;酚羟基、醛基和甲基形成ABC三取代有10种结构。总共16种,除去B
的结构后有15种。其中核磁共振氢谱只有4组峰的是 。
(7)和苯甲醛相比,B分子羰基碳所连甲基产生的空间位阻更大;且甲基为推电子基团,羰基碳正电
性更弱,反应更困难。
4