文档内容
2025~2026学年高三4月质量检测卷
化 学
考生注意:
1.本试卷分选择题和非选择题两部分。满分100分,考试时间75分钟。
2.答题前,考生务必用直径0.5毫米黑色墨水签字笔将密封线内项目填写清楚。
3.考生作答时,请将答案答在答题卡上。选择题每小题选出答案后,用2B铅笔把答题卡上对
应题目的答案标号涂黑;非选择题请用直径0.5毫米黑色墨水签字笔在答题卡上各题的答
题区域内作答,超出答题区域书写的答案无效,在试题卷、草·稿纸·上·作答·无效。
4.本卷命题范围:高考范围。
5.可能用到的相对原子质量:H1 C12 N14 O16 Na 23 Mg 24 A1 27 S32
Cl 35.5 K39 Fe 56 Co 59 Cu 64 Zn 65
一、选择题(本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符
合题目要求的)
1.中华文明历史悠久,文物是历史的见证。下列文物主要成分属于金属材料的是
A.青花瓷瓶 B.青铜剑 C.丝绸卷轴 D.竹简
2.工业上常用氨氧化法制硝酸,其中一步反应为4NH?+502继化4NO+6H?O。下列说法
正确的是
A. NO是极性分子 B.H?O的电子式:H+[:?:]2-H+
C.中子数为7的N:}N D. NH?中N的杂化方式为sp2
3.下列实验装置(夹持装置略)及操作均正确且能达到实验目的的是
选项 A B C D
实验 配制0.100 0 mol·L-1的
制备并收集SO? 分离乙酸乙酯和乙醇验证NH?易溶于水
目的 NaCl溶液
浓硫酸 NH?
实验 水
装置 铜粉
酚酞
溶液
【高三4月质量检测卷·化学 第1页(共6页)】4.下列有关物质用途的说法正确的是
A.因液氨汽化吸热,可用作制冷剂
B.聚氯乙烯可用于制作食品保鲜膜
C.因铝合金硬度小,常用于制造门窗
D.因二氧化硫能与碱反应,可用于葡萄酒保鲜
5.有机物d的合成路线如图所示(反应条件及其他产物已省略)。下列说法正确的是
○一分”mo-
A.化合物a的分子式为C?H?O B.化合物b可发生取代、氧化、消去反应
C.1mol化合物c最多与8 mol H?反应 D.化合物d分子中存在两个手性碳原子
6.下列事实与解释相符的是
选项 事实 解释
A
HF的沸点高于HCI HF分子间存在氢键
B CH?的键角大于NH? C的电负性小于N
C
I?在CCL中的溶解度大于在水中 I和CCL都是极性分子
D
金属Cu能导电 Cu中有自由移动的离子
1.~
7.化合物c的合成原理如下。下列说法正确的是
A.a的空间结构为三角锥形 B.化合物b属于烃
C.1个c分子中含有18个σ键 D.a、c中B的价层电子对数相同
8.设NA为阿伏加德罗常数的值,下列说法正确的是
A.1mol D?O中含有中子的数目为10NA
B.标准状况下,22.4L乙醇所含有分子的数目为NA
C.1L0.1 mol·L-1Na?S溶液中含有S2一的数目为0.1NA
D.标准状况下,22.4L由N?和O?组成的混合气体中含有原子的数目为NA
9.下列离子方程式正确的是
A.Fe与稀硫酸反应:2Fe+6H+—2Fe3++3H?个
B.向H?S溶液中加人CuSO?溶液,生成黑色沉淀:Cu2++S2-——CuS↓
C.用惰性电极电解MgCl?溶液:2H?O+2c-通电20H-+H?↑+Cl?↑
D.侯氏制碱(饱和食盐水中通人NH?和CO?):NH?+CO?+H?O+Na+—NaHCO?↓
+NH
【高三4月质量检测卷·化学 第2页(共6页)】10.短周期主族元素X、Y、Z、W的原于序数依次增大,X的原子核外只有1个电子,基态Y原子
的s能级电子数是p能级电子数的2倍,Z与Y同主族,常温下W的单质是黄色固体。下
列说法正确的是
A.原子半径:W>Z>Y>X B.最简单氢化物的热稳定性:Y>Z
CX与Y形成的化合物一定只含极性键 D.最高价氧化物对应水化物的酸性:Z>W
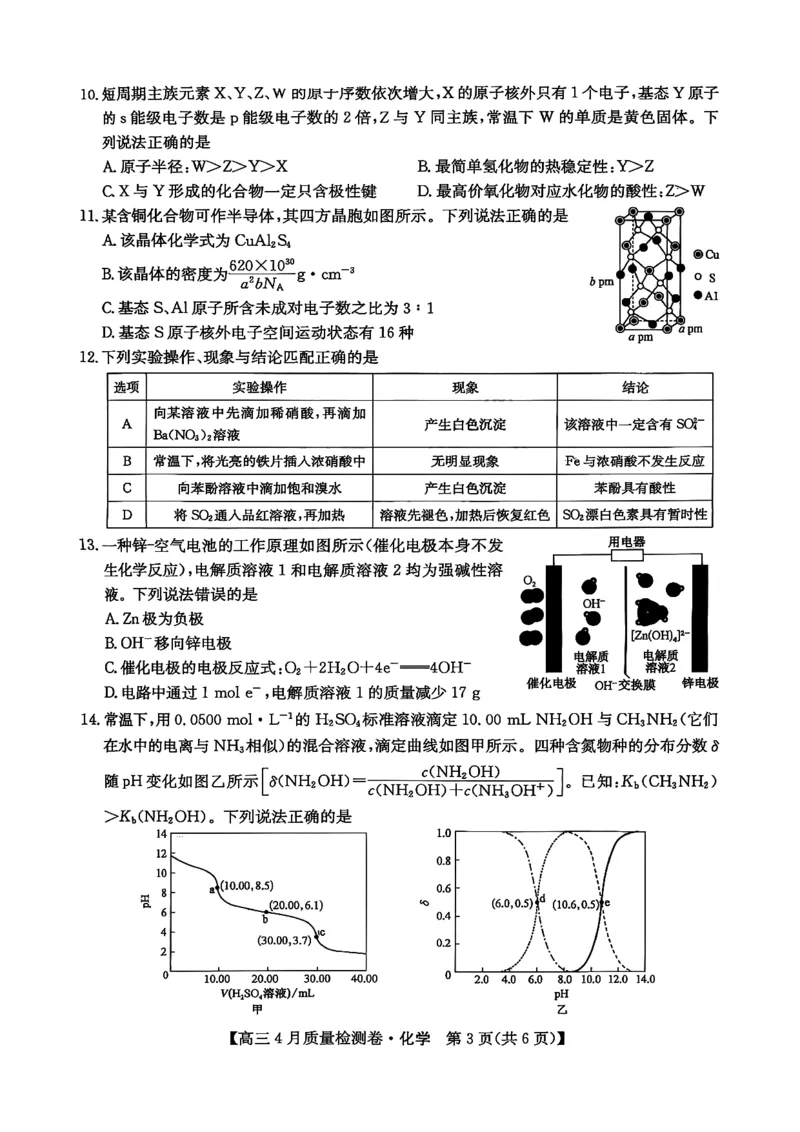
11.某含铜化合物可作半导体,其四方晶胞如图所示。下列说法正确的是
A.该晶体化学式为CuAl?S
62060°8·cm? ◎ ◎Cu
B.该晶体的密度为 o
bpm S
Q ●A1
C.基态S、Al原子所含未成对电子数之比为3:1
D.基态S原子核外电子空间运动状态有16种 a pm apm
12.下列实验操作、现象与结论匹配正确的是
选项 实验操作 现象 结论
向某溶液中先滴加稀硝酸,再滴加
A 产生白色沉淀 该溶液中一定含有SOR-
Ba(NO?)?溶液
B
常温下,将光亮的铁片插人浓硝酸中 无明显现象 Fe与浓硝酸不发生反应
C
向苯酚溶液中滴加饱和溴水 产生白色沉淀 苯酚具有酸性
D
将SO?通人品红溶液,再加热 溶液先褪色,加热后恢复红色 SO?漂白色素具有暂时性
13.一种锌-空气电池的工作原理如图所示(催化电极本身不发 用电器
生化学反应),电解质溶液1和电解质溶液2均为强碱性溶
液。下列说法错误的是
OH-
A.Zn极为负极
[Zn(OH)?]2-
B.OH-移向锌电极
电解质 电解质
C.催化电极的电极反应式:O?+2H?O+4e?—4OH- 溶液1 溶液2
催化电极 OH-交换膜 锌电极
D.电路中通过1 mol e,电解质溶液1的质量减少17g
14.常温下,用0.0500 mol·L-1的H?SO?标准溶液滴定10.00 mL NH?OH与CH?NH?(它们
在水中的电离与NH?相似)的混合溶液,滴定曲线如图甲所示。四种含氮物种的分布分数δ
随pH变化如图乙所示[8(NH?OH)=cNH?OH]H?CHH?OH+5].
已知:K?(CH?NH?)
>K?(NH?OH)。下列说法正确的是
14 1.0
12
0.8
10
a(10.00,8.5) 0.6
8
召 (20.00,6.1) 0 (6.0,0.5) d (10.6,0.5) e
6 0.4
b
4 ic
(30.00,3.7) 0.2
2
0 10.00 20.00 30.00 40.00 0 2.0 4.0 6.0 8.0 10.0 12.0 14.0
V(H?SO?溶液)/mL pH
甲 乙
【高三4月质量检测卷 学 第3页(共6页)】A.常温下,K?(NH?OH)=10-10.6__ _______
B.b点处满足:c(CH?NH3)+c(NH?OH+)<2c(SO一)
C.原混合溶液中c(NH?OH)=0.100 0 mol·L-1,c(CH?NH?)=0.200 0 mol·L-1
D.图乙中pH=10.6时,有c(CH?NH3)=c(CH?NH?)、c(NH?OH+)=c(NH?OH)
二、非选择题(本题共4小题,共58分)
15.(14分)高铁酸钠(Na?FeO?,易溶于水,不溶于乙醇,在强碱性溶液中较稳定,在酸性溶液中
快速产生O?)是一种绿色多功能水处理剂,具有强氧化性和絮凝作用,广泛用于杀菌消毒、
去除重金属离子(如Mn2+)。某化学兴趣小组在实验室中利用次氯酸盐在碱性环境中氧化
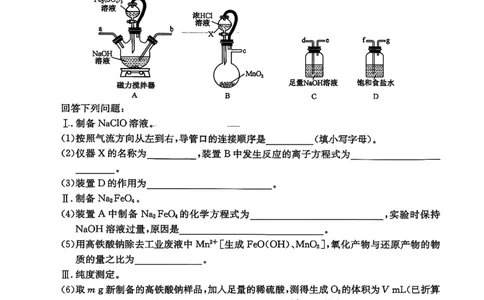
Fe3+制备高铁酸钠,实验装置(控温仪器、夹持仪器已省略)如图所示。
Fe?(SO?)?
溶液
浓HCI
a 溶液
b
— X e f= g
de
NaOH C
溶液
MnO? 望
足量NaOH溶液 饱和食盐水
磁力搅拌器
A B C D
回答下列问题:
I.制备NaCIO溶液。
(1)按照气流方向从左到右,导管口的连接顺序是______(填小写字母)。
(2)仪器X的名称为________,装置B中发生反应的离子方程式为
_。
(3)装置D的作用为_
Ⅱ.制备Na?FeO4。
—。
(4)装置A中制备Na2FeO?的化学方程式为_ ,实验时保持
NaOH溶液过量,原因是_____
(5)用高铁酸钠除去工业废液中Mn2+[生成FeO(OH)、MnO?],氧化产物与还原产物的物
质的量之比为_________。
Ⅲ.纯度测定。
(6)取mg新制备的高铁酸钠样品,加人足量的稀硫酸,测得生成O?的体积为V mL(已折算
成标准状况下)。该样品的纯度为_______×100列出算式)。
16.(14分)一种从废催化剂(主要成分为CoO、CoS、Al?O?,还含少量NiO、Fe?O?等)中回收铝
与钴的工艺流程如图所示。
空气 NaOH溶液 稀盐酸 NaOH溶液 萃取剂(RH) 试剂X(NH)?C?O?
废催化剂
NiO CoC?O·2H?O
焙烧 碱浸 酸浸 除铁 萃取 反萃取 沉钴
Fe?O?
气体A Fe(OH)? 萃取余液 萃取剂(RH)
过量试剂a
滤液- 沉铝→Al(OHD?
【高三4月质量检测卷·化学 第4页(共6页)】已知:部分金属阳离子生成氢氧化物沉淀时溶液的pH如表所示。
Co2+ Fe3+ Ni2+
金属阳离子
开始沉淀 7.0 2.3 7.1
沉淀完全 9.0 3.2 9.2
回答下列问题:
_____
。
(1)基态Co原子的价层电子排布式为 _,该元素在元素周期表中的位置为
_。
(2)“焙烧”时,采用“多层逆流焙烧”法,即混合料与空气逆向而行,该方法的优点是______
(3)“焙烧”时CoS参与反应的化学方程式为_____
(4)“除铁”时,控制pH的范围为________;试剂a可能为___(填化学式,任写一种)。
(5)“沉钴”前的溶液中c(Co2+)=1mol·L-1,“沉钴”后所得滤液中c(C?O2-)=1.0×
10-?mol·L-1,则沉钴率=___________[列出算式,K(CoC?O?)=a,沉钴率=
因沉淀始c的C2)×100不考虑溶液体积变化]。 20
残留的固体质量/g
18
16
(6)在空气中加热18.3g CoC?O?·2H?O,其残留的固体质量与 a(275,14.7)
14
12
温度的关系如图所示。c点对应固体的成分是_____
10
(填化学式,c点生成的固体为Co的氧化物)。 b(400,8.0) c(1000,7.5)
8
6
17.(15分)乙醇是重要的化工原料。回答下列问题:
200 400 600 800 1000 1200
I.乙醇催化重整制取氢气,反应机理如下: 温度/℃
反应1:C?H?OH(g)+H?O(g)—2CO(g)+4H?(g) △H?;
反应ii:CO(g)+H?O(g)CO?(g)+H?(g) △H?=-41.2kJ·mol-1。
(1)相关化学键的键能如下表,则△H?=________kJ·mol?1,反应i的△S_
(填“>”“<”或“=”)0。
化学键 C一H H—H C=O(CO中) C—C C—0 H—0
键能/kJ·mol-1 413 436 1071 348 351 463
(2)在密闭容器中充人一定量的C?H?OH(g)、H?O(g),仅发生反应i,达到平衡后,为了提
高乙醇的转化率和氢气产率,可以采取的措施是________(填字母)。
A.升高温度 B.增大压强 C.分离出CO D.选择高效催化剂
(3)压强为po下,在恒压密闭容器中充人1mol C?H?OH(g) 100 100
B (573,85)
和3 mol H?O(g)发生反应i、反应ii,平衡时 CO?和
80 80
选择性/% 转化率/%
CO的选择性、C?H?OH的转化率随温度的变化曲线如 60 (573,60) 60
例如:CO的选择性=n(CO九COnCO?) 40 40
图所示。 b
生成
20 20
(573,15) o
×100%]
0L
285 573 858
TIK
①表示CO选择性的曲线是__________(填字母)。
【高三4月质量检测卷·化学 第5页(共6页)】一一一
__
__
②573 K时,反应Ⅱ的Kp=________(保留1位小数)。
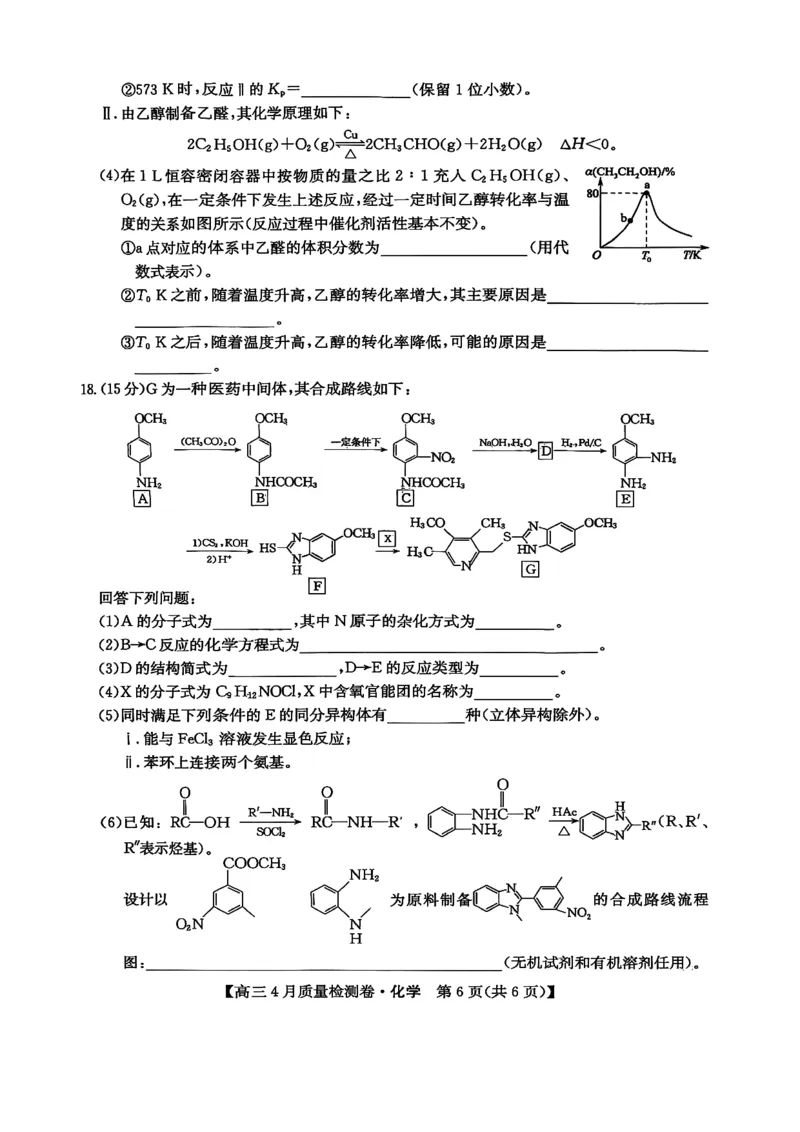
Ⅱ.由乙醇制备乙醛,其化学原理如下:
2C?H?OH(g)+O?(g)二2CH?CHOg)+2H?O(g) △H<0。
(4)在1L恒容密闭容器中按物质的量之比2:1充人 C?H?OH(g)、 a(CH?CH?O a H)/%
80
O?(g),在一定条件下发生上述反应,经过一定时间乙醇转化率与温
be
度的关系如图所示(反应过程中催化剂活性基本不变)。
①a点对应的体系中乙醛的体积分数为_________(用代 0 T。 T/K
数式表示)。
___。
②T。K之前,随着温度升高,乙醇的转化率增大,其主要原因是_________
③T。K之后,随着温度升高,乙醇的转化率降低,可能的原因是________
18.(15分)G为一种医药中间体,其合成路线如下:
_______
日
回答下列问题: _________。
(1)A的分子式为________,其中N原子的杂化方式为_____。
(2)B→C反应的化学方程式为_________
(3)D的结构简式为_________,D→E的反应类型为________。
(4)X的分子式为C?H??NOCl,X中含氧官能团的名称为________。
ma
(5)同时满足下列条件的E的同分异构体有____种(立体异构除外)。
i.能与FeCl?溶液发生显色反应;
ii.苯环上连接两个氨基。
(6)已知:
o,
R”表示烃基)。
设计以 为原料制备[ 的合成路线流程
H
图:_ (无机试剂和有机溶剂任用)。
【高三4月质量检测卷·化学 第6页(共6页)】